肺血管阻力对左心衰竭患者植入埋藏式心脏复律除颤器后室性心律失常事件的预测价值
2018-07-30陈灏璟张娟潘昌胡作英张航
陈灏璟,张娟,潘昌,胡作英,张航
慢性心力衰竭(心衰)是许多心血管疾病的终末阶段。国外研究显示,人群中慢性心衰的发病率为1.5%~2.0%,在65岁以上人群中达6%~10%[1]。半个多世纪前,美国的Framingham研究表明,慢性心衰患者中心脏骤停的发生率是普通人群的6~9倍,慢性心衰明显增加心脏性猝死和全因死亡风险[2]。临床研究证实,埋藏式心脏复律除颤器(ICD)和心脏再同步治疗除颤器(CRT-D)可显著降低这类患者的住院率和死亡率[3-5],因此被指南推荐为大部分左心室射血分数(LVEF)显著降低心衰患者的Ⅰ类适应证。
有研究显示,LVEF降低心衰患者中肺动脉高压的发生率为40%~75%[6]。肺动脉收缩压(PASP)升高是慢性心衰患者预后的独立危险因素,对全因死亡和心血管死亡均有预测价值[7]。
目前,肺血管阻力(PVR)对心衰患者室性心律失常的预测作用尚不明确。此外,对于可能从ICD治疗中获益的心衰患者来说,PVR对其预后的预测价值也不清楚。本研究旨在评估PVR对因左心衰竭植入ICD患者室性心动过速(室速)以及因心衰再住院或全因死亡的复合终点事件的预测价值。
1 资料与方法
研究对象:入选2010-01至2016-12期间在南京市第一医院因左心衰竭植入ICD或CRT-D的患者共122例,其植入标准基于ICD或CRT-D的一级预防和二级预防[8]。所有患者在手术前接受最优的药物治疗。本研究经医院伦理委员会审核,所有患者均知情并签署同意书。
超声心动图检查:所有患者在植入装置前行右心及常规左心超声心动图检查,具体方法参照美国超声心动图学会(ASE)2010年推荐的超声心动图评估右心功能指南[9],常规测量主动脉内径(AOD)、升主动脉内径(AAO)、肺动脉内径(RPA)、心尖四腔心切面右心室(RVD)左右径、心尖四腔心切面右心房左右径(RAL)及上下径(RAT)、四腔心切面右心房面积(RAA)、三尖瓣环位移(TAPSE)、二维面积变化分数(FAC)、三尖瓣血流多普勒速度(E、A、E/A、DT)、三尖瓣环组织多普勒速度(e’、a’)、左心房前后径(LAD)、左心室舒张期前后径(LVDd)、左心室收缩期前后径(LVDs)、室间隔舒张末期厚度(IVSd)、左心室舒张末期后壁厚度(LVPWd)、缩短分数(FS)、每搏输出量(SV)、心排血量(CO)、LVEF。同时,利用三尖瓣反流(TR)速度法测定PASP[PASP≈右心室收缩压(RVSP)=三尖瓣反流最大压差(△P)+右心房收缩压 (RASP)=4×三尖瓣最大反流速度(V2)+RASP];利用肺动脉反流(PR)速度法测定肺动脉平均压[mPAP,mPAP=4×舒张早期肺动脉反流峰值速度(V2peakPR)]和肺动脉舒张末期压力[PAEDP,PAEDP=4×舒张末期肺动脉反流速度(PREDV)2+ 右心房压力(RAP)];利用三尖瓣反流峰值速度与右室流出道时间流速积分比(TRV/TVIRVOT)的方法来测定 PVR[PVR=TRV(m/s)/TVIRVOT(cm)×10+0.16]。
起搏器程控:在植入设备后,对设备功能进行了完整的评估,依据2015 美国心律学会/欧洲心律学会/亚太心律学会/拉美心脏起搏与电生理协会埋藏式心脏复律除颤器程控及测试优化专家共识[10]对所有患者进行参数设置,具体如下:(1)起搏模式及频率设置:根据是否存在心动过缓起搏适应证选择起搏模式;对于CRT-D再同步起搏比例提升至98%以上;使用自动优化AV/VV间期功能;(2)心动过速检测设置:对于一级预防患者,将识别频率程控至200次/min,对于二级预防患者,检测频率提高至低于记录到的VT频率10~20次/min且不低于188次/min;将室上性心动过速鉴别诊断频率区间至至少200次/min;关闭SVT鉴别诊断超时功能;预先开启T波过感知识别功能;开启导线故障的早期预警功能;(3)心动过速治疗设置:所有患者都设定了抗心动过速(ATP)治疗的室速检测区,Burst模式优先,ATP刺激数至少8个;将心室颤动的初始电击能量设置为最大除颤能量。
术后随访和观察指标:术后进行心律失常、心衰、基础病的常规治疗,采用门诊及住院复查的方式于术后1、3个月及之后每隔6个月进行临床评估和器械随访,搜集随访资料。评估心律失常的识别和治疗情况,根据ICD工作情况及室速事件发生调整ICD各项参数,若发生电击等ICD治疗事件及时就医。所有ICD/CRT-D程控结果由至少两位不同的电生理专科医师进行阅读判断,确认器械诊断是否准确,治疗是否及时、有效,并根据检查结果给予适当调整。观察终点:主要终点为患者因室速接受ICD恰当治疗,ICD恰当治疗被定义为患者发生室速或心室颤动后接受的ATP或电击治疗;次要终点为随访期间患者因心衰再住院或全因死亡。
统计学方法:采用SPSS20.0统计学软件进行统计学分析,计量资料采用±s表示,组间比较采用t检验;计数资料采用例数(%)表示,组间比较采用卡方检验和精确概率fisher检验,Cox回归分析发生室速的独立危险因素;Kaplan-Meier对ICD患者室速发生率进行估计,组间比较采用Log-rank检验,P<0.05被认为差异有统计学意义。
2 结果
122例患者的基线特征:共入选左心衰竭患者122例,其中男性97例,女性25例,平均年龄(63±8)岁;缺血性心肌病40例(32.8%),非缺血性心肌病82例(67.2%);平均纽约心脏协会(NYHA)心功能分级(2.9±0.5)级,平均LVEF(29.6±8.1)%;植入ICD 55例(45.1%),植入CRT-D 67例(54.9%);一级预防74例(60.7%),二级预防48例(39.3%);随访期间,应用螺内酯、血管紧张素转换酶抑制剂/血管紧张素Ⅱ受体拮抗剂、β受体阻滞剂、胺碘酮的患者分别有71例(58.2%)、97例(79.5%)、83例(68%)、27例(22.1%)。
122例患者的超声心动图主要参数:所有患者术前行超声心动图检查,测得平均LAD(49.1±9.2)mm,LVDd(62.9±11.6)mm,LVDs(50.7±13.7)mm,RAL(60.2±13.4)mm,RAT(54.4±10.5)mm,RAA(19.27±19.0)cm2,RVD(29.6±4.2)mm,PASP(45.1±15.3)mmHg(1 mmHg=0.133 kPa),PADP(18.4±5.1)mmHg,mPAP(27.4±14.6)mmHg,CO(2.9±1.7)L/min,PVR(2.6±0.8)WUs;三尖瓣反流:轻度16例(13.1%),中度93例(76.3%),重度13例(10.6%);TAPSE(12.1±2.6)mm。
左心衰竭患者植入ICD后主要终点事件发生情况及预测因素分析:所有患者平均随访4.2年,36例(29.5%)患者记录到121次ICD恰当治疗,其中ATP治疗32例(26.3%)共72次,电击治疗16例(13.1%)共39次。将发生和未发生主要终点事件的患者基线临床资料进行比较后发现,两类患者在一级或二级预防、PASP、PVR及TAPSE之间差异均有统计学意义(P均<0.05,表1)。单因素Cox回归分析提示,一级或二级预防(HR=3.550, 95%CI: 1.950~5.650, P<0.01)、PVR(HR=3.170, 95%CI: 1.406~7.160, P<0.01)与心衰患者出现室速并接受ICD恰当治疗显著相关;进一步多因素分析表明,PVR是心衰患者出现室速并接受ICD恰当治疗的独立危险因素(HR=1.630, 95% CI: 1.170~2.010,P<0.01),见表 2。
表1 发生和未发生主要终点事件的患者基线临床资料比较(±s)

表1 发生和未发生主要终点事件的患者基线临床资料比较(±s)
注:CRT-D:心脏再同步治疗除颤器;ICD:埋藏式心脏复律除颤器;ACEI:血管紧张素转换酶抑制剂;ARB:血管紧张素Ⅱ受体拮抗剂。主要终点:出现室性心动过速并接受ICD恰当治疗。1 mmHg=0.133 kPa
年龄 (岁) 62.1±14.1 63.9±10.4 0.485肺血管阻力 (WUs) 3.1±0.9 2.4±0.7 <0.001
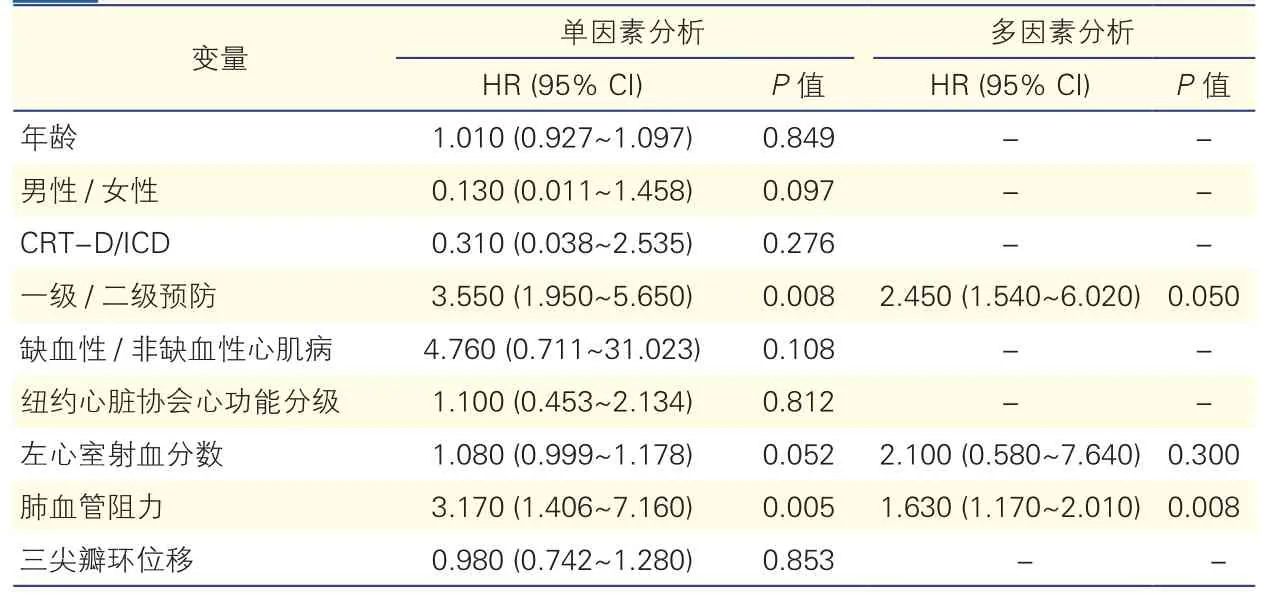
表2 左心衰竭患者植入ICD后主要终点事件预测因素的Cox回归分析结果
不同PVR左心衰竭患者植入ICD后主要终点事件发生率比较(图1):在PVR≥2.5 WUs的患者中,28例(45.2%)出现室速并接受ICD恰当治疗,而在PVR<2.5 WUs的患者中,仅有8例(13.3%)出现室速并接受ICD恰当治疗(P<0.01);Kaplan-Meier分析显示,PVR≥2.5 WUs的患者植入ICD后主要终点事件的发生率明显高于PVR<2.5 WUs的患者(P=0.002)。

图1 不同肺血管阻力左心衰竭患者植入ICD后主要终点事件发生率比较
左心衰竭患者植入ICD后次要终点事件发生情况及预测因素分析:随访期间,122例患者中因心衰再住院或全因死亡的患者有31例;其中心衰再住院29例(23.7%),共住院31次;死亡18例(14.7%),因心衰死亡6例,猝死4例(1例恶性心律失常、1例肺栓塞、2例原因不明),心肌梗死1例,脑血管意外3例,肺部感染3例,肿瘤1例。将发生与未发生次要终点事件的患者的基线临床资料进行比较后发现,两者的PASP和PVR差异均有统计学意义(P均<0.001,表3)。Cox单因素和多因素回归分析均提示,PVR高是心衰患者次要终点事件的独立预测因素(单因素分析:HR=3.140, 95% CI: 1.536~3.134, P=0.007;多因素分析:HR=2.030, 95% CI: 1.210~3.120,P<0.01),见表4。
不同PVR左心衰竭患者植入ICD后次要终点事件发生率比较(图2):在PVR≥2.5 WUs的患者中,24例(38.7%)死亡或因心衰再住院,而在PVR<2.5 WUs的患者中,仅7例(11.7%)死亡或因心衰再住院(P<0.01)。Kaplan-Meier分析显示,PVR≥2.5 WUs的患者中次要终点事件的发生率显著高于PVR<2.5 WUs的患者(P<0.05)。
表3 发生和未发生次要终点事件的患者基线临床资料比较(±s)
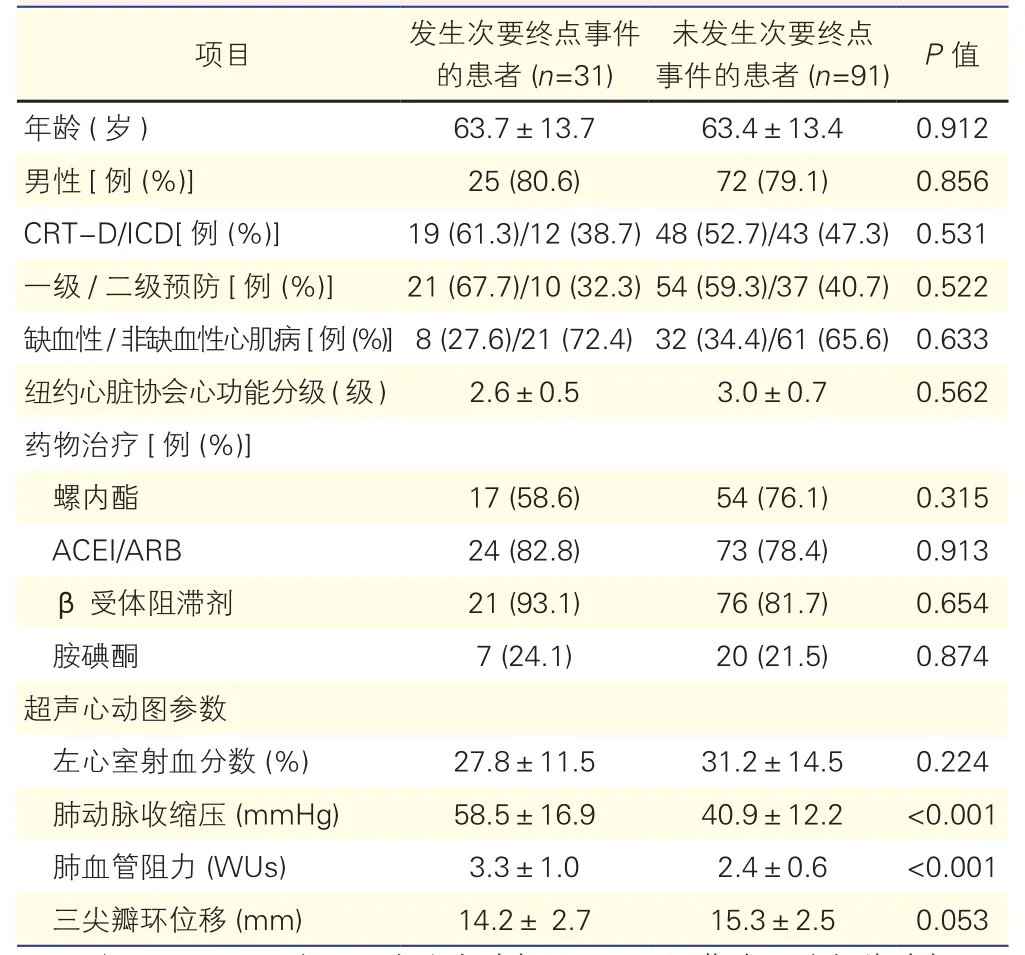
表3 发生和未发生次要终点事件的患者基线临床资料比较(±s)
注:CRT-D:心脏再同步治疗除颤器;ICD:埋藏式心脏复律除颤器;ACEI:血管紧张素转换酶抑制剂;ARB:血管紧张素Ⅱ受体拮抗剂。次要终点:因心力衰竭再住院或全因死亡的复合终点。1 mmHg=0.133 kPa
年龄(岁) 63.7±13.7 63.4±13.4 0.912肺血管阻力 (WUs) 3.3±1.0 2.4±0.6 <0.001
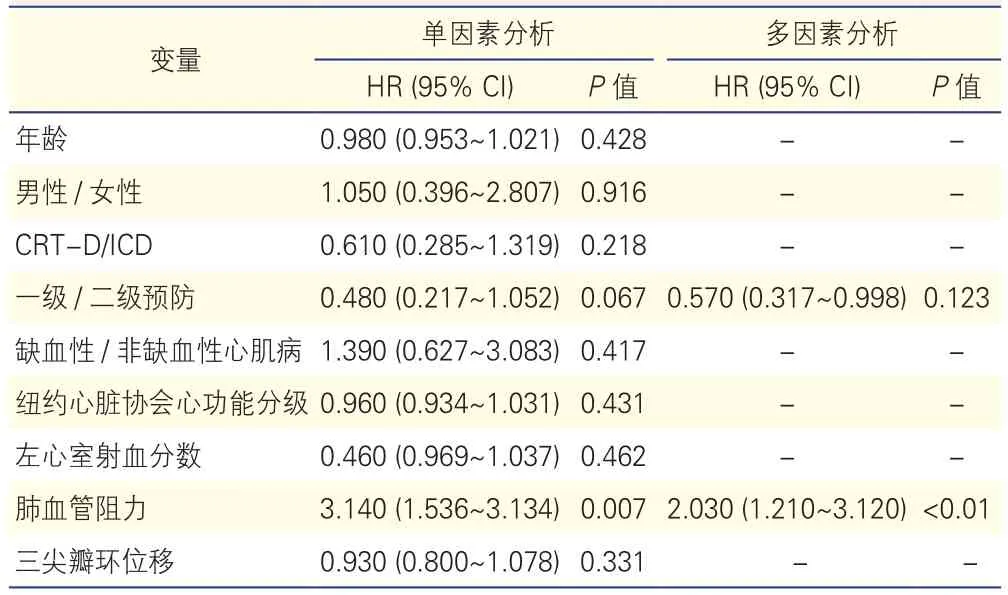
表4 左心衰竭患者植入ICD后次要终点事件预测因素的Cox回归分析结果

图2 不同肺血管阻力左心衰竭患者植入ICD后次要终点事件发生率比较
3 讨论
PVR是反映肺循环血流动力学和肺血管结构改变程度的重要指标。本研究观察了PVR与因左心衰竭植入ICD的患者室性心律失常的关系,结果显示,PVR升高不仅是慢性心衰患者出现室速并接受ICD恰当治疗的独立危险因素,还是心衰患者植入ICDCRT-D后因心衰再住院或全因死亡的独立预测因子。
在LVEF下降的左心衰竭患者中,由于其左心室舒张末期压力增高,肺静脉压增大,肺静脉充血,引起淤血性肺动脉重构,包括内膜纤维化及新生内膜和中膜增厚、小动脉机化[11],跨肺压力阶差增高,诱发肺动脉收缩,导致PVR增高,称为“毛细血管前和后混合性肺动脉高压”[12]。和PVR正常的肺动脉高压患者相比,混合性肺动脉高压由于肺动脉结构和功能本身发生的主动性改变参与了肺动脉压力的升高[13],因此PVR升高更显著,预后更差[6]。PVR升高进一步导致左心室前负荷过度下降,使得LVEF进一步恶化。肺动脉压力升高导致右心室后负荷增加,加重慢性心衰患者右心室重构,引起右心功能不可逆损害,最终导致左心、右心功能衰竭[14,15]。在肾素-血管紧张素-醛固酮系统激活、电解质失衡及离子通道改变、机械-电反馈等多种机制的参与下,进一步导致慢性心衰患者室性心律失常发生风险增加[16,17]。
ICD用于识别并治疗室速。我们发现,PVR升高是心衰患者出现室速并接受ICD恰当治疗的独立危险因素,提示高PVR患者发生室速的可能性更大,植入ICD后接受ICD恰当治疗的几率更大,患者的生存获益更高。值得注意的是,主要终点的多因素分析显示,一级/二级预防的P值恰为0.05,提示一级/二级预防与心衰患者发生室速并接受ICD恰当治疗间的差异边缘显著。这提示我们在以后的研究中可以进一步以一级或二级预防患者为样本分别进行分析,或增加样本量,来进一步评估一级/二级预防和慢性心衰患者室性心律失常发生的相关性。
有研究表明,PVR水平与心衰患者心室重构和心衰死亡显著相关;PVR越高,因心衰住院及全因死亡的风险越大[18,19]。Tatebe等[20]在一项观察性研究中纳入了158例慢性心衰导致肺动脉高压的患者,平均随访2.6年后发现, PVR越高、跨肺压力阶差越大,死亡率越高。有研究提示,PVR升高是慢性心衰患者死亡的独立预测因素[21]。本研究利用Cox单因素和多因素回归分析发现,PVR升高为植入ICD或CRT-D的心衰患者因心衰再住院和全因死亡复合终点事件的独立预测因素,提示高PVR患者ICD植入术后因心衰再住院和全因死亡的风险增加。此外,本研究共记录到全因死亡患者18例(14.7%),仅3例患者接受至少一次ICD电击治疗,说明ICD电击和死亡并无明显关联,接受ICD电击治疗并不增加死亡风险。
右心导管检查是诊断肺动脉高压的金标准,但目前研究多采用多普勒超声心动图作为诊断肺动脉高压的方法,而国内外肺动脉高压超声心动图的诊断标准尚未统一,所以这类研究受到超声心动图估测PASP准确性的限制[7]。在本研究中,我们采用Abbas等[22]推荐的方法定量分析左心衰竭患者的PVR;根据相关指南[9]规定,本法对于PVR不超过8 WUs者,与心导管所测值相关性良好;在本研究中PVR最高者仅5.7 WUs,因此准确性较高。本研究中Kaplan-Meier分析显示,PVR≥2.5 WUs的患者植入ICD后发生室速并接受ICD恰当治疗以及因心衰再住院或全因死亡的发生率均显著高于PVR<2.5 WUs患者,提示PVR为2.5 WUs可能是慢性心衰患者植入ICD后室速等高危事件发生风险高低的判定截点。因此,高PVR患者植入ICD获益更大,监测PVR对ICD植入后室速的发生及患者的长期预后有一定的预测价值。
本研究的局限性:(1)样本量较小,需进一步积累病例对研究结果进行验证;(2)本研究仅用多普勒超声心动图估测患者PVR水平,期待以后开展多中心、大样本的临床试验,用右心导管检查进一步测量患者的PVR水平,来检验多普勒超声心动图对PVR水平的测量准确性。
总之,本研究发现,高PVR的慢性心衰患者植入ICD后发生室速并接受ICD恰当治疗的几率更大,因心衰再住院和全因死亡的风险更高。利用术前多普勒超声心动图检测慢性心衰患者的PVR,可以更精确地对接受ICD治疗的患者进行危险分层,因此具有重要的临床意义。
