基于两种旋转调强全中枢放射治疗技术的剂量学研究*
2018-07-16解传滨丛小虎戴相昆陈高翔葛瑞刚鞠忠建曲宝林
江 楠 解传滨 丛小虎 戴相昆 陈高翔 葛瑞刚 鞠忠建 曲宝林
全脑全脊髓照射(craniospinal irradiation CSI)主要应用于容易沿脑膜或脑脊液播散转移的脑恶性肿瘤的治疗,有着较高的5年生存率[1-2]。由于CSI靶区贯穿全脑至脊髓圆锥部整个人副体中枢轴区域,照射范围较大,患者极易出现较大不良反应,如恶心、呕吐及骨髓抑制等[3]。因此,在保证全中枢靶区接受足够剂量照射的基础上,如何进一步降低各危及器官(organ at risk,OAR)的受照剂量成为临床研究的重点。
螺旋断层放射治疗(helical tomotherapy,HT)和容积旋转调强放射治疗(volumetric modulated arc therapy,VMAT)作为目前较为先进的放射治疗技术,在临床上得到了广泛的应用。HT从360°分51个射野方向对复杂靶区实行螺旋照射,最大治疗长度可达160 cm,在提高靶区适形度的同时可最大限度地保护周围正常组织,具备了实施CSI的技术优势[4]。VMAT是在机架旋转的同时通过改变剂量率和多叶准直器(multi-leaf collimator,MLC)射野形状来实现靶区剂量覆盖的一种动态调强技术,并可通过多中心计划优化的方式实现对较长靶区的高度适形照射,使其在全中枢照射的临床应用成为可能[5-6]。本研究通过比较快速容积(rapid arc,RA)旋转调强放射治疗与HT两种旋转调强技术在全中枢照射中的剂量学差异,为临床应用标准的选择提供参考。
1 资料与方法
1.1 一般资料
回顾性选取2015年6月至2017年8月在解放军总医院放射治疗科接受CSI的8例患者,其中男性3例,女性5例;年龄3~26岁,中位年龄14.5岁;髓母细胞瘤术后4例,急性髓系白血病移植后2例,T淋巴母细胞瘤2例。所有患者均行全中枢定位扫描,完成靶区及相应OAR勾画,分别设计HT及RA两种旋转调强计划,处方剂量为36 Gy/20 F。
1.2 仪器设备
定位扫描采用大孔径C T模拟定位机(德国SIEMENS);pinnacle9.3系统(荷兰Philips);HT计划设计采用Hi.ART4.3计划系统(美国Accuray);RA计划设计采用Eclipse10.0计划系统(美国Varian)。
1.3 靶区定义及处方剂量
患者固定装置为头肩模+体模及头颈肩一体板;定位扫描范围自头顶至坐骨结节,扫描层厚为5 mm。由医师在pinnacle9.3系统上进行全脑全脊髓的勾画,定义为临床靶区(clinical target volume,CTV),并完成晶体、眼球、肺、心脏、肝脏、肾脏及小肠等相关OAR的勾画,CTV外放5 mm定义为计划靶区(planning target volume,PTV),并将Body轮廓排除PTV定义为正常组织(normal tissue,NT)。处方剂量36 GY/20 F。
1.4 调强放射治疗计划
(1)HT计划。计划设计采用计算网格为Fine,射野宽度(field width,FW)设置为5.05 cm,螺距值(pitch)设置为0.43,调制因子(modulation factor,MF)设置为2.0,并将晶体外放3 mm区域设置为全屏蔽模式(completed block)。
(2)RA计划。计划设计采用Clinac iX直线加速器(美国Varian)6 MV的X射线多中心衔接优化的方式,根据患者靶区长度设为2~4个中心,每个中心采用2个全弧照射(顺时针180.1°~179.9°,逆时针179.9°~180.1°),为避免射野衔接处剂量冷热点的出现,相邻中心射野重叠要求>2 cm。将全脑部位2个射野的准直器设置为90°,其余中心射野的准直器分别设置为5°和355°。
1.5 计划评估
靶区剂量评估包括:①靶区剂量(D95%)及覆盖度体积(V95%);②近似最大剂量(D2);③近似最小剂量(D98%);④平均剂量(Dmean)以及剂量分布的均匀性指数(homogeneity index,HI);⑤适形度指数(conformity index,CI),其计算为公式1:

式中Vptv1为处方剂量覆盖靶区的体积;Vptv为靶区体积;Vt为处方剂量的体积。
CI值越接近1,表明靶区适形度越高;其靶区HI的计算为公式2:

HI值越接近0,表明靶区剂量均匀性越好[7]。各OAR评估通过剂量-体积直方图(dose-volume histogram,DVH)读取各剂量学参数,并根据各器官临床剂量限制要求分别对其Dmax、Dmean及V5,V10,V20,V30等剂量学参数进行统计学分析比较,最后通过总机器跳数及计划实施时间来评估两种计划的实施效率。
1.6 统计学方法
采用IBM SPSS statistics 22.0统计软件进行数据分析。采用配对t检验的方式对两种计划的各剂量学参数进行统计分析,以P<0.05为差异有统计学意义。
2 结果
2.1 靶区剂量参数比较
通过对两种计划靶区各剂量参数分析比较发现,两种旋转调强技术均能得到较好的靶区剂量分布,并且达到了相当的靶区剂量覆盖度及靶区均匀性。在靶区适形度方面,RA技术有略优于HT技术的优势,CI值分别为0.90±0.06和0.86±0.01,但差异无统计学意义(t=2.532,P>0.05),见表1。
表1 RA和HT计划的靶区参数统计学比较
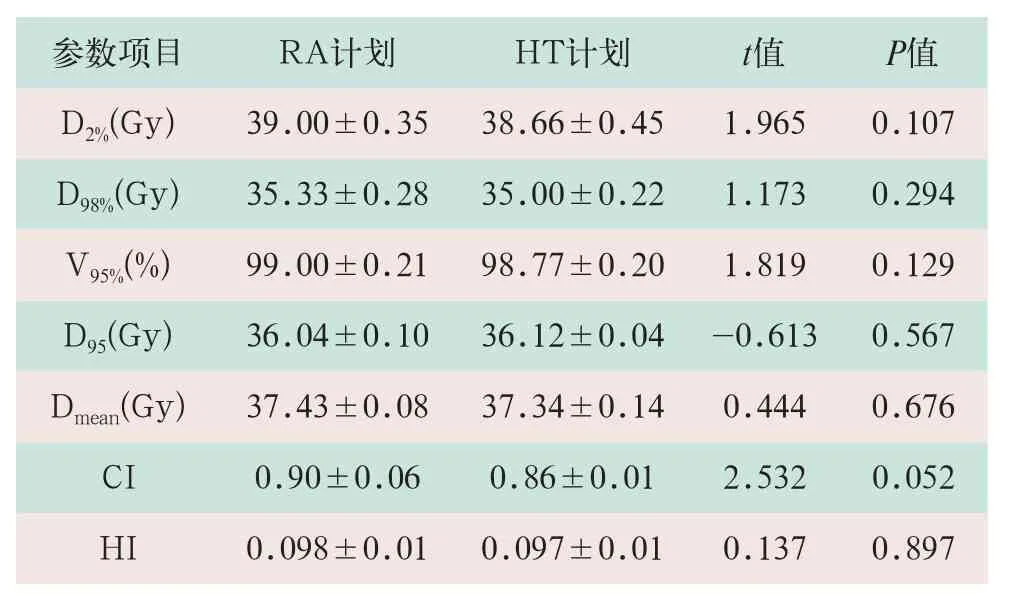
表1 RA和HT计划的靶区参数统计学比较
注:表中CI为适形指数;HI为均匀指数。
参数项目 RA计划 HT计划 t值 P值D2%(Gy) 39.00±0.35 38.66±0.45 1.965 0.107 D98%(Gy) 35.33±0.28 35.00±0.22 1.173 0.294 V95%(%) 99.00±0.21 98.77±0.20 1.819 0.129 D95(Gy) 36.04±0.10 36.12±0.04 -0.613 0.567 Dmean(Gy) 37.43±0.08 37.34±0.14 0.444 0.676 CI 0.90±0.06 0.86±0.01 2.532 0.052 HI 0.098±0.01 0.097±0.01 0.137 0.897
2.2 OAR剂量参数比较
通过对两种计划各OAR剂量学参数进行比较发现,两种计划仅达到了各器官的临床剂量限制要求。HT计划通过射野屏蔽设置得到的晶体Dmax明显低于RA计划,但眼球Dmean却较RA计划高出了40.8%;而在腮腺、口腔、肺、肝脏、胃、肾脏以及小肠的各百分体积参数比较中,HT计划均低于RA计划,且V5除心脏以外,两种计划的其他OAR剂量学参数比较均具有统计学意义(t=17.523,t=8.421,t=5.862,t=5.001,t=5.334,t=4.020,t=3.369;P<0.05);V10除口腔、肺脏外其他器官差异均有统计学意义,而V20只有腮腺、肝脏及肾脏差异有统计学意义(t=2.318,t=2.768,t=2.423;P<0.05);在Dmean比较中,除胃和小肠的差异无统计学意义外,其他器官HT计划均明显低于RA计划;而对NT的剂量参数评估发现,除V10外,RA计划均较优于HT计划,但差异均无统计学意义,见表2。
2.3 计划实施效率评估
通过对两种计划总机器跳数及计划实施时间比较发现,RA计划实施效率要明显高于HT计划,HT总机器跳数和计划实施时间分别为RA计划的6.5倍和1.16倍,表明RA技术具有更高的射线利用率,见表3。
表2 RA和HT计划OAR参数统计学比较

表2 RA和HT计划OAR参数统计学比较
RA计划 HT计划 t值 P值晶体 Dmax(Gy) 6.30±0.23 5.40±0.26 2.355 0.038眼球 Dmean(Gy) 9.44±0.35 13.03±1.71 -2.108 0.059口腔Dmean(Gy) 9.32±0.477 7.31±0.44 10.793 0.000 V5(%) 99.98±0.02 67.75±3.83 8.421 0.000 V10(%) 31.27±8.07 19.6±3.10 2.082 0.092 V20(%) 0.04±0.04 1.00±0.75 -1.353 0.234腮腺Dmean(Gy) 12.57±0.30 8.43±0.24 9.445 0.000 V5(%) 79.98±0.06 70.01±5.92 17.523 0.000 V10(%) 56.46±4.03 31.66±2.14 8.730 0.000 V20(%) 4.37±1.42 1.10±0.32 2.318 0.041肺Dmean(Gy) 6.27±0.25 5.92±0.25 2.095 0.060 V5(%) 57.83±2.14 44.50±3.00 5.862 0.000 V10(%) 12.81±3.33 9.54±1.41 1.110 0.291 V20(%) 1.14±0.38 1.28±0.40 -0.491 0.633心脏Dmean(Gy) 12.83±0.99 8.22±0.43 0.003 0.003 V5(%) 99.96±0.03 94.94±2.32 2.158 0.083 V10(%) 47.67±14.37 21.25±4.32 2.783 0.039 V20(%) 5.99±2.92 0.19±0.12 2.023 0.099肝脏Dmean(Gy) 8.30±0.69 5.63±0.74 5.160 0.004 V5(%) 73.93±5.50 59.23±5.63 5.001 0.004 V10(%) 32.62±7.25 10.18±2.75 4.308 0.008 V20(%) 0.71±0.26 0.03±0.02 2.768 0.039肾脏Dmean(Gy) 5.69±0.19 4.64±0.11 5.271 0.000 V5(%) 40.07±2.46 26.55±1.57 5.334 0.000 V10(%) 10.43±1.18 4.04±0.87 4.462 0.001 V20(%) 0.75±0.23 0.24±0.12 2.423 0.034胃Dmean(Gy) 8.70±0.51 6.37±0.27 5.555 0.003 V5(%) 91.29±3.79 73.29±5.62 4.020 0.010 V10(%) 28.57±7.97 5.01±2.18 3.732 0.014 V20(%) 0.25±0.14 0.03±0.03 1.528 0.187小肠Dmean(Gy) 10.86±1.17 9.00±0.77 1.889 0.118 V5(%) 88.79±5.20 83.89±5.30 3.369 0.020 V10(%) 50.78±8.74 34.48±8.47 2.064 0.094 V20(%) 6.38±3.63 1.63±0.60 1.393 0.222正常组织Dmean(Gy) 7.00±0.79 7.29±0.54 -1.098 0.353 V5(%) 48.43±3.66 49.79±2.67 -1.108 0.349 V10(%) 23.09±4.05 21.65±2.44 0.800 0.482 V20(%) 6.57±1.89 7.38±1.36 -1.368 0.265
表3 RA和HT计划实施效率比较

表3 RA和HT计划实施效率比较
注:表中RA为快速容积治疗;HT为螺旋断层放射治疗。
治疗计划 参数项目机器跳数(MU) 计划实施时间(s)RA 1128±105.45 450±38.73 HT 7381.17±706.14 522.72±49.04 t值 -9.422 -3.679 P值 0.000 0.014
3 讨论
随着放射治疗技术的发展,现代放射治疗已经发展到精确定位、精确计划以及精确治疗的高级阶段,以二维射野计划为基础的CSI已渐渐淡出历史舞台。三维适形放射治疗(three dimensional conformal radiation therapy,3D-CRT)的出现使CSI进入精确放射治疗时代[8]。采用左右等中心半野对穿实现对全脑部分的照射,通过等中心接野并周期性移动射野衔接边界的办法来完成全脊髓部分的照射,并最大可能避免接野处靶区局部剂量冷热点的累加,但也不同程度的造成了相应靶区部分剂量欠量情况的出现[9]。普通调强放射治疗(intensity modulated radiation therapy,IMRT)技术在CSI临床应用中有效改善了靶区剂量分布,并明显降低了正常器官受量,但临床实施的复杂程度及相邻射野间的剂量衔接等问题禁锢了其在CSI临床应用的普及与推广[10]。
近年来,以HT及VMAT为代表的治疗新技术的临床推广应用,为放射治疗的发展带来了革命性的改变,也为CSI技术的不断完善与发展提供了可能[11-12]。有研究报道,HT在CSI中的剂量学优势,但其临床实施需要特殊的螺旋断层放射治疗装置。而RA技术可以在普通加速器上予以实施,因此更便于在一般放射治疗单位的普及开展[13-15]。但是,由于CSI超长靶区的特性,对于普通加速器最大40 cm射野限制,计划设计必须采用多中心方法。虽然其计划系统具备了多野多中心同计划优化的技术优势,在计划阶段实现了射野间的无缝衔接,但患者实际治疗摆位过程中,通过图像引导对各中心体位进行校准所带来的轻微体位变化势必带来相邻射野在患者体内剂量衔接的不确定度,这也是RA技术在CSI应用中亟需解决的问题[16-17]。而HT治疗计划只能有一个中心,仅凭治疗前单次影像配准很难保证较长靶区在整个治疗过程患者体位的准确性[6]。有单位通过在治疗实施半程时进行治疗中断,并通过创建后续计划进行重新摆位校准,以实现对患者体位的及时误差校对。但由此也带来了中断前后剂量衔接不确定性,因此建议在不同的治疗次间选择不同的中断节点以减少由此带来的影响。本研究所采用的办法为在HT每次治疗前分别对头部及胸腹部进行两次图像扫描并读取配准误差,取两者平均值进行评估校准后进行治疗的实施,然而,该方法对靶区外放要求及体位校准所带来的患者实际受照剂量影响还需进一步的临床研究。
由于Clinac iX加速器X轴铅门动态调强的推荐宽度为15 cm,本研究在RA计划设计之初将Y轴铅门设置成与靶区纵轴方向相一致的方式,以尽量减少射野中心的数量,但是优化得到的靶区剂量均匀性较差,分析发现是由于全脑部位靶区横向范围较大,15 cm宽度的射野在旋转的过程中无法实现对全脑靶区的较好覆盖,因此将该部分射野准直器角度进行了旋转90°的设置,使得Y轴铅门与旋转弧的切线方向垂直[19]并调整射野宽度与靶区大小相一致,其他部分射野准直器保持初始设置。通过这种办法有效解决了靶区剂量均匀性较差的问题,最终RA计划得到了与HT近乎相当的靶区剂量均匀性。而在对两种计划靶区剂量适形度的比较中,RA计划体现出了略优于HT的趋势,分析发现是由于在HT计划设计中为了有效保护晶体,对LENS外放3 mm区域进行了射野全屏蔽的设置,即经过该区域射野的MLC处于关闭状态,加之较大射野宽度(5.05 cm)设置所导致的纵向剂量延伸,不可避免的造成了晶体周边全脑靶区剂量的欠量,尤其在晶体纵向边缘这种现象更为明显。
本研究针对两种旋转调强技术在全弧照射的情况下进行了比较研究,而为保护相关器官及解决由于旋转照射所带来的低剂量区域较高的问题,有学者报道了在旋转调强CSI计划设计方面的改进办法。Wang[14]等提出在全脑部位采用280°照射弧,在面部进行80°避让的方式以有效降低面部器官受照剂量,而对于脊髓部位则采用前后2个140°照射弧,避让左右两侧各40°射野以降低肺脏等器官的低剂量区域。但在应用Eclipse计划系统射野避让模块时,计划优化的次数会受到系统的限制,因此在射野角度减少的情况下对于计划设计者提出了更高的要求。文婷等[18]在HT全中枢计划设计中,通过勾画辅助轮廓进行射野限制的方式有效降低了各OAR的平均剂量,同时治疗时间增加了1.23倍。但是辅助区域的勾画范围和大小尚无统一共识。而对于女性患者卵巢保护的问题,本研究中未加以考虑,解传滨等[5]通过螺旋断层调强放射治疗技术和断层径照调强放射治疗技术接野分段式计划设计,实现了对女性卵巢的保护,而RA治疗技术在女性患者卵巢保护中的可行性还需进一步的临床研究论证。
对于全脑全脊髓照射,两种旋转调强技术均能得到较好的靶区剂量分布,在重要器官的保护上,HT因束流调制能力较强而存在较为明显的优势,而RA治疗射线利用率更高。
