肺内多发结节的CT表现分析
2018-07-03过丽芳张建梅王仁贵赵桐温廷国张春燕关晓姣傅岩王燕文杨永革
过丽芳 张建梅 王仁贵 赵桐 温廷国 张春燕 关晓姣 傅岩 王燕文 杨永革
肺内多发性结节是临床常见的一种影像学表现形式,可出现于多种疾病,但最常见于肺结核及肺转移瘤两种疾病,而部分慢性炎症和少见的淋巴管瘤等累及肺部时也可表现为多发肺结节。这些疾病影像学表现非常近似,鉴别诊断存在一定的困难。笔者收集2011年3月至2017年8月于首都医科大学附属北京世纪坛医院进行治疗的以肺内多发结节病变为主要征象的53例确诊患者,对其CT表现特点进行分析。
资料和方法
一、 患者资料
一般资料:收集2011年3月至2017年8月我院收治的经临床、实验室、穿刺或手术病理证实的,以肺内多发结节病变为主要征象的患者53例。其中,肺结核19例、肺转移瘤23例、肺慢性炎症5例、弥漫性淋巴管瘤6例。男28例(52.8%),女25例(47.2%),年龄5~76岁,平均(44.3±15.3)岁。本组23例肺转移瘤的原发肿瘤为腺癌20例(乳腺癌3例、胃癌1例、结肠癌5例、直肠癌10例、肺癌1例),宫颈鳞癌1例,右颌下腺腺样囊腺癌1例,右膝滑膜肉瘤1例。临床表现为咳嗽、咳痰、胸闷、胸痛、气促、咯血等;23例肺转移瘤患者中10例无明显呼吸道症状。6例弥漫性淋巴管瘤患者中,肺外表现包括全身多发囊性病变1例、右腋下肿物1例、双侧阴囊肿胀1例、下肢淋巴水肿3例。
本组患者确诊依据:(1)肺结核患者全部符合肺结核的诊断标准[1]。 (2)肺转移瘤患者全部符合肺转移瘤的诊断标准[2]。(3)肺慢性炎症:均经抗感染治疗患者肺部病灶逐渐吸收消失。(4)弥漫性淋巴管瘤:2例经病理学诊断;4例因受取材方法、部位和组织标本量等因素的影响,最后依赖临床、病理和影像学综合判断确诊。
二、CT检查和研究方法
1.CT检查方法:采用德国西门子Simatom Plus 16排螺旋CT和荷兰Philips Brilliance iCT仪(256排螺旋CT)扫描系统。管电压120 kV,管电流120~150 mA;层厚5 mm,层间距5 mm,螺距0.9;图像重建层厚为0.9 mm,视野(FOV)为250 mm×250 mm。6例弥漫性淋巴管瘤患者,均经足背部皮下表浅淋巴管注入超液态碘油5~20 ml(480 mg I/ml,GUERBET)行直接淋巴管造影检查,根据对比剂到达胸导管入口的时间(约10~300 min)再行胸腹部MSCT扫描。5例行CT增强扫描,采用碘普罗胺 (370 mg I/ml;拜耳医药广州分公司)和碘佛醇(320 mg I/ml;江苏恒瑞医药) 20~80 ml,以1.5~5.0 ml/s的流率用高压注射器经肘静脉或锁骨下静脉置管注射。
2. 研究方法及纳入标准:将肺结核组、肺转移瘤组、肺慢性炎症组、弥漫性淋巴管瘤组分为4组,观察结节大小、分布、边缘、密度、病灶邻近胸膜增厚情况、是否伴有纵隔或肺门淋巴结肿大。4组患者的肺内结节均多于3个以上,直径3~30 mm。肺慢性炎症组患者共87个结节;肺结核组患者共156个结节;肺转移瘤组患者共615个结节;肺弥漫性淋巴管瘤组患者共115个结节。
三、统计学处理

结 果
一、肺内结节大小和分布情况
肺结核与肺慢性炎症呈小叶中心分布,肺转移瘤呈随机分布,弥漫性淋巴管瘤肺结节沿淋巴管周围分布。肺内结节大小情况:肺结核结节最大径范围为3~24 mm,其中13例(68.4%,13/19)达10~20 mm;肺转移瘤结节最大径范围为3~24 mm,其中18例(78.3%,18/23)达10~20 mm;肺慢性炎症结节最大径范围为3~30 mm,其中3例(3/5)为3~8 mm;弥漫性淋巴管瘤结节最大径范围为4~12 mm,3例(3/6)为3~8 mm。
二、肺内结节CT表现
1. 肺结核、肺转移瘤及肺慢性炎症的CT征象(表1):5例肺慢性炎症患者的肺内结节(共87个),69个(79.3%;69/87)呈类圆形;18个(20.7%;18/87)结节病灶边缘欠光滑,并呈局限片状浸润影及索条状影(图1~4);其中1例(临床怀疑为肺癌)行胸部CT增强检查,肺内结节呈均匀的明显强化,平扫CT值范围约18~25 HU,增强后CT值升高>25 HU(与平扫相比)。肺结核结节(共156个)均呈类圆形;128个结节边缘光滑(82.1%,128/156);28个结节边缘见分叶毛刺(17.9%,28/156),其中25个结节分叶浅而模糊、无明显切迹(89.3%;25/28),3个(10.7%;3/28)结节分叶较深,并可见稀疏的、边缘扭曲的长毛刺或棘样突起。19例肺结核中5例(26.3%;5/19)伴有溶解空洞(共43个;27.5%;43/156),肺结核空洞壁厚、内壁较光滑,其中4例空洞结核病灶周围可见卫星灶,3例可见偏向肺门侧有引流支气管,引流支气管壁呈均匀增厚。19例肺结核中的4例患者,临床怀疑为恶性病变而行胸部CT增强扫描,增强后肺内结节呈环形强化或包膜样强化,其内干酪样坏死成分无强化(图5~9)。肺转移瘤(23例)615个结节均呈类圆形,369个结节(60.0%,369/615)观察到分叶边缘锐利的细短毛刺;本组20例腺癌及1例(91.3%,21/23)鳞癌肺转移瘤病灶均出现空洞(共111个),空洞表现为4种形态:囊样空洞(壁薄而均匀,壁厚约1~2 mm)29个(26.2%,29/111)、小环形空洞(壁较均匀,壁厚约2~4 mm)25个(22.5%,25/111)、空泡样空洞38个(34.2%,38/111)、不规则空洞(壁厚>4 mm,内壁不光整,伴壁结节)19个(17.1%,19/111);以空泡样空洞最多见,且30个(78.9%,30/38)空泡样结节边缘见分叶、毛刺,且均出现在腺癌肺转移患者中。2例直肠癌肺转移同时具有以上4种空洞形态,全部出现空洞结节患者的空洞病灶均是与肺内多发实性瘤灶共存(图10~13)。肺慢性炎症、肺结核及肺转移瘤伴有纵隔或肺门淋巴结肿大例数分别为:0例、6例(31.6%,6/19)、8例(34.8%,8/23)。

表1 肺结核、肺转移瘤与肺慢性炎症多发结节的CT扫描征象比较
注括号外数值为“结节个数”,括号内数值为“发生率(%)”
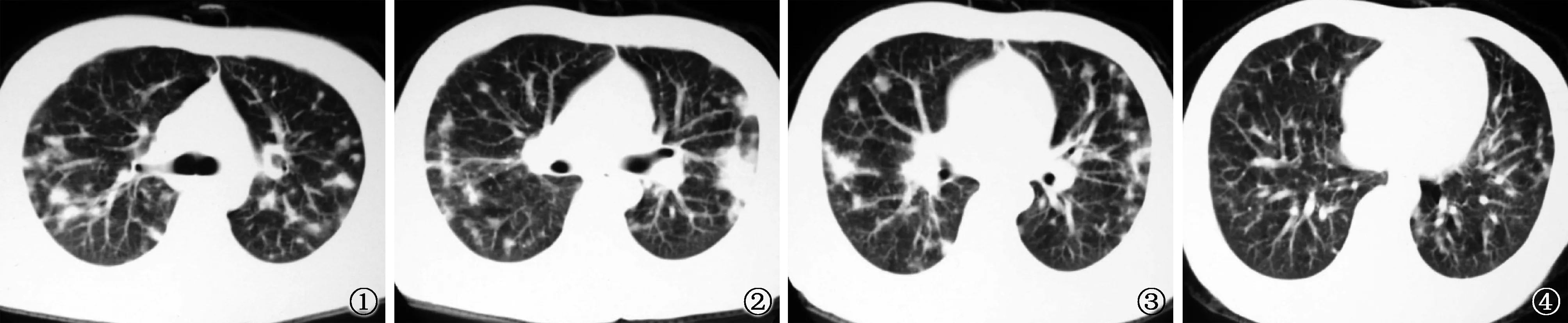
图1~4 男,21岁,肺慢性炎症。图1及图2显示双肺上叶及双肺下叶背段肺内及胸膜下多发结节;图3显示右肺中叶、左肺上叶舌段及双肺下叶背段肺内及胸膜下多发结节;图4显示右肺中叶内侧段、左肺上叶舌段及双肺下叶基底段散在结节。图1~4所示结节特点为:分布上以双肺上叶为主,双肺下叶相对较少,结节大小不等,相对较大病灶边缘模糊;图2显示左肺舌段及图3显示右肺中叶外侧段结节病灶边缘欠光滑,并呈局限片状浸润影及索条状影
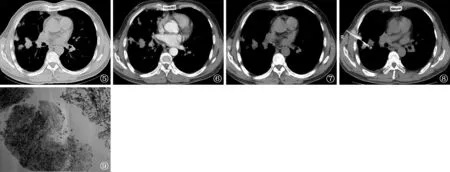
图5~9男,47岁,肺结核。图5 为CT扫描肺窗,显示右肺内及胸膜下多发结节,较大结节边缘不规则,见条索状影与邻近病变相连。图6,7分别为CT增强扫描动脉期、静脉期纵隔窗,病灶内多发灶性干酪坏死区呈低密度并边缘明显强化。图8为对右肺中叶最大结节穿刺示意图。图9为穿刺获取标本的病理图,诊断为增殖性结核(HE ×10)
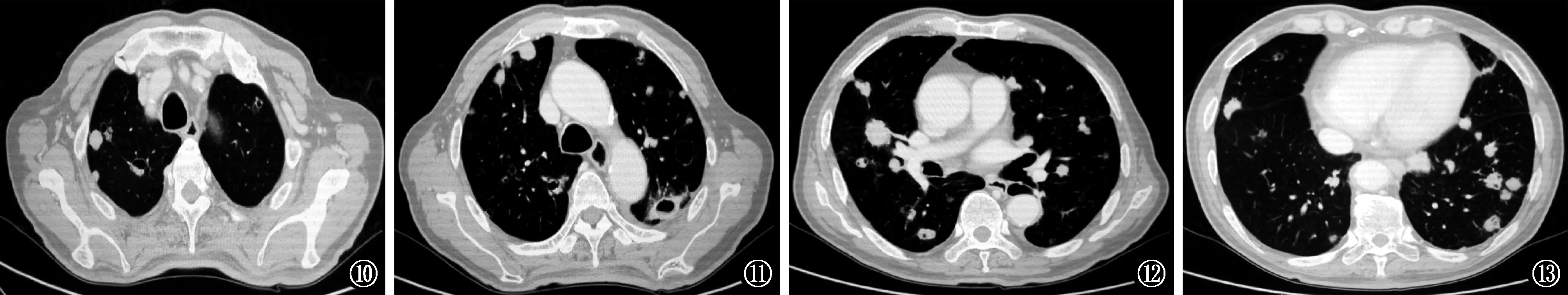
图10~13 男,76岁,直肠癌双肺转移瘤。可见双肺多发随机分布的实性结节及空洞结节。图10见不规则空洞及小环形空洞;图11见囊样空洞、空泡样空洞、小环形空洞及不规则空洞;图12,13见空泡样空洞。部分小实性结节边缘光滑、余实性结节及空洞结节边缘见分叶、短毛刺或棘状突起

图14~17 女,25岁,弥漫性淋巴管瘤。图14,15 为胸部CT扫描,显示双肺小叶中心及胸膜下多发结节影,直径≤5 mm,边缘光滑,未见分叶及毛刺,部分与血管关系密切。图16 为腹部CT扫描,显示脾脏体积增大,肝脏及脾脏见多发囊状低密度结节,边缘光滑。图17 为右肩关节脂肪抑制T2WI,显示肺内结节及右侧腋窝类圆形高信号,肝脏见多发结节状稍高及明显高信号影。肝脏及脾脏病灶术后标本病理检查诊断为淋巴管血管混合瘤
肺慢性炎症与肺转移瘤、肺结核与肺转移瘤出现结节边缘无分叶且边缘光滑的比率差异有统计学意义(χ2=47.613,P=0.000;χ2=88.095,P=0.000),肺慢性炎症与肺结核出现结节边缘无分叶且边缘光滑的比率差异无统计学意义(χ2=0.273,P=0.601),肺结核与肺转移瘤出现钙化的比率差异有统计学意义(χ2=270.707,P=0.000),肺结核与肺转移瘤出现空洞的比率差异有统计学意义(χ2=7.048,P=0.008),肺慢性炎症与肺转移瘤、肺结核与肺转移瘤出现病灶邻近胸膜增厚粘连的比率差异有统计学意义(χ2=23.670,P=0.000;χ2=49.650,P=0.000),而肺慢性炎症与肺结核出现病灶邻近胸膜增厚粘连的比率差异无统计学意义(χ2=0.387,P=0.534)。
2. 弥漫性淋巴管瘤的CT表现:6例患者肺内结节均表现为边缘光滑,密度较低且均匀,纵隔窗未见显示,故未与其他组进行比较。
6例弥漫性淋巴管瘤患者均累及2个以上脏器,肺内表现为多发结节。2例还表现为支气管血管束增粗、小叶间隔增厚;2例同时表现为肺不张;4例出现单(双)侧中至大量胸腔积液;2例可见心包积液。肺外表现:2例四肢、躯干皮下软组织增厚,呈“网格状”改变,边界清晰;2例右腋窝皮下软组织、1例双侧阴囊、2例肝脏、3例脾脏(其中1例手术标本病理诊断为肝脏及脾脏淋巴管血管混合瘤,见图14~17)内多发、边界清楚的薄壁囊性病灶,单房或多房,囊壁或分隔薄且光滑;3例骨骼内多发、囊状骨质缺损,边缘不规则或伴有硬化缘。直接淋巴管造影显示胸导管梗阻2例,胸导管梗阻及右颈干反流1例,胸导管梗阻及支气管纵隔干反流1例,支气管纵隔干反流1例,左侧腰、髂淋巴管反流1例。
讨 论
肺结节(pulmonary nodules)通常是指直径不超过3 cm的肺内类圆形病灶[3]。多发性肺内结节常见于肺部感染、肺部肿瘤和少数肺部先天性异常等患者。CT检查是肺内多发性结节诊断与鉴别的重要方法[4]。
一、肺内多发结节的分布特点
肺内多发性结节应按照“小叶中心性结节、随机结节和淋巴管周围结节”的分类[5]进行分析:(1)小叶中心分布。主要特点是在不与胸膜及小叶间隔相连的前提下,分布于小叶中心位置。多见于肺结核及肺部炎症等。病理检查肺慢性炎症结节因存在渗出或增殖纤维化等炎性改变,其结节分布通常缺乏典型的小叶中心性结节特点,本组5例肺慢性炎症均见边缘模糊的结节,边缘见局限的片状浸润影及索条状影,与肺转移瘤和原发肿瘤均明显不同。肺结核的结节与肺慢性炎症结节有差异,肺结核结节边缘或光滑或轻度不规则,部分伴有局限的溶解空洞,或者与卫星病灶并存,有学者认为卫星病灶是诊断肺结核的重要依据之一[6]。(2)随机性分布。其随机分布于小叶间隔、小叶中心、胸膜下等位置,多见于肺转移瘤。本组肺转移瘤均有原发性肿瘤史,结节多发,大小不等,以中下肺野多见。(3)淋巴管内及其周围分布:结节主要分布于淋巴管内及其周围。淋巴管位于支气管血管束、小叶间隔及胸膜下[7]。弥漫性淋巴管瘤为淋巴组织发育障碍、淋巴管增殖扩张类疾病,肺内表现为位于沿淋巴管内及其周围分布的结节,结节可位于小叶中心、小叶间隔和胸膜下,呈多发性结节,且胸膜下分布较为多见。
二、肺内多发结节的病理与CT表现特点分析
本组肺结核、肺转移瘤及肺慢性炎症患者均可见结节边缘分叶、毛刺征象,且60.0%(369/615)的肺转移瘤结节有边缘分叶、毛刺征象。肺部良恶性病变的鉴别诊断有一定困难,但仔细观察,肺结核及肺慢性炎症的良性结节与肺转移瘤的分叶及毛刺有所不同:结核及炎症结节的分叶多为浅而模糊,无明显切迹,边缘可见棘样突起或稀疏长毛刺,且棘样突起的特点是数量较少、基底较宽,为纤维组织增生所致;而转移瘤之类的肺恶性病变大多为多弧度深分叶的脐切迹征象,毛刺细短、锐利。另外,发生在肺近胸膜处的结核球及肺慢性炎症产生的炎性结节,由于慢性炎症刺激,常引起病灶相邻部位的脏、壁层胸膜增厚粘连,而肺转移瘤就是邻近胸膜的病灶也很少出现明显的胸膜增厚粘连。本组肺结核、肺转移瘤及肺慢性炎症邻近胸膜出现增厚粘连改变的发生率分别为45.5%、18.5%、41.4%,肺慢性炎症与肺转移瘤、肺结核与肺转移瘤两组间比较差异有统计学意义, 而肺慢性炎症与肺结核两组间比较差异无统计学意义。
空洞不仅见于结核球,也可出现于部分转移瘤。有文献报道,空洞性肺转移瘤的发生率约占4%~9%[8],其成因尚不完全明确,可能与鳞癌中心角化物排空、腺癌黏液样变后黏液排空、肿瘤血供不足引起坏死、肿瘤继发脓肿、化疗等因素有关。原发肿瘤主要为鳞状细胞癌及腺癌,其中鳞状细胞癌以男性头颈部与女性生殖器肿瘤多见,腺癌主要来自结肠及乳腺癌。本研究21例肺转移瘤出现空洞结节(91.3%,21/23),发生率远高于文献报道的8.3%[3],可能与本研究收集患者的原发肿瘤病理组织学类型有关(20例为腺癌、1例为鳞癌)。于小平等[2]发现,囊样空洞仅见于鳞癌,不见于腺癌,而且在鳞癌中所占比例最高,说明囊样空洞是鳞癌区别于腺癌的独特类型。吴斌和戴元荣[9]发现,腺癌肺转移也可出现囊样空洞,与前者研究结果不符。因此,囊样空洞并不是鳞癌区别于腺癌的独特方式。本组空泡样空洞(34.2%)>囊样空洞(26.2%)>小环形空洞(22.5%)>不规则空洞(17.1%),腺癌肺转移亦出现多发囊样空洞,但以空泡样空洞最多见。空泡样空洞在病理上往往为未被肿瘤侵犯的肺组织、小叶支气管或细支气管的断面及乳头状突起之间的气腔,多见于腺癌。本组30个(78.9%)空泡样空洞均有分叶、毛刺,且均出现在腺癌肺转移的患者中,进一步证实转移瘤的组织学结构、生长方式往往和原发肿瘤相似。结核空洞与肺转移瘤不同,CT扫描多表现为结核结节内的裂隙状、新月形及类圆形空洞,边缘部分清楚或部分模糊;洞壁厚薄不一,空洞内壁多规则光整(92.7%),多数病变无内壁结节及分隔,洞壁多无强化,仅少数洞壁有轻度强化[10];此外,其他肺野内小叶中心性结节及树芽征改变,有助于肺结核的诊断。不同性质病变CT增强扫描的表现有所差别:康本武和冉隆中[11]发现,恶性结节呈速升缓降型,肺感染的炎性结节呈逐渐上升、速降型,结核呈缓慢上升并为无明显峰值型。有学者研究发现,95%的肺结核CT增强扫描后CT值无增加,时间CT值曲线低平,其形态学特征50%为病灶无任何强化,44.5%为包膜细条样强化,仅极少数病灶表现为广泛强化和边缘强化[12]。而肺慢性炎症的结节CT增强扫描多表现为明显强化,呈均匀或不均匀强化。当肿瘤、肺结核与肺慢性炎症结节形态特征存在重叠难以鉴别时,结合CT增强扫描进行观察,将有助于诊断。
多数学者认为,淋巴管瘤是胚胎发育过程中淋巴组织发育障碍、淋巴管增殖扩张所致,多为先天性亦可继发于手术及外伤后,可发生于人体任何含有淋巴管道的部位,可侵犯骨骼、结缔组织和内脏器官等[13-15]。淋巴管瘤同时发生在2个不同脏器内,或同一脏器内至少有2个以上相对独立的淋巴管瘤则为弥漫性淋巴管瘤病(diffuse lymphangiomatosis,DLA),临床上尤为罕见,影像学表现复杂多样[16-17]。弥漫性淋巴管瘤常呈弥漫性或多灶性分布,常表现为累及多个部位、多发的大小不等的囊性病变,故与肺结核、肺转移瘤及肺慢性炎症较易鉴别。本研究中,弥漫性淋巴管瘤患者呈现的肺内结节与其他3种疾病不同,CT扫描均表现为边缘光滑、密度较低且均匀的结节,纵隔窗大部分无法显示,而其他3种疾病的结节形态及密度则具有多样性。
综上所述,CT扫描可以准确地显示肺结节的大小、形态、边缘、密度、强化方式及与邻近结构的关系;同时,密切结合临床病史及其他肺外CT扫描表现,对诊断和鉴别诊断至关重要。
[1] 中华医学会结核病学分会.肺结核诊断和诊疗指南.中国实用乡村医生杂志,2013,20(2):7-11.
[2] 于小平,王平,梁赵玉.空洞型肺转移瘤的CT表现及与原发灶病理类型的关系.临床放射学杂志,2003,22(3):199-202.
[3] 王华斌,李苏建,卢光明.多层螺旋CT评估孤立性肺结节的临床研究进展.放射学实践,2010,25(1):105-108.
[4] 张洁,于洪志,吴琦,等.活动性肺结核淋巴管周围受累的CT影像和临床特征分析.中华医学杂志,2016,96(3):167-171.
[5] 范红燕,侯艳军,赵彦民.肺内多发小结节的CT 诊断与鉴别诊断.放射学实践,2003,18(10):718-720.
[6] 陈亮,钟球,刘文,等. 肺结核球误诊为周围型肺癌及两者的CT表现分析. 中国防痨杂志,2015,37(2):178-182.
[7] 王建国,郭佑民,杨广夫. 肺小叶中心分布结节影的CT与HRCT鉴别诊断.实用放射学杂志,2001,17(9):707-709.
[8] 杨欣,杨州,李唯.肺部多发空洞性病变的CT诊断.实用医学影像杂志,2011,12(3):152-155.
[9] 吴斌,戴元荣.空洞型肺转移瘤CT表现的临床分析.实用医学杂志,2007,23(23):3722-3723.
[10] 李成海,赵泽钢,周新华.肺内多发空洞病变的CT影像分析.中国防痨杂志,2016,38(5):369-374
[11] 康本武,冉隆中.螺旋CT动态增强扫描对良、恶性肺结节的鉴别.吉林医学,2009,30(10):922.
[12] 周新华.肺结核的影像学诊断.中国防痨杂志,2014,36(8):638-642.
[13] Shaffer K,RosadodeChristenson ML,Patz EF Jr,et al.Thoracic lymphangioma in adults:CT and MR imaging features.Am J Roentgenol,1994,162(2):283-289.
[14] Dubois J,Garel L,Abela A,et al.Lymphangiomas in children:percutaneous sclerotherapy with an alcoholic solution of zein.Radiology,1997,204(3):651-654.
[15] Wadsworth DT,Newman B,Abramson SJ,et al.Splenic lymphangiomatosis in children.Radiology,1997,202(1):173-176.
[16] 孙小丽,沈文彬,王仁贵,等. 弥漫性淋巴管瘤病的多层螺旋CT淋巴管成像表现.中华放射学杂志,2014,48(7):582-585.
[17] 王仁贵,陈孝柏,段永利,等.MSCT直接淋巴管造影在弥漫性肺淋巴管瘤病中的诊断价值.中国医学影像技术,2012,28(2):185-189.
