OAM联合自体骨移植治疗牙周骨下袋缺损临床研究
2018-06-22杨晓生
杨晓生
(河南省洛阳市疾病预防控制中心口腔科 洛阳 471023)
牙周组织长期处于慢性炎症状态会形成牙周袋,引起牙槽骨吸收,晚期可导致牙周骨下袋形成,严重影响口腔咀嚼功能,损害患者健康。临床治疗以修复牙周组织,促使已损牙周组织再生,形成新附着为主。牙周基础治疗可减轻患牙炎症反应,但无法修复骨缺损。近年来,自体骨移植在牙周病治疗中应用广泛,取得良好的治疗效果[1]。但自体骨获取量较少,难以满足治疗需要,需与其他材料联合使用。骨形成蛋白诱导活性材料(OAM)为重组合异种骨,具有骨传导及诱导功能,可促进牙周组织再生,诱导新骨形成[2]。本研究旨在观察骨形成蛋白诱导活性材料联合自体骨移植治疗牙周骨下袋缺损的临床效果。现报道如下:
1 资料与方法
1.1 一般资料 选取2016年2月~2017年2月洛阳市疾病预防控制中心门诊收治的牙周骨下袋缺损患者64例为研究对象,按照手术方法分为对照组和观察组各32例。对照组男17例,女15例;年龄32~64岁,平均年龄(47.72±5.38)岁。观察组男 18例,女14例;年龄33~63岁,平均年龄(48.21±5.69)岁。两组患者性别、年龄等一般资料比较,差异无统计学意义,P>0.05,具有可比性。本研究经洛阳市疾病预防控制中心医学伦理委员会审批通过。
1.2 纳入及排除标准 (1)纳入标准:单牙发病;口腔卫生良好;符合牙周骨下袋缺损相关诊断标准;患者及其家属均知晓本研究,并自愿签署知情同意书。(2)排除标准:合并传染性疾病;合并心脑血管疾病;牙周手术禁忌证;合并精神异常疾病;治疗依从性差。
1.3 治疗方法 术前两组均行全口洁治、根面平整、口腔卫生指导等牙周基础治疗,采用Williams探针反复检查牙菌斑控制情况,根面平整术后4~5周复查并记录牙周探诊深度(PDD)、龈沟出血指数(SBI),用根尖片检查牙周骨缺损情况;两组均行牙周翻瓣术,患牙做龈缘内斜切口,最大程度保留牙龈。在此基础上,观察组行骨形成蛋白诱导活性材料与自体骨移植联合引导组织再生术治疗,牙周骨缺损部位植入蛋白诱导活性材料与自体骨的混合物,比例为1∶1,修整胶原膜,完全覆盖牙周骨缺损部位,冠方邻近釉牙骨质界,根方延展至骨边缘下约2 mm,可吸收线悬吊固定膜。对照组行自体骨移植联合引导组织再生术治疗,牙周骨缺损部位植入自体骨,其他手术操作与观察组相同。术后两组均用复方氯己定含漱液(国药准字H20058018)漱口,3次/d;口服阿莫西林(国药准字 H44021006)0.5 g/次,2次/d。术后8 d拆线,3、6个月复查PPD、SBI。
1.4 观察指标 (1)比较两组术前、术后3个月、6个月PPD、SBI水平。(2)采用简明健康状况调查量表(SF-36)评估术前、术后6个月两组生活质量,包括生理功能、精神状态、躯体疼痛等方面,总分100分,评分越高,生活质量越好。
1.5 统计学方法 采用SPSS22.0统计学软件对数据进行分析,计量资料用(x±s)表示,进行t检验,计数资料用百分数表示,进行χ2检验,P<0.05为差异具有统计学意义。
2 结果
2.1 两组PPD比较 术前两组PPD比较,差异无统计学意义,P>0.05;术后3、6个月观察组PPD水平低于对照组,P<0.05。见表1。
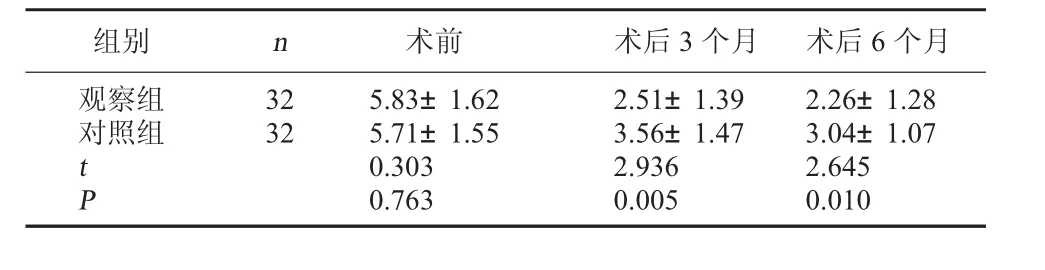
表1 两组PPD比较(mm,x±s)
2.2 两组SBI比较 两组术前SBI比较无明显差异,P>0.05;术后3、6个月,两组SBI均明显降低,术后组内比较有明显差异,P<0.05,但组间术后比较无明显差异,P>0.05。见表2。
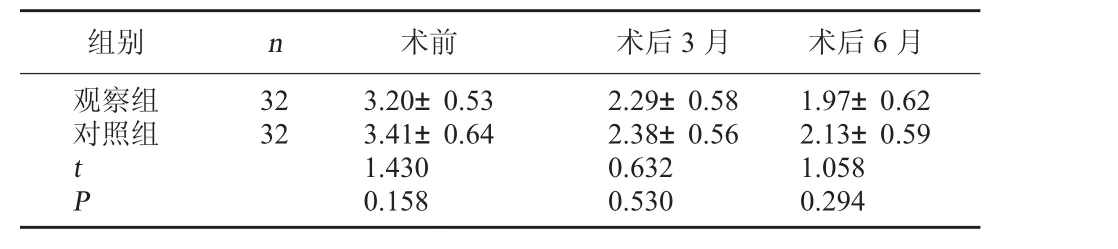
表2 两组SBI比较(分,x±s)
2.3 两组SF-36评分比较 术前两组SF-36评分比较无明显差异,P>0.05;术后6个月,观察组生理功能、精神状态、躯体疼痛等方面评分均明显高于对照组,P<0.05。见表3。
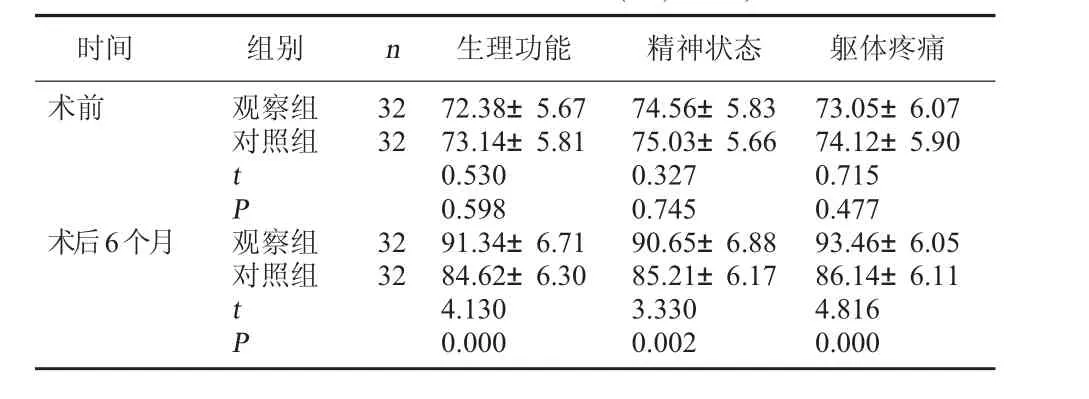
表3 两组SF-36评分比较(分,x±s)
3 讨论
牙周基础治疗虽可消除炎症,但无法满足患者修复牙周骨下袋的需要。临床常采用植骨术及引导组织再生术治疗。引导组织再生术采用生物膜封闭牙周骨缺损部位,诱导牙周骨下袋恢复,但生物膜仅具有屏障作用,活性细胞不足,无法主动诱导牙周组织再生,牙周组织难以完全恢复[3~4]。采用合适材料修复牙周组织缺损,恢复牙周骨形态,对促进牙骨质、牙槽骨等功能的再生具有重要作用。
自体骨为治疗牙周骨下袋缺损常用材料,术中从邻牙或不规则骨吸收区获得,可提供结构性支持,发挥骨传导、骨诱导、骨生成功能,但临床难以获得足够的自体骨,需与人工材料混合使用。夏金圣[5]报道显示,采用骨诱导活性材料修复牙槽突裂骨缺损,其修复效果接近于自体骨移植,安全可靠。骨形成蛋白诱导活性材料由重组人骨形成蛋白-2与去抗原载体组成,骨形成蛋白可诱导骨形成,并能复合不同性质载体,组成骨修复材料,还能促进牙周膜细胞分化,刺激骨钙素合成、矿化结节形成。骨形成蛋白-2虽能促使牙槽骨再生,但半衰期短、用量大,费用较高,而复合其他载体材料可减缓骨形成蛋白降解,延长诱导时间,与自体骨混合,存在较多的靶细胞及自体血,加之良好的缓释载体,可满足诱导成骨的必备条件,而去抗原载体具有三维多孔型空间结构,符合骨缺损区需要,有利于新生血管及骨组织长入[6]。本研究结果显示,术后两组SBI均明显降低,但组间无明显差异,P>0.05。表明骨诱导活性材料与自体骨对SBI的影响具有一致性。此外,术后3、6个月,观察组PPD低于对照组,生活质量高于对照组,P<0.05,说明该手术方法可有效促进牙周组织修复,改善患者生活质量。与黄飞等[7]报道基本一致。综上所述,骨形成蛋白诱导活性材料与自体骨移植联合引导组织再生术治疗牙周骨下袋缺损,可促进牙周组织修复,显著改善患者生活质量,具有一定的临床价值。
[1]王兴,刘洪臣.自体骨移植修复种植位点骨缺损的研究进展[J].口腔颌面修复学杂志,2016,17(1):49-52
[2]梅幼敏,宦泓,吴煜卓,等.骨形成蛋白诱导活性材料联合引导组织再生术治疗牙周骨下袋的临床研究[J].口腔医学,2013,33(9):601-603
[3]张海鹰.牙周基础治疗对侵袭性牙周炎患者的影响分析[J].世界最新医学信息文摘,2017,17(25):101,103
[4]罗正文,刘济远,李佳,等.引导组织再生生物膜应用于拔牙术后牙槽骨缺损修复的临床研究[J].口腔医学研究,2017,33(7):782-786
[5]夏金圣.骨诱导活性材料修复牙槽突裂骨缺损的可行与可靠性[J].中国组织工程研究,2015,19(47):7619-7623
[6]杨玉鹏,赵海静,谷建琦,等.钛芯与骨形成蛋白复合材料修复即刻种植牙槽骨缺陷的评价[J].中国组织工程研究,2017,21(22):3536-3540
[7]黄飞,丁洁,刘世森,等.骨形成蛋白诱导活性材料联合自体骨移植治疗牙周骨下袋缺损的临床疗效研究[J].新疆医科大学学报,2017,40(4):452-454
