曲妥珠单抗合长春瑞滨治疗Her-2阳性晚期乳腺癌临床研究
2018-06-22周丽华
周丽华
(河南省安阳市肿瘤医院药剂科 安阳 455001)
目前我国乳腺癌发病率已高居女性恶性肿瘤首位,2012年统计数据显示,我国乳腺癌发病率约为42.55/10万,严重威胁着女性生命安全[1]。近年来随着分子生物学技术和综合诊疗规范化水平的增加,乳腺癌患者的生存率有了明显提升,但晚期乳腺癌患者5年生存率仍然较低,且20%~30%的乳腺癌患者存在Her-2高表达[2]。Her-2是一种原癌基因,每个人体内的细胞膜表面均有少量Her-2蛋白,在细胞生长因子信号传递途径中发挥着重要作用。当癌细胞内的Her-2基因高度表达时,细胞膜上会产生过多的Her-2蛋白,刺激癌细胞的疯狂增长,增强其侵袭转移能力。因此Her-2阳性乳腺癌患者的病情较为凶险,极易出现复发转移[3]。化疗联合靶向治疗是目前晚期乳腺癌常用治疗手段,但具体应用方案尚未统一定论。本研究旨在探讨Her-2阳性晚期乳腺癌患者采用曲妥珠单抗联合长春瑞滨的治疗效果及对其生存率的影响。现报告如下:
1 资料与方法
1.1 一般资料 选取我院2010年10月~2012年6月收治的Her-2阳性晚期乳腺癌患者82例,按随机数字表法分为对照组和观察组各41例。对照组年龄 31~66 岁,平均年龄(50.73±10.56)岁;雌激素受体(ER)阳性23例,孕激素受体(PR)阳性18例;术后复发转移38例,首诊转移3例;均发生腋下淋巴结转移,1个部位转移者30例,多个部位转移者11例。观察组年龄32~68岁,平均年龄(51.12±11.06)岁;ER阳性24例,PR阳性17例;术后复发转移39例,首诊转移2例;均发生腋下淋巴结转移,1个部位转移者32例,多个部位转移者9例。两组一般资料比较差异无统计学意义,P>0.05,具有可比性。本研究经我院伦理委员会审批通过。
1.2 纳入及排除标准 (1)纳入标准:经术中病理组织或活检穿刺确诊;经荧光原位杂交技术(FISH)检测,Her-2呈阳性表达;自愿签署知情同意书。(2)排除标准:肝肾功能障碍者;骨髓抑制者;伴有内分泌系统疾病者;合并凝血功能障碍或存在血液系统疾病者;甲状腺功能障碍者。
1.3 方法 对照组采用曲妥珠单抗(批准文号J20110020)+卡培他滨(国药准字H20133364)治疗:疗程第1天静脉滴注曲妥珠单抗6 mg/kg(首次剂量为8 mg/kg),第1~14天口服卡培他滨2 000 mg/m2,1次/d。观察组采用曲妥珠单抗+长春瑞滨(国药准字H20067722)治疗:疗程第1天静脉滴注曲妥珠单抗6 mg/kg(首次剂量为8 mg/kg),疗程第1天和第8天静脉滴注长春瑞滨25 mg/m2。两组均21 d为1个疗程,持续用药4~6个疗程。
1.4 观察指标 (1)比较两组临床疗效。(2)统计两组不良反应发生情况。(3)随访5年,比较两组1年、2年、3年、4年、5年生存率。
1.5 疗效评价标准[4]根据RECIST1.0实体瘤疗效评价标准进行判定,完全缓解:靶病灶全部消失,无新病灶出现,肿瘤标志物正常,持续≥4周;部分缓解:靶病灶最大径之和较前缩小≥30%,持续≥4周;疾病稳定:靶病灶最大径之和缩小未达30%,或增大未达20%;疾病进展:靶病灶最大径之和较前增加≥20%,或出现新病灶。疾病控制率=(完全缓解+部分缓解+疾病稳定)/总例数×100%。
1.6 统计学分析 数据处理采用SPSS20.0统计学软件,计量资料以(x±s)表示,采用t检验,计数资料用率表示,采用χ2检验,P<0.05为差异具有统计学意义。
2 结果
2.1 两组临床疗效比较 观察组疾病控制率显著高于对照组,P<0.05,差异具有统计学意义。见表1。
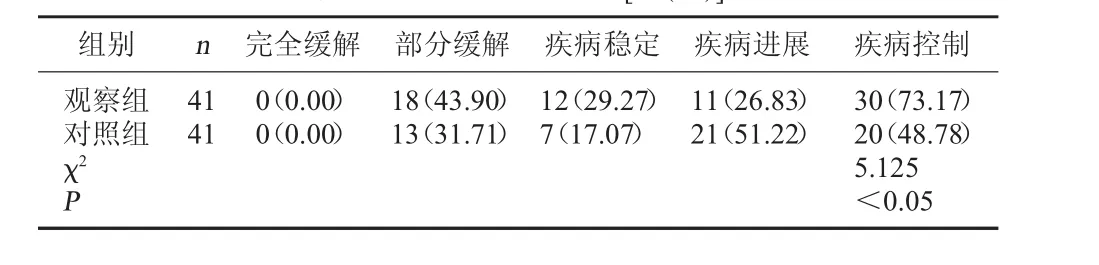
表1 两组临床疗效比较[例(%)]
2.2 两组不良反应发生情况比较 两组手足综合征、末梢神经炎、胆红素升高、转氨酶升高、中性粒细胞减少、白细胞降低以及消化道症状等不良反应发生率比较,差异均无统计学意义,P>0.05。见表2。
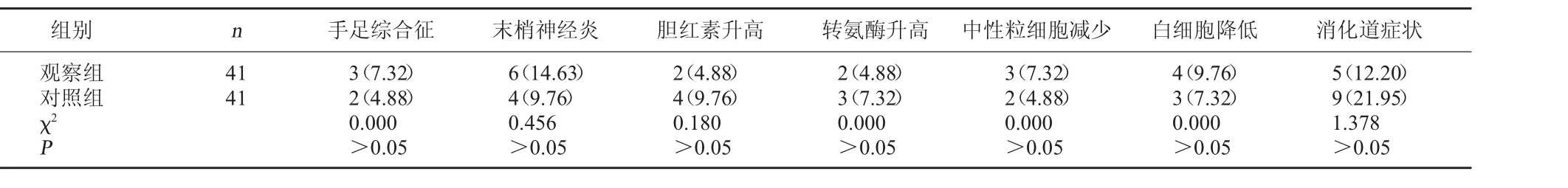
表2 两组不良反应发生情况比较[例(%)]
2.3 两组生存情况比较 两组1、2、3、4、5年生存率比较差异均无统计学意义,P>0.05。见表3。
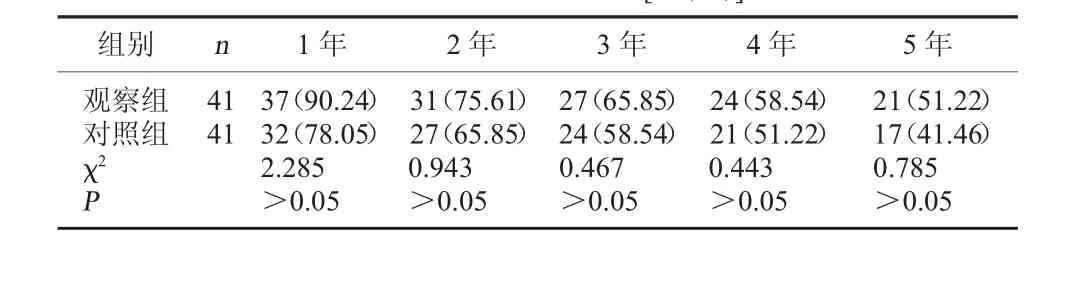
表3 两组生存情况比较[例(%)]
3 讨论
近年来,乳腺癌发病率及病死率呈持续上升趋势,但随着医疗技术的不断进步,以化疗为主的综合疗法成为乳腺癌治疗的重要手段,患者生存期不断延长。乳腺并不是维持人体生命活动的重要器官,原位乳腺癌并不致命,但由于乳腺癌细胞丧失了正常细胞的特性,细胞之间连接松散,极易脱落。癌细胞一旦脱落,游离的癌细胞可随血液或淋巴液散播至全身,尤其是乳腺癌Her-2阳性患者,肿瘤发生侵袭、转移的风险更高[5~6]。
曲妥珠单抗是抗Her-2单克隆抗体,主要由中国仓鼠卵巢CHO细胞经过一系列的纯化及病毒灭活后得到,其主要通过附着于Her-2上来阻止人体表皮生长因子在Her-2上的附着,从而阻断癌细胞的生长,且能够刺激自身免疫细胞对抗癌细胞。Her-2阳性乳腺癌患者可从曲妥珠单抗药物治疗中受益。研究指出[7],单用曲妥珠单抗治疗Her-2阳性晚期乳腺癌客观缓解率可达33.3%,与化疗药物长春瑞滨联用可进一步提高疾病控制率,延长患者生存周期。长春瑞滨属长春碱半合成衍生物,可抑制着丝点微管蛋白的聚合,阻滞癌细胞有丝分裂,使细胞分裂停留于有丝分裂的中期,从而起到抗肿瘤作用。卡培他滨是一种新型化疗药物,经肠黏膜迅速吸收后,可在肝脏经胸苷磷酸化酶转化为5-FU的抗代谢氟嘧啶脱氧核苷氨基甲酸酯类药物,干扰癌细胞中RNA及蛋白质合成,抑制其分裂增殖,是晚期原发性乳腺癌或转移性乳腺癌、结肠癌、直肠癌、胃癌的常用化疗药物。
本研究结果显示,观察组疾病控制率高于对照组(P<0.05);两组手足综合征、末梢神经炎、胆红素升高、转氨酶升高、中性粒细胞减少、白细胞降低以及消化道症状等不良反应发生率比较差异无统计学意义(P>0.05);两组 1、2、3、4、5 年生存率比较差异均无统计学意义(P>0.05)。说明曲妥珠单抗联合长春瑞滨治疗Her-2阳性晚期乳腺癌效果确切,可显著提高疾病控制率,且不增加不良反应发生率,安全性较高。综上所述,曲妥珠单抗联合长春瑞滨治疗Her-2阳性晚期乳腺癌效果确切,安全性高,但本研究纳入样本量较少,期望以后能有多中心、大样本量研究深入分析其具体作用机制。
[1]李康宪,谭方明,薛莲芳.曲妥珠单抗治疗HER-2阳性晚期乳腺癌临床有效率的Meta分析[J].临床和实验医学杂志,2016,15(9):868-870
[2]施胜钰,傅佩芬,陈建华,等.曲妥珠单抗联合长春瑞滨治疗人表皮生长因子受体2阳性晚乳腺癌疗效分析[J].中国医师进修杂志,2017,40(4):353-357
[3]王小松,谢宁,杨小红,等.联合或单独应用卡培他滨治疗晚期转移性乳腺癌的疗效及影响因素[J].中国老年学杂志,2014,34(22):6322-6324
[4]崔剑锋.曲妥珠单抗联合长春瑞滨治疗HER-2阳性晚期乳腺癌患者的疗效分析[J].实用药物与临床,2017,20(7):759-762
[5]黄玉琴.注射用曲妥珠单抗对人表皮生长因子受体2阳性晚期乳腺癌化疗患者血清肿瘤标志物及免疫功能的影响[J].中国综合临床,2017,33(8):748-752
[6]董超,杨润祥,任宏轩,等.赫赛汀联合NP(长春瑞滨+顺铂)方案治疗蒽环类耐药晚期乳腺癌的临床分析[J].现代肿瘤医学,2014,22(7):1564-1566
[7]郭继红,徐兵河,马飞,等.曲妥珠单抗联合不同化疗方案治疗人表皮生子因子受体2阳性晚期乳腺癌的疗效和安全性[J].中华肿瘤杂志,2014,36(5):372-376
