正交设计试验优选绿茶提取物脂质体的制备
2018-06-19张志勤韩国柱
张志勤 王 栋 韩国柱
(1 大连市皮肤病医院药剂科,辽宁 大连 116021;2 大连医科大学药理教研室,辽宁 大连 116044)
绿茶提取物主要成分为茶多酚,美国FDA已于2006年批准自绿茶中提取的茶多酚制成软膏用于临床治疗人类乳头瘤病毒所致尖锐湿疣,这是美国FDA第一个批准的现有的植物药制剂,在世界引起很大反响,因而绿茶提取物具有十分广泛的应用前景和研究价值[1-4]。
应用正交设计优选绿茶提取物纳米脂质体最佳处方和工艺,采用先进的仪器分析技术对其建立定性、定量方法,保证制剂质量可控,从而研发出绿茶提取物的新型给药系统—纳米脂质体,以期提高绿茶提取物疗效,降低其不良反应。
1 仪器与试药
绿茶提取物——大连市皮肤病医院制剂室提供;EGCG等对照品(纯度>98%)——上海友思生物技术有限公司;Utimate 3000高效液相色谱仪——美国戴安公司;TU-1901双光束紫外可见分光光度计——北京谱析通用仪器有限公司。
2 方法和结果
2.1 绿茶提取物的制备:取绿茶500 g,用无水乙醇1000 mL浸泡2 d不时搅拌,滤过,用旋转蒸发仪减压蒸发,而后将蒸发残留液置于圆底瓶皿中,在水浴锅上蒸发至干,放入90 ℃恒温干燥箱中干燥12 h,置研钵中研磨至细粉状,即得。
2.2 绿茶提取物纳米脂质体的制备:卵磷脂和胆固醇各100 mg,加入氯仿30 mL,在旋转蒸发仪上蒸发,瓶内壁形成一层均匀的膜脂,加入乙醚9 mL溶解后,加入含有绿茶提取物的磷酸盐缓冲液(pH 7.0)15 mL,然后在超声仪上进行超声直至形成稳定的水/油(W/O)型乳剂[5]。
2.3 绿茶提取物纳米脂质体包封率的测定:精密吸取1mL的绿茶提取物脂质体,离心30 min,取上清液,定容至50mL,离心后进液相,代入回归方程,得未包入脂质体中药物量(P游离)。精密吸取1mL的绿茶提取物脂质体于离心试管中,同法制得,得总药物量(P总)。包封率(%)=(P总-P游离)/P总×100。
2.4 正交设计优选绿茶提取物纳米脂质体处方:通过L9(34)正交设计优选绿茶提取物脂质体的最佳制备工艺,主要对四个关键性因素考察,实验结果见表1、表2。
由表2实验结果可知绿茶提取物脂质体处方优选的最佳方案是A1B1C2D2,即胆固醇:卵磷脂比例1∶1,绿茶提取物浓度10 mg/mL,磷酸盐缓冲液pH 7.0,超声时间20 min。
2.5 HPLC法测定绿茶提取物脂质体中活性成分的含量方法学的建立:建立一种反相高效液相色谱法以测定绿茶提取物脂质体中有效成分的含量。采用C18反相色谱柱,以乙腈-0.1%枸橼酸溶液(15∶85)为流动相,在紫外最大吸收波长处检测,峰面积内标法定量,见图1。
3 讨 论
3.1 研制绿茶提取物的一种新型给药系统绿茶提取物脂质体,通过正交设计优选比较不同因素对脂质体的影响,确定最佳制备工艺,脂质体作为皮肤局部给药的载体能够降低药物的不良反应,具靶向性和长效性,为临床治疗皮肤科疾病提供一种新的高效低毒的外用剂型纳米脂质体乳膏剂。
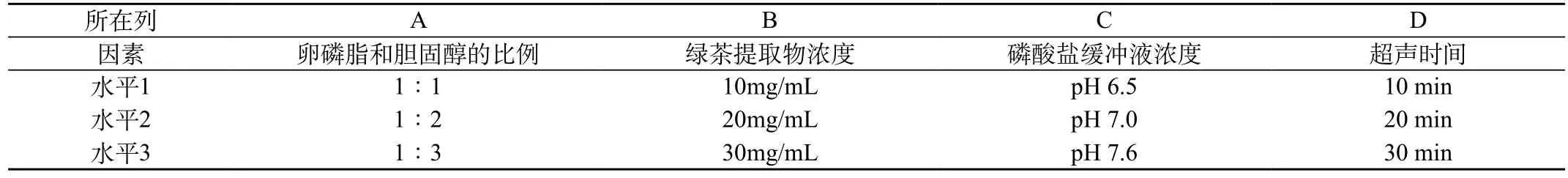
表1 绿茶提取物脂质体的因素水平

表2 绿茶提取物脂质体的实验计划表
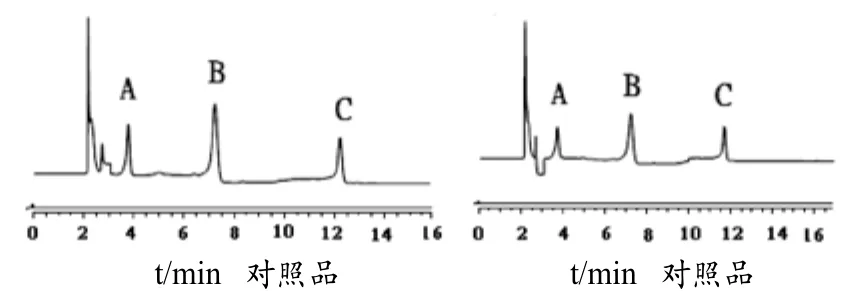
图1 A:EGC;B:EGCG;C:ECG
3.2 研究绿茶提取物纳米脂质体的HPLC全新含量测定方法在国内外文献中未见相关报道。首次运用HPLC法对绿茶提取物纳米脂质体中主要成分EGCG进行定性、定量。
[1] 朱盛山.药物新剂型[M].北京:化学工业出版社,2003:408-470.
[2] 姜华,高原,杨景明.中药脂质体的研究进展[J].当代医学,2009,15(28):12-13.
[3] 隋丽华,郭珉.茶多酚皮肤药理学的研究进展[J].医药导报,2003,22(11),795-797.
[4] 任文霞,李建科.逆向蒸发法制备茶多酚脂质体及质量评价[J].生物加工过程,2009,7(2):68-73.
[5] 旷英姿,马全红,郝小桢,等.茶多酚脂质体的制备研究[J].中国生化药物杂志,2006,17(1):28-31.
