替诺福韦治疗NAs经治耐药或应答不佳的慢性乙肝患者临床效果及安全性
2018-05-15李慧姣王慧雯杜漫刘宇郭莉黄艳芬陆惠洁江建宁
李慧姣,王慧雯,杜漫,刘宇,郭莉,黄艳芬,陆惠洁,江建宁
(1 广西医科大学第一附属医院,南宁530021;2 广西艾滋病防治研究重点实验室;3 柳州市人民医院;4 广西医科大学第二附属医院;5 北海市人民医院)
HBV感染呈世界性流行[1,2]。目前,临床上主要通过核苷(酸)类药物(NAs)抑制HBV复制来控制慢性乙肝进展,但部分患者长期接受NAs治疗会出现耐药或应答不佳,导致治疗失败[3,4]。对NAs经治耐药或应答不佳的慢性乙肝患者多采用NAs联合治疗,常用方案为恩替卡韦(ETV)联合阿德福韦(ADV),但NAs联合应用可导致肾功能损害、低磷性骨病等不良反应。替诺福韦(TDF)亦为NAs,具有高效抗HBV活性及高耐药基因屏障,是美国和欧洲抗HBV的一线用药[5~7];但国内上市较晚,关于其临床疗效和安全性的报道较少。为此,本研究观察了TDF治疗NAs经治耐药或应答不佳的慢性乙肝患者临床疗效及安全性。
1 资料与方法
1.1 临床资料 选择2013年3月~2017年7月广西医科大学第一附属医院收治的NAs经治耐药或应答不佳的慢性乙肝患者121例。所有患者符合《慢性乙型肝炎防治指南》(2010年版)[8]中的诊断标准。纳入标准:①既往服用NAs抗病毒治疗(包括ETV、ADV、拉米夫定、替比夫定单独或联合应用)后耐药或应答不佳者;②换用TDF或ETV+ADV联合治疗疗程24周以上者。排除标准:①合并甲肝、丙肝、丁肝等其他病毒性肝炎者;②乙肝病毒携带者或非活动性HBsAg携带者;③合并急性肝炎、代谢性肝病、自身免疫性肝炎、失代偿性肝硬化以及肝癌者;④艾滋病感染者;⑤伴有严重心肺疾病、肾功能不全等慢性疾病者。入院后根据治疗方案不同分为TDF组72例、ETV+ADV组49例。其中,TDF组男46例、女26例,年龄(38.10±9.18)岁,基线HBV DNA(4.72±1.89)copies/mL;ETV+ADV组男38例、女11例,年龄(38.24±8.96)岁,基线HBV DNA(4.63±1.67)copies/mL。两组性别、年龄、基线HBV DNA具有可比性。本研究经广西医科大学第一附属医院医学伦理委员会批准,患者均知情同意。
1.2 治疗方案 两组从换用TDF或ETV+ADV时为观察基线,TDF组口服TDF 300 mg/d,ETV+ADV组口服ETV 0.5 mg/d、ADV 10 mg/d,治疗24周以上。观察终点为治疗48周,不足48周者以末次观察时间为观察终点。
1.3 血清病毒学及生化指标检测 两组分别于治疗基线及治疗4、12、24、36、48周时采集外周静脉血,离心留取血清,保存备检。①血清HBV DNA含量及HBV DNA不可测率:采用荧光定量PCR法检测血清HBV DNA含量,检测下限为5.0×102copies/mL,低于检测下限为HBV DNA不可测,统计各时间HBV DNA不可测率。②HBeAg阴转率及血清学转换率:采用酶联免疫吸附试验检测血清HBeAg水平。血清HBeAg水平0~0.5 PEIU/mL为HBeAg阴性,≥0.5 PEIU/mL为HBeAg阳性。HBeAg阴转:既往HBeAg阳性患者HBeAg转为阴性。HBeAg血清学转换指既往HBeAg阳性、抗-HBe阴性患者HBeAg阴转并出现抗-HBe。统计各时间HBeAg阴转率及血清学转换率。③ALT复常率:采用速率法检测血清ALT水平。正常范围:男性9~60 U/L,女性7~45 U/L。ALT复常指既往ALT异常患者ALT恢复正常。统计各时间ALT复常率。④肾功能:采用日立7600型全自动生化分析仪检测肾功能。根据肾脏病饮食改良简化公式[9]及美国肾脏病预后质量指南[10]评估肾功能。
1.4 安全性观察 治疗期间,观察患者耐受情况,统计不良反应情况。
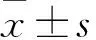
2 结果
2.1 两组不同时间血清HBV DNA含量及HBV DNA不可测率比较 见表1、2。
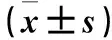
表1 两组不同时间血清HBV DNA含量比较
注:与ETV+ADV组治疗同时间比较,*P<0.05;与同组基线比较,#P<0.05。

表2 两组不同时间血清HBV DNA不可测率比较
注:与ETV+ADV组治疗同时间比较,*P<0.05。
2.2 两组不同时间HBeAg阴转率和HBeAg血清学转换率比较 TDF组基线HBeAg阳性58例,累积48周HBeAg阴转19例、HBeAg血清学转换8例,HBeAg阴转率和血清学转换率分别为32.76%(19/58)、13.79%(8/58);ETV+ADV组HBeAg阳性41例,累积48周HBeAg阴转8例、HBeAg血清学转换3例,HBeAg阴转率和血清学转换率分别为19.51%(8/41)、7.32%(3/41)。两组治疗48周HBeAg阴转率和血清学转换率比较差异均无统计学意义(P均>0.05)。
2.3 两组不同时间ALT复常率比较 TDF组和ETV+ADV组基线ALT异常率分别为29.17%(21/72)、22.45%(11/49)。治疗4、12、24、36、48周,TDF组ALT复常率分别为28.57%(6/21)、57.14%(12/21)、90.47%(19/21)、95.24%(20/21)、100%(21/21),ETV+ADV组ALT复常率分别为27.27%(3/11)、54.55%(6/11)、90.91%(10/11)、90.91%(10/11)、100%(11/11)。两组各时间ALT复常率比较差异均无统计学意义(P均>0.05)。
2.4 安全性评价 TDF组4例、ETV+ADV组2例基线肾小球滤过率正常,治疗过程出现肾功能轻度异常,未影响治疗。两组治疗期间耐受性均较好,未出现横纹肌溶解、乳酸酸中毒等严重不良反应,无病情加重或死亡。
3 讨论
TDF最早于2001年被美国FDA批准用于治疗人类免疫缺陷病毒(HIV)感染。随后研究发现,在HIV合并HBV感染患者中,TDF还能强效抑制HBV复制[11,12],并于2008年被美国FDA批准用于治疗慢性乙肝。TDF是无环磷酸盐类NAs,可在细胞内被磷酸化生成具有药理活性的代谢产物替诺福韦二磷酸,与底物脱氧核糖竞争结合插入DNA,进而抑制HBV逆转录过程,阻止病毒DNA复制[13],是目前抗病毒能力强且耐药屏障高的药物。国外学者Hu等[14]研究发现,TDF对拉米夫定、ADV等其他NAs耐药的经治患者,具有较好的抗病毒效果,且不良反应小、患者耐受性好。随着2014年TDF在中国上市,2016年12月国家将TDF纳入医保报销目录,TDF在慢性乙肝治疗中的应用已大幅度提高。以往NAs经治耐药或应答不佳的慢性乙肝患者主要采用NAs联合治疗,如ETV+ADV。国外研究认为,TDF单药或NAs联合治疗均是挽救NAs经治耐药或应答不佳的慢性乙肝患者治疗方案。但由于TDF在我国上市时间较短,其用于治疗NAs经治耐药或应答不佳的慢性乙肝患者临床效果及安全性的报道较少。
血清HBV DNA含量是评估抗病毒疗效的最常用指标。抗病毒治疗时间延长不仅能提高抑制HBV DNA复制效果,还能增加HBV DNA不可测率。本研究结果显示,随着抗病毒治疗进展,TDF组和ETV+ADV组血清HBV DNA含量均呈下降趋势,且TDF组治疗12、24、36、48周时血清HBV DNA含量均低于ETV+ADV组。随抗病毒治疗时间延长,两组HBV DNA不可测率均明显升高,但TDF组治疗12、24、36、48周时HBV DNA不可测率均高于ETV+ADV组。提示对NAs经治耐药或应答不佳的慢性乙肝患者,TDF单药能早期快速抑制病毒复制,其效果优于ETV+ADV。
HBeAg阴转和血清学转换是HBeAg阳性患者抗病毒治疗终点,是停药的重要指标。ALT复常可反映肝脏损伤与修复过程,表明肝脏炎症得到改善。本研究两组累积48周HBeAg阴转率和血清学转换率比较差异均无统计学意义,与林厚熊[15]研究结果基本一致。两组至治疗24周时,ALT异常者大部分恢复正常,至治疗48周时,ALT复常率均达到100%;但两组各时间ALT复常率比较差异均无统计学意义,与杨丹红等[16]研究结果基本一致。表明两种方案治疗NAs经治耐药或应答不佳的慢性乙肝患者均能快速实现ALT复常。
TDF和ADV主要经肾脏排泄,均不排除随着用药时间延长可能引起的肾功能损害。Han等[17]研究发现,长期TDF或ADV抗病毒治疗可引起肾功能损害。本研究TDF组4例、ETV+ADV组2例在治疗过程中出现肾功能轻度异常。两组治疗期间耐受性均较好,未出现横纹肌溶解、乳酸酸中毒等严重不良反应,无病情加重或死亡。说明两种治疗方案均较安全。
综上所述,对NAs经治耐药或应答不佳的慢性乙肝患者,TDF单药和ETV+ADV治疗均有较好的临床效果,但TDF在病毒抑制方面优于ETV+ADV,可作为NAs经治耐药或应答不佳的慢性乙肝患者优选治疗方案。
参考文献:
[1] Liang X, Bi S, Yang W, et al. Evaluation of the impact of hepatitis B vaccination among children born during 1992-2005 in China[J]. J Infect Dis, 2009,200(1):39-47.
[2] Liang X, Bi S, Yang W, et al. Epidemiological serosurvey of hepatitis B in China--declining HBV prevalence due to hepatitis B vaccination[J]. Vaccine, 2009,27(47):6550-6557.
[3] Tenney DJ, Rose RE, Baldick CJ, et al. Long-term monitoring shows hepatitis B virus resistance to entecavir in nucleoside-naive patients is rare through 5 years of therapy[J]. Hepatology, 2009,49(5):1503-1514.
[4] Sun J, Xie Q, Tan D, et al. The 104-week efficacy and safety of telbivudine-based optimization strategy in chronic hepatitis B patients: a randomized, controlled study[J]. Hepatology, 2014,59(4):1283-1292.
[5] 王贵强,王福生,成军,等.慢性乙型肝炎防治指南(2015年更新版)[J].临床肝胆病杂志,2015,31(12):1941-1960.
[6] European Association for the Study of the Liver. EASL 2017 clinical practice guidelines on the management of hepatitis B virus infection[J]. J Hepatol, 2017,67(2):370-398.
[7] Liaw YF, Kao JH, Piratvisuth T, et al. Erratum to: Asian-Pacific consensus statement on the management of chronic hepatitis B: a 2012 update[J]. Hepatol Int, 2012,6(4):809-810.
[8] Snow-Lampart A, Chappell B, Curtis M, et al. No resistance to tenofovir disoproxil fumarate detected after up to 144 weeks of therapy in patients monoinfected with chronic hepatitis B virus[J]. Hepatology, 2011,53(3):763-773.
[9] Lee SK, Song MJ, Kim SH, et al. Safety and efficacy of tenofovir in chronic hepatitis B-related decompensated cirrhosis[J]. World J Gastroenterol, 2017,23(13):2396-2403.
[10] Kim YJ, Sinn DH, Gwak GY, et al. Tenofovir rescue therapy for chronic hepatitis B patients after multiple treatment failures[J]. World J Gastroenterol, 2012,18(47):6996-7002.
[11] 中华医学会肝病学分会.慢性乙型肝炎防治指南2010年更新版[J].中华实验和临床感染病杂志(电子版),2011,5(1):79-100.
[12] Levey AS, Coresh J, Greene T, et al. Expressing the modification of diet in renal disease study equation for estimating glomerular filtration rate with standardized serum creatinine values[J]. Clin Chem, 2007,53(4):766-772.
[13] Castro AF, Coresh J. CKD surveillance using laboratory data from the population-based National Health and Nutrition Examination Survey (NHANES)[J]. Am J Kidney Dis, 2009,53(3 Suppl 3):S46-S55.
[14] Hu CY, Liu YM, Liu Y, et al. Pharmacokinetics and tolerability of tenofovir disoproxil fumarate 300 mg once daily: an open-label, single-and multiple-dose study in healthy Chinese subjects[J]. Clin Ther, 2013,35(12):1884-1889.
[15] 林厚熊.替诺福韦与恩替卡韦治疗HBeAg阳性初治慢性乙型肝炎患者的临床疗效[J].山东医药,2016,56(33):92-94
[16] 杨丹红,赵年丰,潘红英,等.替诺福韦酯挽救治疗核苷(酸)类药物多重耐药慢性乙型肝炎患者的疗效观察[J].中华肝脏病杂志,2015,23(1):75-76.
[17] Han Y, Zeng A, Liao H, et al. The efficacy and safety comparison between tenofovir and entecavir in treatment of chronic hepatitis B and HBV related cirrhosis: a systematic review and Meta-analysis[J]. Int Immunopharmacol, 2017(42):68-175.
