熔盐氮化法制备六方氮化硼纳米片
2018-04-27,,,
, ,,
(武汉科技大学,省部共建耐火材料与冶金国家重点实验室,武汉 430081)
0 引 言
六方氮化硼(h-BN)具有熔点高、导热系数高、热膨胀系数低、介电常数低、带隙宽、绝缘性好、化学稳定性好、抗氧化性好以及润滑性优良等特点,在结构陶瓷、功能陶瓷、耐火材料、涂料和化妆品等领域有着良好的应用前景[1-3]。h-BN陶瓷的成型、烧结及性能与h-BN粉体的纯度、粒径大小及分布、颗粒形态等密切相关,因此高活性h-BN粉体的制备显得尤为重要。
目前,制备h-BN粉体的方法主要有固相反应法、溶剂热法、自蔓延高温合成法和化学气相沉积法等[4-6]。固相反应法采用碳热还原氧化硼来合成BN,其合成温度高、反应时间长,且产物需要除碳处理;溶剂热法通常以有毒的有机溶剂为原料,且反应周期较长;自蔓延高温合成法的反应过程难以控制;化学气相沉积法的成本高、产率低,难以满足工业生产要求。因此,寻找合适的低成本、绿色无毒的h-BN粉体的制备方法具有重要意义。
熔盐法是一种简单易行、重复性高的无机粉体材料制备方法,该方法以安全无毒且可回收利用的熔盐为介质来促进反应物的扩散以及相互之间的反应,具有合成温度低、反应时间短,合成粉体纯度高、粒径小等优点,并且还可以通过改变熔盐种类和含量来控制产物形貌[7-9]。近年来,熔盐法被广泛用于合成各种氮化物,如TiN[10]、AlN[11]和Si3N4[12]等,也有一些学者对熔盐法制备BN粉体进行了研究,如YE等[13]以硼砂为硼源、金属镁粉为还原剂、氯化钾为熔盐介质,在800~1 300 ℃反应3 h合成出了h-BN粉体,但该合成反应需要使用镁粉还原剂,得到h-BN纯相的反应温度较高(1 200 ℃以上),且产物需要酸洗。
为了低温合成高活性h-BN粉体,作者以NaCl-KCl为熔盐介质、以硼砂和三聚氰胺为原料,采用熔盐氮化法制备h-BN纳米片,研究了反应温度、熔盐和反应物的质量比、氮和硼的物质的量比对产物物相组成的影响,并表征了纯相h-BN粉体的显微结构和氮气吸附脱附性能。
1 试样制备与试验方法
1.1 试样制备
试验原料有硼砂(分析纯,国药集团化学试剂有限公司)、三聚氰胺(化学纯,天津泰兰德化学试剂有限公司)、NaCl(分析纯,国药集团化学试剂有限公司)、KCl(分析纯,国药集团化学试剂有限公司)和氮气(纯度99.999%)等。
以NaCl和KCl为熔盐介质,三聚氰胺和硼砂为反应物,按照NaCl和KCl质量比为44∶56,氮和硼的物质的量比(氮硼比)分别为1∶1,2∶1,4∶1,熔盐与反应物的质量比(盐料比)分别为0∶1,1∶1,2∶1进行配料,混合均匀后放入氧化铝坩埚中,在80 ℃干燥5 h,再置于GSL-1600X型刚玉管式炉中,在流通氮气气氛下于900~1 200 ℃反应3 h,产物经去离子水清洗,过滤,干燥后待用。
1.2 试验方法
使用Philips X-Pert Pro型X射线衍射仪(XRD)对产物进行物相分析,采用铜靶,Kα射线,扫描范围为0°~90°。使用FEI Nova 400 Nano型扫描电子显微镜(SEM)和JEOL JEM-2100型透射电子显微镜(TEM)观察产物的微观形貌;利用PHOENIX型X射线能量色散谱(EDS)进行微区成分分析。采用autosorb-1型全自动比表面积及孔径分析仪测试产物的氮气吸附脱附等温线,计算BET比表面积。
2 试验结果与讨论
2.1 反应温度对产物物相组成的影响
由图1可知,当反应温度为900,1 000 ℃时,产物主要由h-BN相(ICDD:01-073-2095)和少量杂质相组成;当反应温度升高至1 100,1 200 ℃时,产物为h-BN相,没有杂质相存在。与传统的硼砂-三聚氰胺固相反应法相比,熔盐氮化法得到h-BN纯相的反应温度降低了约100 ℃[14]。
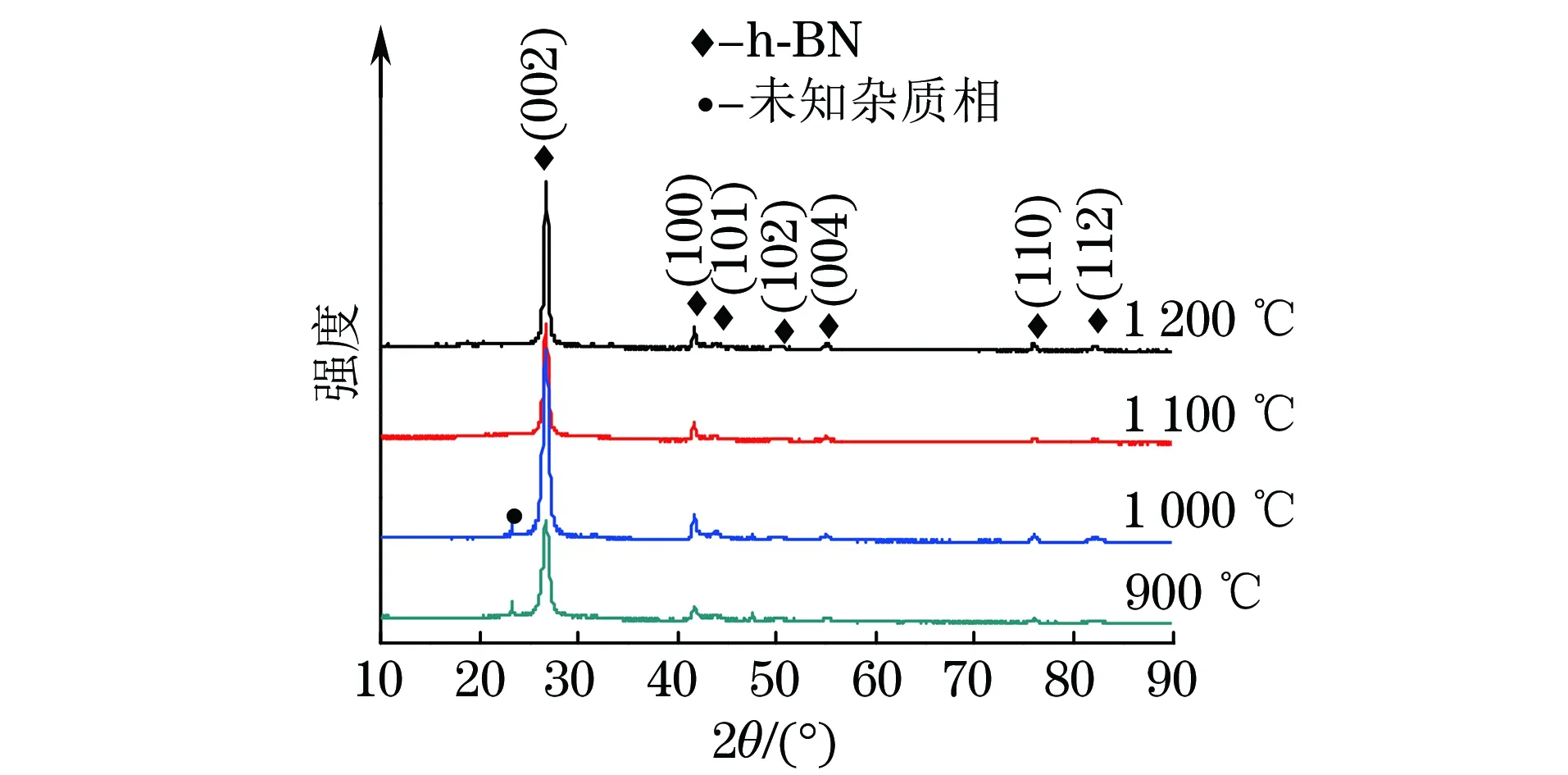
图1 盐料比为2∶1,氮硼比为2∶1时不同温度反应产物的XRD谱Fig.1 XRD patterns of reaction products at different temperatures withsalt to reactant ratio of 2∶1 and N to B ratio of 2∶1
2.2 盐料比对产物物相组成的影响
由图2可知:当氮硼比为2∶1,反应温度为1 000 ℃时,不同盐料比下所得产物中均存在h-BN相;当盐料比由0∶1增至1∶1时,产物中还存在杂质相的衍射峰且该衍射峰强度减弱,说明h-BN相的纯度升高;当盐料比增至2∶1时,杂质相的衍射峰消失,产物中只存在h-BN相,说明熔盐含量的增加促进了h-BN的生成。这是因为反应物在熔盐介质中的充分溶解有利于其扩散和相互之间的反应,从而促进h-BN的生成。
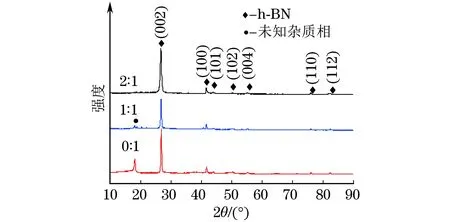
图2 氮硼比为2∶1,不同盐料比时1 000 ℃反应产物的XRD谱Fig.2 XRD patterns of reaction products at 1 000 ℃ with N to Bratio of 2∶1 and different ratios of salt to reactant
2.3 氮硼比对产物物相组成的影响
由图3可知:当盐料比为2∶1,氮硼比为1∶1时, 1 000 ℃反应产物中存在h-BN相和Na2Al2B2O7杂质相(ICDD:00-053-1124),杂质相是由于反应过程中三聚氰胺分解产生的含氮气体逸出导致氮源不足,使得硼砂与氧化铝坩埚反应而生成的;当氮硼比增至2∶1和4∶1时,产物中均只存在h-BN相,表明氮含量的增加有利于h-BN的生成。
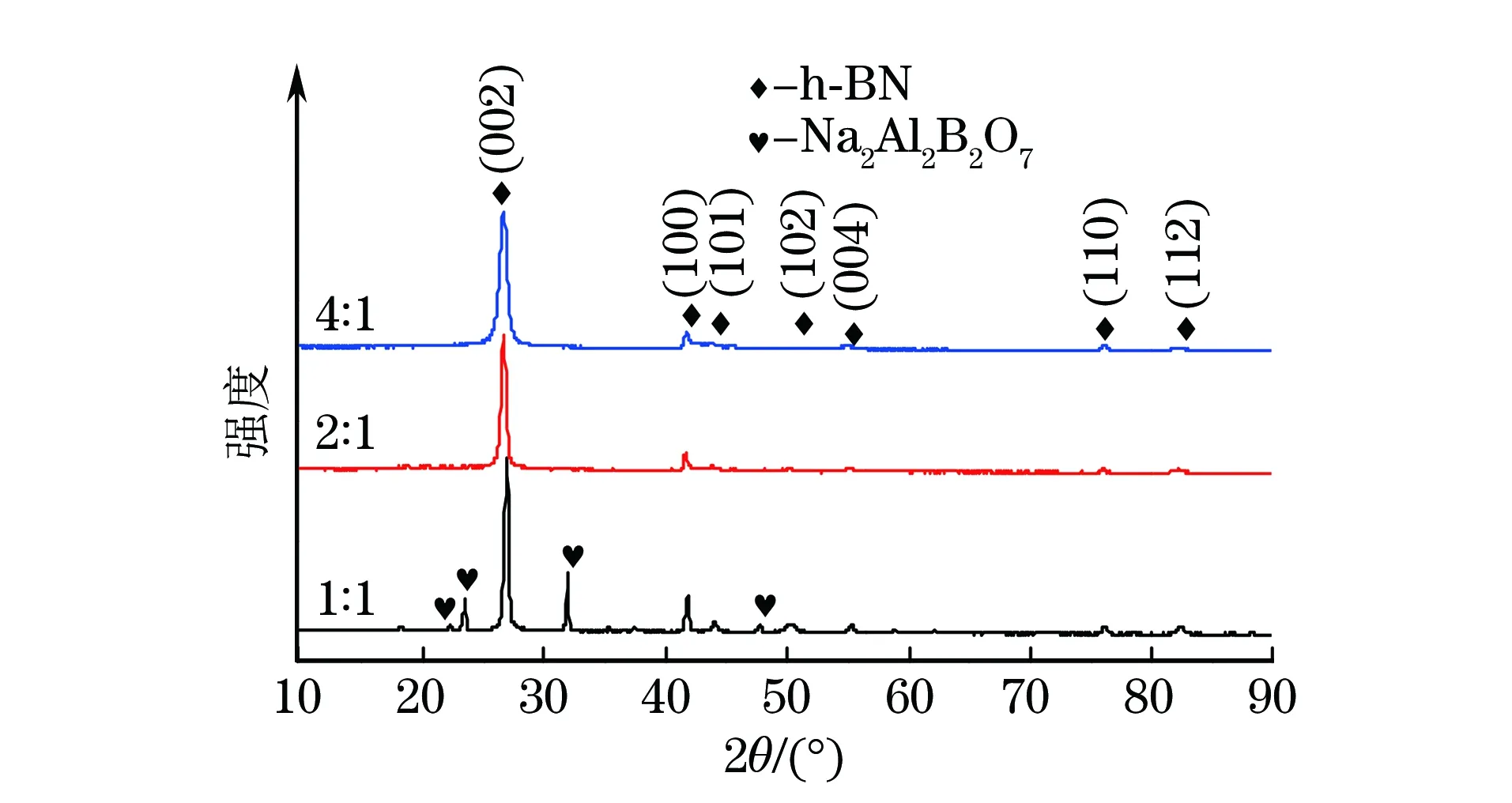
图3 盐料比为2∶1,不同氮硼比时1 000 ℃反应产物的XRD谱Fig.3 XRD patterns of reaction products at 1 000 ℃ with salt toreactant ratio of 2∶1 and different ratios of N to B
综上可知,当盐料比为2∶1,氮硼比为2∶1和4∶1时,在1 100,1 200 ℃反应3 h均可得到纯相h-BN粉体。下面以盐料比为2∶1,氮硼比为2∶1,1 100 ℃反应3 h所得h-BN粉体为例进行显微结构和比表面积分析。
2.4 h-BN粉体的显微结构
由图4可知:h-BN粉体为片状颗粒,粒径为50~200 nm,粉体发生明显团聚;粉体颗粒由硼和氮元素组成,进一步证明该片状颗粒为BN。EDS谱中的铝元素来源于铝制样品台,金元素来源于制样时喷涂的金。
由图5可知:h-BN粉体呈片状,其长度为50~200 nm、厚度为10~40 nm;选区电子衍射(SAED)花样为多晶环结构,晶面间距分别对应h-BN的{100},{101},{110}和{112}晶面族;从片状h-BN侧面的高分辨透射电镜(HRTEM)图中可观察到明显的晶格条纹,晶面间距约0.34 nm,对应h-BN的{002}晶面族。综上可知,在盐料比为2∶1,氮硼比为2∶1,反应温度为1 100 ℃的条件下合成了h-BN纳米片。

图5 盐料比为2∶1,氮硼比为2∶1时1 100 ℃反应所得h-BN粉体的TEM形貌、SAED花样和HRTEM形貌Fig.5 TEM image (a), SAED pattern (b) and HRTEM image (c) of h-BN powder prepared at 1 100 ℃ with salt to reactant ratio of2∶1 and N to B ratio of 2∶1
2.5 h-BN粉体的比表面积
由图6可知:h-BN粉体的氮气吸附脱附等温线属于典型的IV型吸附等温线,存在明显的迟滞回线,迟滞环属于H3型,这进一步证明了试验合成的h-BN粉体为片状,且h-BN粉体在较高的相对压力范围内没有表现出任何吸附限制。计算得到h-BN粉体的BET比表面积为82 m2·g-1,远高于一般固相反应法合成的(2~40 m2·g-1)[15]。综上所述,所合成的h-BN粉体具有较高的活性。
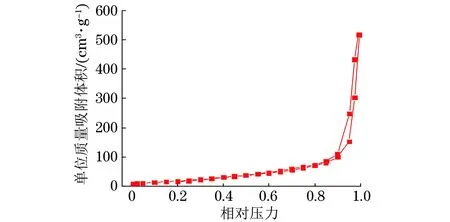
图6 盐料比为2∶1,氮硼比为2∶1时1 100 ℃反应所得h-BN粉体的氮气吸附脱附等温线Fig.6 N2 adsorption-desorption isotherms of h-BN powder prepared at1 100 ℃ with salt to reactant ratio of 2∶1 and N to B ratio of 2∶1
3 结 论
(1) 以NaCl-KCl为熔盐介质,以硼砂和三聚氰胺为反应原料,采用熔盐氮化法制备了h-BN粉体,当盐料比为2∶1,氮硼比为2∶1时,h-BN粉体的纯度随反应温度的升高而增加,在1 100 ℃反应后粉体中仅存在h-BN相,该反应温度比采用传统固相反应法的降低约100 ℃。
(2) 当氮硼比为2∶1,反应温度为1 100 ℃时,盐料比的增加有利于h-BN的生成;当盐料比为2∶1,反应温度为1 100 ℃时,氮硼比的增加有利于h-BN的生成。
(3) 当盐料比为2∶1,氮硼比为2∶1时,在1 100 ℃反应3 h后能得到纯相h-BN纳米片,其长度为50~200 nm,厚度为10~40 nm,比表面积为82 m2·g-1,该h-BN纳米片的活性较高。
参考文献:
[1] JIANG X F, WENG Q, WANG X B, et al. Recent progress on fabrications and applications of boron nitride nanomaterials: A review[J]. Journal of Materials Science & Technology, 2015, 31(6): 589-598.
[2] YIN J, LI J, HANG Y, et al. Boron nitride nanostructures: Fabrication, functionalization and applications[J]. Small, 2016, 12(22): 2942-2968.
[3] ARENAL R, LOPEZ-BEZANILLA A. Boron nitride materials: An overview from 0D to 3D (nano) structures[J]. Wiley Interdisciplinary Reviews: Computational Molecular Science, 2015, 5(4): 299-309.
[4] PAINE R, NARULA C K. Synthetic routes to boron nitride[J]. Chemical Reviews, 1990, 90(1): 73-91.
[5] 何冬青, 梁嘉鸣, 梁兵. 六方氮化硼颗粒制备方法研究进展[J]. 材料导报, 2015, 29(5): 92-96.
[6] 李俊生, 张长瑞, 李斌. 氮化硼陶瓷先驱体研究进展[J]. 硅酸盐通报, 2011, 30(3): 567-571.
[7] LIANG F, TIAN L, ZHANG H, et al. Low temperature synthesis of LiSi2N3nanobelts via molten salt nitridation and their photoluminescence properties[J]. RSC Advances, 2016, 6(73): 68615-68618.
[8] TIAN L, LI J, LIANG F, et al. Molten salt synthesis of tetragonal carbon nitride hollow tubes and their application for removal of pollutants from wastewater[J]. Applied Catalysis B: Environmental, 2018, 54: 315-321.
[9] LIU J, HUANG Z, HUO C, et al. Low-temperature rapid synthesis of rod-like ZrB2powders by molten-salt and microwave co-assisted carbothermal reduction[J]. Journal of the American Ceramic Society, 2016, 99(9): 2895-2898.
[10] DING J, DENG C, YUAN W, et al. The synthesis of titanium nitride whiskers on the surface of graphite by molten salt media[J].Ceramics International,2013,39(3):2995-3000.
[11] 田亮, 梁峰, 张杰峰,等. 熔盐氮化法低温合成AlN粉体[J]. 陶瓷学报, 2017, 38(3): 352-355.
[12] DING J, ZHU H, LI G, et al. Catalyst-assisted synthesis of α-Si3N4in molten salt[J]. Ceramics International, 2016, 42(2): 2892-2898.
[13] YE L, ZHAO L, LIANG F, et al. Facile synthesis of hexagonal boron nitride nanoplates via molten-salt-mediated magnesiothermic reduction[J]. Ceramics International, 2015, 41(10): 14941-14948.
[14] 张相法, 梁浩, 孟令强, 等. 六方氮化硼的制备方法及在合成立方氮化硼中的应用[J]. 金刚石与磨料磨具工程, 2012(4):14-18.
[15] 胡昆鹏, 袁颂东, 罗意, 等. 高比表面氮化硼的制备方法研究进展[J]. 江汉大学学报(自然科学版), 2013, 41(1): 55-60.
