HER2、EGFR蛋白表达和HER2基因表达在胃癌中的临床意义*
2018-04-26汪亮亮魏淑飞郑美蓉
汪亮亮 曹 芳 魏淑飞 李 婷 徐 晓 郑美蓉
(1九江学院临床医学院/附属医院病理科;2九江学院基础医学院病理教研室 江西九江 332000)
胃癌现在是中国常见的恶性肿瘤之一,每年新发的病例达到40多万人,发病率在恶性肿瘤排第一位,在恶性肿瘤的死亡率中排名第二位。目前国内诊断的胃癌多数是中晚期胃癌,只是手术治疗为主,辅以放化疗,但对一些晚期胃癌的患者治疗效果不明显。目前新辅助治疗为晚期胃癌的患者提供了新的选择,因此胃癌分子生物学方面的研究和靶向药物治疗方面的研究十分多,成为肿瘤治疗的热点之一。HER2和EGFR(又称HER1)同属于表皮生长因子受体家族,有文献报道这两种基因在胃癌的表达会升高。该实验是应用免疫组化(IHC)的方法对HER2、EGFR(HER1)蛋白在胃癌中的表达情况进行检测,对HER2免疫组化表达2+的进行分子检测(FISH),分析它们与肿瘤发生的性别、年龄、组织学、浸润深度、脉管侵犯、淋巴结转移情况及病理分期的相关性,以期为晚期胃癌的治疗、预后提供相关的参考依据。
1 临床资料
1.1 一般资料
随机选取2014年-2017年10月期间在九江学院附属医院外科住院并进行手术治疗的胃癌病人129例,其中男85例,女44例;年龄38-86岁,平均年龄62.03±6.78岁;≥60岁81例,<60岁44例。所有患者术前均未进行放化疗,病理术后均诊断为腺癌。
1.2 方法
1.2.1 常规病理 所有手术标本均在切除30min内加入10%中性福尔马林固定24h,取材、脱水、石蜡包埋,4微米厚切片,HE染色后,由2名病理医生诊断。
1.2.2 免疫组化 免疫组化采用MaxEnVision法,3 μm厚切片,DAB显色,苏木精复染,中性树胶封片。所用抗体HER2、EGFR均购自福州迈新公司,所有抗体均按照说明书操作。
1.2.3 HER2荧光原位杂交 原位杂交仪为德国DAKO公司,HER2荧光原位杂交试剂盒购自广东安必平公司,按说明书操作。
1.3 结果判读
1.3.1 HE结果判断 采用美国癌症联合委员会(AJCC)癌症分期手册(第六版)修订的胃癌 TNM 病理分期标准。组织学分型按 Lauren 分型[1]标准分为高分化腺癌、中分化腺癌、低分化腺癌(包括印戒细胞癌或黏液腺癌)。
1.3.2 HER-2免疫组化过表达结果判断 所有免疫组化切片均由 2名资深病理科医生双盲独立观察评估。HER2阳性染色呈棕黄色颗粒,位于细胞膜,其结果判定采用Herceptest进行IHC检测分析并根据修订的评分系统[2]进行评分。无着色/少于10%肿瘤细胞有细胞膜着色(0/阴性)(见图1);大于10%的肿瘤细胞呈现微弱、不完整的细胞膜着色(1+/阴性)(见图2);大于 10%的肿瘤细胞呈现弱至中度完整的细胞膜着色(2+/可疑阳性)(见图3);大于10%的肿瘤细胞呈现强的、完整的细胞膜着色(3+/阳性)(见图4)。此评分系统中,将0及+归为阴性,2+归为可疑阳性,做FISH检测明确是否阳性,3+归为阳性。
1.3.3 EGFR 过表达结果判断 阳性染色呈棕黄色颗粒,定位于细胞膜。肿瘤细胞不着色/<10%的肿瘤细胞着色为阴性(-)(见图5),≥10%的肿瘤细胞着色为阳性,并根据肿瘤阳性细胞数所占比例分为:10~25%(+),26~50%(++),50~75%(+++),>75%(+++)。++以上认为阳性(见图6和图7)。
1.3.4 HER-2荧光原位杂交(FISH)结果判读 计数30个细胞核内橘红色的Her2基因荧光信号和17号染色体的绿色荧光信号,统计其比例(30个细胞核中红信号总数/30个细胞核中绿信号总数)。Her-2阳性定义为为Fish阳性(Her2基因荧光信号/17号染色体的绿色荧光信号>2) (见图8)。

图1 HER-2(0)
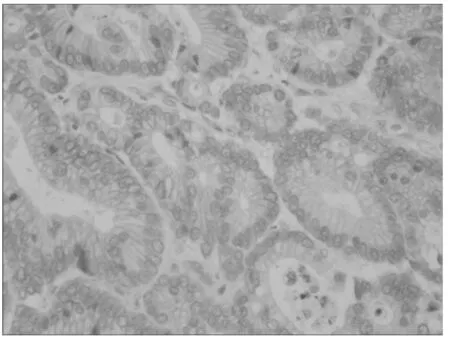
图2 HER-2(+)

图3 HER-2(2+)

图4 HER-2(3+)

图5 EGFR(-)
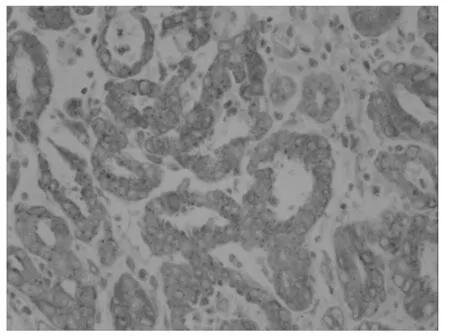
图6 EGFR(+)
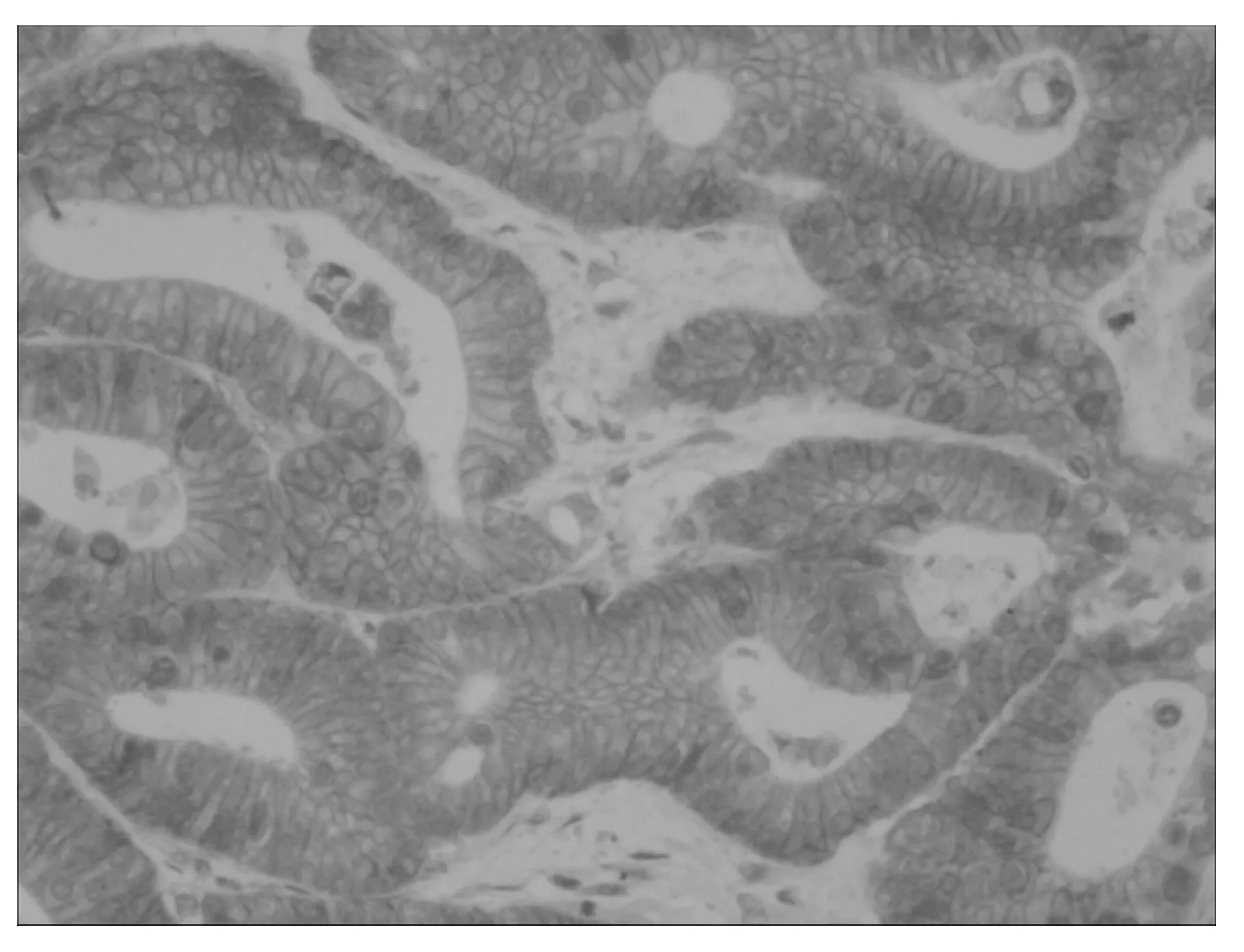
图7 EGFR(+)

图8 荧光原位杂交(FISH)检测Her-2阳性,呈簇状分布。
1.4 统计方法
原始数据采用EXCEL建立表格,经整理核对后导入SPSS19.0统计软件,统计分析方法采用二分类Logistic多因素回归分析,对胃癌患者的性别、年龄、组织学、浸润、脉管、淋巴结情况及病理分期与因变量HER2、EGFR表达的关系进行分析。同时采用spearman等级相关分析对HER2、EGFR表达的相关性进行检验,以p<0.05表示有统计学意义。
2 结果
2.1 HER2蛋白在胃癌中的表达情况
129例患者中HER2(3+)的病例和HER2(2+)经FISH证实有扩增的病例共13例,阳性率10.78%(13/129);HER2的阳性表达与分化程度、病理分期有相关性(p<0.05),而与性别、年龄、浸润深度、脉管侵犯、淋巴结转移无相关性(p<0.05),详见表1。
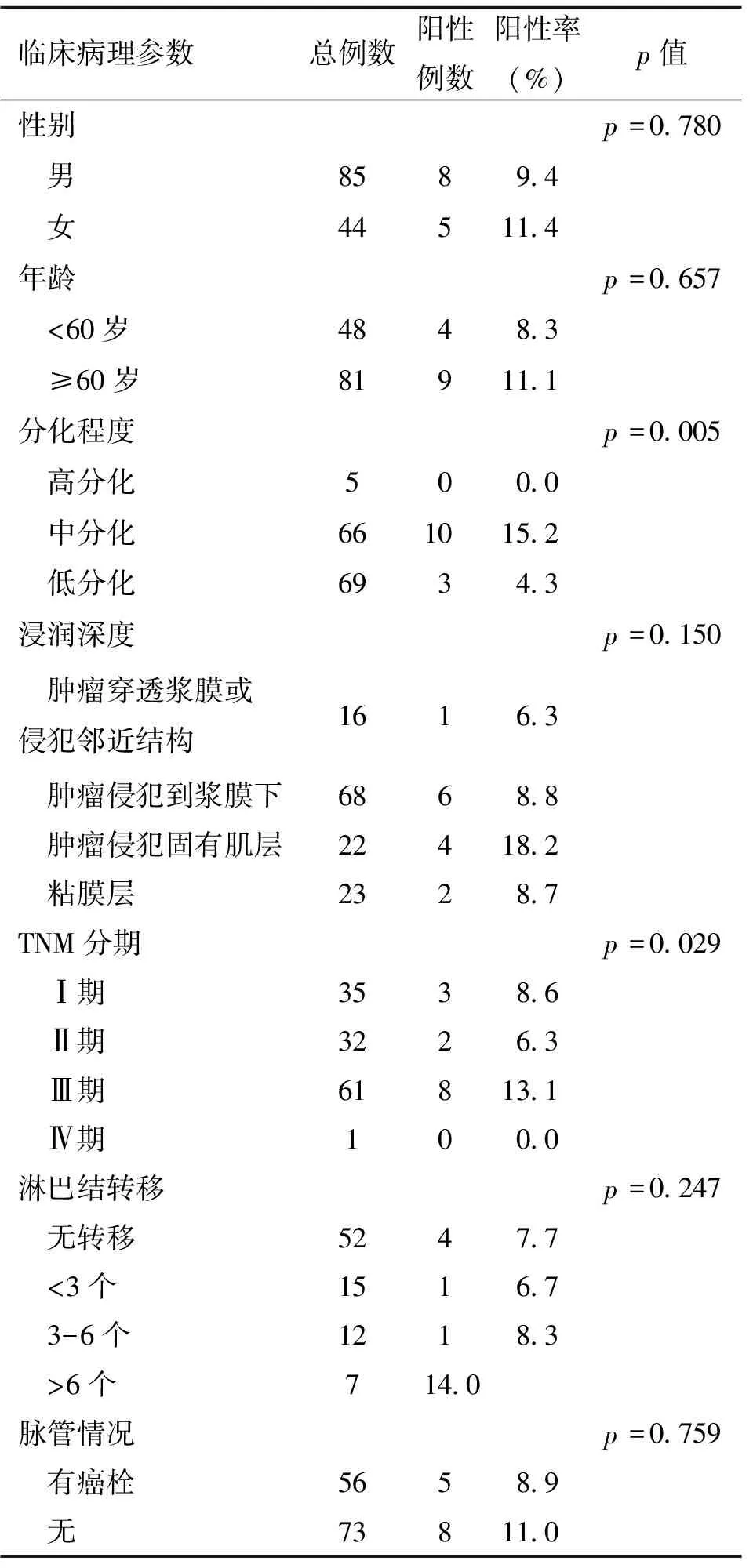
表1 HER2蛋白在胃癌中的表达情况
2.2 EGFR蛋白在胃癌中的表达情况
EGFR蛋白阳性率20.93%(27/129),阳性表达与分化程度、病理分期有相关性(p<0.05),而与性别、年龄、浸润深度、脉管侵犯、淋巴结转移无相关性(p>0.05),详见表2。

表2 EGFR蛋白在胃癌中的表达情况
2.3 HER2、EGFR表达的相关性
spearman等级相关分析对HER2、EGFR表达的相关性进行检验,统计分析结果显示,两者表达无相关性(p=0.094)。
3 讨论
HER2是表皮生长因子受体家族成员,表皮生长因子受体家族成员一共有4个,分别是HER1(EGFR)、HER2、HER3、HER4。它们影响着肿瘤细胞的分子生物学结构,包括肿瘤细胞的增增殖、凋亡、黏附性和肿瘤的分化[1]。当人体内和HER2大量扩增是,会激活多种信号传导途径,从而引起细胞的不规律增殖和不凋亡,从而引起癌变[4]。
研究发现,在乳腺癌、胃癌、膀胱癌、卵巢癌等多种恶性肿瘤中HER2会出现蛋白的过表达和基因的扩增。 20%-30%的乳腺浸润性导管癌患者的 HER2会出现蛋白的过表达和基因的扩增[5-7]。表达越高,预后就越差[8]。一些文献报到胃癌HER2的过表达率和基因扩增率为9-38%[9-10], 该研究HER2的阳性表达率为10.78%(13/129), 与以前的研究结果一致。
国外的一些研究报道HER2的过表达与肿瘤的大小、浸润深度、淋巴结的转移和病理分期有关[11],一些研究报道说与组织学类型有关[12]。该研究发现HER2的过表达与肿瘤的分化程度、病理分期有相关性(p<0.05),而与性别、年龄、脉管浸润、淋巴结转移无相关性(p>0.05)。由此可证明HER2的过表达与胃癌的预后差有关。
EGFR是原癌基因CerBb-1的产物,与配体结合以后激活PTK蛋白,从而促进肿瘤细胞的增殖,血管增生,侵袭和转移,而抑制肿瘤细胞的凋亡。已证实在食管癌、乳腺癌、胃癌、肠癌等多种肿瘤中有EGFR蛋白表达;但文献报道在胃癌中EGFR蛋白表达率从9%-62.7%,差异性较大。该研究EGFR表达率20.93%(27/129),与文献报道的相一致。
文献报道的胃癌临床病理指标与EGFR蛋白表达关系存在不一致。一些研究认为 EGFR 的表达与肿瘤的浸润深度、 病理分期、 Lauren 分型、脉管侵犯、淋巴结转移及远处转移等有相关性,与性别、年龄、肿瘤发生部位无相关性。 一些研究证实 EGFR 的高表达与年龄、肿瘤分化程度相关。研究证实 EGFR 高表达的胃癌患者预后较不表达者差,多因素分析提示 EGFR 的高表达可能为一个独立的预后不良的标志。该研究发现EGFR蛋白表达阳性与分化程度、病理分期有相关性(p<0.05),而与性别、年龄、浸润深度、脉管侵犯、淋巴结转移无相关性(p>0.05)。
HER2与EGFR同属于表皮生长因子受体家族成员,两者在胃癌中均有高表达,且临床参数关系密切,两者的表达是否有关联性文献报告也不一致。该研究通过spearman等级相关分析对HER2、EGFR表达的相关性进行检验,统计分析结果显示,两者表达无相关性(p=0.094),说明HER2和EGFR可以分别作为独立的预后因素。
综上所述,HER2、EGFR在正常胃粘膜中不表达,在胃癌中均有高表达,均是与肿瘤的分化程度、病理分期有相关性(p<0.05),而与性别、年龄、浸润深度、脉管侵犯、淋巴结转移无相关性(p>0.05)。文章研究的结果,为临床晚期胃癌患者的治疗方式的选择、靶向药物的选择、预后评估提供理论依据。
参考文献:
[1]Gravalos C,Jimeno A. HER-2 in gastric cancer: a new prognostic factor and a novel therapeutic target [J]. Ann Oncol,2008, 19(1): 1523.
[2]Hofmann M,Stosso,Shi D,et al.Assessmen to a HER2 scoring system for gasticcancer:results from avalidation study[J].Histopathology,2008,52(7):797.
[3]Press MF, Slamon DJ, Flom KJ, et al. Evaluation of HER-2/neu gene amplification and overexpression [J].J Clin Oncol,2002, 20(4): 3095.
[4]Slamon DJ, Godolphin W, Jones LA, et al. Studies of the HER-2/neu proto-oncogene in human breast and ovarian cancer [J]. Science 1989,244(1): 707.
[5]Takehana T, Kunitomo K, Kono K, et al. Status of c-erbB-2 in gastric adenocarcinoma:a comparative study of immunohistochemistry,fluorescence in situ hybridization, and enzyme-linked immuno-sorbent assay [J].Int J Cancer,2002, 98(2): 833.
[6]Tanner M, Hollme′n M, Junttila TT, et al. Amplification of HER-2 in gastric carcinoma:association with Topoisomerase IIa gene amplification, intestinal type, poor prognosis and sensitivity to trastuzumab [J]. Ann Oncol,2005, 16(5): 273.
[7]Bernhard H, Neudorfer J, Gebhard K, et al.Adoptive transfer of autologous, HER2-specific,cytotoxic T lymphocytes for the treatment of HER2-overexpressing breast cancer[J]. Cancer Immunol Immunother,2008, 57(4): 271.
[8]Meza-Junco J, Au HJ, Sawyer MB. Trastuzumab for gastric cancer[J]. Expert Opin Biol Ther ,2009, 9(6): 1543.
[9]Park DI, Yun JW, Park JH, et al.HER-2/neu amplification is an independent prognostic factor in gastric cancer[J]. Dig Dis Sci 2006,51(1): 1371.
[10]Yonemura Y, Ninomiya I, Yamaguchi A, et al. Evaluation of immunoreactivity for erbB-2 protein as a marker of poor short-term prognosis in gastric cancer [J]. Cancer Res,1991, 51(3): 1034.
[11]Lordick F, Bang YJ, Kang YK, et al. HER-2 /neu-positive advanced gastric cancer: similar HER-2 /neu-positivity levels to breast cancer [J]. Eur Jcancer. 2007, 5(4): 27.
