泰山虫草滴丸的制备及质量评价
2018-04-13
(泰山医学院,山东 泰安 271016)
泰山虫草(Cordyceps taishanensis Liu, Yuan et Cao)是一种虫生真菌,寄生在鳞翅目昆虫蛹体上,并在合适的条件下从蛹体上长出子实体。由于野生资源稀缺,现多为人工培养。其中的虫草素、腺苷具有抗病毒、抗菌、抑制肿瘤的作用;次黄嘌呤核苷可治疗白细胞和血小板的减少[1]。研究表明,泰山虫草中的核苷类及次黄嘌呤等成分及微量元素的含量均高于冬虫夏草[2-3],因此泰山虫草作为优良的药材及冬虫夏草的代用品,已经引起了重视,其作为保健品也具有良好的开发前景[4]。冬虫夏草及泰山虫草常见的应用形式包括子实体、口服液、超微粉、养生酒、养生茶、虫草胶囊等。为了实现释药迅速、生物利用度高、制备简便且携带运输方便的目标,本研究拟将泰山虫草提取物制备成滴丸,从而丰富泰山虫草的下游产品,为泰山虫草资源的综合开发提供理论和实践基础。
1 材料与仪器
泰山虫草为本实验室培养。试剂均为分析纯︰乙酸乙酯(天津市中和盛泰化工有限公司);浓硫酸(无锡嘉宏化工贸易有限公司);蒽酮(国药集团化学试剂有限公司);液体石蜡(天津市化学试剂二厂);无水乙醇(天津市永大化学试剂有限公司);PEG2000,PEG4000,PEG6000(天津天泰精细化学品有限公司);蔗糖(天津市永大化学品有限公司);醋酸钠(天津市永大化学品有限公司);甲醇(天津市永大化学品有限公司)。腺苷(上海金穗生物科技有限公司,99%)。
旋转蒸发仪(上海亚荣生化仪器厂 RE-52A型);电子分析天平(赛多利斯科学仪器北京有限公司 BT-25S型);超声波清洗器(昆山市超声仪器有限公司 KQ3200E型);数显智能控温磁力搅拌器(巩义市予华仪器有限责任公司 SZCL-2A型);低速离心机(上海安亭科技仪器厂 TDL-4OB型);恒温水浴锅(上海亚荣生化仪器厂 HW.SY21-K型);循环水式多用真空泵(河南省予华仪器有限公司 ZRS-8G型);恒温干燥箱(天津泰斯特仪器有限仪器公司 101-3AB型);紫外-可见分光光度计(上海元析仪器有限公司 UV-8000A型);高效液相色谱仪(大连依利特分析仪器有限公司 UV230II型)。
2 方法
2.1 泰山虫草有效成分的提取
泰山虫草子实体100 g置于90 ℃恒温干燥箱内烘干1 h,干燥子实体用研钵捣碎后置于500 ml圆底烧瓶,加入95%乙醇溶液500 ml,回流1h,残渣再依次用60%乙醇和蒸馏水500 ml依次回流提取1h。合并提取液,保温80℃静置,上清液用纱布滤过,滤液用旋转蒸发仪浓缩至30 g,得到泰山虫草浸膏。
2.2 泰山虫草滴丸的制备及优化
2.2.1泰山虫草滴丸的制备典型的制备过程如下:称取PEG 5.0 g,置100 ml烧杯中,80 ℃水浴加热,水浴熔化后加入虫草浸膏5.0 g,搅拌均匀,在80℃保温条件下以 20 d/min 速度采用下行滴制法滴入5℃恒温的液体石蜡中。
2.2.2泰山虫草滴丸的处方优化为了考察PEG分子量对产品质量的影响,分别以PEG2000,PEG6000和PEG2000∶PEG6000=1∶1的混合物为作为基质,浸膏与基质的质量比分别取2∶1,1∶1,1∶2,按照2.2.1方法制备滴丸,以泰山虫草滴丸的滴制过程、滴丸硬度和形状、表面性状为考察指标,选定最佳处方。
2.3 泰山虫草滴丸的质量评价
2.3.1重量差异根据《中国药典》2015 版四部通则 0108 丸剂项下重量差异项下测定法操作,取泰山虫草滴丸 20 丸,精密称量滴丸的总质量,再分别精密称量每粒滴丸的质量,计算丸重差异。
2.3.2多糖浓度的测定方法硫酸—蒽酮法显色液的配制:取洁净100 ml烧杯,加入16 g蒸馏水,搅拌条件下缓慢滴加64 g浓硫酸,加入80 mg蒽酮,5 ml乙酸乙酯,搅拌均匀,得到硫酸—蒽酮显色液[7]。精密量取样品1.0 ml,与显色液5.5 ml混合摇匀,置85 ℃水浴中加热10 min,取出放至室温,以蒸馏水1.0 ml同法处理后作为空白,在波长625 nm测定吸光度。
配置浓度分别为12.5 μg/ml,25 μg/ml,50 μg/ml,100 μg/ml,200 μg/ml和250 μg/ml的一系列蔗糖标准溶液,按照上述方法测定,以吸光度(x)为横坐标,浓度(y,μg/ml)为纵坐标,回归得到标准曲线:y=161.91x-3.70622。R2= 0.9999,故在浓度为12.5 μg/ml~250 μg/ml之间吸光度与浓度成良好的线性关系。
2.3.3腺苷浓度测定方法腺苷的测定采用高效液相色谱(HPLC)法。色谱柱:依利特SinoChrom ODS-BP(250×4.6 mm),填料直径5 μm;流动相为20 mM醋酸钠∶甲醇=8∶2;流速1.0 ml/min;温度为室温;进样量20 μl;检测波长260 nm。首先配置溶液浓度为0.245 μg/ml,0.49 μg/ml,0.98 μg/ml,9.8 μg/ml,98 μg/ml的一系列腺苷标准溶液,用HPLC法测定峰面积,以峰面积(x)为横坐标,浓度(y,mg/ml)为纵坐标,回归得到得腺苷溶液的标准曲线y=0.0215x-0.0615,R2= 1。样品测得峰面积代入标准曲线求得浓度。
2.3.4滴丸中有效成分的溶出速度测定取1.80 g滴丸,依据 2015 版《中国药典》四部 0931 溶出度与释放度测定法第一法,溶剂:800 ml蒸馏水,转速:100 r/min,按照药典的方法操作,在5 min,15 min,30 min,1 h,2 h,3 h,5 h 分别取样 5 ml,立刻用 0.45 μm的微孔滤膜过滤,取续滤液0.5 ml进样20 μl,测定腺苷含量;继续取续滤液1.0 ml,加入2.0 ml乙醇,摇匀后在4摄氏度冰箱中保存4 h,4000 rpm离心2 min,弃去上清液,沉淀以1.0 ml水复溶后按照2.3.2方法测定多糖含量。干燥的泰山虫草子实体粉末过四号筛,称取3.00 g,按上述同法测定腺苷及多糖的浓度。溶出度计算:分别以最后一个取样点测得腺苷及多糖含量为100%,计算其他各时间点溶出度。
3 结果与讨论
3.1 滴丸的制备及条件优化
泰山虫草的有效成分较为复杂,因此采用不同浓度的乙醇和水分别提取,有利于提取出各种极性的有效成分。为保证重现性,泰山虫草提取液合并后需减压浓缩至一定浓度。将提取液分别浓缩至20 g,30 g和40 g,与PEG基质(由PEG2000和PEG6000等量混合而成)按照1∶1的质量比在80℃水浴加热条件下进行混合试验。结果显示,当提取液浓缩至20 g时便不能分散于PEG基质中,这是因为基质PEG具有吸水性,而浓缩液中除了水分之外主要为多糖和蛋白质,当PEG夺取浓缩液中的水分后便会使多糖及蛋白质析出。但若仅将提取液浓缩至40 g,则过多的水分会使PEG基质无法凝固。因此最终确定三次提取液合并后浓缩至30 g为宜。
将浓缩至30 g的提取物与基质按1∶1质量比混合,制备的泰山虫草滴丸。考察滴制过程发现以PEG2000作基质,滴丸冷凝较慢,降落至底部后仍未完全冷凝,因此产品均粘连;而以PEG6000 作基质,加如提取物后整个体系黏度极大,滴制时不能形成液滴,而是呈条状流出滴制口;故最终选择PEG2000与PEG6000等量混合作为滴丸基质。
3.2 泰山虫草滴丸的质量评价
3.2.1外观及重量差异虫草提取物与PEG2000和PEG6000按照2∶1∶1的比例混合制备滴丸,成品表面光洁,颜色均匀,无拖尾或气泡。20粒滴丸的平均丸重为0.0402 g;超出差异限度(12%)的有两丸,分别超出15%和16%,符合药典要求。
3.2.2泰山虫草滴丸中多糖及腺苷溶出度的测定多糖和腺苷是泰山虫草中有效成分的典型代表,故以这两种成分为指标,评价泰山虫草滴丸中小分子和大分子有效成分的溶出度。腺苷的溶出曲线如图1所示。滴丸在30 min时腺苷溶出度达到99.69%,而相同条件下子实体粉末中腺苷只溶出了41.1%,直到3 h后,子实体粉末才基本溶出完全。滴丸中多糖的溶出速度也明显快于子实体粉末,由图2可见,滴丸中的多糖在15 min时便溶出了98.51%,而子实体粉末中的多糖在4h后才溶出完全。因此,制备成滴丸后,泰山虫草中的有效成分溶出速度显著快于子实体粉末,其原因是所用载体为亲水性的聚乙二醇,有效成分高度分散在基质中,伴随着基质的溶出而实现速释。
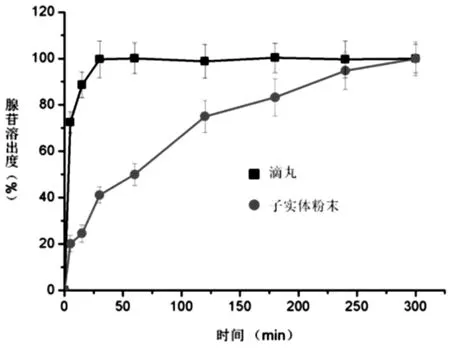
图1 泰山虫草滴丸与子实体粉末中腺苷的溶出曲线
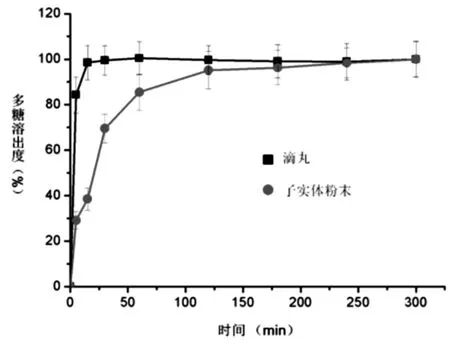
图2 泰山虫草滴丸与子实体粉末中多糖的溶出曲线
本研究对泰山虫草滴九的制备工艺进行了优化,成功制备了泰山虫草滴丸,制备工艺为泰山虫草浸膏2份,与1份PEG2000和1份PEG6000在80℃条件下充分混合,滴入5℃的液体石蜡中。制成的滴丸具有较好的外观,重量差异符合药典标准,其有效成分腺苷和多糖的体外溶出速度较子实体粉末显著提高。制备的泰山虫草滴丸为实现泰山虫草的综合利用以及丰富泰山虫草的下游产品提供了有益借鉴,具有一定的开发前景。
参考文献:
[1]张秀波,刘玉升.泰山虫草的研究进展[J].环境昆虫学报,2009,31(3):280-284.
[2]赵雪梅,毕研平,苏延友,等.泰山虫草菌丝体与冬虫夏草有效成分的TLCS分析[J].食品与发酵工业.2008,34(03):126-129.
[3]赵雪梅,张辉,苏延友,等.泰山虫草菌丝体与天然冬虫夏草化学成分初步分析[J].中药材.2008,32(12):1828-1830.
[4]黄秀华,方书亮,温鲁.用高虫草素菌粉开发药品和保健[J].中国医药科学.2012,2(13):157-158.
