苦参碱金属配合物的合成及抑菌活性研究
2018-04-08王永宏刘存寿
刘 涵,李 海,王永宏,2,刘存寿,3,张 兴,2
(1.西北农林科技大学 无公害农药研究服务中心,陕西杨凌 712100;2.陕西省生物农药工程技术研究中心,陕西杨凌 712100; 3.西北农林科技大学 资源环境学院,陕西杨凌 712100)
农药配合物主要是将农药有效成分与金属盐形成配合物,由于无机配合物杀菌剂具有高效、低毒、少污染、低成本等特点,利用某些配位聚合物的抑菌活性,开发缓释新型农药也同样具有潜在重大经济效应,同时也可为开发新农药开辟蹊径[1-2]。
中药配位学说认为,中药有效成分不是单纯的有机成份,也不是单纯的微量元素,微量元素在中药有效成分产生药理作用的过程中起着重要作用[3-4]。大量试验证明农药活性物质与金属形成配合物后,生物活性增强。徐海珍等[5]合成PMBP的铜、锌、镍、钴及锰金属配合物,发现其配合物抑菌活性均强于配体。杨春龙等[6]合成丙环唑金属配合物ML2CL2(M=Zn、Cu、Co)和ML4CL2(M=Ni、Mn),各金属配合物对蔬菜灰霉病菌、小麦纹枯病菌、小麦赤霉病菌、水稻恶苗病菌、黄瓜炭疽病菌的毒力均高于配体,其中锌配合物对各种植物病原菌抑菌效果最好。Keskioglu等[7]以哌嗪Schiff碱为配体合成相应的铬、铁、钴配合物,并研究它们的抑菌活性,发现该Schiff碱无抑菌活性,其相应配合物却具有良好的抑菌效果。中国科学院海洋所李鹏程[8]研制出一种新型的杀菌活性强且低毒的杀菌剂——甲壳低聚糖金属配合物杀菌剂,该药物制备方法已获国家发明专利。
苦参碱(Matrine,图1)主要是从豆科植物苦参的干燥根、果实中分离鉴定的一种生物碱[9-10]。其药理作用广泛,医学上具有抗肿瘤、抗溃疡、抗心律失常、抗病毒以及治疗慢性肝炎等作用[11-12];在农业上,具有杀虫、抑菌、杀鼠、促进植物生长等活性[13-14],同时对灰霉病、疫病、赤霉病具有一定抑制效果[15]。过渡金属元素因具有能量相近原子轨道,配位能力强以及电负性较大等优点,容易与有机物形成稳定的配合物[16]。苦参碱分子结构中内酰胺结构可被皂化生产羧酸衍生物[17],而羧酸类衍生物因氧原子配位能力强和灵活多样的配位模式而备受化学家的青睐[18-19]。因此,本研究选用过渡金属铁、锌与苦参碱进行配位,采用元素分析、红外光谱分析、差热热重同步分析、单晶衍射分析等方法对配合物进行结构表征。同时通过苦参碱金属配合物对番茄灰霉病菌、小麦赤霉病菌、以及马铃薯晚疫病菌的抑菌活性进行研究,将具有生物活性的苦参碱和金属离子有机地结合起来提高抑菌活性、扩大抑菌谱和使用范围,将为该杀菌剂的研究与开发注入新的活力。
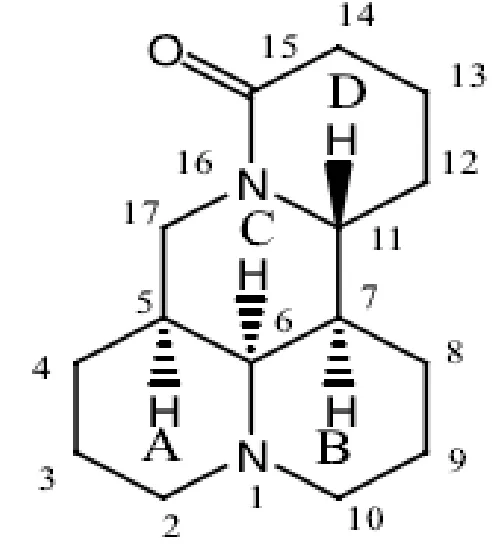
图1 苦参碱结构Fig.1 Structure of matrine
1 材料与方法
1.1 试验材料与仪器
苦参碱(Matrine, C15H24N2O)φ=98%、番茄灰霉病菌(Botrytiscintrea)、小麦赤霉病菌(Fusariumgraminearum)、马铃薯晚疫病菌(Phytophthorainfestans)均由西北农林科技大学无公害农药研究服务中心提供,无水乙醇、氯化锌、氯化铁、盐酸等为分析级试剂。
Avatar300 红外光谱仪、AutAnalyel元素分析仪、TA-60WS+DTG-60A&TA-60WS+ DTG-60A差热热重同步分析仪、APEXIJ DVO4096*4096像素单晶衍射仪、UX220H型电子分析天平等。
1.2 试验方法
1.2.1苦参碱配合物合成苦参碱铁配合物合成:取苦参碱2.484 g、盐酸0.365 g于刻度为20 mL试管底部,加入15 mL无水乙醇的缓冲层(先慢后快),最上面逐滴滴入10 mol/L氯化铁无水乙醇溶液1 mL,静置2 h使溶液扩散,即有苦参碱铁配合物黄色晶体生成。
苦参碱锌配合物合成:取苦参碱2.484 g、氯化锌1.363 g与盐酸0.365 g,在室温下溶于无水乙醇(10 mL),其中乙醇慢慢挥发后得到浅黄色晶体,为苦参碱锌配合物。
1.2.2苦参碱配合物结构表征红外分析方法将苦参碱铁、锌2种金属配合物分别按照样品与干燥碘化钾质量比1∶100混合进行压片,置于红外光谱仪上检测400~4 000 cm-1红外光谱。
差热热重同步分析在流速为100 mL/min空气气氛中进行,用10 ℃/min升温速率从室温加热至600 ℃,测定所得配合物的差热热重同步分析。
选取合适大小单晶用X-射线进行单晶衍射试验,在Brucker APEXⅡCCD衍射仪上收集数据,采用MoKα射线(λ=0.071 073 nm)石墨单色器检测,采用ω-2θ扫描方式收集晶体数据。全部衍射数据经Lp因子校正,用直接法进行晶体结构解析。随后采用多轮差值Fourier合成法确定非氢原子和氢原子坐标,对非氢原子坐标进行各向异性参数矩阵的最小二乘法修正。
1.3 苦参碱及其金属配合物抑菌活性测定
采用生长速率法[20]测定苦参碱及其配合物对番茄灰霉病菌、小麦赤霉病菌、马铃薯晚疫病菌的抑菌活性。具体做法如下:将苦参碱及其金属配合物用灭菌水稀释为4 000 、6 000、8 000、10 000 mg/L 4个质量浓度梯度的药液,待供试样品充分溶解后,分别取上述不同稀释度溶液1 和9 mL于PDA培养基混合均匀,制成终质量浓度分别是400、600 、800、1 000 mg/L的带药培养基,待培养基凝固后,于含药平板中部接种直径5 mm的菌饼,并设置清水空白对照,各处理重复3次。24 ℃恒温培养室培养3~5 d,待空白对照的菌落长满培养皿后,十字交叉测量各菌落直径2 次,取其平均值,计算菌丝生长抑制率:生长抑制率=[1-(药剂处理的菌落生长直径)-菌饼直径/(空白对照菌落生长直径-菌饼直径)]×100%。
2 结果与分析
2.1 配合物元素分析表征
表1表明,苦参碱铁配合物中C、H、N的质量分数测试值为(%):C,40.31;H,5.65;N,6.28,通过元素质量分数比例给出配合物中金属与配体个数比例约为1∶1,可能分子式为C15H25Cl4FeN2O。该分子式中C、H、N的质量分数计算值为(%):C,40.45;H,5.38;N,6.37,结果表明配合物元素分析测试值和计算值误差基本都在允许范围之内,说明该分子式确定符合元素分析结果,初步推断出配合物分子式为C15H25Cl4FeN2O。同理可推断苦参碱锌配合物分子式为C15H25Cl3N2OZn,符合元素分析结果。
2.2 配合物的红外光谱
配体以及配合物红外光谱数据见表2,苦参碱内酰胺C=O伸缩振动出现在1 633 cm-1处,而苦参碱铁、锌配合物分别红移到1 594 cm-1与1 574 cm-1处,相较于配体分别红移39 cm-1和59 cm-1,相比于苦参碱铁配合物,苦参碱锌配合物内酰胺C=O伸缩振动键红移最大,说明氯化锌对苦参碱内酰胺C=O伸缩振动产生较大影响。配体苦参碱的N-H和C-N谱分别在2 858、1 333 cm-1处,锌配合物的谱带在2 870、1 336 cm-1,二者差异较小,表明氯化锌的加入对苦参碱N-H和C-N谱影响不大,而铁配合物的N-H和C-N谱带消失,表明氯化铁加入引起配体苦参碱在该段波长电子密度降低,引起谱带数目减少。
2.3 配合物的差热热重同步分析
苦参碱金属配合物样品差热热重同步分析结果表明(表3),苦参碱铁配合物小于100 ℃均无失重现象,说明配合物不含结晶水,这与元素分析结果一致。170 ℃以及315 ℃处放热峰为配合物分步氧化峰,且在170~400 ℃有明显失重,可能失去1个苦参碱分子和4个氯原子,最终分解产物为Fe2O3,残留率为14.81%(以Fe2O3计算的理论残重率为15.72%))。苦参碱铁配合物与苦参碱锌配合物的热重曲分析结果基本相同,唯一不同的在于热峰(分别为175 ℃和400 ℃),最终产物ZnO残留率为17.18%(以ZnO理论计算的残留率为16.82%),这与元素分析结果基本一致。
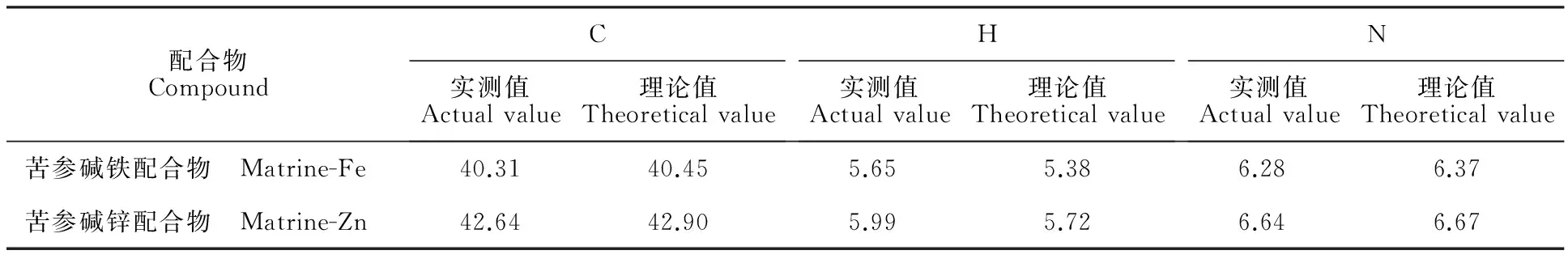
表1 配体与配合物元素分析Table 1 Elemental analysis of the ligand and complexes %

表2 配体以及配合物红外光谱Table 2 Important IR absorption bands of ligand and complexes cm-1

表3 配合物的差热热重同步分析Table 3 TG data of complexes
2.4 配合物单晶衍射
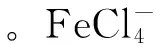
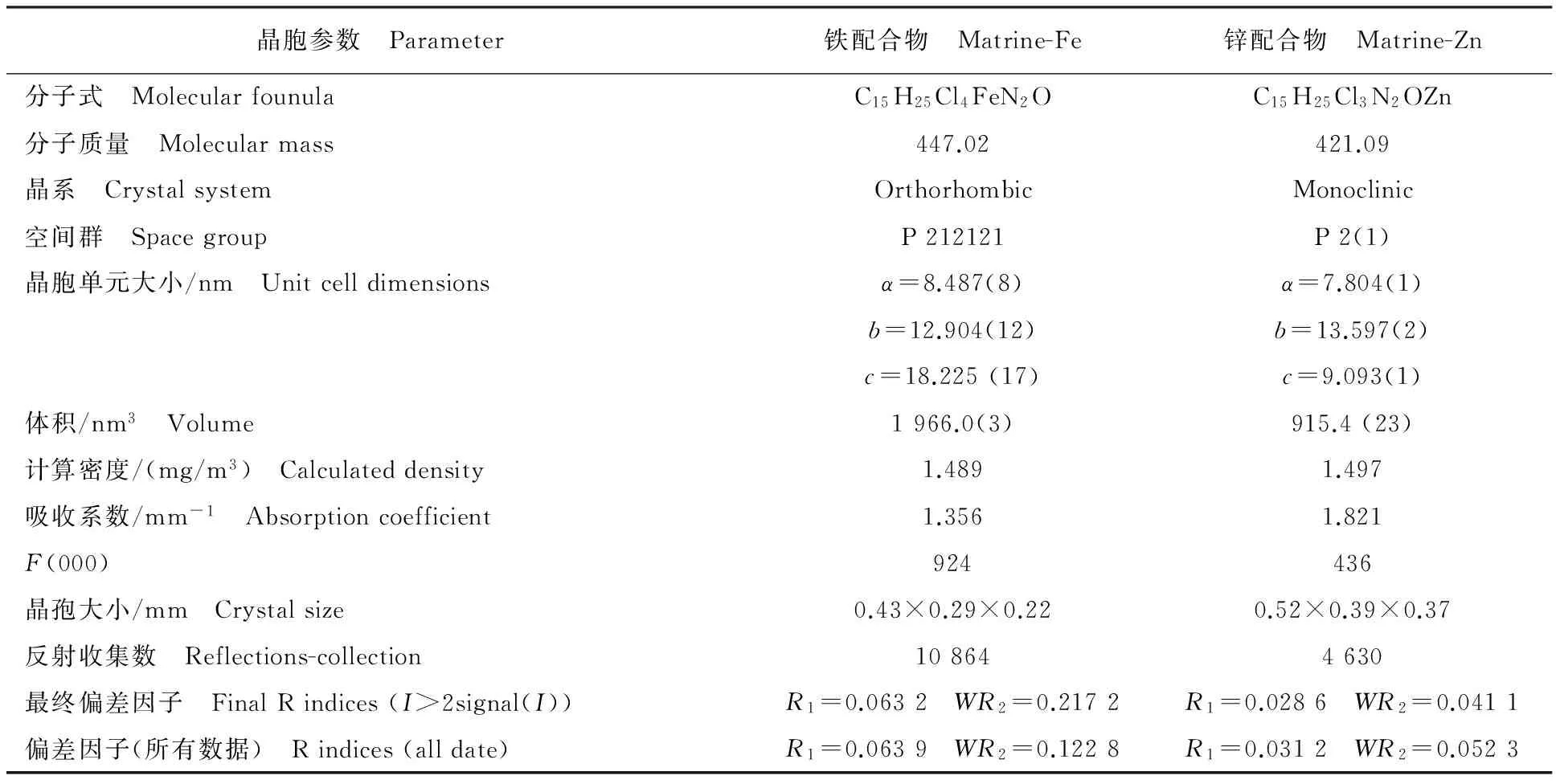
表4 铁、锌金属配合物晶体学数据和结构修正系数Table 4 Crystallographic data and X-ray experiment details for Fe and Zn complexes
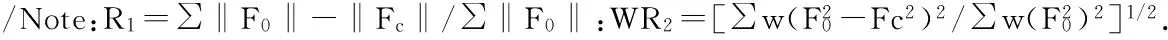
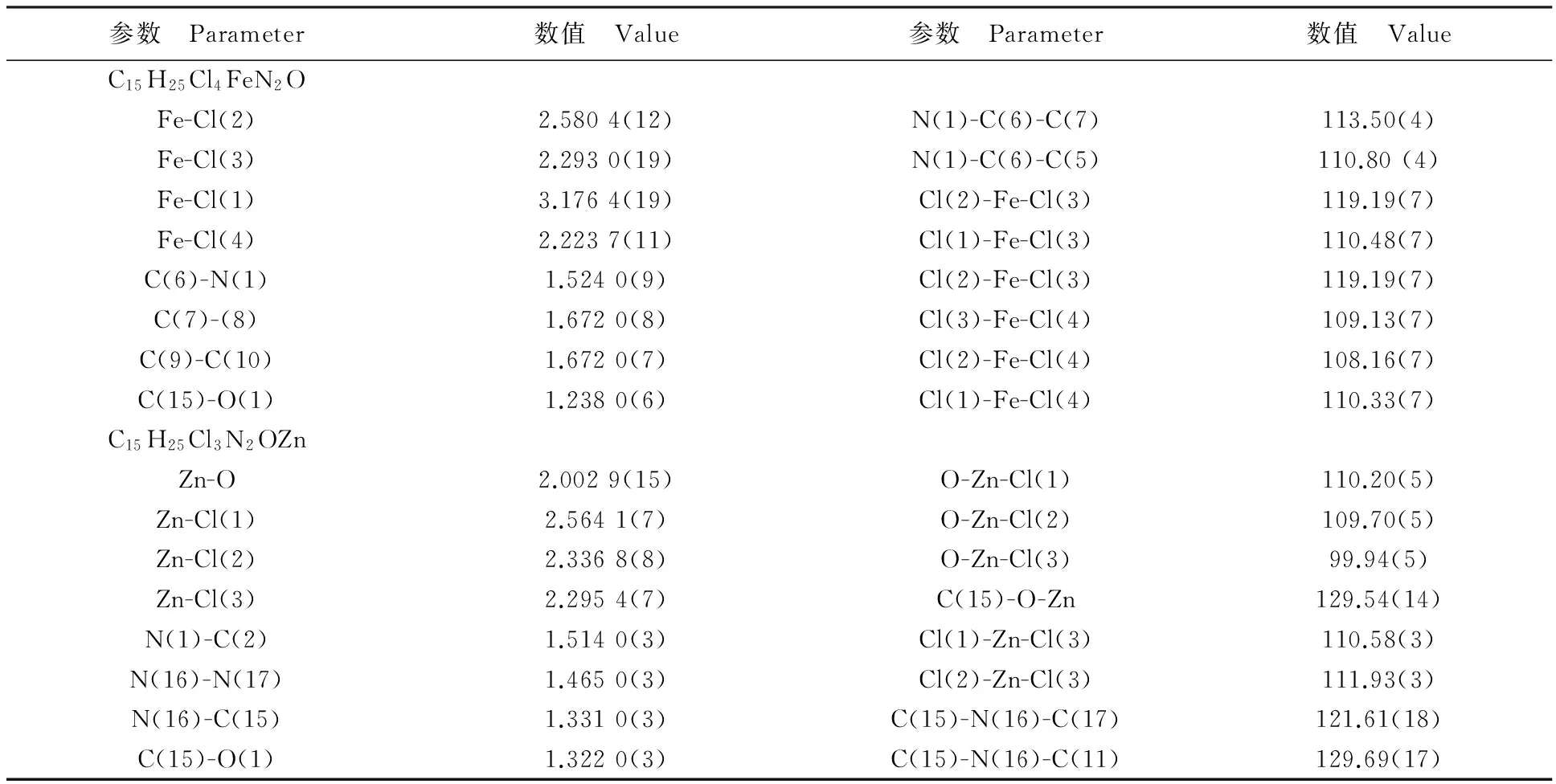
表5 铁、锌金属配合物的重要键长(Å)和键角(°)Table 5 Key bond lengths and angles of Fe and Zn complexes
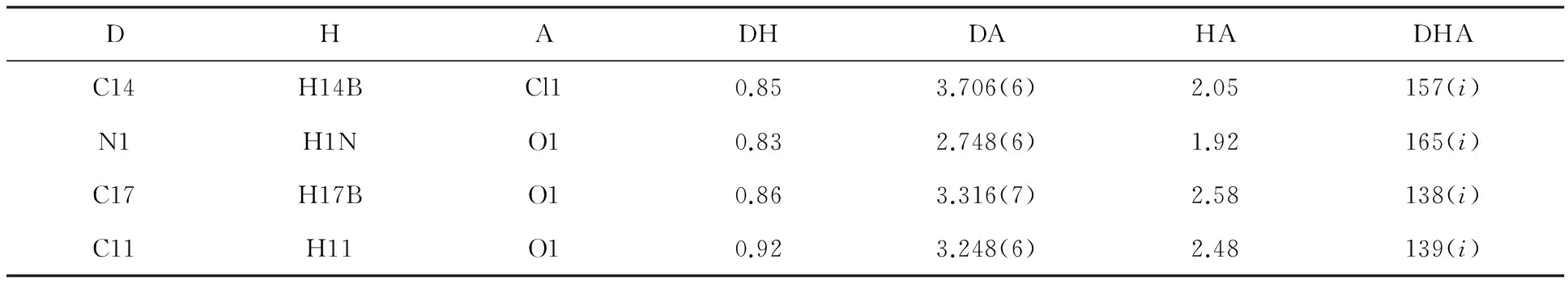
表6 苦参碱铁配合物之间的氢键(Å,°)Table 6 Selected hydrogen bond of Matrine-Fe(Å,°)
注 Note:Symmetry codes:(i)=X+1/2,-y+1/2,-Z+1。

图2 苦参碱铁配合物中Fe3+的配位环境Fig.2 Coordination code of Fe3+ of Matrine-Fe
苦参碱锌配合物分子式为C15H25Cl3N2OZn,为1分子苦参碱与1分子氯化锌配位,属于单斜晶系,空间群为P2(1),单晶大小(0.52×0.39×0.37) mm。晶胞参数α=7.804(1),b=13.597(2),c=9.093(1),V=915.49(23),F(000)=436最终偏差因子R1=0.028 6,WR2=0.041 1(对I>2σ(I)的衍射点),R1=0.031 2,R2=0.052 3(对所有衍射点)。锌原子是三配位,分别与2个氯原子和来自配体苦参碱上的羰基氧原子连接。这些原子与锌原子之间的键角为2.295 4(7)~2.564 1(7)。配合物C=O双键键长增大为1.322(3),而苦参碱Fe(Ⅲ)配合物晶体结构中C=O双键键长只为1.238(6),说明羰基氧原子参与配位,这与红外分析结果一致。苦参碱锌配合物形成配位型配合物,配位环境见图3。
2.5 配合物的抑菌活性
从表7可知,质量浓度为800 mg/L时,配体苦参碱对番茄灰霉病菌的抑制率为9.0%,铁配合物的抑制率为12.8%,表明二者的抑菌活性无显著差异(P>0.05),而锌配合物的抑制率为64.1%,显著高于配体苦参碱的抑菌活性(P<0.05)。苦参碱铁、锌配合物对小麦赤霉病菌的抑制率分别为79.8%和76.4%,均显著高于配体苦参碱的抑菌活性(23.8%)。在相同质量浓度下,苦参碱对马铃薯晚疫病菌的抑制率为68.7%,铁配合物为69.9%,锌配合物为95.2%,配合物与配体均有一定的抑菌活性,锌配合物的抑菌活性显著高于配体。
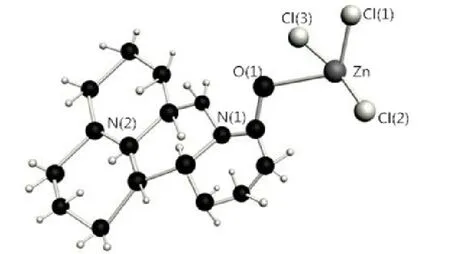
图3 苦参碱锌配合物中Zn2+配位环境Fig.3 Coordination code of Zn2+ of Matrine-Zn
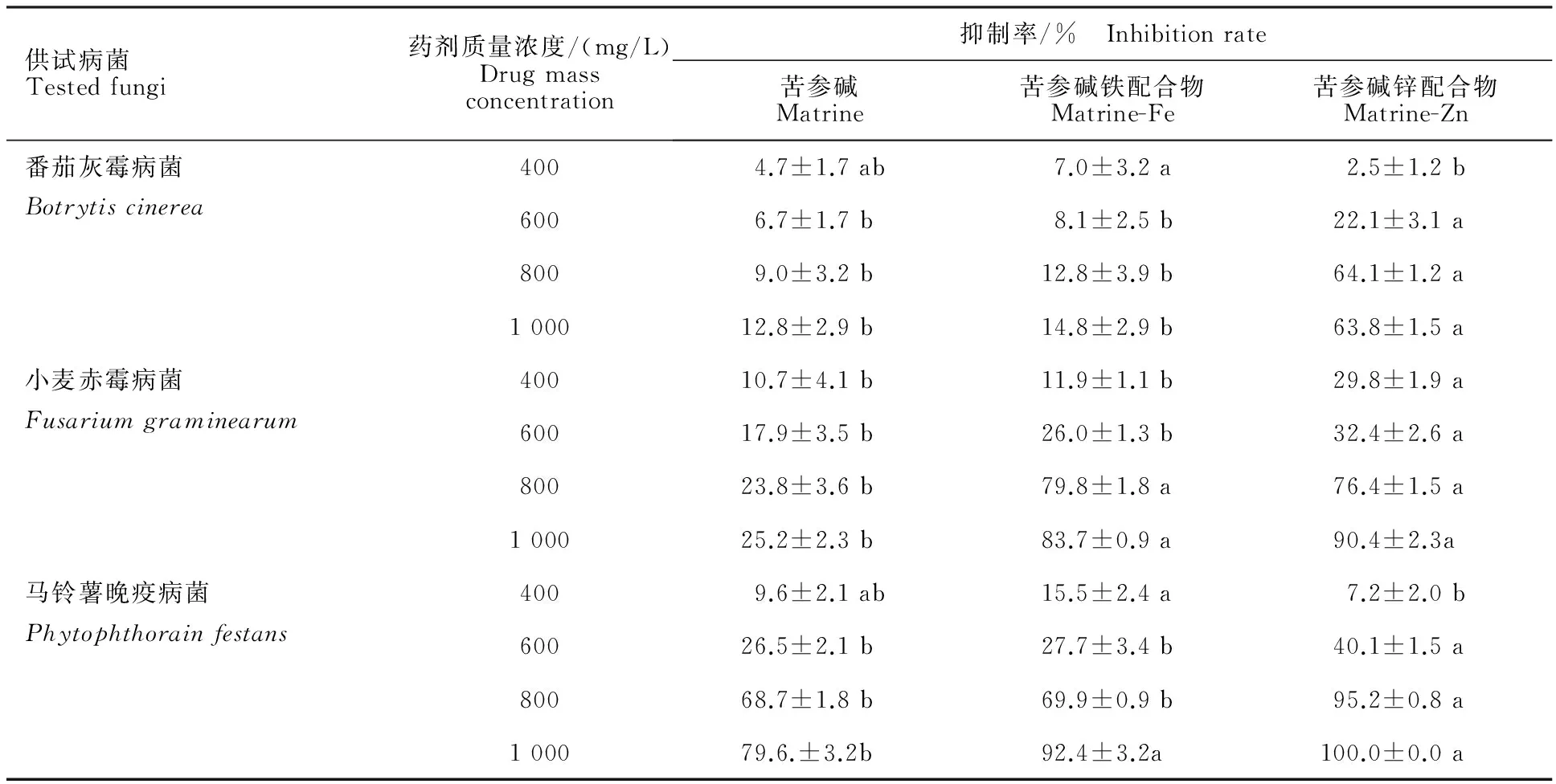
供试病菌Testedfungi药剂质量浓度/(mg/L)Drugmassconcentration抑制率/% Inhibitionrate苦参碱Matrine苦参碱铁配合物Matrine-Fe苦参碱锌配合物Matrine-Zn番茄灰霉病菌4004.7±1.7ab7.0±3.2a2.5±1.2bBotrytiscinerea6006.7±1.7b8.1±2.5b22.1±3.1a8009.0±3.2b12.8±3.9b64.1±1.2a100012.8±2.9b14.8±2.9b63.8±1.5a小麦赤霉病菌40010.7±4.1b11.9±1.1b29.8±1.9aFusariumgraminearum60017.9±3.5b26.0±1.3b32.4±2.6a80023.8±3.6b79.8±1.8a76.4±1.5a100025.2±2.3b83.7±0.9a90.4±2.3a马铃薯晚疫病菌4009.6±2.1ab15.5±2.4a7.2±2.0bPhytophthorainfestans60026.5±2.1b27.7±3.4b40.1±1.5a80068.7±1.8b69.9±0.9b95.2±0.8a100079.6.±3.2b92.4±3.2a100.0±0.0a
注:同行数据后不同小写字母表示差异显著(P<0.05)。
Note:Different lowercase letters in the same rows indicate significant difference (P<0.05).
3 讨论与结论
通过元素分析、红外光谱分析、差热热重同步分析以及单晶衍射分析等方法研究苦参碱铁锌2种金属配合物的结构表征,结果表明:苦参碱铁配合物分子式为C15H25Cl4FeN2O,正交晶系,空间群为P212121,为离子型配合物,苦参碱锌配合物分子式为C15H25Cl3N2OZn,单斜晶系,空间群为P2(1),为配位型配合物,它们都为1分子苦参碱与1分子金属离子配位形成。抑菌活性测试结果表明,苦参碱金属配合物的抑菌活性相较于配体明显提高。
配位型配合物红外光谱分析除连接原子键长以及峰位置发生改变外,对其他原子分析结果并无多大影响[21]。本研究发现苦参碱锌配合物的红外光谱除配体上羰基键长以及峰位置发生变化外,其他原子红外分析结果相较于配体基本一致,表明氯化锌可能直接与苦参碱羰基进行配位,此结果与田裕昌等[22]研究结果一致。金属与配体形成共轭体系,可能引起电子密度降低,红外光谱吸收谱带数目减少[23]。本试验中,苦参碱铁配合物红外光谱分析中发现其N-H和C-N谱带消失,表明苦参碱与氯化铁形成共轭体系,引起红外吸收谱带数目减少,此研究结果与陈镇东等[24]研究氮杂查耳酮类化合物形成共轭体系后红外光谱吸收谱带数目减少结果一致。
苦参碱金属配合物抑菌活性提高主要原因可能是苦参碱与金属离子协同作用的结果。本研究结果表明,在质量浓度为800 mg/L时,对番茄灰霉病菌,锌配合物的抑菌活性最好,其抑制率是配体的7.1倍。对小麦赤霉病菌,金属配合物的抑菌活性较配体相比都明显提高,其抑制率约为配体的3.3倍,其中铁配合物抑菌率最高,其次是锌配合物。对马铃薯晚疫病菌,配体与配合物都有一定的抑菌活性,其中锌配合物的活性最好,为95.2%。苦参碱金属配合物抑菌活性均高于配体,且随着质量浓度的升高有不同程度的增强,此研究结果与雷美康等[25]研究三唑类杀菌剂金属配合物抑菌活性均高于配体的结果类似。研究证实,金属配合物抑菌活性提高的原因是配合物的缓释功能以及配体与金属离子的协同作用结果[26-27]。苦参碱与金属配合后生物活性提高是否一定与苦参碱金属配合物缓释功能、以及苦参碱与金属离子协同作用有关,尚需深入研究。另外由于只对2 种苦参碱金属配合物进行室内离体抑菌活性研究,并未进行盆栽及小区试验,其田间试验数据是否与室内毒力测定结果一致,有待进一步研究。
参考文献Reference:
[1]郭明,伍周玲,王春歌,等.黄芩苷—金属配合物的合成及其抗肿瘤活性研究[J].药学学报,2014,49(3):337-345.
GUO M,WU ZH L,WANG CH G,etal.Synthesis and anti-tumor activity of Baicalin-metal complex[J].ActaPharmaceuticaSinica,2014,49(3):337-345.
[2]胡春燕,温世和,聂旭亮,等.烯唑醇配合物的合成,晶体结构与抑菌活性研究[J].江西农业大学学报,2015,37(1):73-78.
HU CH Y,WEN SH H,NIE X L,etal.Synthesis of Diniconazole complexes and their crystal structures and antibacterial activities[J].ActaAgriculturaeUniversitatisJiangxiensis,2015,37(1):73-78.
[3]刘文胜,罗维早,张志荣,等.中药研究的新学说—中药配位化学[J].华西药学杂志,2001,16(4):293-294.
LIU W SH,LUO W Z,ZHANG ZH R,etal.The new theory on research of traditional Chinese medicine coordination chemistry of traditional Chinese medicine[J].WestChinaJournalofPharmaceuticalSciences,2001,16(4):293-294.
[4]张雁冰,魏爱卿,李玲,等.河南马桑中氨基酸和微量元素的测定[J].郑州大学学报(理学版),2005,37(3):90-91.
ZHANG Y B,WEI A Q,LI L,etal.Determination of amino acids and trace elements fromCoriariasinicaMaxim in Henan[J].JouranalofZhengzhouUniversity(NaturalScienceEdition),2005,37(3):90-91.
[5]徐海珍,张欣,王瑾玲.1-苯基-3甲基-4-苯甲酰基-吡唑啉酮-5与Mn(Ⅱ)配合物的合成和晶体结构[J].应用化学,2003,20(3):250-253.
XU H ZH,ZHANG X,WANG J L.Synthesis and crystal structure of Mn(Ⅱ)complex of 1-phenyl-3-methyl-4-benzo-yl-pyra-z-olone-5[J].ChineseJournalofAppliedChemistry,2003,20(3):250-253.
[6]杨春龙,罗金香,谢学群,等.丙环唑配合物的合成、缓释性能及生物活性研究[J].无机化学学报,2007,23(7):1259-1263.
YANG CH L,LUO J X,XIE X Q,etal.Propiconazole complexes:synthesis,controlled release properties and biological activities[J].ChineseJournalInorganicChemistry,2007,23(7):1259-1263.
[7]KESKIOGLU E,GUNDUZALP A B,CETE S,etal.Cr(Ⅲ),Fe(Ⅲ) and Co(Ⅲ) complexes of tetradentate(ONNO) Schiff base ligands:synthesis,characterization,properties and biological activity[J].SpectrochimicaActaPartAMolecular&BiomolecularSpectroscopy,2008,70(3):634-640.
[8]李鹏程.一种新型低毒农作物杀菌剂的制备方法:ZL200410050480.9[P].2009-07-27.
LI P CH.The invention relates to a preparation method of a new type of low toxicity crop bactericide:ZL2004100-50480.9[P].2009-07-27.
[9]张庆霞,李秀丽,纪瑛,等.苦参根水浸液对黄瓜种子萌发和幼苗生长的影响[J].西北农业学报,2011,20(2):140-142.
ZHANG Q X,LI X L,JI Y,etal.Effects of water extract fromSophoraflavescensroots on germination and growth of Cucumissativus[J].ActaAgriculturaeBoreali-occidentalisSinica,2011,20(2):140-142.
[10]冯俊涛,石勇强,张兴. 56种植物抑菌活性筛选试验[J].西北农林科技大学学报(自然科学版),2001,29(2):13-14.
FENG J T,SHI Y Q,ZHANG X.Screening studies on fungistasis of 56 plant extracts[J].JournalofNorthwestA&FUniversity(NaturalScienceEdition),2001,29(2):13-14.
[11]张丽华,陈邦恩,潘明佳.苦参碱药理作用研究进展[J].中药,2009,40(6):1000-1003.
ZHANG L H,CHEN B E,PAN M J.Research progress on pharmacological action of matrine[J].ChineseTraditionalandHerbalDrugs,2009,40(6):1000-1003.
[12]ZHANG J Q,LI Y M,TAO L,etal.Antitumor effect of matrine in human hepatoma G2 cells by inducing apoptosis and au-tophagy[J].WorldJournalofGastroenterology,2010,16(34):4281.
[13]YU J L,LI J H,CHENG R G,etal.Effect of matrine on transforming growth factor β1 and hepatocyte growth factor in rat liver fibrosis model[J].AsianPacificJournalofTropicalMedicine,2014,7(5):390-393.
[14]郑永权,姚建仁,邵向东.苦参化学成分及农业应用研究概况[J].农药科学与管理,2000,21(1):17-18.
ZHENG Y Q,YAO J R,SHAO X D.Review on the constituents and agricultural application ofSophoraflavescensAit[J].PesticideScienceandAdmnistration,2000,21(1):17-18.
[15]郑永权,姚建仁,邵向东.苦参杀虫抑菌活性成分研究[J].农药学学报,1999,1(3):91-93.
ZHENG Y Q,YAO J R,SHAO X D.Study on bio-active compounds fromSophoraflavescensA it[J].ChineseJouranalofPesticideScience,1999,1(3):91-93.
[16]俞志刚,刘波,姜兆华.1-苯基-3-甲基-4-萘乙酰基-吡唑啉酮-5(PMNAP)缩2-氨基苯并咪唑(2-AB)席夫碱及其过渡金属配合物的合成、光谱表征与质谱鉴定[J].有机化学,2009,(8):1217-1222.
YU ZH G,LIU B,JIANG ZH H.Synthesis,characterization by spectra and identification by HPLC-MS of Schiff base derived from 1-phenyl-3-methyl-4-naphthyl-aceto-4,5-dihydropyrazol-5-one(PMNAP) and 2-aminobenz- imidazole(2-AB) and its t-ransitional metal complexes[J].ChineseJournalofOrganicChemistry,2009,(8):1217-1222.
[17]KOBASHI S,TAKIZAWA M,KUBO H,etal.Antinociceptive effects of N-acyloctahydropyrido[3,2,1-ij][1,6]naphthyridine in mice:structure-activity relation study of matrine-type alkaloids part Ⅱ[J].Biological&PharmaceuticalBulletin,2003,26(3):375-379.
[18]李凯,王君,蒋湘顺,等.金属-氨基多羧酸类配合物分子和晶体结构的研究(Ⅳ)--〔H_6edta〕〔V~Ⅲ(edta)(H2O)〕2·4H2合物的合成及结构测定[J].辽宁大学学报(自然科学版),1997,24(3):8-13.
LI K,WANG J,JIANG X SH,etal.Investigation on molecular and crystal structures of metal complexes with ami-nopolycarboxylic acids(Ⅳ )- synthesis and structure of 〔H6e d t a 〕〔V Ⅲ(e d t a )(H2O )〕2· 4H2O[J].Journa-lofLiaoningUniversity(NaturalSciencesEdition),1997,24(3):8-13.
[19]刘静,张丽丹,韩春英,等.含钕和铜的吡啶羧酸类配合物的合成和性能研究[J].北京化工大学学报(自然科学版),2013,12(1):37-40.
LIU J,ZHANG L D,HAN CH Y,etal.Synthesis and characterization of a neodymiun-copper(Ⅱ) coordination polymer w-ith 2,5-pyridinedicarboxylic acid[J].JournalofBeijingUniversityofChemicalTechnology(NaturalScience),2013,12(1):37-40.
[20]王德龙,冯俊涛,张兴.天名精内酯酮酯类衍生物的抑菌活性及构效关系初步分析[J].西北农业学报,2013,12(11):89-93.
WANG D L,FENG J T,ZHANG X.Antifungal activities of carabrone ester derivatives and preliminary analysis of structure activity relationship[J].ActaAgriculturaeBoreali-occidentalisSinica,2013,12(11):89-93.
[21]张培志,傅群英,池仁霞,等.三唑酮金属配合物的缓释作用[J].浙江科技学院学报,2003,15(3):143-145.
ZHANG P ZH,FU Q Y,CHI R X,etal.Triadime for metal complexes for controlled release[J].JournalofZhejiangUniversityofScienceandTechnology,2003,15(3):143-145.
[22]田裕昌,何雄,韦星船,等.分光光度法测定苦参碱配合物的组成[J].广州化工,2012,40(14):131-132.
TIAN Y CH,HE X,WEI X CH,etal.Determination of composition of matrine complexs by spectrophoto metry[J].GuangzhouChemicalIndustry,2012,40(14):131-132.
[23]周靖欣,焦体峰,李旭辉,等.新型偶氮苯共轭席夫碱化合物的合成与表征[J].广州化工,2011,39(1):10-12.
ZHOU J X,JIAO T F,LI X H,etal.Synthesis and characterization of new azobenzene conjugated schiff base compounds[J].GuangzhouChemicalIndustry,2011,39(1):10-12.
[24]陈镇东,吴养洁,尹孟本,等.三岔共轭体系中的结构效应(Ⅵ)——氮杂查耳酮类化合物红外光谱中的同系线性规律[J].高等学校化学学报,1980,5(1):67-72.
CHEN ZH D,WU Y J,YIN M B,etal.The structural effect in forked conjugative systems(Vl)-the rule of Homologous Linearity for I.R spectra of azachalcone compounds[J].ChemicalJournalofChineseUniversities,1980,5(1):67-72.
[25]雷美康,张培志,马中华,等.水-甲苯体系中三唑酮铜配合物的合成、表征及抑菌活性[J].农药,2008,47(5):337-338.
LEI M K,ZHANG P ZH,MA ZH H,etal.Synthesis,characterization and bactericidal activity of the complex of triadime for and copper chloride in water/toluene system[J].Agrochemicals,2008,47(5):337-338.
[26]YANG C L.Propiconazole complexes:synthesis,controlled release properties and biological activities[J].ChineseJournalofInorganicChemistry,2007,23(7):1259-1263.
[27]PRASAD B P,KANTAM M L,CHOUDRY B M,etal.New pesticide metal complexes for controlled release[J].PesticideScience,1990,28(2):157-165.
