HCFC-141b水合物蓄冷密度的测定
2018-04-04朱明贵孙志高李翠敏黄海峰
朱明贵,孙志高,李 娟,李翠敏,黄海峰
(苏州科技大学 环境科学与工程学院,江苏 苏州 215009)
蓄冷空调系统被广泛应用在绿色节能建筑中,一方面缓解了白天城市电网用电负荷,另一方面节约建筑高峰用电成本。常见的蓄冷方式主要有水蓄冷、冰蓄冷、共晶盐蓄冷等[1]。近年来,制冷剂水合物蓄冷逐渐步入人们的视野[2-6]。由于水合物蓄冷可以在零度以上储存相变潜热,水合物相变潜热与冰相当,克服了冰蓄冷系统中制冷机组运行效率低和水蓄冷密度低的缺点。利用水合物相变潜热来储存能量,关键在于其快速大量的生成。关于水合物蓄冷性能的研究大多集中在水合物相变潜热的测定与及其促进方法上。
蓄冷密度是水合物蓄冷的一个关键参数,其确定方法主要分为两大类。一类是计算法,依据实验测定的温度、压力等相平衡物性数据,由Clausius-Clapeyron方程计算获得[7-8]。另一类是实验测定法,主要有卡计法、差热法(DTA)、差示扫描量热法(DSC)等[9-13]。
课题组前期将正癸酸-十二醇复合相变材料添加到HCFC-141b水合物中,有效促进了水合物的生成[14]。文中利用混合量热法[15-16]测量HCFC-141b乳液体系中形成的水合物蓄冷密度,研究了复合相变材料、吐温80对水合物蓄冷密度的影响。
1 试验研究
1.1 试验材料及装置
试验材料包括:HCFC-141b,购置于浙江中龙制冷剂有限公司,纯度≥99.5%;有机相变材料正癸酸(CA)和十二醇(DE),均购置于天津市光复精细化工研究所,分析纯;吐温80,无锡市晶科化工有限公司生产;蒸馏水,试验室自制。试验装置主要由高低温交变试验箱、反应容器、真空保温瓶、数据采集器、计算机、温度传感器等组成,如图1所示。高低温交变试验箱用于控制试验温度,温控范围-40~150℃,控制精度±0.1℃。反应容器为长10 cm、直径25 mm的玻璃试管。温度传感器为T型热电偶,记录水合物反应体系和水温度变化,测量精度为Ⅰ级。
1.2 试验过程
采用熔融共混法按质量比1∶1复配正癸酸和十二醇有机相变材料,获得相变温度为12℃左右的有机复合相变材料[14]。将一定量的蒸馏水、有机复合相变材料、吐温80加入到量杯中,用高速均质乳化机以10 000 r/min的速度搅拌10 min。随后将称取的HCFC-141b(按理想配比1∶2.62)慢慢地逐滴加入到量杯中继续搅拌10 min,制得乳白色液体。将乳液倒入反应器中,插入热电偶。设置空气浴初始温度为20℃,待温度平衡后设定温度为0℃并开启数据采集器,记录试验过程中体系温度的变化,获取水合物生成过程温度变化曲线,试验体系如表1所列。
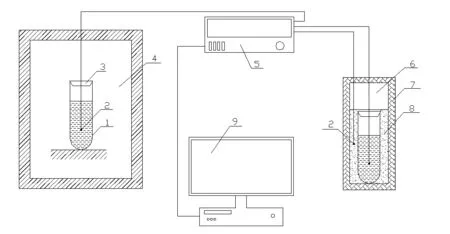
图1 试验装置
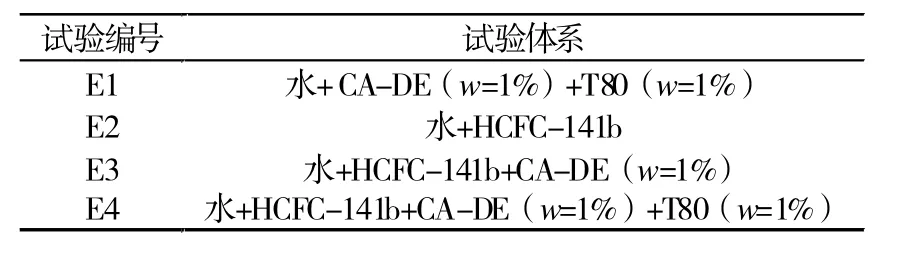
表1 试验体系
待水合物生成结束后重新设置空气浴温度为4℃左右,并稳定2~3 h,消除水合物形成过程中可能存在的冰的影响。称取适量的温水注入保温瓶中,插入热电偶,记录温度变化。由于HCFC-141b沸点为32℃,因此试验所选用的温水温度在20~25℃之间。将装有水合物的反应器快速放入保温瓶中,将保温瓶放入自制的保温箱中。水合物在温水的加热下逐渐分解,记录该过程中水及水合物体系的温度。
1.3 实验理论分析
水合物实际水合率很难直接测量,因此本试验在理想配比的基础上假设给定的HCFC-141b全部生成水合物,计算出单位质量水合物的蓄冷量。蓄冷量包括分解前水合物的温差显热、HCFC-141b水合物的相变潜热、分解后水和HCFC-141b的温差显热、吐温80的温差显热、有机相变材料的温差显热及其相变潜热。蓄冷量的计算公式为
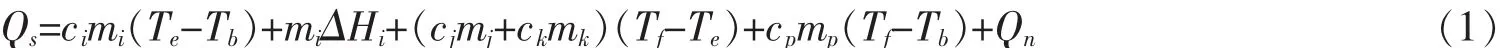
式中,Qs为蓄冷量,kJ;ΔHi为水合物潜热,kJ/kg;ci、cj、ck、cp分别为水合物、 水、HCFC-141b、 吐温 80 的比热容,kJ/(kg·℃);Tb、Te、Tf分别为水合物初始温度、水合物相变温度、水合物融化后平衡温度,℃。 mi、mj、mk、mp分别为水合物质量、水的质量、HCFC-141b质量、吐温80质量,kg;Qn为有机相变材料的总热量,kJ。由于吐温80和有机相变材料添加量只有1%,影响甚微,可以忽略。
温水放热量由公式(2)计算获得。

式中,Qh为温水放热量,kJ。 ch为常温水比热容,kJ/(kg·℃);mh为温水质量,kg;Th为温水初始温度,℃。
由能量守恒定律可得,温水降温所放出的热量等于水合物体系、玻璃试管、轻质硅胶塞获得的热量及混合过程的热损失的和。

式中:Qh为温水放热量,kJ。 cb为玻璃比热容,kJ/(kg·℃);mb为玻璃试管质量,kg。 QL为常温水与水合物混合过程中的能量损失,kJ,Qw为硅胶塞吸收的热量,kJ。由于保温瓶保温性能良好,且外置保温箱,在短时间内,混合过程中体系损失热量很小,可以忽略。轻质硅胶塞所吸收的热量也可以忽略。由式(1)和式(3)可以计算出水合物相变潜热ΔHi。
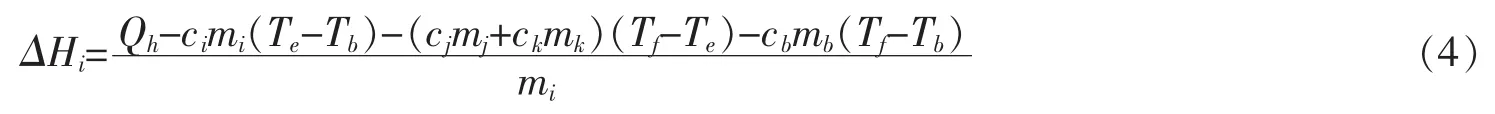
2 试验结果与分析
2.1 验证性试验
上述分析中忽略了硅胶塞、吐温80、有机相变材料的吸热及损失热,通过测量冰的相变潜热对该方法进行验证。称取一定量的水、吐温80和有机相变材料倒入反应器中,置于高低温交变试验箱中,设置空气浴温度为-5℃左右。待冰生成完全后,将反应器放入装有温水的保温瓶中,进行E1试验并记录温度变化。表2列出了冰融化潜热的计算参数和结果,发现计算值均略小于理论值335 kJ/kg,一方面在低温反应体系快速置入温水过程中,从环境吸收了部分热量,另一方面由于最后的平衡温度低于环境温度,后期静态条件下温水与反应体系温度平衡时间长,也会导致体系从环境中吸收部分热量,最后导致平衡温度略大于理论值。
试验所测得冰的相变潜热与理论值的平均相对误差为2.45%,且都在5%以内,证明了试验分析方法是可行的,可以用于测量HCFC-141b水合物的相变潜热。
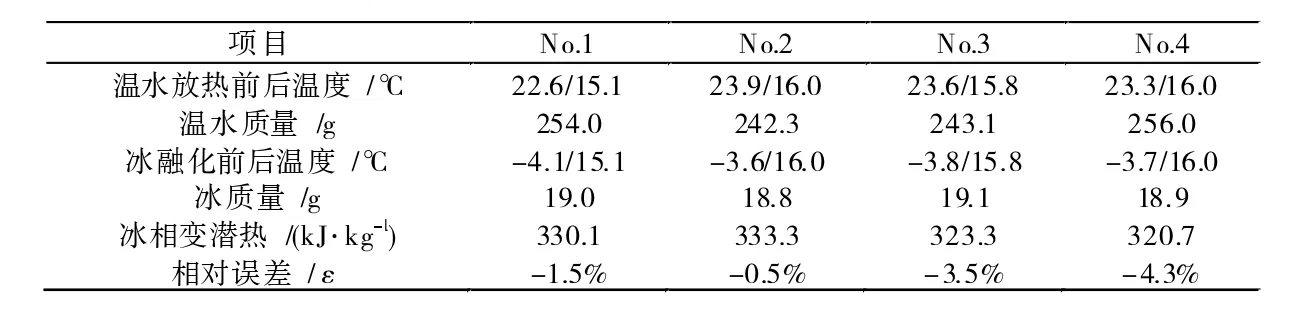
表2 冰融化潜热的计算参数与结果
2.2 水合物蓄冷量
2.2.1 纯水体系中HCFC-141b水合物蓄冷量
表3列出了三组试验体系E2的水合物蓄冷密度,平均蓄冷密度为57.8 kJ/kg。可以看出其蓄冷密度远远低于其相变潜热344 kJ/kg。这是由于单一的HCFC-141b与水是不容的,密度较大的HCFC-141b相沉降在水相下面,它们只在两相的交界面接触,因此,其反应生成的水合物量少,水合物蓄冷密度低。对于试验编号No.2,温度在1.8~17.3℃且同等质量条件下,纯水的蓄冷量计算为1.34 kJ,而试验体系的蓄冷量(反应物显热和潜热之和)仅为1.54 kJ,可见静态纯水体系中HCFC-141b水合物蓄冷优势并不明显。
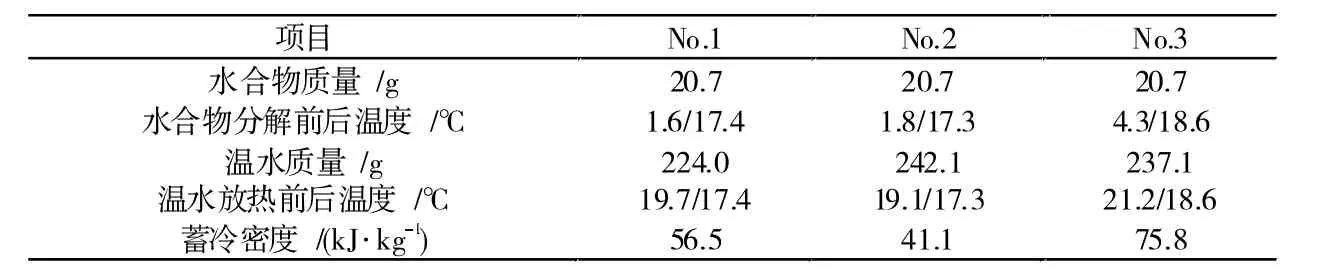
表3 纯水体系下水合物蓄冷密度的计算参数和结果

图2 温水与水合物温度变化曲线
2.2.2 有机相变材料对HCFC-141b水合物蓄冷量的影响
图2是添加有机相变材料试验体系E3体系水合物溶解过程温度变化曲线。起初水合物温度快速上升,HCFC-141b水合物从温水中吸收热量,此过程为水合物的显热换热,反应后体系仍为固态。当温度达到8℃左右时,温度曲线变的平缓,此时HCFC-141b水合物由固相转变为液相并不断溶解,吸收大量的热量,温度基本稳定不变。待水合物完全溶解后,反应体系又变为显热换热,试验体系的温度快速上升。当温水温度和试验体系介质的温度相近时,由于温差变小,能量传递驱动力变小,热量传递速度降低,最终达到平衡。表4为水合物融化潜热的测量结果,试验体系E3的HCFC-141b水合物平均蓄冷密度约为201 kJ/kg,远高于纯水体系中水合物的蓄冷密度。这是由于相变材料降低了体系的表面张力,增加了HCFC-141b与水的接触面积,水合反应得以充分进行。
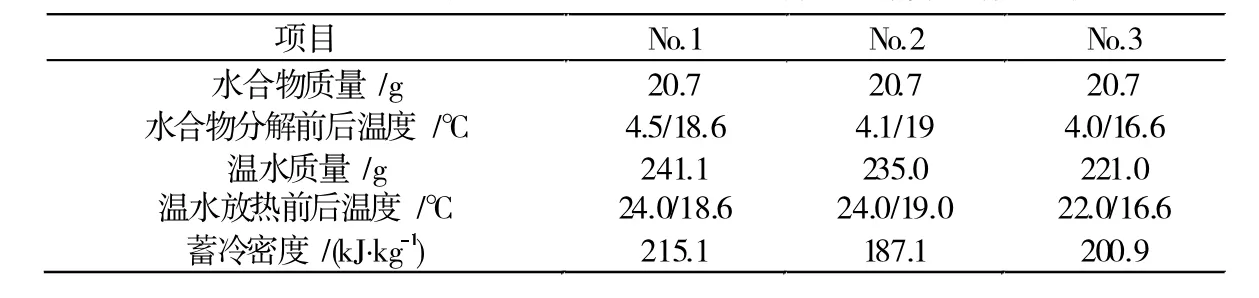
表4 有机相变材料作用下水合物蓄冷密度的计算参数和结果
2.2.3 有机相变材料与吐温80协同作用对HCFC-141b水合物蓄冷量的影响
表5列出了试验体系E4融化潜热的测量结果,平均蓄冷密度为268.1 kJ/kg,较只添加CA-DE的水合体系蓄冷密度提高了19.5%,而且三次测量结果相差不大。可以看出在添加了有机相变材料的基础上再添加吐温80能更好的促进两相的融合,增加水合物生成量,减小水合物形成的随机性。图3是三组不同体系HCFC-141b水合物形成温度曲线。HCFC-141b乳液体系局部发生相变时,会诱导整个体系快速相变,温度快速升高。纯水体系E2水合物温升最高点只有3℃,且生成时间长,诱导时间长达105 min。只添加有机相变材料的体系温升能够达到7.3℃;有机相变材料与吐温80协同作用下,反应体系的温升最高,达到7.7℃并维持较久的生长时间。可见有机相变材料和吐温80协同作用能有效提高水合体系中水合物的生成量。

图3 HCFC-141b水合物生成过程
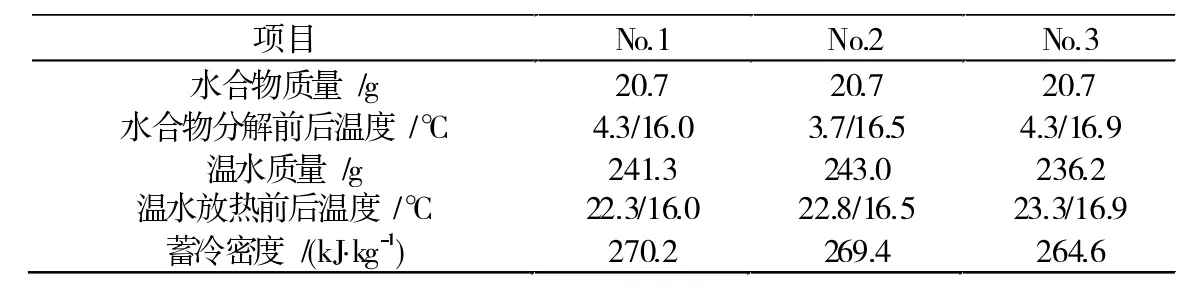
表5 复合相变材料与吐温80协同作用下水合物蓄冷密度的计算结果
3 结论
利用混合量热法测量并计算了HCFC-141b水合物蓄冷密度,分析了有机相变材料和吐温80对水合物蓄冷密度的影响,具体结论如下。
(1)纯水体系中水合物生成量少,蓄冷密度低,对比水蓄冷无明显优势。
(2)有机相变材料能够提高HCFC-141b的蓄冷量,平均蓄冷密度可达201 kJ/kg,乳液体系能够增大制冷剂与水的接触面积,促进水合物形成,提高水合物的蓄冷密度。
(3)有机相变材料与吐温80协同作用,能够在仅添加有机相变材料的基础上提高19.5%的蓄冷量,进一步提高了水合物蓄冷密度。
(4)有机相变材料能够有效缩短HCFC-141b水合物形成的诱导时间,与吐温80协同作用可以降低水合物生成量的随机性。
参考文献:
[1]李欣笑,杨东哲,石鹤,等.基于全年负荷模拟和空调日负荷预测控制策略的冰蓄冷系统可行性研究[J].暖通空调,2015(10):91-96.
[2]叶楠,张鹏.TBAB水合物晶体生长过程的实验研究[J].过程工程学报,2011,11(5):823-827.
[3]马鸿凯,孙志高,焦丽君,等.添加剂对静态条件下HCFC-141b水合物生成的促进作用[J].制冷学报,2016,37(1):101-105.
[4]FATEMEH N, AMIR A I,FARSHAD V,et al.Thermodynamic modeling of hydrate dissociation conditions for refrigerants R-134a,R141b and R-152a[J].International Journal of Refrigeration,2012,35(7):1914-1920.
[5]李刚,谢应明,刘道平,等.四丁基溴化铵-四氢呋喃系蓄冷水合物[J].过程工程学报,2009,9(1):186-189.
[6]LI Jingping,LIANG Deqing,GUO Kaihua,et al.Formation and dissociation of HCFC134a gas hydrate in nano-cupper suspension[J].Conversion and Management,2006,47(2):201-210.
[7]胡亚飞,蔡晶,徐纯刚,等.气体水合物相变热研究进展[J].化工进展,2016,35(7):2021-2032.
[8]DIMITRIOS A,NIKOS V.Modelling gas hydrate thermodynamic behaviour:theoretical basis and computational methods[J].Fluid Phase Equilibria,1996,123(1/2):107-130.
[9]SUM A K,KOH C A,SLOAN E D.Clathrate hydrate:from laboratory science to engineering practice[J].Industrial and Enginering Chemistry Research,2009,48(16):7457-7465.
[10]梁德青,郭开华,樊栓狮,等.HCFC-141b气体水合物融解热的DSC测试[J].工程热物理学报,2002,23(s1):49-51.
[11]波普,尤德.差热分析:DTA技术及其应用指导[M].北京:北京师范大学出版社,1982.
[12]孙志高.气体水合物相平衡及储气特性研究[D].上海:上海交通大学,2002.
[13]梁德青.新型蓄冷介质制冷剂气体水合物相平衡热力学研究[D].上海:上海交通大学,2001.
[14]朱明贵,孙志高,杨明明,等.有机相变材料促进HCFC-141b水合物生成实验[J].化工进展,2017,36(4):1265-1269.
[15]张龙名,李璞,李娜,等.混合量热法测定水合物浆体蓄冷密度[J].制冷学报,2014,35(6):47-52.
[16]李成浩,孙志高,张爱军,等.乳液浆体蓄冷性能实验研究[J].制冷学报,2016,37(6):66-70.
