不同原料生物炭对铵态氮的吸附性能研究
2018-03-26宋婷婷王知文杨殿林居学海张贵龙
宋婷婷 ,赖 欣 ,王知文 ,方 明 ,杨殿林 ,居学海 ,李 洁 *,张贵龙 *
(1.沈阳农业大学植物保护学院,沈阳 110866;2.农业部环境保护科研监测所,天津 300191;3.东北农业大学资源与环境学院,哈尔滨 150030;4.农业部农业生态与资源保护总站,北京 100125)
生物炭(Biochar)是由作物秸秆、木屑等生物质材料,经高温热解而产生的一类富碳的固态物质,是黑炭范畴的一种,一般呈碱性[1],具有比表面积大、孔隙度高[2-3]和离子交换量大[4]等特性,对水体、土壤无机离子[5]及有机污染物等具有一定的吸附能力。研究表明,玉米穗轴制备的生物炭能够有效吸附溶液铵态氮(NH+4-N),最大吸附量达 22.6 mg·g-1[6]。Kizito 等[7]研究发现,稻壳生物炭和木屑生物炭对猪场粪便发酵液中NH+4-N具有较大的吸附作用,最大吸附量分别为39.80、44.60 mg·g-1。关于生物炭对NH+4-N的吸附机制,有研究认为,生物炭表面含氧官能团和pH值是影响其NH+4-N吸附量的主要因素,新制备的生物炭对NH+4-N具有较低的吸附能力,经过一段时间氧化或通过氧化剂处理能够显著增加吸附能力[8]。低pH值(3.6~7)的生物炭对NH+4-N的吸附能力较低,当pH值增加到7时,吸附量增加2~3倍[9],李卓瑞等[10]研究证实竹炭通过阳离子交换作用吸附铵离子。王章鸿等[11]对橡木生物炭的研究表明,比表面积、表面碱性官能团和表面氧化物与氨态氮吸附有关。生物炭的制备原料分布广泛,其性能因制备原料不同而异。Kizito等[12]通过固定床柱试验表明硬木屑生物炭对污水NH+4-N的吸附能力较玉米穗轴生物炭和混合木屑生物炭大,且吸附量随NH+4-N浓度升高而增加。常温下(25℃)秸秆生物炭对铵离子的吸附能力约为竹炭的4倍,主要是秸秆炭表面孔隙的平均孔径大于竹炭,对四面体结构的铵根离子吸附的空间位阻较小,导致其对铵离子的吸附容量较大[13]。生物炭的制备原料决定其孔隙度、表面官能团分布、灰分元素及pH值等性质,而对NH+4-N的吸附多与其自身性质有关,因此,不同原料生物炭对NH+4-N的吸附能力不尽相同,对比研究不同原料生物炭对NH+4-N吸附作用,筛选高性能NH+4-N吸附材料,对于削减水体NH+4-N负荷和阻控土壤NH+4-N流失具有积极意义。
本研究以花生壳、玉米秆、杨木屑及竹屑为原料分别制取生物炭,利用电镜扫描(SEM)和傅立叶红外光谱(FTIR)分析技术,结合生物炭对铵态氮(NH+4-N)的固液相批量吸附试验,观察四种原料生物炭对NH+4-N的吸附特征,解析生物炭对NH+4-N吸附过程及行为,对比研究不同原料生物炭对NH+4-N的吸附能力,为筛选制备高效NH+4-N吸附炭基材料提供理论依据。
1 材料与方法
1.1 试验材料
1.1.1 生物炭的制备
本试验以玉米秆、花生壳、杨木屑、竹屑四种生物质为原料。收集玉米秆、花生壳、杨木屑及竹屑风干、粉碎、研磨过20目筛,在500℃下制取生物炭。具体的操作过程:启动温度为60℃,以8℃·min-1幅度升温至500℃,保持120 min,然后保持通N2状态冷却至室温,冷却后,将生物炭研磨过100目筛,干燥保存备用,不同材料制备生物炭的基本组分等分析如表1所示。
1.1.2 吸附溶液配制
常温状态下将硫酸铵[(NH4)2SO4]溶解于去离子水中,配制1000 mg·L-1的母液,然后将母液稀释为所需的不同浓度。
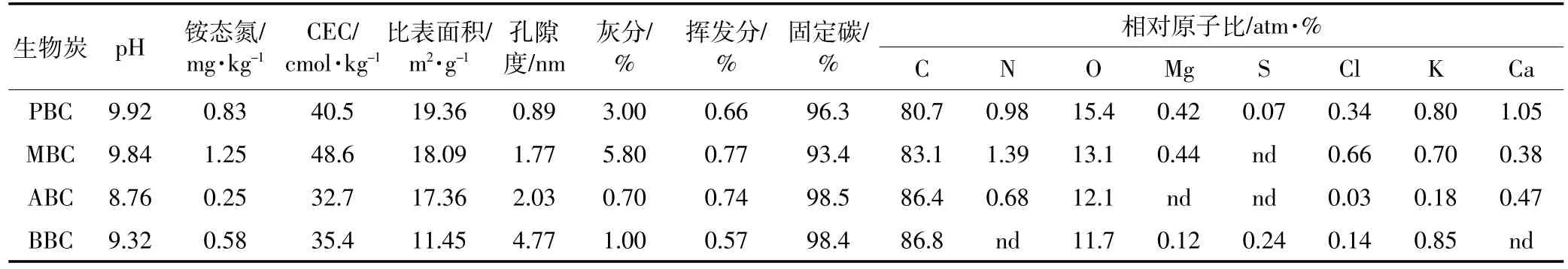
表1 生物炭组分分析和化学性质Table 1 The proximate analysis and chemical properties of biochar
1.2 测定方法
pH测定参考GB/T 12496.7—1999;阳离子交换量采用火焰分光光度计进行测定;生物炭的比表面积、孔径采用比表面积分析仪测定;灰分含量测定采用缓慢灰化法,参照GB/T 17664—1999;挥发分的测定参照GB/T 2001—1991;固定碳的计算方法为固定碳(%)=100-灰分-挥发分;采用X射线光电子能谱(XPS)测定生物炭相对原子含量(%)。
傅里叶变化红外光谱分析(FITR):用傅里叶变换红外光谱仪(Nicolet 380,Nicolet Corp,美国)测定生物炭的红外光谱,采用KBr压片制样,扫描波数范围为 400~4500 cm-1。
扫面电镜图(SEM):采用TM-1000型扫描电镜(HIECH Corp,中国台湾),冷场发射式,观察生物炭样品的大小、形状和表面特征。
溶液铵态氮(NH+4-N)浓度采用全自动连续流动分析仪(AA3,Bran+Luebbe Corp,德国)测定。
1.3 试验设计
1.3.1 吸附最适pH值确定试验
称取0.2 g制备好的四种不同生物炭分别放入100 mL的塑料瓶中,用HCl/NaOH调节50 mL的50 mg·L-1NH+4-N 溶液 pH 分别为 2.00、3.00、4.00、5.00、6.00、7.00、8.00、9.00、10.00、11.00、12.00,混合后的溶液在25℃、200 r·min-1的恒温振荡器中振荡24 h,静置,过滤,流动分析仪测定溶液中NH+4-N浓度,每个处理重复4次。根据公式(1)计算出单位质量生物炭对NH+4-N的吸附量:

式中:qe为单位质量生物炭对NH+4-N的吸附量,mg·g-1;C0为溶液中 NH+4-N 的起始浓度,mg·L-1;Ce为吸附平衡时液相中NH+4-N的浓度,mg·L-1;V为吸附平衡溶液的体积,L;m为生物炭的加入量,g。
1.3.2 生物炭等电位点的测定
向100 mL的塑料瓶中加入50 mL NaCl(0.1 mol·L-1)溶液,用HCl/NaOH调节pH值在2~12之间,用N2吹脱3~5 min以去掉溶解在溶液中的CO2,此时的pH记作pH0,将0.2 g四种不同生物炭分别加入瓶中,振荡24 h,测定上清液pH值,记作pHf,分别以(pH0-pHf)为纵坐标,pH0为横坐标,其中 pH0-pHf=0即为等电点,记作pHpzc。
1.3.3 动力学吸附测定
取50 mL 800 mg·L-1的NH+4-N溶液,分别加入玉米秸秆、花生壳、杨木屑、竹屑四种生物炭0.2 g,恒温振荡,吸附试验的条件为温度(25±0.5)℃,pH值7.00。分别于 5、10、20、30、40、50、60、90、120、180 min取出样品,过滤后测定滤液中NH+4-N浓度,每个处理重复4次。分别利用准一级动力学方程、准二级动力学方程、Elovich方程和离子扩散方程对实验数据进行拟合,分析生物炭吸附NH+4-N的时间与吸附量之间的关系,推断吸附反应机制:
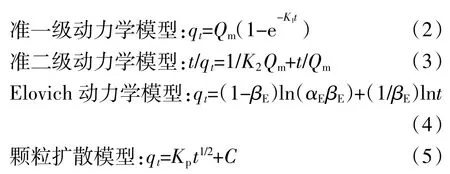
式中:qt为t时刻生物炭吸附NH+4-N的吸附量,mg·g-1;Qm为吸附状态达到平衡时生物炭吸附NH+4-N的吸附量,mg·g-1;K1、K2和 Kp分别是准一级吸附、准二级吸附和颗粒内扩散速率常数;αE为初始吸附速率常数;βE为解吸附速率常数。
1.3.4 吸附等温线测定
称取四种生物炭各0.2 g于不同的100 mL塑料瓶 中,分别 加 入 20、40、60、80、100、200、400、600、800、1000 mg·L-1不同浓度的(NH4)2SO4溶液 50 mL,用HCl/NaOH调节溶液pH=7.00±0.3,每个处理4次重复,混合后的溶液在25℃、200 r·min-1的恒温振荡器中振荡24 h,静置,过滤,流动分析仪测定溶液中NH+4-N的溶度。按公式(1)计算出单位质量生物炭对NH+4-N的吸附量,根据计算出的结果,分别用Langmuir模型[14,16]和 Freundlich 模型[15]对数据进行拟合。
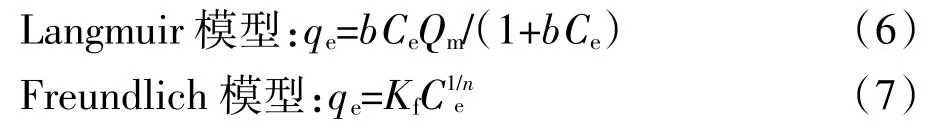
式中:qe为单位质量生物炭对NH+4-N的吸附量,mg·g-1;Ce为吸附平衡时液相中 NH+4-N 的浓度,mg·L-1;b为吸附平衡常数,L·g-1;Kf、n为吸附过程的经验系数;Qm为达到平衡时生物炭吸附NH+4-N的吸附量,mg·g-1。
1.4 数据处理与分析
数据处理以及表格的绘制采用Microsoft Excel 2010,图表的制作采用Origin 9.1和OMNIC。
2 结果与分析
2.1 吸附前后扫描电镜图
采用扫描电镜对四种生物炭吸附NH+4-N前、后的微观结构进行表征(图1)。吸附NH+4-N前,四种生物炭表面均存在明显的孔隙结构,表面粗糙、凹凸不平,其中,杨木屑生物炭(图1c)表面的孔隙大且密集,花生壳生物炭(图1a)次之,再次是玉米秸秆生物炭(图1b),最后是竹屑生物炭(图1d)且其表面近乎没有孔隙,这种明显的差异可能与原料本身性质有关。吸附后生物炭表面附着颗粒或粉末物质,孔隙被填充,表面变得较为平坦,由图可更加直观地看出生物炭吸附NH+4-N后的状态。
2.2 吸附前后傅里叶红外光谱图

图1 不同原料生物炭对NH+4-N吸附前后扫描电镜图(×2000倍)Figure 1 SEM(×2000 times)before and after NH+4-N adsorption of different raw materials
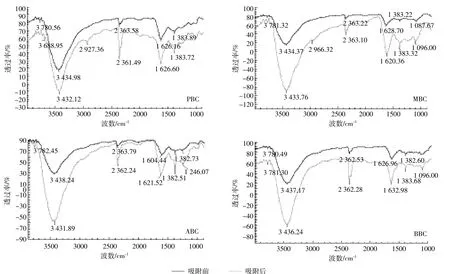
图2 不同原料生物炭对NH+4-N吸附前后的FT-IR谱图Figure 2 FT-IR spectra of NH+4-N before and after adsorption of biochar on different raw materials
由图2可知,四种原料生物炭吸附NH+4-N前后出峰的位置大致相同,表明它们所含有的官能团类似。3800~3156 cm-1范围吸收峰主要由分子间氢键缔合的-OH伸缩振动引起的[17],四种生物炭均在该范围内出现了吸收峰,且吸附后峰值减小,出峰位置发生了蓝移,峰形变窄,表明生物炭表面的羟基(-OH)均参与了对NH+4-N的吸附。1628 cm-1左右的吸收峰为芳香环羰基(-C=O)的伸缩振动[17],四种生物炭吸附后波峰明显变窄,说明生物炭表面-C=O参与了吸附。波数为1383 cm-1左右出现的吸收峰为醇或酚中(-C-O)的伸缩振动,吸附后,四种生物炭吸收峰强度都变弱,波峰变窄,说明该基团也参与了对NH+4-N的吸附。
PBC和MBC在2927、2966 cm-1处出现吸收峰,此处是由脂肪烃或者环烷烃中的甲基(-CH3)和亚甲基(-CH2)伸缩振动产生[17],而ABC和BBC在此处基本看不到峰,说明PBC和MBC中的甲基和亚甲基同时参与了吸附过程。1300~1000 cm-1为醇类羟基(-OH)的弯曲振动和醚类(-O-)的伸缩振动[17],图中仅BBC吸附后波峰发生了偏移,说明BBC表面的醇羟基或者醚类等活性基团参与了吸附,而PBC、MBC和ABC表面的醇羟基或者醚类基没有参与NH+4-N吸附过程。
2.3 pH值对不同原料生物炭吸附效果的影响
随溶液pH值逐渐升高,PBC、MBC、ABC和BBC四种原料生物炭对NH+4-N的吸附量呈逐渐增加趋势(图3)。当溶液pH<4时,四种生物炭对NH+4-N的吸附量随pH上升大幅度增加,当溶液在pH4~8时,四种生物炭对NH+4-N的吸附量变化趋于平缓,不再显著增加。当pH>8时,生物炭对NH+4-N的吸附量又呈现快速增加趋势。由四种生物炭零电荷点测定曲线可知,四种生物炭的pHpzc范围在5.50~6.50,即该pH范围内生物炭表面正负电荷近乎相等,超过该范围,说明生物炭表面呈负电,有利于吸附溶液中NH+4-N等阳离子(图4)。
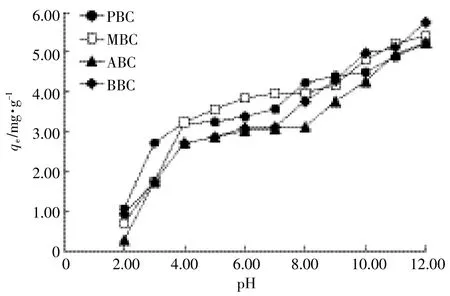
图3 不同原料生物炭在初始pH值梯度下对NH+4-N的吸附Figure 3 Adsorption of NH+4-N of biochar from different raw materials at different pH gradients
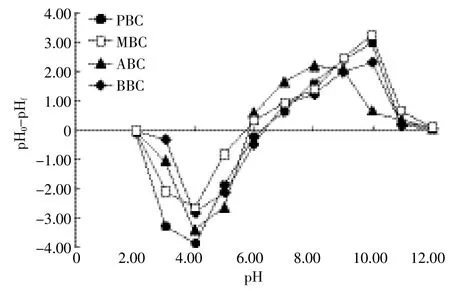
图4 不同原料生物炭的零电荷点测定曲线Figure 4 Point of zero surface charge of biochar from different raw materials
2.4 不同原料生物炭对NH+4-N的动力学吸附特征
由图5可知,四种原料生物炭在溶液初始浓度为800 mg·L-1的体系中,在20 min内吸附量快速增加,当超过20 min后,生物炭对NH+4-N的吸附量随着时间增加缓慢,当时间延长至50 min左右,生物炭对NH+4-N的吸附达到了最大饱和吸附,再随着时间的增加,吸附量并没有显著变化。用伪一级动力学方程、伪二级动力学方程、Elovich方程和颗粒内扩散模型对吸附数据进行拟合(表2),伪二级动力学方程拟合系数 R2为 0.978(PBC)、0.979(MBC)、0.998(ABC)、0.977(BBC),显著高于其他三个方程,并且Qm值与实际所测得值较为接近,因此伪二级动力学方程能够更好地描述生物炭对NH+4-N的动力学吸附过程。生物炭对NH+4-N的吸附可分为快速反应和慢速反应,根据伪二级动力学参数K2值进行判断,四种生物炭对NH+4-N的吸附主要是由快速反应所控制。
2.5 不同原料生物炭对NH+4-N的等温吸附特征
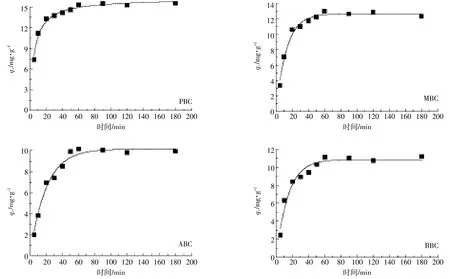
图5 不同原料生物炭对溶液中NH+4-N的动力学吸附线Figure 5 Kinetic adsorption lines of NH+4-N in solution of different raw materials biocar
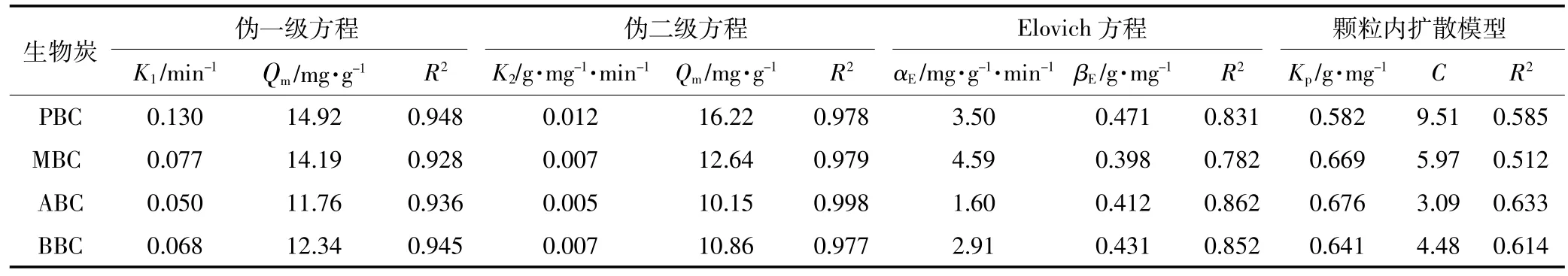
表2 NH+4-N在PBC、MBC、ABC、BBC上的动力学参数Table 2 Kinetic parameters of NH+4-N on PBC,MBC,ABC,BBC
图6为不同原料生物炭在各平衡浓度下对NH+4-N的等温吸附特征曲线。随溶液平衡浓度升高,四种原料生物炭对NH+4-N的吸附量呈逐渐增加趋势,当溶液浓度低于100 mg·L-1时,随着NH+4浓度的增加,生物炭对NH+4-N的吸附量上升幅度不明显,约为 1.5~6.4 mg·g-1,当溶液浓度大于 100 mg·L-1时,NH+4-N的吸附量呈现明显的上升,幅度为4.5~15.0 mg·g-1。当溶液 NH+4浓度接近 800 mg·L-1时,生物炭对NH+4-N的吸附量达到饱和,此时再增加溶液浓度,吸附量不再显著增加。其中PBC的饱和吸附量为15 mg·g-1,MBC 为 12.5 mg·g-1,ABC 为 9.5 mg·g-1,BBC为10.5 mg·g-1,四种生物炭对NH+4-N的吸附能力总体表现为 PBC>MBC>BBC>ABC。用 Langmuir模型和Freundlich模型方程分别对四种生物炭吸附NH+4-N的过程进行拟合,结果表明Langmuir模型能够更好地描述生物炭对NH+4-N的等温吸附行为(表3),由此可以判断生物炭对NH+4-N的吸附是以单分子层的化学吸附为主导。Freundlich模型对数据的拟合回归系数R2
F>0.950,达到了显著水平,且 n 值介于 1~10,说明吸附容易进行。由此说明,各生物炭对NH+4-N的吸附存在单分子层吸附的同时也存在多分子层吸附。
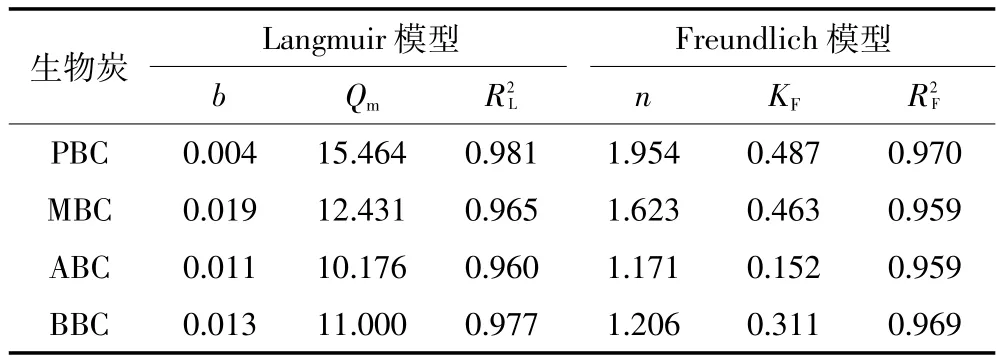
表3 NH+4-N在PBC、MBC、ABC、BBC上的等温吸附参数Table 3 Isothermal adsorption parameters of NH+4-N on PBC,MBC,ABC,BBC
3 讨论
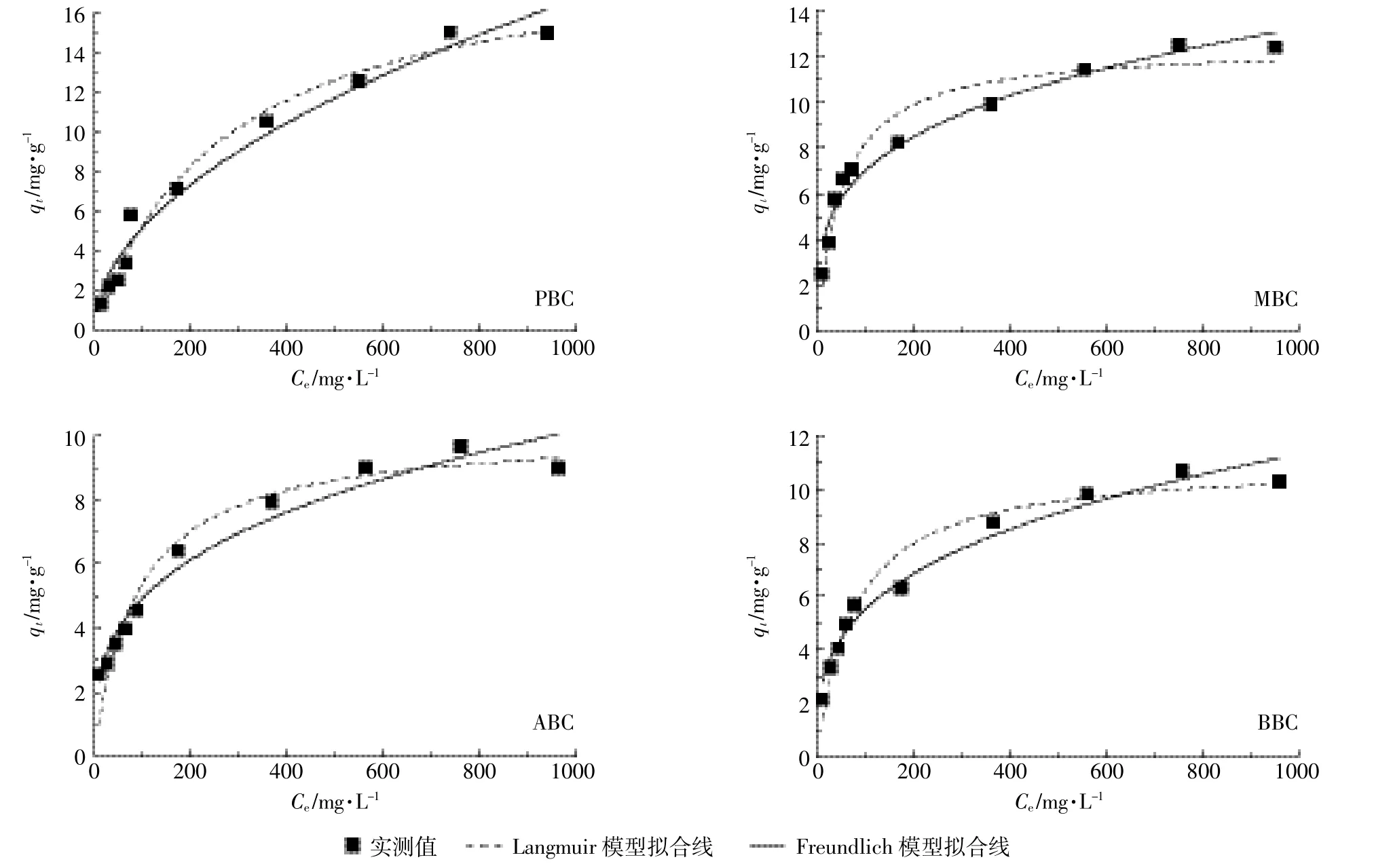
图6 不同原料生物炭对溶液中NH+4-N的等温吸附线Figure 6 The thermodynamic adsorption line of NH+4-N in the solution of different raw materials
扫描电镜图能够直观地表征NH+4-N在生物炭表面的累积,对比吸附前后扫描图可以明显的看出,四种原料生物炭吸附NH+4-N后,粗糙的表面变得平滑,表面沟槽被颗粒物质填充,原有孔隙基本上被堵塞。这样的吸附特征与Uchimiya等[18]研究结果相符。结合吸附前后的傅立叶红外光谱图,NH+4-N吸附前后3800~3156、1383、1300~1000 cm-1处的羟基吸收峰均发生了改变,说明四种生物炭表面的羟基官能团在对NH+4-N的吸附中都起到了主要作用。此外,除分布的-OH、-C=O等官能团,PBC和MBC表面分布的-CH3和-CH2,及BBC表面分布的-O-也参与了对溶液中NH+4-N的吸附。这些含氧官能团,可通过形成氢键[19-21]、氧化还原反应[22]以及离子电荷[23]等作用吸附溶液中的NH+4-N。Chen等[24]、徐楠楠等[25]研究结果显示,不同生物炭材料对NH+4-N的吸附作用基团不一样,可能与不同物质吸收强度不同有关。虽然本研究所用生物炭均为500℃高温下制备得到,但其电导率、孔隙度等理化特征均差异显著,其参与官能团也存在显著差异。PBC和MBC表面羰基、羧基、酚羟基及甲基、醚键等含氧官能团的加入可为生物炭表面提供更多的NH+4-N吸附点位,有利于吸附进行。
生物炭对NH+4-N的吸附也会受到溶液pH值和初始浓度的影响。邵明艳[26]研究指出,生物炭吸附NH+4-N的量随溶液pH升高而增加。溶液的pH不仅会影响生物炭表面的电荷性质,而且会影响吸附质的离子化程度及存在状态,生物炭表面具有较多的官能团,当溶液的pH较高时,表面的官能团会被去质子化,呈现负电,利于阳离子吸附。本研究进一步通过零电荷点测定曲线表明,在pH>7.00的条件下,pH溶液>pHpzc生物炭,此时生物炭表面呈负电,有利于吸附NH+4-N等阳离子。加之生物炭本身呈碱性,产生利于阳离子吸附的活性位点,从而提高了对NH+4-N等阳离子的吸附容量。本研究结果还显示,所用四种生物炭(PBC、MBC、ABC 和 BBC)对溶液中的 NH+4的吸附量都随着溶液浓度的增高而增大,当达到吸附平衡后(800 mg·L-1),吸附量不再随溶液浓度的增大而发生显著的变化,即吸附趋于饱和,该结果与翟由涛等[27]、Li等[28]相似。其机制在于,一定范围内,溶液浓度增大,物质传输驱动力更大,体系更有利于对NH+4-N的吸附,导致生物炭对NH+4-N的吸附均会随溶液浓度升高而逐渐升高[29]。
生物炭对NH+4-N的吸附在一定时间内会达到平衡,张扬等[30]研究表明生物炭对NH+4-N的吸附在60 min左右能达到吸附平衡,且与生物炭的基本理化性质有关。本研究四种生物炭达到吸附平衡的时间均为50 min左右,生物炭吸附离子达到平衡的时间与其物理化学性质有关,与生物炭表面分布的阳离子结合位点有关,结合位点多,达到吸附平衡的时间就短,反之,吸附时间就会变长。因此,伪二级动力学方程能够更好地描述生物炭对NH+4-N的动力学吸附过程,说明生物炭对NH+4-N的吸附速率主要由化学吸附决定[17]。
生物炭因其具有特殊的结构以及表面性质而对一些离子有吸附作用。生物炭对NH+4-N的吸附多数都符合准一级动力模型或者准二级动力模型[31-33],本研究四种生物炭对NH+4-N的吸附都符合准二级动力模型,说明四种生物炭对NH+4-N的吸附都是通过单分子层化学吸附作用实现。Thi等[34]通过改性玉米芯吸附水体中的NH+4-N,发现其吸附过程可以进一步用Langmuir方程进行描述,其吸附为单分子层的化学吸附,丛日环等[35]也有同样的结论。然而,Li等[28]研究发现,小麦秸秆生物炭对水体中NH+4-N的吸附可以用Freundlich模型更好地描述,认为吸附是非均一的多层物理吸附。本研究以PBC、MBC、ABC和BBC四种不同原料生物炭为研究对象,结果显示,四种生物炭对NH+4-N的吸附均符合Langmuir模型,即说明四种生物炭对NH+4-N的吸附均是由单分子层化学吸附为主导。结合SEM图和FTIR图谱,综合分析认为四种生物炭对NH+4-N吸附均是由表面所含有的官能团控制,尤其是含氧官能团的化学吸附占主导作用,而生物炭的孔隙结构并不是主要影响因素。Padhye等[36]和Chen等[37]也有类似的发现。
4 结论
(1)NH+4-N通过表面累积或孔道填充吸附于生物炭上。四种生物炭表面分布的含氧官能团(-OH、-C=O、-C-O)都参与了对NH+4-N的吸附,此外,PBC和 MBC 表面分布的甲基(-CH3)和亚甲基(-CH2),及BBC表面分布的醚类(-O-)也参与了对溶液中NH+4-N的吸附。
(2)Langmuir方程能够较好地描述四种原料生物炭对NH+4-N的等温吸附行为。伪二级动力学方程可以较好地描述四种生物炭对NH+4-N的动力学吸附过程,四种生物炭均在50 min内达到吸附平衡。四种原料生物炭对NH+4-N的吸附均为单分子层化学吸附,且由快速反应所控制。
(3)在溶液 pH=7.00、初始浓度为 800 mg·L-1的吸附体系中,四种生物炭对NH+4-N的吸附能力大小表现为PBC>MBC>BBC>ABC。PBC对NH+4-N的最大吸附量为 15 mg·g-1,MBC 为 12.5 mg·g-1,ABC 为 9.5 mg·g-1;BBC 为 10.5 mg·g-1。四种生物炭中吸附性最好的是花生壳生物炭(PBC)。
[1]Lehmann J,Joseph S.Biochar for environmental management:An introduction[M]//Lehmann J and Joseph S(Eds),Biochar for environmental management-science and technology.Earthscan Publisher,UK and USA,2009:1-9.
[2]Xie T,Reddy K R,Wang C W,et al.Characteristics and applications of biochar for environmental remediation:A review[J].Critical Review in Environmental Science and Technology,2015,45:939-969.
[3]Liang B,Lehmann J,Solomon D,et al.Black carbon increases cation exchange capacity in soils[J].Soil Science of America a Journal,2006,70(5):1719-1730.
[4]Gray M,Johnson M G,Dragila M I,et al.Water uptake in biochars:The roles of porosity and hydrophobicity[J].Biomass and Bioenergy,2014,61:196-205.
[5]Hale S E,Alling V,Martinsen V,et al.The sorption and desorption of phosphate-P,ammonium-N and nitrate-N in cacao shell and corn cob biochars[J].Chemosphere,2013,91(11):1612-1619.
[6]Manolikaki I,Mangolis A,Diamadopoulos E.The impact of biochars prepared from agricultural residues on phosphorus release and availability in two fertile soils[J].Journal of Environmental Management,2016,181:536-543.
[7]Kizito S,Wu S,KipkemoiKirui W,et al.Evaluation of slow pyrolyzed wood and rice husks biochar for adsorption of ammonium nitrogen from piggery manure anaerobic digestate slurry[J].Science of the Total Environment,2015,505:102-112.
[8]Yao Y,Gao B,Zhang M,et al.Effect of biochar amendment on sorption and leaching of nitrate,ammonium,and phosphate in a sandy soil[J].Chemosphere,2012,89(11):1467-1471.
[9]Bing W,Johannes L,Kelly H,et al.Adsorption and desorption of ammonium by maple wood biochar as a function of oxidation and pH[J].Chemosphere,2015,138:120-126.
[10]李卓瑞,韦高玲.不同生物炭添加量对土壤中氮磷淋溶损失的影响[J].生态环境学报,2016,25(2):333-338.LI Zhuo-rui,WEI Gao-ling.Effects of different biomass additions on leaching loss of nitrogen and phosphorus in soil[J].Journal of Eco-Environmental Science,2016,25(2):333-338.
[11]王章鸿,郭海艳,沈 飞,等.热解条件对生物炭性质氮和磷吸附性能的影响[J].环境科学学报,2015,35(9):2805-2812.WANG Zhang-hong,GUO Hai-yan,SHEN Fei,et al.Effects of pyrolysis conditions on nitrogen and phosphorus adsorption properties of biochar properties[J].Journal of Environmental Science,2015,35(9):2805-2812.
[12]Kizito S,Wu S B,Wandera S M,et al.Evaluation of ammonium adsorption in biochar-fixed beds for treatment of anaerobically digested swine slurry:Experimental optimization and modeling[J].Science of the Total Environment,2016,563(564):1095-1104.
[13]刘玉学,吕豪豪,石 岩,等.生物质炭对土壤养分淋溶的影响及潜在机理研究进展[J].应用生态学报,2015,26(1):304-310.LIU Yu-xue,LÜ Hao-hao,SHI Yan,et al.Effects of biomass coke on leaching of soil nutrients and its potential mechanism[J].Journal of Applied Ecology,2015,26(1):304-310.
[14]Chatterjee S,Woo S H.The removal of nitrate from aqueous solutions by chitosan hydrogel beads[J].Journal of Hazardous Materials,2009,164:1012-1018.
[15]Hameed B H,Daud F B M.Adsorption studies of basic dye on activated carbon derived from agricultural waste:Hevea brasiliensis seed coat[J].Chemical EngineeringJournal,2008,139:48-55.
[16]Demiral H,Gunduzoglu G.Removal of nitrate from aqueous solutions by activated carbon prepared from sugar beet bagasse[J].Bioresource Technology,2010,101(6):1675-1680.
[17]Xie T,Reddy K R.Characteristics and applications of biochar for environmental remediation:A review[J].Critical Review in Environmental Science and Technology,2015,45(9):939-969.
[18]Uchimiya M,Lima I M,Klasson K T,et a1.Immobilization of heavy metal ions(CuⅡ,CdⅡ,NiⅡ and PbⅡ)by broiler litter derived biochars in water and soil[J].Journal of Agricultural and Food Chemistry,2010,28(9):5538-5544.
[19]Bhatnagar A,Hogland W,Marques M,et al.An overview of the modification methods of activated carbon for its water treatment applications[J].Chemical EngineeringJournal,2013,219(3):499-511.
[20]Hale S E,Alling V,Martinsen V,et al.The sorption and desorption of phosphate-P,ammonium-N and nitrate-N in cacao shell and corn cob biochars[J].Chemosphere,2013,91(11):1612-1619.
[21]Trakal L,Veselská V,Safarík I,et al.Lead and cadmium sorption mechanisms on magnetically modified biochars[J].Bioresource Technology,2016,203:318-324.
[22]Sumaraj,Lokesh P,Padhye.Influence of surface chemistry of carbon materials on their interactions with inorganic nitrogen contaminants in soil and water[J].Chemosphere,2017,584:532-537.
[23]Saleh M E,Mahmoud A H,Rashad M.Peanut biochar as a stable adsorbent for removing NH+4-N from wastewater:A preliminary study[J].Advance Environmental Biology,2012,6(7):2170-2176.
[24]Chen B L,Zhou D D,Zhu L Z,et al.Sorption characteristics and mechanisms of organic contaminant to carbonaceous biosorbents in aqueous solution[J].Science in China Series B:Chemistry,2008,51(5):464-472.
[25]徐楠楠,林大松,徐应明,等.玉米秸秆生物炭对Cd2+的吸附特性及影响因素[J].农业环境科学学报,2014,33(5):958-964.XU Nan-nan,LIN Da-song,XU Ying-ming,et al.Adsorption characteristics and influencing factors of Cd2+from corn stalk[J].Journal of A-gro-Environment Science,2014,33(5):958-964.
[26]邵明艳.土壤中的无机氮与重金属的相互影响[J].科技信息,2009(35):875-878.SHAO Ming-yan.Interaction between inorganic nitrogen and heavy metals in soil[J].Technology Information,2009(35):875-878.
[27]翟由涛,杭小帅,干方群.改性高岭土对废水中磷的吸附性能及机理研究[J].土壤,2012,44(1):55-61.ZHAI You-tao,HANG Xiao-shuai,GAN Fang-qun.Study on adsorption performance and mechanism of phosphorus in wastewater by modified Gaolin[J].Soil,2012,44(1):55-61.
[28]Li J H,Lv G H,Bai W B,et al.Modification and use of biochar from wheat straw(Triticum aestivum L.)for nitrate and phosphate removal from water[J].Desalination and Water Treatment,2016,57(10):4681-4693.
[29]Gai X P,Wang H Y,Liu J,et al.Effects of feedstock and pyrolysis temperature on biochar adsorption of ammonium and nitrate[J].PLoS ONE,2014,9(12):e113888.
[30]张 扬,李子富,张 琳,等.改性玉米芯生物碳对氨氮的吸附特性[J].化工学报,2014,65(3):960-966.ZHANG Yang,LI Zi-fu,ZHANG Lin,et al.Adsorption characteristics of modified carbon corn bio-ammonia on ammonia nitrogen[J].Journal of Chemical Industry,2014,65(3):960-966.
[31]Ding Y,Liu Y X,Wu W X,et al.Evaluation of biochar effects on nitrogen retention and leaching in multi-layered soil columns[J].Water Air and Soil Pollution,2010,213(1/2/3/4):47-55.
[32]李瑞月,陈 德,李恋卿,等.不同作物秸秆生物炭对溶液中Pb2+、Cd2+的吸附[J].农业环境科学学报,2015,34(5):1001-1008.LI Rui-yue,CHEN De,LI Lian-qing,et al.The adsorption of Pb2+and Cd2+in solution by biochar of different crop straw[J].Journal of Agro-Environment Science,2015,34(5):1001-1008.
[33]Fuertes A B,Arbestain M C,Sevilla M,et al.Chemical and structural properties of carbonaceous products obtained by pyrolysis and hydrothermal carbonization of corn stover[J].Australian Journal of Soil Research,2010,48:618-626.
[34]Thi M V,Van T T,Dinh P D,et al.Removing ammonium from water using modified corncob-biochar[J].Science of the Total Environment,2017,579:612-619.
[35]丛日环,张 丽,鲁艳红,等.长期秸秆还田下土壤铵态氮的吸附解吸特征[J].植物营养与肥料学报,2017,23(2):380-388.CONG Ri-huan,ZHANG Li,LU Yan-hong,et al.Adsorption and desorption characteristics of ammonium nitrogen in soil under long-term straw returning to field[J].Journal of Plant Nutrition and Fertilizer,2017,23(2):380-388.
[36]Padhye L P,Wang P,Karanfil T,et al.Unexpected role of activated carbon in promoting transformation of secondary amines to N-Nitrosamines[J].Environmental Science and Technology,2010,44(11):4161-4168.
[37]Chen L,Chen X L,Zhou C H,et al.Environmental-friendly montmorillonite-biochar composites:Facile production and tunable adsorption-release of ammonium and phosphate[J].Journal of Cleaner Production,2017,156:648-659.
