西藏黑木耳的小鼠急性毒性实验研究
2018-03-18付珂周游王张
付珂,周游,王张
黑木耳(Auricularia auricula(L.ex hook.)Underw)使用历史悠久,营养价值极高,具有保健功能[1]。性平、味甘,能润肺清肠,具有益气强身、活血、止血等功效,也是中医治疗寒湿性腰痛的辅药[2]。其中西藏黑木耳又称莫若那布,目前收载于《中华藏本草》,子实体治肺虚咳嗽,脾虚泄泻[3]。主要含有黑色素、多糖、多酚和黄酮等多种活性成分[4],营养价值和药用价极高,在西藏林芝等地区使用甚广,从育种到栽培再到多样性分析都有深入的研究[5-7]。
目前未见西藏黑木耳急性毒性的公开报道,故根据国家食品药品监督管理局制定的《中药、天然药物急性毒性研究技术指导原则》(2005年)[8]开展相关研究,为后续开展量效关系、有效性、作用机制和血清药化、药代动力学等研究提供安全剂量范围参考。
1 材料与方法
1.1 试验药物
西藏黑木耳采自四川省甘孜藏族自治州理塘县下木拉乡上马岩村,经王张副研究员鉴定为Auricularia auricula(L.ex hook.) Underw;生理盐水(四川科伦药业股份有限公司,批号 L216090608)。
1.2 动物
昆明种小鼠,SPF级,雌雄各半,48只,体重20±2 g,由成都达硕实验动物有限公司提供,实验动物生产许可证号:SCXK(川)2015-030,《实验动物质量合格证》号:№ 51203500002809。实验前动物于室内适应环境饲养 3 d,室内温度(25±1)℃,自由饮水,喂食辐射灭菌维持饲料,实验动物使用许可证号SYXK(川)2014-124。
1.3 试剂
血常规测试用试剂:溶血剂(批号1708014)、稀释剂(批号1707022)和清洗剂(批号1708018)均来自江西特康科技有限公司。血液生化指标测试用试剂盒均来自上海特康科技有限公司,见表1。
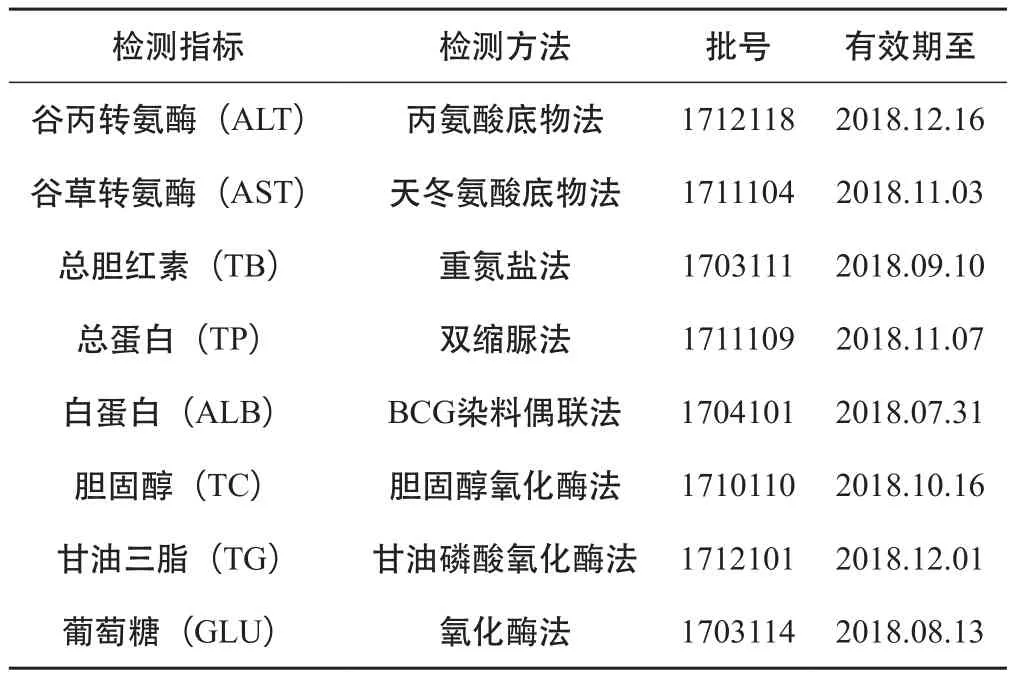
表1 血液生化指标测试用试剂盒情况
1.4 仪器
全自动三分群血液分析仪(型号TEK-Ⅱ MINI,江西特康科技有限公司生产);全自动生化分析仪(型号TC6010L,江西特康科技有限公司生产);电子称(BS-600L,上海有声衡器有限公司,量程为600 g,精确度为0.1 mg)。
1.5 实验方法
1.5.1 药液的配制 取西藏黑木耳,打粉,过80目药典筛,再转移至小烧杯中,加入生理盐水配制成浓稠混悬液, 并以灌胃针测试至吸取较难但不至于无法吸取的浓稠度为西藏黑木耳的最大浓度药液(0.3035 g﹒mL-1)。
1.5.2 预实验 取SD 小鼠20只,雌雄各半,给药前禁食不禁水12 h,灌胃给药西藏黑木耳浓稠混悬液1 次(给药体积为小鼠能够接受的最大容积40 mL﹒kg-1,浓度为0.3035 g﹒mL-1),连续观察2 d。结果小鼠状况良好,无动物死亡,无法计算西藏黑木耳的LD50,故正式实验以最大给药量法[9~11]进行西藏黑木耳的急性毒性实验。
1.5.3 正式试验 取SD小鼠40只,雌雄各半,按体重分层后再随机分为空白对照组和西藏黑木耳组,每组20只,雌雄各10只,给药前禁食不禁水12 h。空白对照组灌胃生理盐水, 西藏黑木耳组灌胃西藏黑木耳的最大浓度药液(0.3035g﹒mL-1),给药体积均为40 mL﹒kg-1[12],仅给药1次。连续观察14 d,观察记录小鼠的外观、分泌物、行为活动、自主活动、中毒症状及死亡情况等[13],同时在给药前1 d、给药当天、给药后第7 d和第14 d时, 观察和记录各组动物的体重变化及进食情况。第14 d处死小鼠前,观察未死亡动物的一般情况、天然孔道情况后,将动物眼球取血,每组其中10只,雌雄各半,取0.7~0.9 mL抗凝处理;每组另外10只,雌雄各半,取0.7~0.9 mL凝固后分离血清0.2~0.4 mL,立即送检,测试血常规和血生化指标[14]。
1.6 统计学方法
运用SPSS 19.0软件对实验数据进行处理,计量资料采用均数±标准差(±s)表示,组间比较采用t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 一般状况和尸检结果
30 min内两组小鼠普遍出现精神萎靡、行动迟缓,但均迅速恢复正常,饮食饮水正常,观察期内无动物死亡。此后连续14 d观察中均未见不良反应,其被毛、肤色、鼻、眼、口腔分泌物均未见异常;心血管系统、呼吸系统、运动功能、反射及痛觉未见异常,未见任何中毒症状,无动物死亡。第14 d解剖所有小鼠,内部脏器肉眼未见异常。
2.2 体重及饲料消耗量变化情况
西藏黑木耳经口一次性灌胃给予雌雄小鼠后14d内,雌雄小鼠的体重无明显变化;空白对照组和西藏黑木耳组小鼠的饲料消耗量均呈现先升高后降低的变化趋势,表明西藏黑木耳对饲料消耗量的自然变化没有影响。见表2~3。
表2 一次性灌胃给予西藏黑木耳后14 d 内小鼠体重的变化情况(g,±s)

表2 一次性灌胃给予西藏黑木耳后14 d 内小鼠体重的变化情况(g,±s)
注:与给药前1天比较,# P<0.05,## P<0.01;与空白对照组比较,* P<0.05,** P<0.01
组 别 性别 只数(只) 剂量(g﹒kg-1) 给药前1天 给药后第1天 给药后第7天 给药后第14天空白对照组 雄 10 —— 25.31±0.98 25.70±1.05 29.92±2.85## 32.00±1.04##雌10 —— 24.01±1.26 24.89±1.69 28.03±4.36# 27.42±1.83##西藏黑木耳组 雄 10 12.14 26.10±1.59 27.23±1.59 30.96±2.42## 33.02±1.79##雌10 12.14 24.14±1.60 24.54±1.75 25.89±1.57## 27.47±1.71##
表3 一次性灌胃给予西藏黑木耳后14 d 内小鼠饲料消耗量的情况[g﹒(kg﹒d)-1,±s]

表3 一次性灌胃给予西藏黑木耳后14 d 内小鼠饲料消耗量的情况[g﹒(kg﹒d)-1,±s]
注:与给药前1天比较,# P<0.05,## P<0.01;与空白对照组比较,* P<0.05,** P<0.01
组 别 性别 只数(只) 剂量(g﹒kg-1) 给药前1天 给药后第1天 给药后第7天 给药后第14天空白对照组 雄 10 —— 40.77±5.97 41.61±4.05 24.69±3.21 32.95±9.50雌10 —— 48.43±7.18 13.90±3.25# 29.50±7.67 32.50±6.07西藏黑木耳组 雄 10 12.14 36.83±6.59 49.20±3.40 32.41±7.53 27.19±0.09雌10 12.14 41.05±0.13 41.66±0.23** 28.01±19.49 24.92±0.82#
2.3 血常规
西藏黑木耳经口一次性灌胃给予小鼠后14 d,雄性小鼠的红细胞数、红细胞比积、血小板数、血小板比积、和血小板分布宽度明显增加(P<0.05或P<0.01),雄性小鼠的平均血红蛋白含量十分明显降低(P<0.01);其余各项血液学指标均无明显变化;此外,雌性小鼠的血液学指标亦无明显变化。见表4和5。
2.4 血液生化指标
西藏黑木耳经口一次性灌胃给予小鼠后14 d,雄性小鼠的甘油三酯含量十分明显降低(P<0.01);其余各项血液生化学指标均无明显变化;此外,雌性小鼠的血液生化学指标亦无明显变化。见表6。
2.5 组织病理学
肺脏、心脏、脾脏和肾脏均未见明显病理变化;肝脏、胃组织和脑组织可见轻度病变;脑组织神经细胞体积缩小、排列疏松:空白对照组(雄性和雌性亚组)、西藏黑木耳组(雄性亚组)的亚组均可见2~3例,由于该病变亦见空白对照组的动物,故推测与西藏黑木耳无关;胃粘膜腺体增生、炎症浸润,胃粘膜坏死,局部坏死脱落:空白对照组(雄性和雌性亚组)、西藏黑木耳组(雌性亚组)各有1例,推测与灌胃操作有关,而与西藏黑木耳无关;肝脏普遍都可见空泡变性和少量炎细胞浸润:推测可能和受试动物环境、饮食等因素有关,而与西藏黑木耳无关。总之,本次实验中未见由药物引起的明显的病理变化。
表4 一次性灌胃给予西藏黑木耳后大鼠的血常规测定结果Ⅰ(±s)
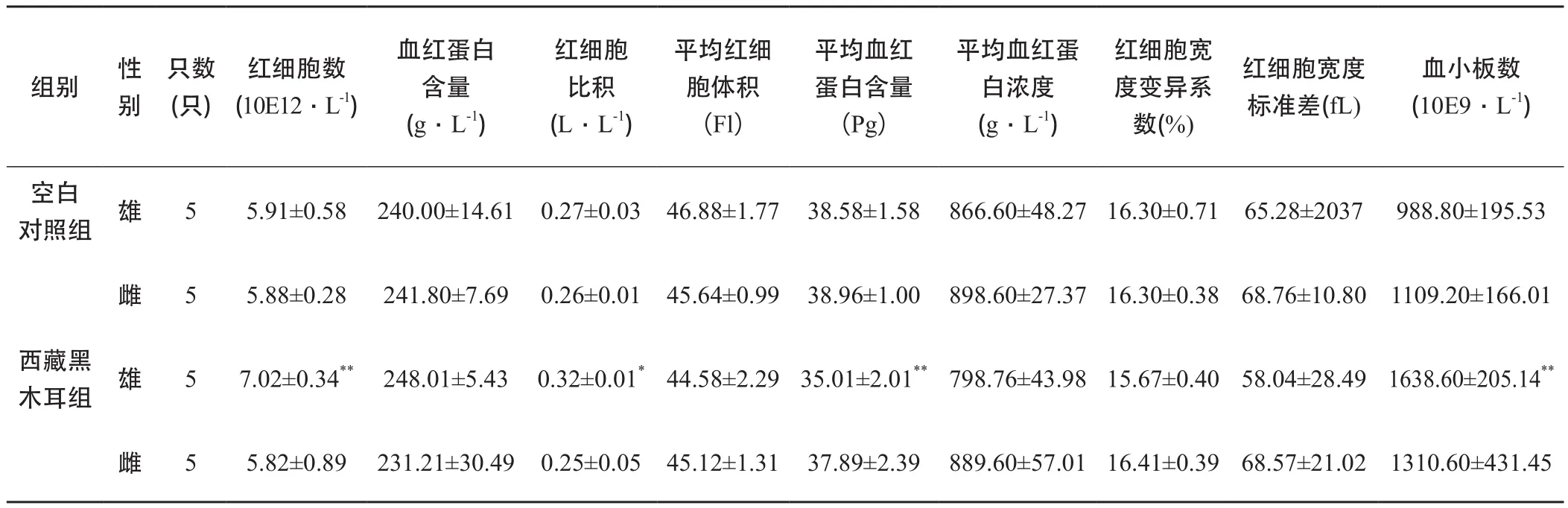
表4 一次性灌胃给予西藏黑木耳后大鼠的血常规测定结果Ⅰ(±s)
注:与空白对照组比较,* P<0.05,** P<0.01
组别 性别只数(只)红细胞数(10E12﹒L-1)血红蛋白含量(g﹒L-1)红细胞比积(L﹒L-1)平均红细胞体积(Fl)平均血红蛋白含量(Pg)平均血红蛋白浓度(g﹒L-1)红细胞宽度变异系数(%)红细胞宽度标准差(fL)血小板数(10E9﹒L-1)空白对照组 雄 5 5.91±0.58 240.00±14.61 0.27±0.03 46.88±1.77 38.58±1.58 866.60±48.27 16.30±0.71 65.28±2037 988.80±195.53雌 5 5.88±0.28 241.80±7.69 0.26±0.01 45.64±0.99 38.96±1.00 898.60±27.37 16.30±0.38 68.76±10.80 1109.20±166.01西藏黑木耳组 雄 5 7.02±0.34** 248.01±5.43 0.32±0.01*44.58±2.29 35.01±2.01**798.76±43.98 15.67±0.40 58.04±28.49 1638.60±205.14**雌 5 5.82±0.89 231.21±30.49 0.25±0.05 45.12±1.31 37.89±2.39 889.60±57.01 16.41±0.39 68.57±21.02 1310.60±431.45
表5 一次性灌胃给予西藏黑木耳后大鼠的血常规测定结果Ⅱ(±s)
注:与空白对照组比较,* P<0.05,** P<0.01
组别 性别只数(只)平均血小板体积(fL)血小板分布宽度(%)白细胞数(10E9﹒L-1)淋巴细胞绝对值(10E9﹒L-1)中间细胞绝对值(10E9﹒L-1)粒细胞绝对值(10E9﹒L-1)淋巴细胞百分比(%)中间细胞百分比(%)粒细胞百分比(%)空白对照组 雄 5 7.18±0.16 18.20±1.09 40.42±3.67 1.82±0.13 0.52±0.04 38.08±3.51 4.46±0.15 1.26±0.05 94.28±0.13雌 5 7.04±0.08 19.62±1.44 40.74±1.27 1.80±0.00 0.50±0.00 38.44±1.27 4.38±0.13 1.24±0.08 94.38±0.13西藏黑木耳组 雄 5 7.00±0.21 20.01±0.89* 38.98±2.03 1.80±0.20 0.49±0.00 36.54±1.89 4.53±0.15 1.27±0.15 94.17±0.25雌 5 6.87±0.08 21.03±1.89 47.20±11.15 2.30±0.50 0.53±0.051 44.60±11.23 4.30±0.11 1.19±0.16 94.59±0.18
表6 一次性灌胃给予西藏黑木耳后大鼠的血液生化指标测定结果(±s)

表6 一次性灌胃给予西藏黑木耳后大鼠的血液生化指标测定结果(±s)
注:与空白对照组比较,* P<0.05,** P<0.01
组别 性别 只数(只)谷丙转氨酶(μ﹒L-1)谷草转氨酶(μ﹒L-1)总红胆素(umo﹒L-1)总蛋白(g﹒L-1)白蛋白(g﹒L-1)球蛋白(g﹒L-1) (mmol﹒L-1) 胆固醇 甘油三酯(mmol﹒L-1)白球比 葡萄糖(mmol﹒L-1)空白对照组 雄 5 125.00±121.79 134.26±66.86 0.84±0.38 53.64±4.06 36.22±1.91 17.42±3.25 2.12±0.32 2.90±1.20 2.78±0.36 7.09±0.28雌 5 56.78±4.48 90.64±21.55 1.12±0.57 54.02±2.64 41.82±8.88 16.20±2.65 2.38±0.34 2.61±0.26 1.74±0.15 5.79±1.44西藏黑木耳组 雄 5 83.87±45.98 145.89±53.12 1.07±0.51 51.10±1.49 34.21±1.50 16.78±1.67 2.13±0.31 3.34±0.52 1.31±0.17** 8.32±1.76雌 5 51.98±13.86 97.01±12.01 1.30±0.8053.23±2.41 38.01±0.79 16.01±2.78 2.51±0.43 3.05±0.91 2.11±0.70 7.01±1.59
3 讨论
西藏黑木耳在西藏地区广泛使用,化学成分复杂,药效物质基础尚不明确。刘振东等[15]通过正相硅胶柱色谱、中压反响柱色谱、凝胶柱色谱、TLC及HPLC等技术从西藏黑木耳中分离、纯化首次得到了7个单体化合物,分别为(22E,24R)-麦角甾-7,22-二烯-3β,5α,6β-三醇(1yy2),(22E,24R)-麦角甾-5,7,22-三烯-3β-醇(Lyy3),3β,5α,9α-三羟基-7,22-(22E,24R)-麦角甾二烯-6-酮(Lyy4),5α,8α-环氧-(22E,24R)-麦角甾-6,22-二烯-3β-醇(Lyy5),5α,8α-环氧-(22E,24R)-麦角甾-6,9(11),22-三烯-3β-醇(Lyy6),(22E,24R)-麦角甾-7,22-二烯-3β,5α,6α,9α-四醇(Lyy7),5-羟甲基-2-异丙-1-醇-2,3-二氢苯并呋喃(Lyy1)。
本文西藏黑木耳的最大给药量为12.14g/kg,此剂量下未见动物死亡、中毒症状和肉眼可见的脏器异常,体重和饲料消耗量无明显变化。其成人日用剂量为3g-10g,即上述给药剂量为成人日用剂量73倍。结果表明,西藏黑木耳毒性低,服用安全。
此外,急性毒性实验血液测试结果表明,与空白对照组比较,西藏黑木耳可明显升高血液中雄性小鼠的红细胞数、红细胞比积、血小板数、血小板比积和血小板分布宽度的含量,降低雄性小鼠的平均血红蛋白含量以及降低血清中雄性小鼠的甘油三酯含量,但均在正常范围内。该变化的机制和毒效物质基础尚不明确,可能与西藏黑木耳所含某些化学成分有关,但是也可能是单次试验的偶然现象,均有待进一步研究。
