正交试验法优选痛利舒颗粒水提工艺
2018-03-16杨龙飞丁晓彦高燕国锦孙启慧赵渤年
杨龙飞,丁晓彦,高燕,国锦,孙启慧,赵渤年
(1.山东中医药大学,山东 济南 250355;2.山东省中医药研究院,山东省中药质量标准研究重点实验室,山东 济南 250014)
痛利舒颗粒是由茵陈、葛根、白芍、栀子等15味中药组成的临床经验方,具有清热利湿、化瘀止痛、益气滋阴之功效,临床上对痛风具有显著的疗效。由于传统汤剂有煎煮不方便、服用量大、质量不可控、不易储存和携带等弊端,为了提高临床疗效、保证药品质量,使该处方更好地服务于临床和广大病患,对汤剂进行了剂型改革。通过对处方的分析,在查阅文献[1-10]和预实验的基础上,根据各药物的理化性质和药理作用,确定了本制剂的提取工艺。该制剂水提取工艺的优化研究,为痛利舒颗粒的工业生产提供了技术支持。
1 仪器、试剂与试药
1.1 仪器
Waters e2695型高效液相色谱仪(美国沃特世公司);Thermo Syncronis C18色谱柱(250 mm×4.6 mm,5 μm);BP211D型电子天平(赛多利斯科学仪器(北京)有限公司)。
1.2 试剂
乙醇、甲醇、磷酸为分析纯;乙腈为色谱纯;高效液相色谱用水为超纯水。
1.3 试药
生地、山药、枸杞、白术、苍术、白芍、栀子、茵陈、葛根、丹参、黄芪、牛膝、地骨皮、泽泻、甘草(山东建联盛嘉中药有限公司中药饮片厂,质量合格);栀子苷(批号:0095-201101RS,云南特法特生物科技有限公司);芍药苷(批号:110736-200731,中国药品生物制品检定所)。
2 方法与结果
2.1 得膏率的测定
按处方量称取饮片,按正交设计分别进行实验,合并滤液,将药液转移至干燥恒重的蒸发皿中,水浴蒸干,于105 ℃条件下干燥3 h,转移至干燥器中冷却30 min,称重并计算各次实验的得膏率:

2.2 栀子苷含量测定
2.2.1 样品溶液的制备
2.2.1.1 对照品溶液的制备
取栀子苷对照品,精密称定,加甲醇制成50 μg/mL的溶液,即得。
2.2.1.2 供试品溶液的制备
取正交试验工艺提取所得干膏1.5 g,精密称定,置锥形瓶中,精密加入甲醇25 mL,称重,超声处理20 min(53 Hz,300 kW),放冷,称重,用甲醇补足减失的重量,滤过,取续滤液10 mL,置25 mL容量瓶中,加甲醇定容至刻度,摇匀,用0.45 μm微孔滤膜滤过,即得[11]。
2.2.1.3 阴性样品溶液的制备
按处方比例称取除栀子以外的其他药味,按照样品制备方法制备阴性样品,取阴性样品约1.2 g,按2.2.1.2项下方法制备,即得。
2.2.2 色谱条件
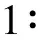
2.2.3 专属性考察
吸取不同样品溶液各10 μL进行测定,结果表明,供试品溶液色谱与对照品溶液色谱在相同保留时间处有相应色谱峰,分离度良好,阴性无干扰。色谱图见图1~3。
2.2.4 线性关系考察
精密吸取不同体积对照品溶液注入液相色谱仪,测定,得回归方程:y=2×106x+9 782.4,r=0.999 5,结果表明,栀子苷在0.10~1.02 μg范围内线性关系良好。
2.2.5 精密度实验
取栀子苷对照品溶液10 μL,连续进样6次,测定,相对标准偏差为1.11%,表明仪器精密度良好。

图1 栀子苷对照品溶液HPLC色谱图Fig.1 HPLC chromatogram of the reference solution of Gardenoside

图2 供试品溶液HPLC色谱图Fig.2 HPLC chromatogram of Tonglishu Granule
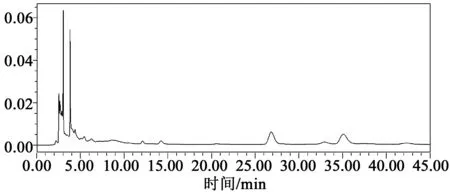
图3 缺栀子阴性样品溶液HPLC色谱图Fig.3 HPLC chromatogram of Gardenia Fructus negative control
2.2.6 重复性实验
取5号干膏粉末1.5 g,平行6份,精密称定,按2.2.1.2项下方法制备供试品溶液,测定,相对标准偏差为2.02%,表明该方法重复性良好。
2.2.7 稳定性实验
取供试品溶液(5号)分别在第0、2、4、8、12、24 h注入液相色谱仪,测定,结果栀子苷峰面积相对标准偏差为1.53%,表明供试品溶液在24 h内稳定。
2.2.8 加样回收实验
取5号干膏粉末0.75 g,平行5份,精密称定,分别精密加入浓度为1.89 mg/mL的栀子苷对照品溶液1 mL,按照2.2.1.2项下方法制备供试品溶液,测定,计算得平均回收率为100.58%,相对标准偏差为2.05%。
2.3 芍药苷的含量测定
2.3.1 样品溶液的制备
2.3.1.1 对照品溶液的制备
取芍药苷对照品,精密称定,加甲醇制成30 μg/mL的溶液,即得。
2.3.1.2 供试品溶液的制备
取正交试验工艺提取的干膏1.5 g,精密称定,置锥形瓶中,精密加入稀乙醇50 mL,称定重量,超声处理30 min(53 Hz,300 kW),放冷,称重,用稀乙醇补足减失的重量,滤过,取续滤液,用0.45 μm微孔滤膜滤过,即得[11]。
2.3.1.3 阴性样品溶液的制备
按处方比例称取除白芍以外的其他药味,按照样品制备方法制备阴性样品,取阴性样品约1.4 g,按2.3.1.2项下方法制备,即得。
2.3.2 色谱条件
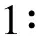
2.3.3 专属性考察
吸取不同样品溶液各10 μL,测定,结果表明,对照品溶液色谱与供试品溶液色谱在相同保留时间处有相应色谱峰,分离度良好,阴性无干扰。色谱图见图4~6。
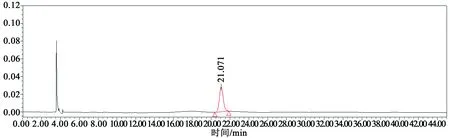
图4 芍药苷对照品溶液HPLC色谱图Fig.4 HPLC chromatogram of the reference solution of Paeoniflorin
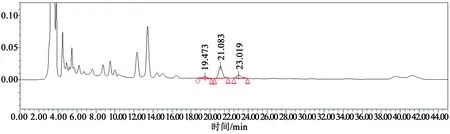
图5 供试品溶液HPLC色谱图Fig.5 HPLC chromatogram of Tonglishu Granule
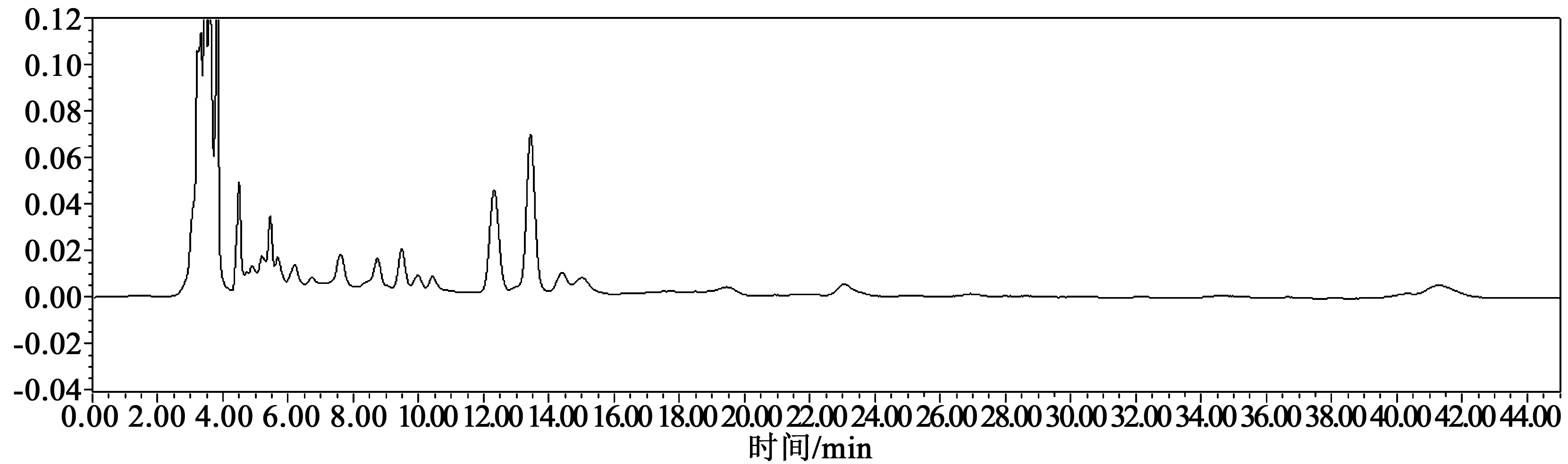
图6 缺白芍阴性样品溶液HPLC色谱图Fig.6 HPLC chromatogram of Radix paeoniae alba negative control
2.3.4 线性关系考察
精密吸取不同体积对照品溶液注入色谱仪,测定,得回归方程:y= 1×106x+24 867, r=0.999 9,结果表明,芍药苷在0.06~0.60 μg范围内呈良好的线性关系。
2.3.5 精密度实验
吸取芍药苷对照品溶液10 μL,连续进样6次, 相对标准偏差为0.30%,表明仪器精密度良好。
2.3.6 重复性实验
取5号干膏1.5 g,平行6份,精密称定,按2.3.1.2项下方法制备供试品溶液,测定,相对标准偏差为2.79%,该方法重复性良好。
2.3.7 稳定性实验
取供试品溶液(5号)分别在第0、2、4、8、12、24 h注入液相色谱仪,测定,计算各样品中芍药苷峰面积相对标准偏差为1.34%,结果表明供试品溶液在24 h内稳定。
2.3.8 加样回收实验
取5号干膏粉末0.75 g,平行5份,精密称定,分别精密加入浓度为33.5 μg/mL芍药苷对照品溶液1 mL,按照2.3.1.2项下方法制备供试品溶液,测定,计算得平均回收率为99.49%,相对标准偏差为1.50%。
2.4 水提工艺的优选
研究资料表明[12-13],栀子、白芍等药味中的有效成分均具有较好的水溶性,且临床应用时多以水煎剂为主,故在预实验的基础上,以水为提取溶剂,采用L9(34)正交试验法,选取加水量(A)、煎煮时间(B)和煎煮次数(C)制定因素水平表,以得膏率、栀子苷及芍药苷含量作为考察指标,优选水提工艺。正交试验因素水平见表1。
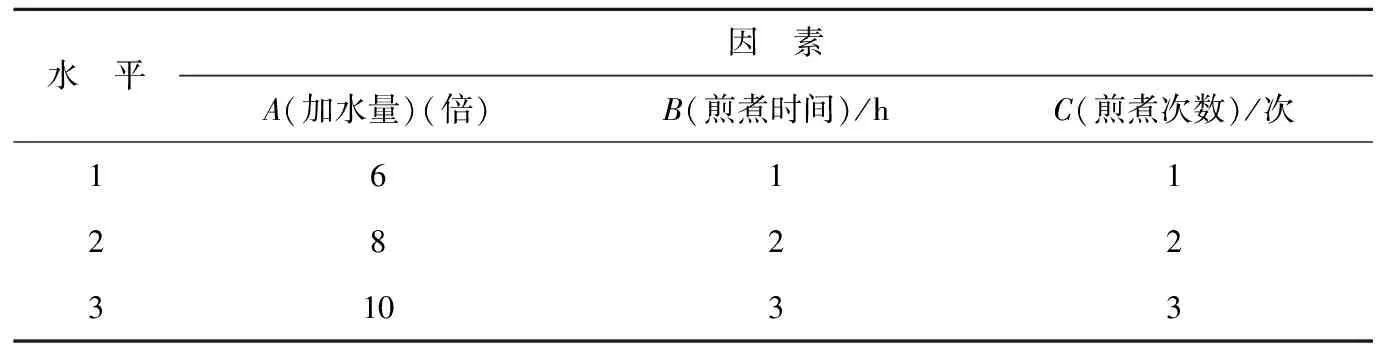
表1 水提工艺正交试验因素水平表Table 1 The orthogonal factor level table of water extraction process
2.5 正交试验结果
评价水煎煮工艺效果的主要指标为栀子苷与芍药苷含量,故将含量测定权重系数定为0.6,芍药苷和栀子苷含量各自为0.3,得膏率在实际生产中也有重要意义,权重系数定为0.4。
综合评分
×0.4。
正交试验结果见表2,方差分析结果见表3。

表2 水煎煮工艺正交试验结果Table 2 Orthogonal test results of water extracting technology
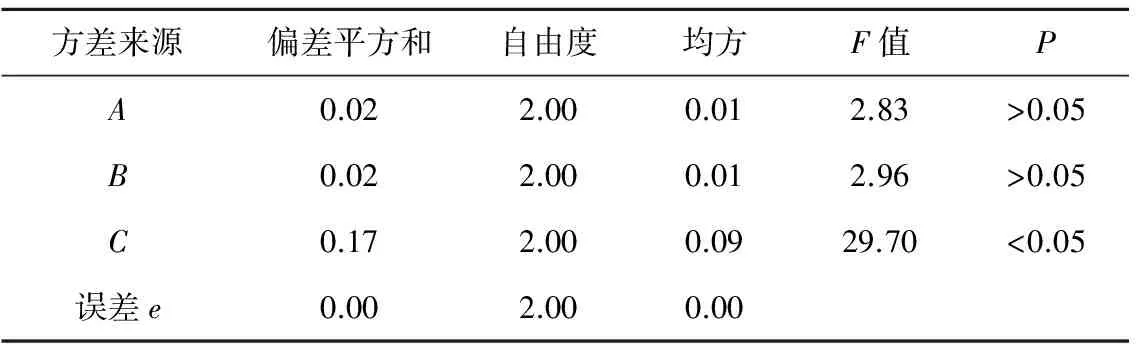
表3 方差分析结果表Table 3 Results of the variance analysis
实验结果表明,水提工艺的煎煮次数(C)对栀子苷与芍药苷的含量和得膏率有显著性影响,以C3为最佳,而对加水量(A)、煎煮时间(B)的影响较小,二者可任选一水平,根据综合评分结果,并考虑到节约能源,降低成本,故选用A2、B2。因此,最佳组合为A2B2C3,即在水提工艺中选用8倍量水,煎煮3次,每次煎煮2 h为水提工艺的适宜条件。
2.6 讨论
痛风在临床上主要表现为高尿酸血症,是由嘌呤类物质代谢紊乱引起的血尿酸浓度持续增高,而使尿酸盐结晶沉积在软组织所导致的一组代谢性疾病[14]。
痛利舒颗粒为多味药组成的复方,在临床上治疗痛风作用显著,且克服了汤剂使用不便、服用量大、不易储存携带等缺陷。为达到提取工艺可控、稳定的目的,本研究采用多指标综合评分来优化提取工艺。根据各药味中成分特点,以水为提取溶剂,成本低、安全性高,且与传统中医用药方法相契合。
指标的选择与综合评分权重比例是根据其药理作用、在制剂中的含量及其在生产中的意义决定的,方中栀子与白芍均可降低血清中尿酸水平[15-16],故将其作为评价提取工艺的主要指标,并采用HPLC测定栀子苷与芍药苷的含量。通过方差分析,最终确定8倍量水,煎煮3次,每次煎煮2 h为水提工艺适宜条件。优选出的提取工艺具有科学性和合理性,可作为痛利舒颗粒生产中提取工艺的参考,并为下一步质量标准的研究制定提供了实验依据。
[1]侯学谦,祝婉芳,曲玮,等.枸杞化学成分及药理活性研究进展[J].海峡药学,2016,28(8):1-7.
[2]李红伟,孟祥乐.地黄化学成分及其药理作用研究进展[J].药物评价研究,2015,38(2):218-228.
[3]徐硕,夏路风,金鹏飞,等.泽泻的化学成分及生物活性研究进展[J].中国医药导报,2015,12(27):47-51.
[4]曹锦花.茵陈的化学成分和药理作用研究进展[J].沈阳药科大学学报,2013,30(6):489-494.
[5]张秀云,周凤琴.地骨皮药效成分及临床应用研究进展[J].山东中医药大学学报,2012,36(3):243-244.
[6]孙政华,邵晶,郭玫.黄芪化学成分及药理作用研究进展[J].中医临床研究,2015,7(25):22-25.
[7]岳美颖,潘媛,敖慧.白术化学、药理与临床研究进展[J].亚太传统医药,2016,12(5):66-68.
[8]欧阳臻,江涛涛,缪亚东,等.苍术的化学成分、道地性和药理活性研究进展[J].时珍国医国药,2006,17(10):1936-1938.
[9]刘娟,刘颖.丹参药理活性成分研究进展[J].辽宁中医药大学学报,2010,12(7):15-17.
[10]楚纪明,马树运,李海峰,等.葛根有效成分及其药理作用研究进展[J].食品与药品,2015,17(2):142-146.
[11]国家药典委员会.中华人民共和国药典2015年版一部[S].北京:中国医药科技出版社,2015.
[12]那莎,郭国田,王宗殿,等.栀子及其有效成分药理研究进展[J].中国中医药信息杂志,2005,12(1):90-92.
[13]张利.白芍的药理作用及现代研究进展[J].中药临床研究,2014,6(29):25-26.
[14]徐娜,陈海生.治疗痛风药物研究进展[J].药学实践杂志,2013,31(1):14-18.
[15]戴芸,杨林,朱莉萍.白芍总苷降尿酸实验研究[J].化学工程师,2016 (3):68-70.
[16]孟兆青,唐朝辉,闫云霞,等.栀子苷降尿酸作用研究[J].世界科学技术-中医药现代化,2014,16(7):1565-1568.
