替莫唑胺化疗方案联合全脑放疗治疗非免疫功能缺陷PCNSL的临床观察
2018-03-16李鸿波
李鸿波
原发中枢神经系统淋巴瘤(primary central nervous system lymphoma,PCNSL)是1种高度恶性的非霍奇金淋巴瘤,一般来说病变不伴全身其他部位,主要局限于脑和脊髓[1-2]。PCNSL属于比较少见的淋巴结外恶性肿瘤,发病率占非霍奇金淋巴瘤的1%~3%。PCNSL可发生于免疫功能缺陷或免疫功能正常者,两者的临床情况有一定差异。近年来,PCNSL在非免疫功能缺陷的正常人群中发病率逐步提高,由于其早期诊断困难、预后较差、复发率较高,严重威胁着我国国民的身体健康。目前在二线挽救治疗中,多采用甲氨蝶呤、放射治疗、替莫唑胺、培美曲塞、自体干细胞移植以及其他化疗药物的单一或联合治疗,临床上尚未确定标准的二线挽救治疗方案[3]。相比较而言,替莫唑胺更容易通过血脑屏障,易被患者接受,对中枢神经系统的作用药物浓度更有效且毒副作用较小,但结合全脑治疗会提高毒副作用。本研究旨在探索替莫唑胺方案联合全脑放疗治疗在非免疫功能缺陷PCNSL患者群体中的临床应用,为今后治疗PCNSL提供临床经验,从而提高PCNSL的治疗水平。
1 资料与方法
1.1 一般资料
168例非免疫功能缺陷PCNSL患者的基本资料:男性90例、女性78例,平均年龄(58.02±3.28)岁,131例(77.97%)患者KPS评分≥70分,病变范围:仅脑部136例(80.95%)、脑部与眼部15例(8.92%)、脑部与脑膜13例(7.73%)、脑部和脊髓4例(2.38%),病灶单发61例(36.30%)、多发107例(63.69%)。临床表现:颅内压高149例(88.69%),嗜睡57例(33.92%),阵发性头痛113例(67.26%),肢体运动障碍107例(63.69%),视力下降及视野缺损87例(51.78%),语言障碍31例(45.58%),吞咽困难29例(17.26%),鞍区转移17例(10.11%),癫痫发作26例(15.47%),共济失调13例(7.73%)。
1.2 纳入标准及排除标准
纳入标准[4]:经检查确诊为原发中枢神经系统淋巴瘤患者;无器官移植、其他恶性肿瘤、自身免疫性疾病;无免疫功能缺陷;HIV抗体均阴性;患者同意参与此次研究。
排除标准:除原发中枢神经系统淋巴瘤外患有其他较为严重的疾病;患者自身免疫功能缺陷;HIV抗体为阳性;患者不愿意配合术后随访;患者不同意参与此次研究。
1.3 治疗方法
本组168例患者均在治疗前进行颅脑磁共振平扫及增强检查,全脑放疗20 Gy/10次后进行复查,观察病灶反应,评估治疗效果。
同步放化疗[5]:确诊后行颅脑放疗,采用6McVX线进行全脑照射,2 Gy/次,1周进行5次;然后进行颅脑MRI检查,继续进行全脑照射至总量到达40 Gy,放疗期间患者同步口服替莫唑胺75 mg/(m2·d)。根据患者情况可行大孔径CT进行三维适形放疗。照射剂量达40 Gy后,对所有患者进行复查,对未完全缓解患者应停止放疗,改为序贯替莫唑胺口服治疗。
毒性检测[6]:分时定期。每个治疗周期中按时进行血细胞分析,每个周期结束后进行神经毒性评估以及常规检查。依据检查结果实时调整口服替莫唑胺剂量,必要时停止本方案治疗。
1.4 评价标准
疗效评价按照肿瘤缓解标准采用国际PCNSL协作组2005版分为:完全缓解(CR)、部分缓解(PR)、稳定病灶(SD)、进展性病灶(PD)。其中有效率评价包括:完全缓解、部分缓解;临床控制率包括:完全缓解、部分缓解、稳定病灶。
1.5 统计学方法
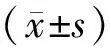
2 结果
2.1 非免疫功能缺陷PCNSL患者放疗疗程周期
全部病例均完成替莫唑胺联合全脑放疗同步化放疗疗程。单药替莫唑胺化疗疗程完成情况:1个周期7例(4.17%),2个周期11例(6.55%),3个周期17例(10.11%),4个周期58例(34.52%),5个周期39例(23.21%),6个周期36例(21.43%),其中23例(13.69%)因经济原因及血液毒性未完成计划化疗周期。
2.2 治疗疗效
CR 51例(30.35%)、PR 63例(37.50%)、SD 23例(13.69%)、PD 31例(18.45%)、有效率为67.86%,临床控制率为81.55%。
2.3 不良反应
治疗过程中出现为不良反应采用WHO标准[7]评定,主要有:恶心呕吐103例(61.30%)、便秘91例(54.16%)、脱发77例(45.83%),皮肤反应43例(25.60%),疲劳感137例(81.54%),骨髓抑制141例(83.93%),急性脑水肿11例(6.55%),白细胞减少133例(79.17%),贫血73例(43.45%),血小板减少27例(16.07%),肝功能异常41例(24.40%),远期神经不良反应7例(4.17%)。
2.4 生存分析
治疗后定期对患者进行随访,以采集数据与收集信息,生存时间3个月患者163例(97.02%),生存时间6个月患者158例(94.04%),生存时间12个月患者149例(88.69%),生存时间15个月患者141例(83.92%),生存时间20个月患者117例(69.64%),生存时间24个月患者97例(57.73%)。
3 讨论
原发中枢神经系统淋巴瘤目前在二线挽救治疗中,多采用甲氨蝶呤、放射治疗、替莫唑胺、培美曲塞、自体干细胞移植以及其他化疗药物的单一或联合治疗,临床上尚未确定标准的二线挽救治疗方案。有研究表明,甲氨蝶呤等药物的单一治疗虽然局控率较高,但复发率却高达60%~80%[8-9]。相比较而言,替莫唑胺更容易通过血脑屏障,对中枢神经系统的作用药物浓度更有效且毒副作用较小,患者容易接受。而全脑放疗治疗可巩固疗效,从而提高患者生存率[7,10]。
因此本研究分析了我院收治的168例非免疫性功能缺陷PCNSL病例,通过深入研究其基本资料、临床表现、化疗周期、化疗疗效、不良反应、生存分析、随访时间等数据信息,对比了国内学者报道的单独应用替莫唑胺的治疗数据[11],研究了替莫唑胺化疗方案联合全脑放疗治疗非免疫功能缺陷PCNSL患者的疗效。本研究结果显示的有效率、平均生存期以及远期生存率均优于国内学者报道的单独应用替莫唑胺的治疗方案。出现这一结果的原因可能是:所有患者均为初次接受全脑放疗,治疗反应较好;替莫唑胺的药物浓度能够有效地杀死肿瘤细胞;淋巴瘤较为敏感等。
综上所述,非免疫功能性PCNSL患者平均生存期较短,易复发,目前尚无标准的治疗方案。替莫唑胺化疗方案联合全脑放疗治疗能够比较有效地提高患者生存率,值得临床推广应用,但具体还需要更长时间的随访观察疗效。
[1] 赵 克,赵 明,徐 欣,等.替莫唑胺联合放疗治疗原发中枢神经系统淋巴瘤的临床效果〔J〕.慢性病学杂志,2016,23(7):816-818.
[2] 郭 韬,梁传栋,陈 尧,等.放射治疗联合替莫唑胺治疗原发中枢神经系统淋巴瘤的研究〔J〕.中华神经医学杂志,2015,14(2):185-186.
[3] 郭军辉.替莫唑胺为主的化疗联合放疗治疗原发中枢神经系统淋巴〔J〕.中国保健营养,2015,25(9):6-10.
[4] Byoung Hyuck Kim,Il Han Kim,Sung-Hye Park,et al.Lo-w-Dose Whole Brain Radiotherapy with Tumor Bed Boost after Methotrexate-Based Chemotherapy for Primary Central Nervous System Lymphoma〔J〕.Cancer Res Treat,2014,46(3):261-269.
[5] Zhao D,Qian L,Shen J,et al.Combined treatment of rituximab,idarubicin,dexamethasone,cytarabine,methotrexate with radiotherapy for primary central nervous system lymphoma〔J〕.J Cell Mol Med,2014,18(6):1081-1086.
[6] Korfel A.A focus on pharmacotherapy for primary central -nervous system lymphoma〔J〕.Expert Rev Hematol,2015,8(5):559-562.
[7] Makino K,Nakamura H,Hide T,et al.Salvage treatment with temozolomide in refractory or relapsed primary central nervous system lymphoma and assessment of the MGMT status〔J〕.J Neurooncol,2014,106(1):155-160.
[8] Ungur R,Tempescul A,Berthou C,et al.ESHAP chemotherapy is efficient in refractory/relapsed primary central nervous system lymphoma:report of four cases〔J〕.Onco Targets Ther,2015,8(3):2771-2776.
[9] Fraser E,Gruenberg K,Rubenstein JL.New approaches in primary central nervous system lymphoma〔J〕.Chin Clin Oncol,2015,4(1):11-15.
[10] Wang XX,Huang HQ,Bai B,et al.Clinical outcomes of patients with newly diagnosed primary central nervous system lymphoma are comparable on treatment with high-dose methotrexate plus temozolomide and with high-dose methotrexate plus cytarabine:a single-institution experience〔J〕.Leuk Lymphoma,2014,55(11):2497-2501.
[11] Pulczynski EJ,Kuittinen O,Erlanson M,et al.Successful change of treatment strategy in elderly patients with primary central nervous system lymphoma by de-escalating induction and introducing temozolomide maintenance:results from a phase Ⅱ study by the Nordic Lymphoma Group〔J〕.Haematologica,2015,100(4):534-540.
