舒芬太尼复合右旋美托咪定用于腹腔热灌注化疗术后患者镇痛的效果观察
2018-03-05盛崴宣
盛崴宣 关 雷
(首都医科大学附属世纪坛医院麻醉科,北京 100038)
常规细胞减灭术(cytoreductive surgery,CRS)和腹腔热灌注化疗(hyperthermic intraperitoneal chemotherapy,HIPC)是治疗结直肠癌腹膜种植转移的有效方法[1,2]。近年来,国际肿瘤学界认为腹膜癌已不完全是癌广泛转移的表现,而是一种区域性转移,并探索发展了一套综合治疗新策略,核心为CRS联合HIPC。其主要优势是CRS切除肉眼可见的病灶,再由HIPC消灭微转移癌和游离的癌细胞[3,4]。此类手术创伤巨大,术后疼痛剧烈,最大限度地减少疼痛和其他副作用对患者的恢复是至关重要的。为达到这个目标, 使用不同类型镇痛药物是当前的推荐方案。右旋美托咪定是一种高效、高选择性α2肾上腺素能受体激动剂,不仅具有镇静、镇痛、抑制交感神经[5]和降低恶心呕吐[6]等作用,且血流动力学稳定,无呼吸抑制。我们采用前瞻性随机对照研究对HIPC患者使用右旋美托咪定(江苏恒瑞医药股份有限公司,批准文号:国药准字H20090248)复合舒芬太尼(宜昌人福药业有限责任公司,批准文号:国药准字H20054147)与单纯使用舒芬太尼术后镇痛进行比较,探索右旋美托咪定复合舒芬太尼用于HIPC术后镇痛的可行性。
1 临床资料与方法
1.1 一般资料
选择2015年1月~2016年4月我院因结肠癌腹膜种植转移行择期HIPC 45例。年龄20~60 岁,体重60~100 kg。美国麻醉医师协会(the American Society of Anesthesiologists,ASA)分级为Ⅰ~Ⅱ级。45例按治疗先后顺序编号,采用随机数字表随机为3组[舒芬太尼3.0 μg/h (A组)、舒芬太尼2.0 μg/h (B组)、舒芬太尼2.0 μg/h +右旋美托咪定4.0 μg/h (C组)],每组15例。3组一般资料比较无统计学差异(P>0.05),见表1。
病例选择标准:术前评估腹膜癌指数(peritoneal carcinomatosis index,PCI)[7]<20;常规检查未发现远处器官(肝脏、肺、脑或全身骨)多处转移或腹膜后淋巴结转移;无小肠系膜中-重度挛缩;无冠心病、心力衰竭、心肌梗死、脑梗死病史,无慢性阻塞性肺疾病;无肝脏、肾脏疾病,无神经肌肉病变,无精神性疾病,无血液系统疾病,无过敏史。
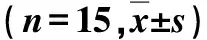
表1 3组一般资料比较
PCI:腹膜癌指数,是最常用的腹膜癌分期系统;CC评分:细胞减灭程度(completeness of cytoreduction)评分[7]
*数据偏态分布,用中位数(最小值~最大值)表示
1.2 方法
患者入室开放外周静脉,监测患者的心率、无创血压、SpO2(飞利浦多功能麻醉监护仪)、脑电双频指数(bispectral index,BIS);桡动脉穿刺置管,应用Vigileo监测有创血压、心输出量(cardiac output,CO)和每搏量变异度(stroke volume variation,SVV),全麻诱导后行中心静脉穿刺置管,监测中心静脉压(central venous pressure,CVP)。给予10 mg地塞米松,全麻诱导采用丙泊酚1.5~2.5 mg/kg、舒芬太尼0.3~0.5 μg/kg,罗库溴铵0.6~0.8 mg/kg行快速插管。在诱导插管后,给予患者机械通气,潮气量为8~10 ml/kg,呼吸频率10~14 次/ min,氧流量2 L/min。术中持续监测呼气末二氧化碳分压,维持在35~45 mm Hg。应用瑞芬太尼0.1~0.3 μg·kg-1·min-1和七氟烷1~1.33 MAC,并间断给予罗库溴铵0.1 mg/kg维持麻醉。
完成CRS后,选择开放式HIPC。首先,将灌注导管置入腹腔,入口管位于膈肌下方,然后用43 ℃生理盐水冲洗盆腹腔,再将化疗药[常用化疗药物为顺铂(20 mg/L)、奥沙利铂(25 mg/L)、丝裂霉素(5 mg/L)和多西他赛(20 mg/L)]加入6 L温热生理盐水(奥沙利铂为5%葡萄糖),经腹腔热灌注化疗仪加热至44~45 ℃后,开始腹腔灌注,灌注速度为100 ml/min,监测腹腔内温度,使腹腔内化疗药液温度保持在(43±0.5)℃,HIPC持续60~90 min,最后用2~3 L生理盐水清洗腹腔。肠道重建可在HIPC之后或之前进行,必要时行造瘘术。最后检查腹腔,减张缝合切口[7]。
手术结束前10~15 min接电子镇痛泵(型号:Graseby9300)行患者静脉自控镇痛(patients controlled intravenous analgesia,PCIA),背景剂量2 ml/h, 按压剂量2 ml/次, 负荷量 2 ml, 锁定时间15 min, 药液量100 ml,舒芬太尼3.0 μg/h (A组)、舒芬太尼2.0 μg/h (B组)、舒芬太尼2.0 μg/h +右旋美托咪定4.0 μg/h (C组)。静脉滴注1次昂丹司琼8 mg和舒芬太尼0.15 μg/kg,患者清醒后拔除气管导管。镇痛泵参数设定:背景剂量2 ml/h,按压剂量2 ml /次,负荷量2 ml,锁定时间15 min,药液量100 ml。
1.3 观察指标
①出血量[吸引瓶内的血量+吸血纱布(大纱布全部浸润为50 ml,小纱布全部浸润为20 ml)、平均动脉压(mean arterial pressure,MAP)、心输出量(cardiac output,CO)、每搏量变异度(stroke volume variability,SVV)。②术后1 h(T1)、2 h(T2)、6 h(T3)、12 h(T4)、24 h(T5)、48 h(T6)疼痛评分采用视觉模拟评分(visual analogue scale,VAS):VAS≤3 分为镇痛优良,4~6 分为基本满意,镇痛良好,≥7 分为无效,镇痛差[8]。③术后1 h(T1)、2 h(T2)、6 h(T3)、12 h(T4)、24 h(T5)、48 h(T6)镇静评分(Ramsay评分[9]:1分为烦躁;2分为安静合作;3分为嗜睡,能听从指令;4分为睡眠状态可被唤醒;5分为呼唤病人反应迟钝;6分为深睡眠状态,呼唤不醒。1分镇静不良,2~4分镇静满意,5~6分镇静过度)。④术后48 h内镇痛泵的按压次数。⑤术后48 h出现的不良反应:恶心或呕吐、心动过缓和呼吸抑制。
1.4 统计学处理
采用SPSS19.0统计软件进行统计学处理。正态分布的计量资料以均数±标准差表示,组间计量资料比较采用单因素方差分析,两两比较用S-N-K检验;偏态分布的计量资料用中位数(最小值~最大值)表示,采用Kruskai-WallisH检验;计数资料采用χ2检验。P<0.05有统计学差异。
2 结果
3组患者出血量和出手术室时MAP、CO、SVV比较无统计学差异(P>0.05),见表2。镇痛、镇静效果:A组和C组在T3~T6时点VAS评分明显低于B组(P<0.05);A组和B组在T5和T6时点Ramsay评分有统计学意义(P<0.05);B组和C组在T3~T6时点Ramsay评分有统计学意义(P<0.05),见表3、4。3组患者PCIA镇痛期间,A组恶心呕吐发生率高于C组(P<0.05);A组和C组在48 h内镇痛泵的按压次数明显少于B组(P<0.05),见表5。
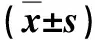
表2 3组手术室指标的比较
*正常<13%,<13%代表液体量充足,表明前负荷良好,重要脏器(肾脏、肝脏等)的灌注充足,患者离开手术室时SVV均在正常范围内
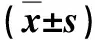
表3 3组VAS评分比较 分
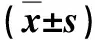
表4 3组Ramsay评分比较 分
表5 3组不良反应和按压次数比较
3 讨论
结直肠癌患者一旦出现广泛腹膜转移,即处于最危险的肿瘤进展阶段,严重威胁患者生命。传统治疗方法[单纯手术和(或)全身化疗]不能使患者生存获益,且中位生存期仅为4~7个月,未能有效改善患者临床症状。目前,CRS联合HIPC已经成为腹膜恶性间皮瘤、腹膜假性黏液瘤及部分经慎重选择的结直肠腹膜转移癌的标准治疗,并在欧美、澳大利亚、日本等国家普遍应用。
由于CRS联合HIPC手术创伤大,疼痛剧烈,术中应严密监测患者的血流动力学各个指标:SVV可以知晓前负荷,通过平均动脉压(MAP)=心输出量(CO)×体循环外周血管阻力,计算体循环外周血管阻力,间接知晓后负荷,以此加强术中对循环的管理。传统镇痛存在的最大顾虑是镇痛药物引起的恶心呕吐和呼吸抑制等副作用,因此,对此类患者如何进行既有效又安全的术后镇痛成为新课题。采用PCIA给药模式,患者在较小背景剂量药物下按需给药,有操作简便、起效迅速、效果可靠等特点[10]。
舒芬太尼是一种新合成的阿片类镇痛药,安全范围大于芬太尼和吗啡,药效比芬太尼强7~10倍,持续时间是其2倍,在阿片类家族中镇痛效果最强[11],被广泛用于术后镇痛。然而随着舒芬太尼用药剂量的加大,呼吸抑制作用等副反应呈现线性的升高[12]。可见,为追求镇痛效果单纯加大舒芬太尼剂量并不可取[13]。
右旋美托咪定是一种高效、高选择性α2受体激动剂,具有剂量依赖性的镇静、镇痛、抑制交感活性效应,治疗量下不会引起心血管和呼吸的并发症[8]。它主要通过作用于神经中枢的蓝斑核,激动突触前膜α2肾上腺素能受体,通过抑制去甲肾上腺素的释放,终止疼痛信号的传导,激动突触后膜受体,抑制交感神经活性。特点包括:半衰期短,静脉注射快速分布半衰期约为6 min,消除半衰期约为2 h,通过激活蓝斑核α2受体使患者处于一种类似于正常睡眠的“可唤醒”的镇静状态;此外,右美托咪定在产生类似自然非快动眼睡眠镇静的同时,还具有良好镇痛作用[14],可以通过激动α2 C 受体亚型起到与阿片类药物协同镇痛的效应,减少阿片类药物的用量[15],同时,还具有抑制应激反应和抗寒颤[16]等作用。右美托咪定可逆转炎症性痛觉过敏[17],并能减轻疼痛带来的不愉感。
本研究兼顾药物的配伍,选取右美托咪定联合强效阿片类镇痛药舒芬太尼,观察术后镇痛效果和不良反应发生情况。
临床观察疼痛以术后早期为主,2~6 h 达到高峰,24 h后疼痛程度则明显下降,因此,术后镇痛时间窗关键在术后6 h内[18]。本研究结果显示用右美托咪定复合舒芬太尼用于HIPC术后PCIA,C组在T3~T6时间点时VAS评分明显低于B组(P<0.05),但与A组无统计学差异(P>0.05);B组在48 h内按压次数要明显多于其他2组(P<0.05),表明镇痛效果欠佳的原因为舒芬太尼用量减少所致,同时说明右美托咪定与阿片类药物具有协同镇痛的效应,可减少其用量。3组在T1~T6 VAS评分虽均属于镇痛良好,但是A组增加恶心呕吐发生率,B组患者48 h内主动按压次数增加,说明A组镇痛良好建立在增多舒芬用量的基础之上,但增加不良反应,B组舒芬太尼的镇痛泵中的背景剂量不足,需要不断按压镇痛泵,以达到满意的镇痛效果。A、C组在各个时间VAS评分和Ramsay评分无统计学差异(P>0.05),但是A组恶心呕吐发生率明显高于C组(P<0.05),且出现过度镇静导致的呼吸抑制,说明右美托咪定提供相同镇痛、镇静的同时,能减少由于增大阿片类药物的剂量所导致的不良反应的发生。3组患者术后均属于镇静满意,说明右美托咪定提供良好镇静的同时,没有出现过度镇静,体现其“可唤醒”的镇静优势,复合舒芬太尼镇痛术后镇静效果优于单纯使用舒芬太尼。此外,3组心动过缓的发生率虽无统计学差异(χ2=5.833,P=0.054),但是C组发生的例数比其他2组多,可能与样本量小有关,提示右旋美托咪定激动α1肾上腺素能受体的效应不容忽视。
3组患者VAS评分随着时间推移呈现下降趋势,波峰出现在术后T2,T1和T2时3组患者VAS评分无统计学差异 (P>0.05),可能与阿片类药物的半衰期和残余镇痛作用有关。3组T1、T2时点Ramsay评分无统计学差异(P>0.05),原因:①HIPC麻醉时间长,体内镇静药物蓄积所致;②残余阿片类药物和镇静药物的协同作用。
综上所述,右美托咪定用于HIPC术后患者镇痛可减少舒芬太尼使用量,同时降低其恶心呕吐发生率,但术后镇痛的应用剂量仍需进一步研究,以获得更多、更客观的数据,使患者得到满意的术后镇痛。
1 Verwaal VJ, van Ruth S, de Bree E, et al. Randomized trial of cytoreduction and hyperthermic intraperitoneal chemotherapy versus systemic chemotherapy and palliative surgery in patients with peritoneal carcinomatosis of colorectal cancer. J Clin Oncol,2003,21(20):3737-3743.
2 Elias D, Benizri E, Di Pietrantonio D, et al. Comparison of two kinds of in traperitoneal chemotherapy following complete cytoreductive surgery of colorectal peritoneal carcinomatosis. Ann Surg Oncol,2007,14(2):509-514.
3 李 雁.腹膜癌研究之我见.中国肿瘤临床,2012,39(22):1685-1686.
4 崔书中,王佳泓,张相良.肿瘤细胞减灭术联合腹腔热灌注化疗治疗结直肠癌腹膜转移癌.中国肿瘤临床,2012,39(22):1691-1695.
5 刘清仁,季 永.右美托咪定镇痛作用的研究进展.国际麻醉学与复苏杂志,2013,35(3):276-279.
6 葛 蕾,齐敦益.盐酸右美托咪定辅助舒芬太尼术后镇痛研究.徐州医学院学报,2012,32(12):790-793.
7 李 雁,周云峰,杨肖军,等.细胞减灭术加腹腔热灌注化疗治疗腹膜表面肿瘤的专家共识.中国肿瘤临床,2015,42(4):198-206.
8 孙 晶,李元涛,黄晓雷,等.右美托咪定在宫腔镜手术静脉麻醉中的应用.中国微创外科杂志,2013,13(5):425-428.
9 耿雪梅,韩永正,郭向阳.哌替啶复合氟哌利多在无痛人流术中的应用.中国微创外科杂志,2016,16(3):263-265.
10 Na HS, An SB, Park HP, et al. Intravenous patient-controlled analgesia to manage the postoperative pain in patients undergoing craniotomy. Korean J Anesthesiol,2011,60(1):30-35.
11 盛卓人,王俊科,主编.实用临床麻醉学.第4版.北京:科学出版社,2009.156.
12 邵大清,叶志坚,廖俊锋,等.右美托咪定对子宫切除术后舒芬太尼自控静脉镇痛效果的影响.浙江医学,2012,34(10): 36-39.
13 Geller E, Chrubasik J, Graf R, et al. A randomized double-blind comparison of epidural sufentanil versus intravenous sufentanil or epidural fentanyl analgesia after major abdominal surgery. Anesth Analg,1993,76(6):1243-1250.
14 刘 明,孟秀丽,郭向阳.右美托咪定单次负荷量在椎管内麻醉中应用的随机对照研究.中国微创外科杂志,2013,13(10):903-905.
15 Yildiz M, Tavlan A, Tuncer S, et al. Effect of dexmedetomidine on haemodynamic responses to laryngoscopy and intubation: perioperative haemodynamics and anaesthetic requirement. Drugs RD,2006,7(1):43-52.
16 赵喜越,缪剑霞,王良荣,等.比较右美托咪定与曲马多预防围术期寒战效果的Meta分析.温州医科大学学报,2014,44(12):896-900.
17 Willigers HM, Prinzen FW, Roekaerts PM, et al. Dexmedetomidine decrease preoperative lactate release in dogs. Anesth Analg,2003,96(3):657-664.
18 曾少林.罗哌卡因局部麻醉用于论着腹腔镜胆囊切除术后的镇痛效果观察.临床和实验医学杂志,2013,12(18):1470-1472.
