丹参川芎嗪注射液细菌内毒素检查法研究
2018-03-04张馨梅群肖植国
张馨 梅群 肖植国

摘 要:目的 建立丹参川芎嗪注射液细菌内毒素检查法。方法 依据《中国药典》2015年版四部(通则1143)细菌内毒素检查法,通过预干扰预试验和干扰试验,确定丹参川芎嗪注射液最大无干扰的浓度,并进行方法学验证。结果 将丹参川芎嗪注射液稀释20倍,对细菌内毒素检测法无干扰作用。结论 丹参川芎嗪注射液内毒素检查法可用于检查丹参川芎嗪注射液。
关键词:丹参川芎嗪注射液;细菌内毒素检查;凝胶法;干扰试验
中图分类号:R286 文献标识码:A DOI:10.3969/j.issn.1006-1959.2018.24.041
文章编号:1006-1959(2018)24-0139-04
Abstract:Objective Establish a bacterial endotoxin test for Salviae Miltiorrhizae and Ligustrazine Hydrochloride. Methods According to the Chinese Pharmacopoeia's 2015 edition of the four-part (General Rule 1143) bacterial endotoxin test, the maximum interference-free concentration of Salviae Miltiorrhizae and Ligustrazine Hydrochloride was determined by pre-interference pre-test and interference test, and the methodological verification was carried out. Results The Salviae Miltiorrhizae and Ligustrazine Hydrochloride was diluted 20 times, which had no interference effect on the bacterial endotoxin test. Conclusion The endotoxin test of Salviae Miltiorrhizae and Ligustrazine Hydrochloride can be used to check Salviae Miltiorrhizae and Ligustrazine Hydrochloride.
Key words:Salviae Miltiorrhizae and Ligustrazine Hydrochloride;Bacterial endotoxin test;Gel method;Interference test
丹参川芎嗪注射液为复方制剂,浅棕红色澄明液体,用于闭塞性脑血管疾病,如脑供血不全,脑血栓形成脑栓塞及其他缺血性心血管疾病,如冠心病的胸闷、心绞痛、心肌梗塞、缺血性中风、血栓闭塞性脉管炎,收载在国家药品西药标准(化学药品地标升国标第十二册),执行标准WS-10001-(HD-1138)-2002[1],目前标准采用家兔法进行热原检查,该检查方法所用家兔的饲养时间长,操作繁琐,实验结果受家兔的个体差异影响较大。而细菌内毒素检查法具有灵敏、快速、操作简便、结果准确等优点,为建立该品种细菌内毒素检查法的可行性研究提供理论参考。
1材料
1.1试剂与药品 细菌内毒素工作标准品(CSE)(湛江博康海洋生物有限公司,批号:1607302,规格:10 EU/支);鲎试剂(TAL)(湛江安度斯生物科技有限公司,标示灵敏度0.5 EU/ml,批号:1609021,规格:0.1 ml/支;标示灵敏度0.25 EU/ml,批号:1705041,规格:0.1 ml/支;湛江博康海洋生物有限公司,标示灵敏度0.5 EU/ml,批号:1607270,规格:0.1 ml/支;标示灵敏度0.25 EU/ml,批号:1708230,规格:0.1 ml/支);细菌内毒素检查用水(BET水)(湛江博康海洋生物有限公司,批號:1607050,规格:5 ml/支);丹参川芎嗪注射液(贵州拜特制药有限公司,批号:20160445、20161233、20170313,规格:5 ml/支)。
1.2仪器 BET-48G细菌内毒素测定仪(天大天发科技有限公司);ZH-2BLENDER涡式振荡器(天津药典标准仪器厂);Transferpette移液器;AXYGEN带过滤无内毒素枪头。
2方法与结果
2.1鲎试剂灵敏度的复核试验 所用鲎试剂应依法进行灵敏度复核,结果均应符合规定。根据鲎试剂灵敏度的标示值(λ),用BET水分别将CSE溶解并制成2.0λ、1.0λ、0.5λ、0.25λ的细菌内毒素标准溶液,每一个浓度的溶液做4管,用BET水做2支阴性对照管。按《中国药典》2015年版四部(通则1143)[2,3]对TAL进行标示灵敏度复核。由表1可见,2个厂家生产的鲎试剂灵敏度均符合规定。
2.2内毒素限值的计算 根据《中国药典》2015年版四部(通则1143)的有关要求[2],内毒素限值(L)按以下公式计算:L=K/M。式中K为人每千克体重每小时最大可接受的内毒素剂量,注射剂K=5 EU/(kg·h);M为人用每千克体重每小时的最大供试品剂量,根据说明书丹参川芎嗪注射液最大剂量为10 ml,中国人均体重按60 kg计算,M=10 ml/(60kg·1h)=0.167 ml/(kg·h),则L=30 EU/ml。因此,计算出本品的细菌内毒素限值为每1 ml丹参川芎嗪注射液中含内毒素应<30 EU。
2.3干扰预实验最大有效稀释倍数的确定 按药典标准中供试品最大稀释倍数(MVD)计算公式:MVD=CL/λ[2],C为供试品溶液的浓度,L为供试品溶液的内毒素限值,MVD=CL/λ=1.0 ml/ml×30 EU/ml/0.50(EU)=60。
2.4干扰预试验 为了确定丹参川芎嗪注射液在多大浓度下对细菌内毒素(CSE)和鲎试剂(TAL)的反应不存在干扰作用,首先进行干扰试验的预实验[4]。将3批丹参川芎嗪注射液用BET水分别稀释5、10、20、40、60倍作为供试品系列(NPC),同时用上述每一个浓度的溶液制备成含1 EU/ml(2λ)浓度的内毒素溶液作为供试品阳性对照系列(PPC)。用标示灵敏度(λ)为0.50 EU/ml的2个厂家的鲎试剂(TAL)分别与2个系列溶液反应,每一稀释度作2支。BET水作阴性对照(NC),加入2 λ浓度的内毒素标准溶液作为阳性对照(PC),从表2可见丹参川芎嗪注射液存在干扰作用,稀释20倍时,即不再对试验产生干扰。
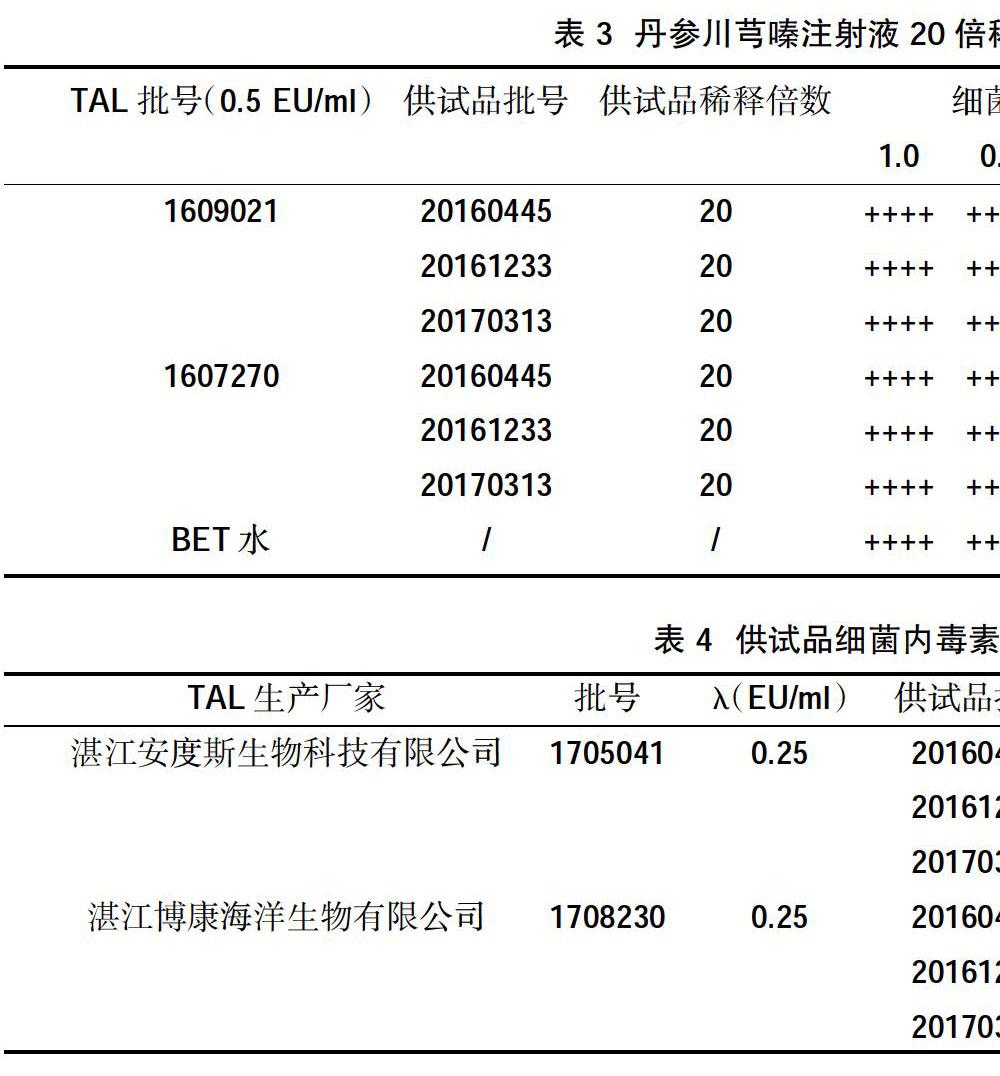
2.5干扰试验 根据预实验结果,在进行正式干扰试验时选择供试品的不干扰浓度为稀释20倍。取3个批号的丹参川芎嗪注射液用BET水分别稀释20倍,分别用稀释20倍的供试品溶液和BET水稀释细菌内毒素标准品(CSE),制成含1.0、0.5、0.25、0.125 EU/ml 4种浓度内毒素的系列溶液。分别与λ=0.5 EU/ml的鲎试剂(TAL)反应,按照《中国药典》2015年版四部通则1143的凝胶限度试验法,进行干扰试验,当阴性对照(NC)为阴性时,结果按公式ES=lg-1(∑Xs/4)和Et=lg-1(∑Xt/4)计算各系列反应终点内毒素浓度的绝对值。式中:Es为内毒素标准对照系列溶液的反应终点浓度的几何平均值;Et为含内毒素的供试品系列溶液的反应终点浓度的几何平均值;Xs和Xt分别为含和不含丹参川芎嗪注射液系列各反应终点细菌内毒素浓度的对数值。由表3可见,ES均在0.5λ~2λ范围内,并且Et在0.5ES~2ES范围内,说明稀释20倍的丹参川芎嗪注射液在此试验条件下,对鲎试剂(TAL)与细菌内毒素(CSE)之间的凝聚反应无干扰作用,符合《中国药典》2015年版四部(通则1143)的判断标准。同时,可以确定丹参川芎嗪注射液对TAL无干扰的浓度>20倍,目前市售的鲎试剂(TAL)均可用于丹参川芎嗪注射液进行细菌内毒素检查。
2.6供试品细菌内毒素检测法的验证 取3个批号的丹参川芎嗪注射液分别用BET水稀释20倍,使用λ=0.25 EU/ml的2个厂家的鲎试剂进行细菌内毒素检查,并按要求做阳性(PPC、PC)、阴性(NPC、NC)对照,3批丹参川芎嗪注射液的内毒素检查结果均符合规定,见表4。
3结论
3.1本文所有表格中“+”表示阳性,“-”表示阴性。其判断标准是形成凝胶且倒转180。不变形、不从管壁滑脱者为阳性;未形成凝胶或形成凝胶不坚固、变形并从管壁滑脱者为阴性。
3.2鲎试剂灵敏度复核试验主要考察鲎试剂灵敏度的标示值(λ)是否准确、人员操作方法是否正确及实验条件是否符合规定[6]。
3.3不同批次供试品对不同厂家的鲎试剂的干扰程度可能存在不同,为了避免因鲎试剂造成的判断失误,在干扰预试验中使用了两个厂家的鲎试剂,对3个批次的丹参川芎嗪注射液进行凝胶限度法内毒素检查,结果显示,两个厂家生产的鲎试剂检验结果相同,同一厂家不同批次的供试品对鲎试剂的反应结果也无差异,因此确定丹参川芎嗪注射液的最大不干扰浓度为稀释20倍。
3.4在干扰实验中,将供试品稀释20倍,用两个厂家的鲎试剂进行干扰验证,结果显示,Es均在0.5λ~2λ范围,3个供试品的Et均在0.5Es~2Es范围,确认在该浓度下供试品无干扰作用。
3.5在内毒素限值确定为30 EU/ml情况下,用灵敏度为0.25 EU/ml的鱟试剂按凝胶限度检查法对3个批次供试品进行细菌内毒素检查,结果均符合规定,表明丹参川芎嗪注射液可适用凝胶限度法进行细菌内毒素检查。
3.6采用凝胶限度检查法检查细菌内毒素,符合《中国药典》2015年版四部(通则1143)的标准,操作简便,结果准确,可以用于质量控制。
3.7《中国药典》2015年版并未收录丹参川芎嗪注射液,也无国家标准对其进行细菌内毒素检查。采用传统的家兔法检查热原,成本高、时间长、影响因素多、灵敏度低。细菌内毒素检查法相比于家兔热原检查法,具有经济、快捷、灵敏和易于标准化的优点,受到了现代药品检验技术的青睐。因此,开展丹参川芎嗪注射液内毒素检查法的研究有着重要的实际意义。
3.8建议将丹参川芎嗪注射液质量标准中的热原检查项改为细菌内毒素检查项,规定每1 ml丹参川芎嗪注射液中含内毒素的量应<30 EU。
