柑青醛合成新铃兰醛反应动力学研究
2018-03-02吴方棣杨自涛范荣玉
吴方棣, 杨自涛, 范荣玉
(武夷学院 福建省生态产业绿色技术重点实验室 福建省竹材工程技术研究中心, 福建 武夷山 354300)
新铃兰醛是一种具有淡雅清香的香料,它的香气持久而不散,并且成本较低,符合广大消费者的要求。近几年来,新铃兰醛在香精中逐步取代了铃兰花香型材料合成的香料铃兰醛。香料市场中例如,纪梵希公司、雅诗兰黛公司、克里斯汀·迪奥公司、宝洁公司等都在香水中添加了新铃兰醛[1-2]。当前,新铃兰醛主要由柑青醛水合制备而成,我国运用松节油合成柑青醛的技术已经比较成熟[3],合成主要有间接水合和直接水合两种方法。直接水合法具有工艺简单、污染小、易于工业化等优点,而有良好的应用前景。因此,近年来对直接水合工艺和动力学的研究成为国内外学者研究的热点。K. Linnow等[4]对水合反应的机理和动力学做了深入研究。王毅等[5]采用半连续反应过程,用离子交换树脂为催化剂,研究了异丁烯水合反应动力学,建立了釜式反应的动力学模型,与实验结果吻合较好。冷冬梅等[6]通过自制催化剂,对油酸与乙醇的酯化反应动力学进行了研究,获得了较优的转化率。郭世卓等[7-8]分别对环戊烯水合和丙烯醛水合本征动力学进行了研究,建立了过程的机理模型。刘小娟等[9]对α-蒎烯直接水合动力学进行了研究,采用拟均相(PH)模型进行拟合,模型计算值与实验值吻合较好。G. D. Yang[10]研究了松节油直接水合过程动力学,采用拟均相(PH)模型进行拟合,获得了反应速率常数方程并计算了反应活化能。D. Cursaru等[11]在多相反应器内,对正丁烯直接水合过程进行了研究,考察了相际传质过程。Y. Liu等[12]等采用阳离子交换树脂作催化剂,研究了莰烯直接水合制备异龙脑反应过程机理及影响因素。
动力学数据是反应器设计、放大和操作控制的基本数据[13],目前国内对柑青醛合成新铃兰醛的动力学研究较少。为此,本文以柑青醛为原料,异丙醇为溶剂,阳离子交换树脂CT-500为催化剂,在消除内、外扩散影响下,考察反应条件对柑青醛水合生成新铃兰醛的影响,建立水合反应动力学模型,为直接水合制备新铃兰醛的工业化过程提供基础数据。
1 实验部分
1.1 仪器和药品
主要仪器:HH-S恒温水浴锅,巩义市站街光亚仪器厂;BS124S电子天平,北京赛多利斯有限公司;S312数显恒速搅拌器,海申生科技有限公司;GC-7850A气相色谱仪,安捷伦。色谱条件:载气为高纯氮,FID检测器;色谱柱为安捷伦19091J-413毛细管柱,规格30 m×0.320 mm。分析条件:进样口温度 240 ℃;采用分流,分流比70∶1;载气流速1.6 mL/min ;气化室温度 250 ℃;检测器温度300 ℃;尾吹流量22.4 mL/min;柱箱温度120~220 ℃;采用程序升温,初始温度120 ℃,保持1 min,然后以10 ℃/min的速度升温至170 ℃,最后以20 ℃/min的速度升温至220 ℃,保持3 min。
主要药品及试剂:柑青醛(质量分数99%),福建浦城县永芳香料厂;癸醇(质量分数98%),阿拉丁;异丙醇(AR),广东光华科技有限公司;CT-500阳离子交换树脂,龙旭化工有限公司;蒸馏水,自制。
1.2 实验方法
采用250 mL间歇搅拌釜式反应器,中间瓶口安装数显恒速搅拌器,两侧分别安装温度计和取样口。在数显恒温水浴锅中进行反应,温度误差控制在±0.2 ℃。先将水浴锅中的水加热至指定的温度,再将柑青醛、水、异丙醇(助溶剂)和催化剂按照比例加入到釜式反应器中,计时开始,间隔一定时间取样,以癸醇为内标物,用气相色谱仪分析组成。
2 结果分析与讨论
2.1 外扩散的影响
该反应是液固催化,即反应物从液相主体到达催化剂外部,再通过催化剂孔隙吸附到活性中心进行反应。通过控制间歇反应釜搅拌转速,来消除外扩散的影响。在反应温度为80 ℃,柑青醛、水、异丙醇物质的量比1∶1∶4,催化剂质量分数7.7%进行反应(粒径为0.6~0.9 mm),改变搅拌转速来考察其对外扩散的影响,实验结果如图1所示。从图1可以看出,搅拌转速从200 r/min增加到400 r/min的过程中,反应速率明显增大;当搅拌转速从400 r/min增加到500 r/min时,反应速率基本不变。可见,当搅拌转速为400 r/min时,能消除外扩散的影响,因此搅拌转速选择400 r/min。
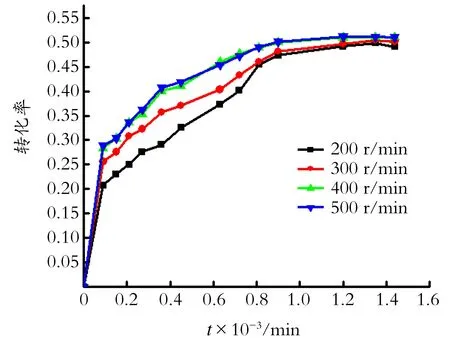
图1 转速对柑青醛转化率的影响Fig.1 The influence of stirring speed on conversion of myrac aldehyde
2.2 内扩散的影响
为了考察内扩散对反应的影响,在反应温度为80 ℃,柑青醛、水、异丙醇物质的量比为1∶1∶4,催化剂质量分数为7.7%,搅拌转速为400 r/min的条件下,选用不同粒径的催化剂进行实验,结果如图2所示。从图2可以看出,3种粒径的催化剂反应速率无明显变化,可见当催化剂粒径小于0.9 mm时,内扩散影响可以忽略。
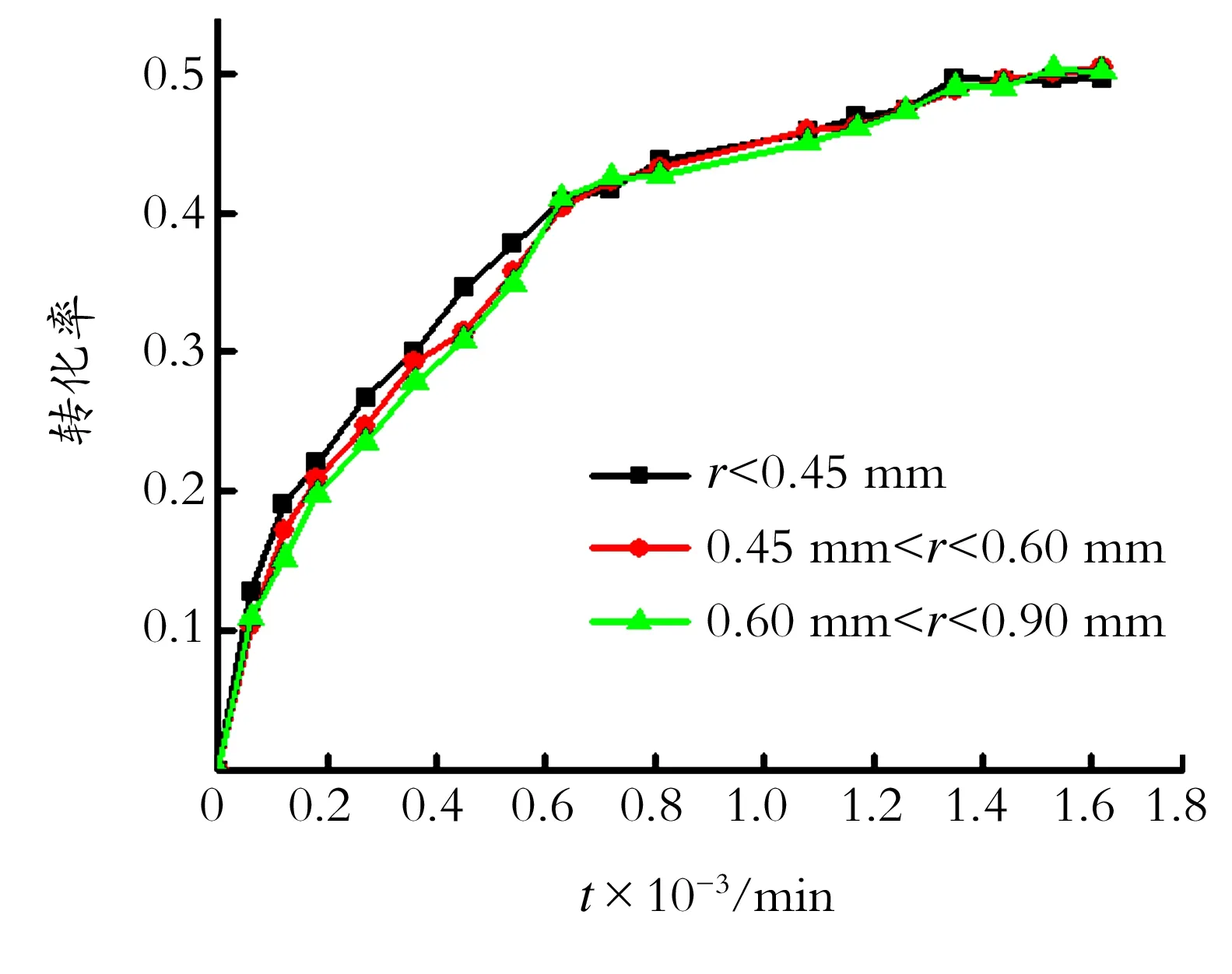
图2 催化剂粒径对柑青醛转化率的影响
Fig.2Theinfluenceofparticlesizeofcatalystonconversionofmyracaldehyde
2.3 反应温度对转化率的影响
在消除内外扩散的影响下,选用催化剂粒径为0.6 ~0.9 mm,搅拌转速为400 r/min,催化剂质量分数为7.7%,柑青醛、水、异丙醇物质的量比为1∶1∶4的条件下,考察反应温度对柑青醛转化率的影响,结果如图3所示。由图3可知,柑青醛水合是一个慢反应,当温度为60 ℃时,反应在25 h左右达到平衡,当温度为80 ℃时,反应在20 h左右达到平衡;温度升高,反应速率增大;同时,达到平衡的转化率也增大,说明柑青醛水合是一个吸热反应。但是当反应温度过高时,柑青醛容易发生聚合反应,所以温度不宜太高。
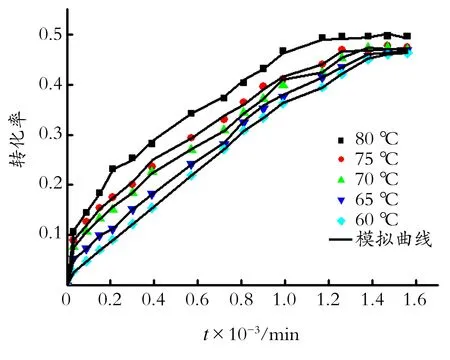
图3 反应温度对转化率的影响
Fig.3Theinfluenceofreactiontemperatureonconversionofmyracaldehyde
2.4 催化剂质量分数对转化率的影响
在消除内外扩散的影响下,选用催化剂粒径为0.6 ~0.9 mm,搅拌转速为400 r/min,反应温度为80 ℃,柑青醛、水、异丙醇物质的量比为1∶1∶4的条件下,考察催化剂质量分数对柑青醛转化率的影响,结果如图4所示。从图4中可以看出,催化剂质量分数增大,反应速率增大,但最终平衡的转化率不变。可见,催化剂质量分数的大小不能改变平衡的状态。
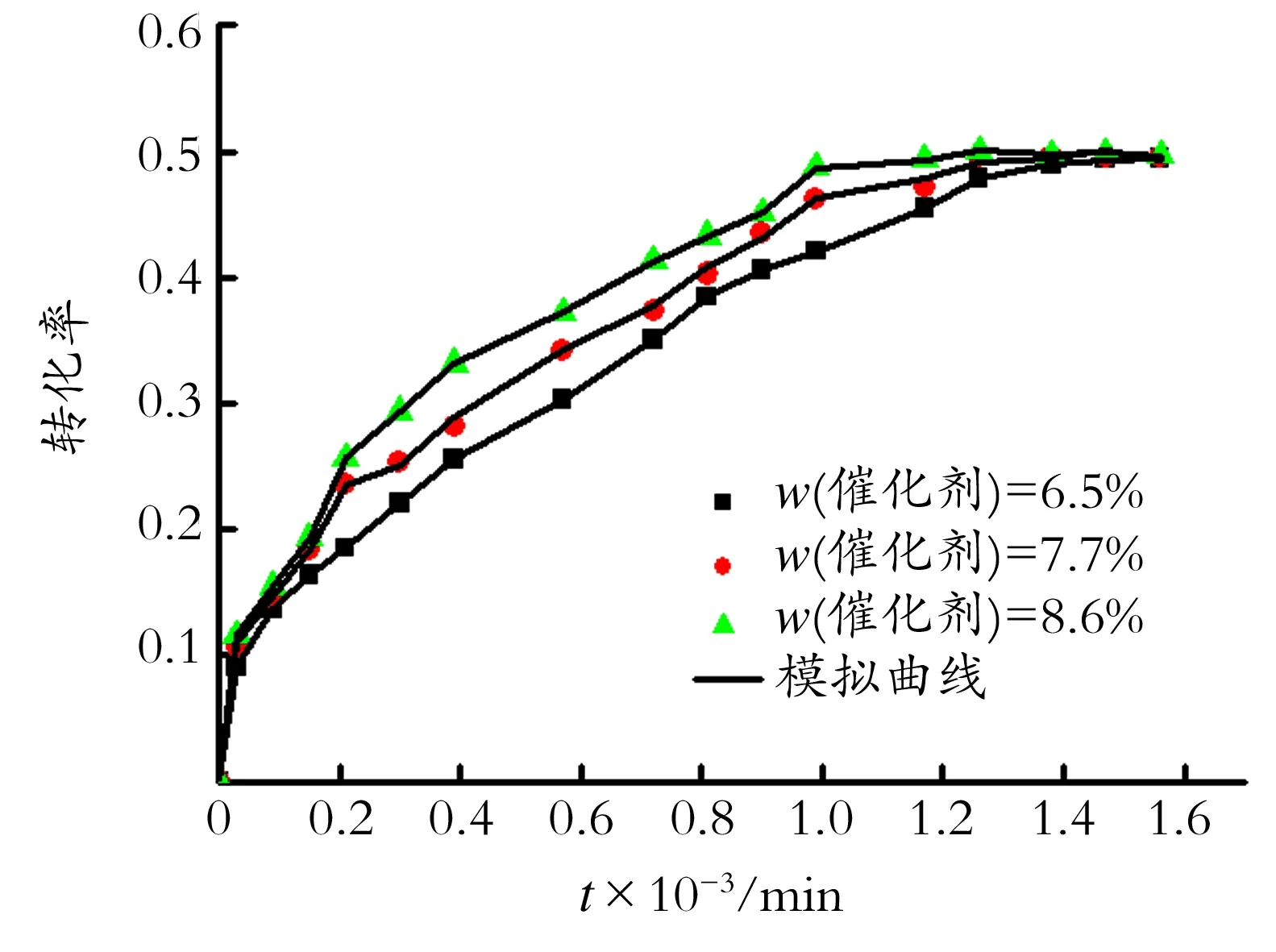
图4 催化剂质量分数对转化率的影响
Fig.4Theinfluenceofmassfractionofcatalystonconversionofmyracaldehyde
3 反应动力学模型
3.1 反应动力学方程
用阳离子交换树脂催化柑青醛水合是液固的非均相催化反应。因此,反应历程包括:(1) 外扩散,原料从液相主体扩散到催化剂外表面;(2) 内扩散,原料从外表面扩散到催化剂内表面活性中心;(3) 吸附,原料吸附于活性中心并反应;(4) 脱附,反应产物从活性中心脱附;(5) 产物经内扩散到达催化剂外表面;(6) 产物由外表面经外扩散进入液相主体。通过选择合适的搅拌转速和催化剂粒径,消除内外扩散,因此反应过程主要受吸附、表面反应和脱附过程控制。
动力学采用LHHW模型方程,模型假设[14]:(1)表面反应是在一个活性中心吸附的柑青醛和与之相邻的另一个活性中心吸附的水之间进行,生成产物新铃兰醛由表面脱附得到;(2)表面反应是反应速率的控制步骤;(3)反应物和生成物竞争吸附于催化剂的活性中心上,且均为单层吸附;(4)催化剂酸性部位为其活性中心。
根据上述假设此反应机理可表示为:

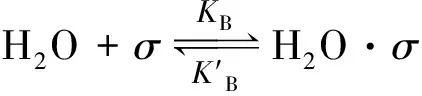
表面反应
(3)
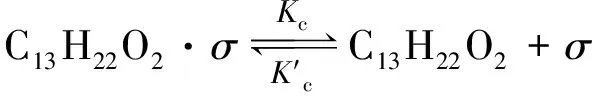
式中,σ表示吸附位,C13H20O·σ、H2O·σ、C13H22O2·σ分别表示吸附态的柑青醛、水、新铃兰醛。
柑青醛和水的净吸附速率分别为:
(5)

新铃兰醛的净脱附速率分别为:
(7)
式中,xi为i组分的摩尔分数,θ为催化剂表面总覆盖度,且
θ=θC13H20O+θH2O+θC13H22O2(8)
根据假设,表面反应为反应速率控制步骤,则柑青醛和水的吸附及新铃兰醛的脱附近似达到平衡,所以,
rA=rB=rC=0(9)
则由式(5)、(6)、(7)得:
ks,C13H20OxC13H20O-ks,C13H20OxC13H20Oθ(10)

ks,H2OxH2O-ks,H2OxH2Oθ(11)

ks,C13H22O2xC13H22O2-ks,C13H22O2xC13H22O2θ(12)
其中,它们的吸附、脱附平衡常数分别定义为:
将式(10)、(11)、(12)代入式(8),得到催化剂表面各组分的覆盖度:
(13)
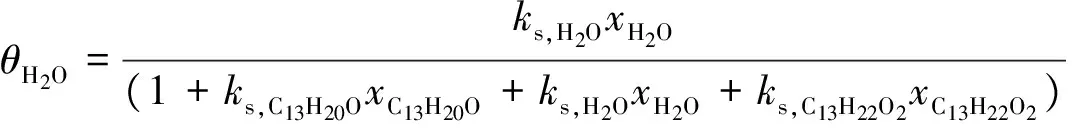
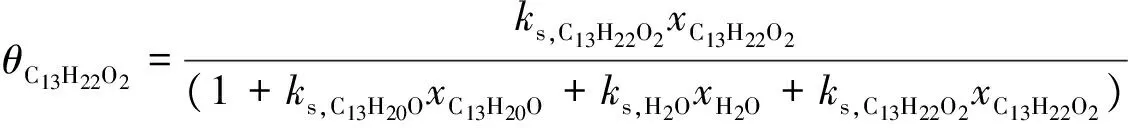
控制步骤是通过表面反应得到,因此得出总反应速率等于表面反应速率。
正向总反应速率:
(16)
逆向总反应速率:
(17)
则净总反应速率:
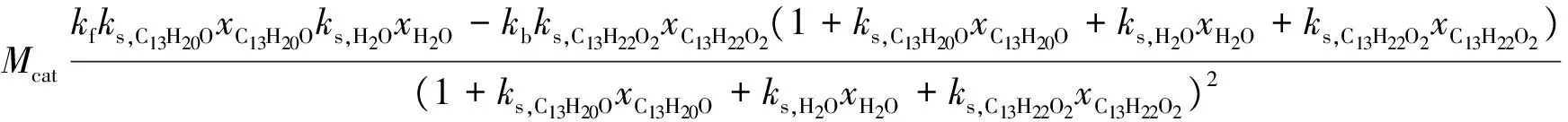
其中,Mcat为催化剂的质量,kg;kf、kb分别为正、逆反应速率常数,mol/(gs);令反应平衡常数Ka为:
(19)
可得水合过程的反应动力学模型方程为:
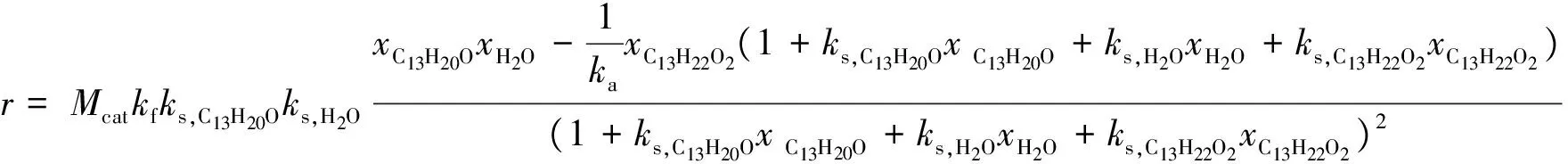
3.2 模型方程参数估算
采用微粒群(PSO)算法,对不同温度下的动力学模型方程参数进行估算,结果如表1所示。从表1可以看出,随着温度升高,正、逆反应速率常数增大,平衡常数增大,说明该过程为吸热反应,升高温度有利于水合反应的进行。

表1 LHHW模型参数Table 1 Parameters of LHHW model
根据范特霍夫方程:
(21)
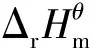
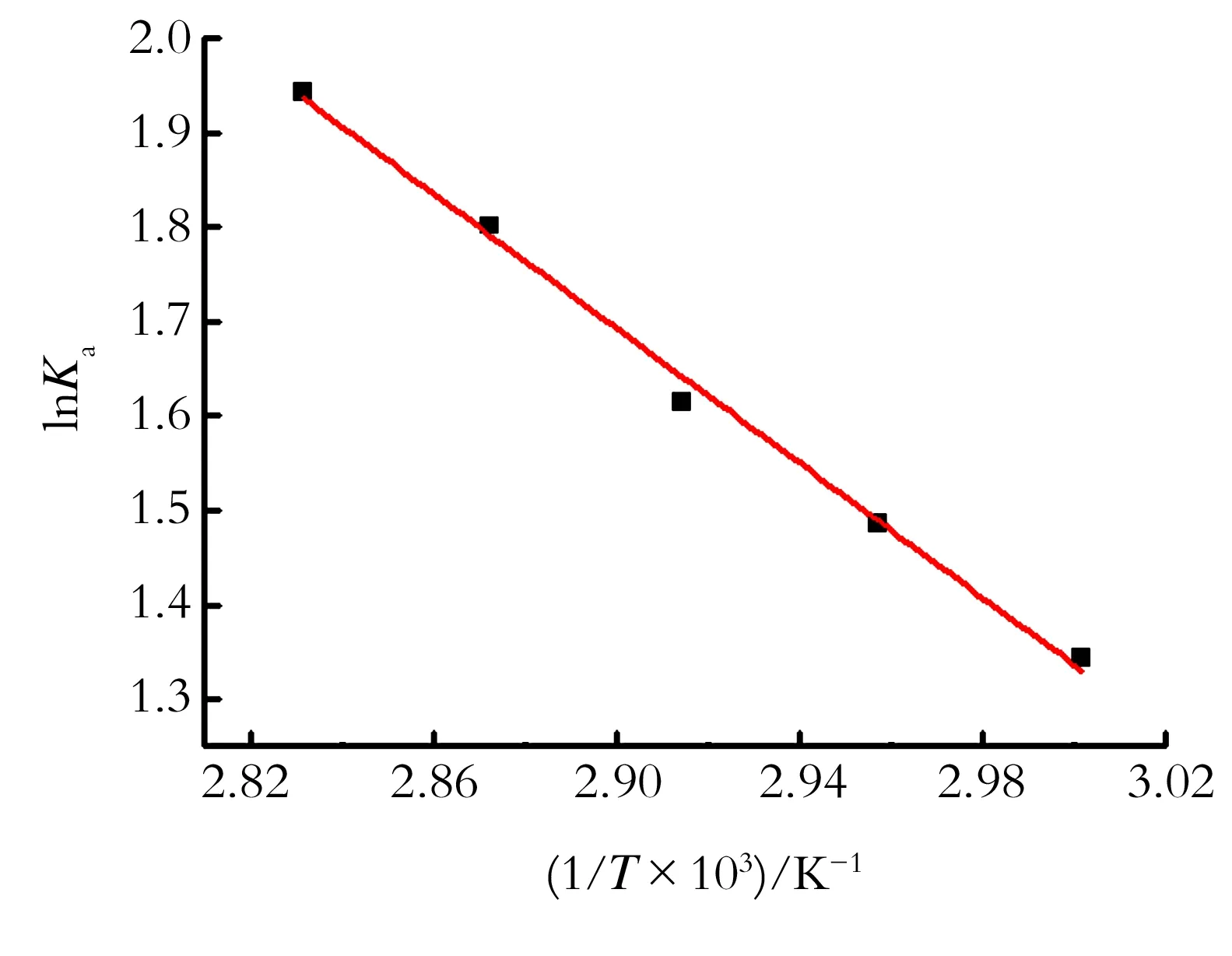
图5 反应平衡常数与温度的关系
Fig.5Relationshipbetweenequilibriumconstantofreactionandtemperture
由最小二乘法拟合得:
(22)
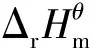
根据阿伦尼乌斯方程:
(23)
对式(23)两边取对数:
(24)
式中,k为反应速率常数,mol/(g·s);A为指前因子,mol/(g·s);E为反应活化能,J/mol。
以lnk对1/T作图,可求得反应活化能E和指前因子A,结果如图6所示。
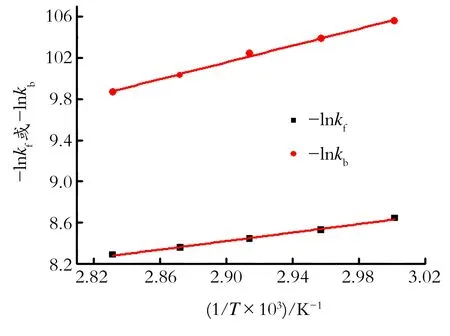
图6 正、逆反应速率常数与温度的关系
Fig.6Relationshipbetweenforwardandbackwardrateconstantofreactionandtemperture
通过最小二乘法拟合,可得到正、逆反应速率常数方程:
(25)
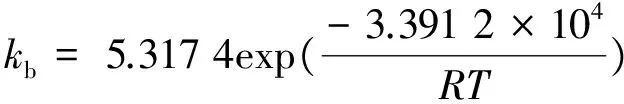
3.3 动力学模型验证
采用拟合得到的模型方程参数,用LHHW模型对实验数据进行拟合,结果如图3、4所示。从图3、4可以看出,模拟结果与实验值基本吻合,实验值与拟合值平均误差不大于3%。可见用该模型方程来描述柑青醛直接水合过程是可行的。
4 结论
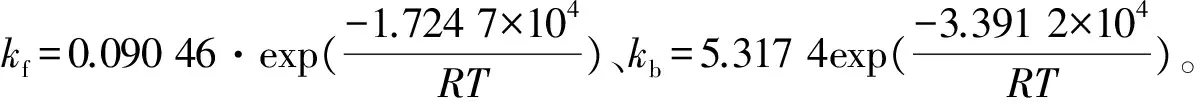
[1] 唐健.新铃兰醛的合成及应用[J].河北化工,2009,32(12):10-11.
Tang J. Synthesis and application of lyral [J].Chemical Industry of Hebei, 2009, 32(12):10-11.
[2] 易封平,毛海舫.合成香料工艺学[M].北京:中国轻工业出版社,2007:126.
[3] 陈艳平, 吴燕翔, 黄智贤. 由柑青醛合成新铃兰醛研究进展[J]. 生物质化学工程, 2008,42(6):61-64.
Chen Y P, Wu Y X, Huang Z X. Progress on the synthesis of lyral from myrac aldehyde [J]. Biomass Chemical Engineering, 2008,42(6):61-64.
[4] Linnow K, Niermann M, Bonatz D, et al. Experimental studies of the mechanism and kinetics of hydration reactions [J]. Energy Procedia, 2014, 48: 394-404.
[5] 王毅, 周明, 许春建. 2NKC-9 离子交换树脂细粉催化异丁烯水合反应动力学[J]. 石油化工,2003, 32(9):775-778.
Wang Y, Zhou M, Xu C J. Kinetics of isobutylene hydration reaction catalyzed by fine powder of NKC-9 ion exchange resin [J]. Petrochemical Technology, 2003, 32(9):775-778.
[6] 冷冬梅, 石采静, 周长行, 等. 碳基固体酸催化剂上的酯化反应动力学研究[J]. 石油化工高等学校学报, 2010, 23(2):16-20.
Leng D M, Shi C J, Zhou C X, et al. The Kinetics study of the esterification on the carbon-based solid acid catalyst [J]. Journal of Petrochemical Universities, 2010, 23(2):16-20.
[7] 郭世卓, 徐泽辉, 周飞, 等. 环戊烯水合反应本征动力学的研究[J]. 石油炼制与化工, 2004, 35(9):34-37.
Guo S Z, Xu Z H, Zhou F, et al. Intrinsic kinetics study on cyclopentene hydration reaction [J]. Petroleum Processing and Petrochemicals, 2004, 35(9):34-37.
[8] 徐泽辉, 郭世卓, 王佩琳, 等. 丙烯醛水合本征动力学的研究[J]. 天然气化工,2001,26(5):18-20.
Xu Z H, Guo S Z, Wang P L, et al. Intrinsic kinetics study on hydration of acrolein [J]. Natural Gas Chemical Industry, 2001, 26(5):18-20.
[9] 刘小鹃,杨高东,张锋, 等. α-蒎烯水合反应动力学研究[J]. 南京大学学报(自然科学版), 2014,50(1):103-112.
Liu X J,Yang G D, Zhang F, et al. Study on the kinetics of α-pinene hydration[J]. Journal of Nanjing University(Natural Sciences),2014,50(1):103-112.
[10] Yang G D, Liu Y, Zhou Z, et al. Kinetic study of the direct hydration of turpentine[J]. Chemical Engineering Journal, 2011, 168(1):351-358.
[11] Cursaru D, Kunz U. Kinetic investigation on direct hydration of n-butene in a multiphase reactor[J]. Rev. Chim. (Bucharest), 2010, 61:1245-1253.
[12] Liu Y, Zhou Z, Yang G D,et al. Study on direct hydration of camphene to isoborneol by cation exchange resins [J]. International Journal of Chemical Reactor Engineering, 2011, 9(1):1-16.
[13] 陈艳平,王碧玉,黄智贤,等.柑青醛合成新铃兰醛水合反应宏观动力学模型研究[J].生物质化学工程, 2010,44(6):18-22.
Chen Y P, Wang B Y, Huang Z X,et al. Study on kinetics model of synthesis of lyral from myrac aldehyde [J]. Biomass Chemical Engineering, 2010,44(6):18-22.
[14] 邱挺, 黄智贤,程春飚,等. 阳离子交换树脂催化合成乙酸正丁酯的动力学[J]. 化学工程与工艺, 2009, 25(4):355-359.
Qiu T, Huang Z X,Cheng C B, et al. Kinetics of synthesis of n-butyl acetate over cation-exchange resin catalyst[J]. Chemical Reaction Engineering and Technology, 2009, 25(4):355-359.
