单分散球状纳米二氧化硅的可控制备方法与机理分析
2018-02-28金永中郑星龙唐春花
王 璐,金永中,陈 建,郑星龙,唐春花
( 四川理工学院材料科学与工程学院,四川 自贡 643000)
引 言
纳米SiO2粒子俗称白炭黑,是一种非常重要的超微无机新材料[1-2],因其粒径很小,可以达到纳米级别,因此具有大比表面积[3],强表面吸附力,高表面能,高化学纯度等特殊性质,以其优越的补强性[4]、稳定性、增稠性[5]和触变性[6]等特性,在众多领域内独树一帜,有着不可取代的作用,因而被广泛用于医药[7]、橡胶填料[8-9]、文物保护[10]、环保、化工[11]等领域。特别是在补强橡胶体系方面,更是需要粒径小、粒径分布窄、单分散性好的纳米SiO2粒子。但是在一种简单的实验条件下合成粒径大小均一、可控、球形形貌较好的SiO2粒子向来是一个较难的问题。
Stöber 法[12]是由Werner Stöber 等人最先发现的一种合成纳米SiO2粒子的方法,该方法可操作性强,制备效率高。具体操作是将正硅酸已酯( Tetraethyl Orthosilicate,TEOS) 加入乙醇和氨水的混合溶液中,通过TEOS水解缩聚生成纳米SiO2粒子。赵立强等人[13]在60 ℃
下制得了粒径约为180 nm 的纳米SiO2粒子,赵丽等人[14]在80 ℃下制得了粒径约为72 nm 的纳米SiO2粒子。这些研究均没有通过调控温度来控制纳米SiO2粒子的粒径变化,粒子团聚较为严重。如果继续升高温度,SiO2粒子的粒径会进一步减小,但也会增加生产成本。因此,探索出一种在温度较低的情况下可控制备纳米SiO2粒子的方法显得十分必要。
本文在Stöber 法的基础上,采用单因素变量控制法,主要研究了催化剂的添加方式,TEOS 浓度和温度对纳米SiO2粒子粒径和形貌的影响,找到了一种能控制粒径大小和粒径分布的方法,以满足多种场合下对不同纳米SiO2粒子的需求,如核壳粒子[15],各种缓释剂载体[16]等,以期为纳米二氧化硅粒子的制备技术提供一定的基础实验数据。
1 实验材料与方法
1.1 实验材料
无水乙醇、氨水、正硅酸已酯( TEOS) 等,均为分析纯,购于成都市科隆化学品有限公司。
1.2 纳米SiO2 粒子的制备
将150 mL 无水乙醇,4 mL 水和12 mL 的氨水(25%) 混合,超声震荡15 min,记为A 液;将一定体积的正硅酸已酯(TEOS)溶于50 mL 无水乙醇,超声震荡25 min,记为B 液。将A 液在一定温度下恒温搅拌10 min 后,缓慢倒入B 液,反应一定时间至溶液呈浑浊状态后进行收集,收集液经过滤、洗涤后得到滤渣,滤渣置于100 ℃的真空干燥箱中干燥2 h 以上,然后测试表征。在传统的Stöber 方法中,TEOS 未经稀释就直接加入无水乙醇和氨水的混合液中,而本实验预先将TEOS 进行稀释,降低其浓度,由此可避免TEOS 在高浓度条件下就被氨水催化生成容易团聚的纳米SiO2粒子。
关于催化剂的选择,尚雪梅[17]和刘羽[18]分别使用了酸性催化剂盐酸和硝酸,但催化效率较低,会延长反应的时间,降低制备效率。王丽[19]等人使用了有机催化剂L-赖氨酸来进行催化反应,但是最终样品的球形度较低。而碱性催化剂氨水催化效率相对较高,制得的纳米SiO2粒子的球形形貌好,且成本较低,因此本次实验选用氨水作为催化剂进行碱催化反应。
1.3 表征方法
采用Hitachi S4800 型扫描电镜( 日立公司) ,EVO-18 型扫描电镜( 德国蔡司公司) 和MIRA-3 型场发射扫描电镜( 捷克TEACAN 公司) 对纳米二氧化硅的SEM 形貌进行观察; 采用Tensor 27 傅里叶红外光谱仪( 德国Bruker 制造公司) 对样品表面基团类型进行测试,波长为400 cm-1~4000 cm-1。
2 结果与讨论
2.1 催化剂添加方式对纳米SiO2 粒子粒径的影响
氨水不同添加方式下纳米SiO2的SEM 图如图1 所示。图1( a) 为制备体系中一次性加入9 mL 氨水来进行反应所生成的纳米SiO2粒子的SEM 图,图1( b) 为体系中先加入6 mL 氨水,反应2 h,然后再添加3 mL 氨水,继续反应生成的纳米SiO2粒子的SEM 图。

图1 氨水不同添加方式下纳米SiO2 的SEM 图
从图1( a) 和1( b) 可知,一次性加入9 mL 氨水所制备的纳米SiO2粒径约为60 nm,单分散性好; 而分2 次依次加入6 mL 与3 mL 氨水所制备的纳米SiO2粒径约为20 nm,但出现了较为轻微的团聚。由此可见在氨水总量相同的情况下,分段添加与一次性添加相比,前者生成的纳米SiO2粒子的粒径可减小至后者的1/3 左右。这是因为在碱性环境中,正硅酸已酯( Si( OC2H5)4) 的水解反应是OH—亲核进攻Si 原子,OH—起催化作用,先只加入6 mL 氨水,氨水的量较少,电子云不易向乙氧基偏移而脱去,使TEOS 水解速率减小,生成的水解产物羟基化物SiR4-x( OH)x(1≤x ≤4,R 为乙氧基) 的量不足以快速地引发脱水缩聚反应生成纳米SiO2粒子,但另一方面所生成的羟基化物SiR4-x( OH)x相互间进行了不完全的缩合反应,形成SiO2粒子形核生长前的核心,这也是为什么先加入6 mL 的氨水,反应相当长一段时间后整个溶液体系仍然呈现透明澄清状态的原因。反应2 h后继续加入3 mL 的氨水,羟基化物SiR4-x( OH)x得以水解完全,以之前形成的核心为生长点,生成SiO2粒子,由于预先添加氨水之后,生成的SiO2粒子生长核心数目较多,又因为添加的TEOS 的量是有限的,所以分段添加氨水能使得粒子粒径显著降低。
从反应体系的宏观变化来看: 第一次添加6 mL 氨水时,整个体系在很长时间内保持无色透明的状态,继续添加3 mL 氨水后,溶液逐渐变为较澄清的乳白色状态并一直维持下去,说明体系中生成了小粒径的纳米SiO2粒子;而直接一次性加入9 mL 的氨水,整个溶液体系在15 min 左右以后开始出现乳白色,30 min 后出现较为浓厚的乳白色,说明生成的SiO2粒子的粒径较大。由此也说明分段添加氨水的方式会使得生成的SiO2粒子粒径显著减小。
2.2 TEOS 用量对纳米SiO2 形貌的影响
不同TEOS 用量下纳米SiO2粒子的SEM 图和粒径大小分别如图2、图3 所示。

图2 不同TEOS 用量下纳米SiO2 的SEM 图
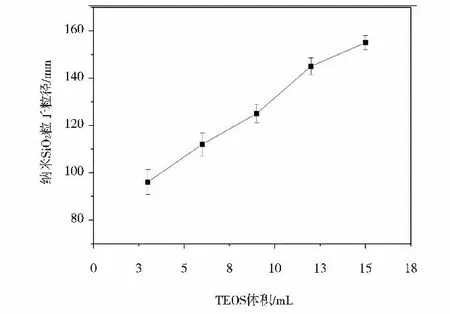
图3 纳米SiO2 的粒径随TEOS 用量的变化
从图2( a) ~2( e) 可知,随着TEOS 用量的增加,整个体系反应物的浓度增大,但纳米SiO2粒子的球形形貌一直保持良好,颗粒与颗粒之间界限明显,单分散性好。由此说明对于制备单分散性好的纳米SiO2粒子来说,预先将TEOS 稀释后再进行反应是十分必要的。从图3 可知,TEOS 用量为3 mL ~15 mL 时,纳米SiO2粒子粒径从90 nm 增至160 nm,即TEOS 每增加3 mL,粒径增幅约为20 nm,表明随着TEOS 用量的增加,SiO2粒子粒径逐渐变大。这可能是因为TEOS 用量的增加使得水解产物羟基化物SiR4-x( OH)x的浓度也会增大,因此,基团与基团之间相互碰撞的几率增大,使得较多的水解产物发生缩聚反应,因此生成的纳米SiO2粒子粒径也随着增大。
2.3 温度对纳米SiO2 形貌的影响
在TEOS 用量为6 mL 的条件下,研究反应温度对纳米SiO2的SEM 图和粒径大小的影响,结果分别如图4、图5 所示。

图4 不同反应温度下纳米SiO2 的SEM 图
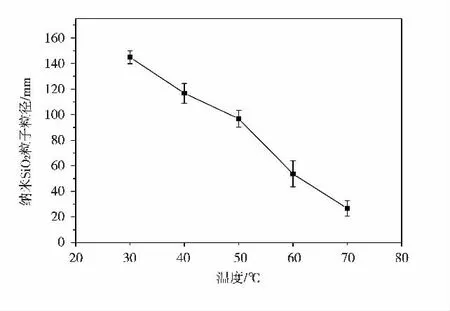
图5 纳米SiO2 的粒径随反应温度的变化
从图4 和图5 可知,当温度逐渐上升时,纳米SiO2的粒径逐渐下降,当温度为30 ℃、40 ℃、50 ℃时,二氧化硅微球具有非常好的球形形貌,粒径大小均一,颗粒与颗粒之间有着明确的轮廓界限,平均粒径分别约为145 nm、117 nm、97 nm。当温度上升至60 ℃和70 ℃时,颗粒平均粒径分别约为54 nm、27 nm,60 ℃时颗粒与颗粒之间形成较为轻微的团聚; 70 ℃时,SiO2粒子大小几乎一致,未出现极大或者极小的颗粒,表明粒径分布窄,颗粒与颗粒之间的界限十分明显,几乎没有团聚,样品稳定性好,将其放置较长一段时间后也没有出现严重的团聚。
Stöber 法制备纳米SiO2粒子的过程中,主要涉及三种类型的反应[20]: ( 1) 生成硅羟基( Si -OH) 的水解反应;(2) 生成水的缩合反应; ( 3) 生成醇的缩合反应。以上反应的表达式分别为:
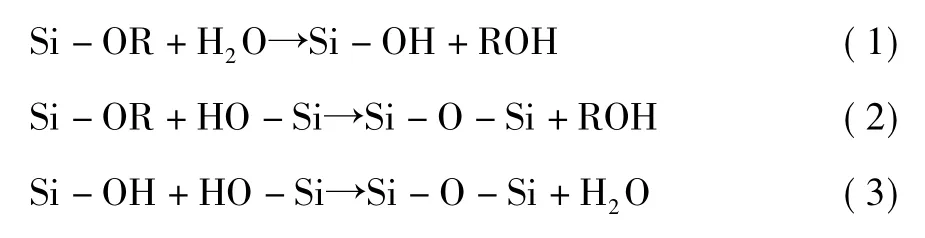
式中,R=C2H5。
TEOS 的水解反应( 1) 是四个乙氧基逐步被羟基取代的过程,期间需要的活化能逐渐增多使得取代的难度增加,而提高反应温度可为此提供更多的能量,使水解反应进行得更彻底。TEOS 完全水解生成的中间产物是形成形貌规整、粒径均一的SiO2粒子的关键,因此适当升高反应温度是有必要的。反应( 2) 和反应( 3) 总的来讲都是形成Si - O - Si 键的缩合反应,这是形成纳米SiO2粒子的核心所在,这两个反应的速率常数都随着反应温度的升高而减小,纳米SiO2的粒径大小可以通过控制其缩合反应的速率来决定。升高温度也有利于小颗粒从其它颗粒表面脱附,使得被覆盖的活性基团能够继续参与反应[13]。从实验结果来看,通过30 ℃~70 ℃的温度调节使SiO2粒子粒径在25 nm ~145 nm 范围内波动,反应温度每增加10 ℃,粒径减幅30 nm 左右,由此实现了通过调节反应温度来调控粒径。
2.4 纳米SiO2 的傅里叶变换红外光光谱分析
不同反应温度下所生成的纳米SiO2的傅里叶变换红外光光谱( Fourier Transform Infraredr,FTIR) 图如图6所示。
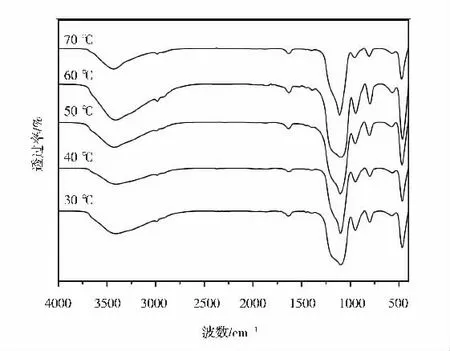
图6 不同反应温度下纳米SiO2 的FTIR 图
从图6 可知,不同反应温度下纳米SiO2的红外光谱图均一致,在460 cm-1~470 cm-1处,有一个较强的吸收峰,此为Si-O-Si 键的弯曲振动峰;在800 cm-1处为O-Si -O弯曲振动吸收峰;940 cm-1~950 cm-1处为Si -OH 伸缩振动吸收峰;1100 cm-1~1110 cm-1处为Si -O -Si 伸缩振动吸收峰;1630 cm-1处为N-H 伯胺伸缩振动吸收峰,这可能是体系中少量的氨水吸附在了二氧化硅表面所致;3400 cm-1~3450 cm-1处为二氧化硅表面的吸附水引起的H-O-H 伸缩振动吸收峰。由此可知1100 cm-1~1110 cm-1处的Si-O-Si 伸缩振动吸收峰最强,460 cm-1~470 cm-1处Si-O-Si 键的弯曲振动峰次之,这两处强峰表明了样品中有大量的桥氧键存在[21-22],证明了正硅酸已酯在水解之后缩聚生成了纳米SiO2粒子。从图6 还可知样品不含有除SiO2特征官能团外的其他的官能团,说明样品纯度高。
3 结 论
(1) 在催化剂氨水总量不变的情况下,分2 次依次添加6 mL 与3 mL 与一次性添加9 ml 相比,前者生成的纳米SiO2粒子的粒径可减小至后者的1/3 左右,其主要原因在于前期添加适量的氨水使得TEOS 水解不完全,但又能形成大量SiO2粒子的形核核心。
(2) TEOS 用量为3 mL ~15 mL 时,纳米SiO2粒子粒径从90 nm 增至160 nm,即TEOS 每增加3mL,粒径增幅约为20 nm,表明随着正硅酸已酯用量的增加,纳米SiO2粒子的粒径逐渐增大。
(3) 反应温度在30 ℃~70 ℃时,纳米SiO2粒子的粒径从145 nm 降至27 nm,即温度每增加10 ℃,粒径减小约30 nm,说明在一定温度范围内,可以通过调控温度来实现对纳米SiO2粒子粒径的控制。反应温度为70 ℃时,制得的纳米SiO2粒子粒径分布窄,球形形貌和单分散状态好,纯度高,稳定性好。
综上所述,从粒径可调节范围,产物最终形貌和单分散状态来看,改变温度是调节纳米SiO2粒子粒径的最有效方式。
