有关化学式计算的教学设计
2018-02-26汪琰
汪琰


一、课程标准、教材以及学生分析
有关相对分子质量的部分包含了相对分子质量的含义、计算相对分子质量、组成物质的各元素的质量比和计算物质中某元素的质量分数等内容,课程标准对这些内容要求不高,教学中注意不要任意扩大与加深。依据化学式的意义,逐一展开有关化学式的计算,应从简单到复杂。
二、教学目标
知识与技能:
(1)了解相对分子质量的含义,并能利用相对原子质量和相对分子质量计算物质的组成。
(2)能看懂商品标签或说明书上标示的物质成分和含量。
过程与方法:
通过交流、活动探究,培养学生利用所学的知识解决实际问题的能力和基本计算能力。
情感态度与价值观:
通过讨论交流、活动探究,发展学生善于合作、勤于思考、勇于实践的精神。
三、教學重、难点
重点
有关相对分子质量、元素质量比和元素质量分数的计算。
难点
物质中某元素质量分数的计算和物质质量与元素质量的互求。
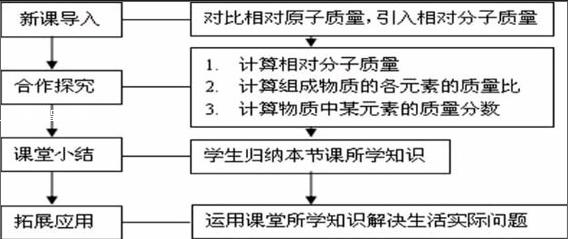
四、教学流程
五、教学设计
【课前准备】收集2种药品、饮料和食品的标签或说明书
【投影】一些食品、药品包装说明书
【设问】分子是由原子构成的,原子具有相对原子质量,那么分子有相对分子质量吗?
指导学生阅读课本P87 什么是相对分子质量。
【设计意图】联系旧知,激发学生探究欲。
【自学交流】怎样计算相对分子质量呢?指导学生阅读课本P87例
【例题演示】规范计算格式
【模仿练习】每个学习小组一位同学在答题板上板演一小题,其他同学在学案上完成。每小题有2~3个学习小组板演。
1、计算下列物质的相对分子质量(写出简单的计算过程)
① H2O2 ② Ca(OH)2 ③ NH4NO3
【讨论交流】学生互纠,概括小结计算相对分子质量的要点:各原子的相对原子质量之和即相对分子质量。
【设计意图】让学生自主参与,获得亲身体验,形成善于质疑,乐于探究的积极态度。
【设问】由于纯净物有固定的组成,所以纯净物中各元素的质量比是固定的。CO2中碳元素与氧元素的质量比是多少?
【例题演示】 规范计算格式
【模仿练习】2、计算下列物质组成元素的质量比(写出简单的计算过程)
① H2O2 ② Ca(OH)2 ③ NH4NO3
【讨论交流】学生互纠,注意计算格式
【设问】知道元素间的质量比的表示方法,我们还能知道某元素的质量分数吗?
【指导自学】课本P87计算物质中某元素的质量分数,强调什么叫某元素的质量分数,如何表示?
【例题演示】规范计算格式
【模仿练习】3、已知铁锈的主要成分是氧化铁,其化学式为Fe2O3,试计算氧化铁中铁元素的质量分数。
【讨论交流】学生互纠,注意计算格式。
【设问】如有1000t氧化铁,则可生产多少吨铁?
【归纳总结】物质中的某元素的质量=物质质量×化合物中该元素的质量分数
【设计意图】创设新题培养学生分析、综合运用能力。
【课堂小结】
【拓展应用】儿童缺锌会引起食欲不振、发育不良。右图为某种补锌口服液说明书的一部分,请回答:(1g=1000mg)
(1)葡萄糖酸锌由
种元素组成。
(2)葡萄糖酸锌中碳、氢元素的质量比为。
(3)葡萄糖酸锌含锌元素的质量分数为(C12H22O14Zn相对分子质量为455,计算结果保留到0.1%)
(4)每支口服液中葡萄糖酸锌的质量为。(计算结果精确到0.1mg)
【设计意图】教给学生查看商品标签中有关成分、含量或纯度。引导学生利用已有知识和经验,学会判断和识别信息。
【拓展提升】根据标签或说明书自编有关化学式计算的题目并解答,下图为某精制碘盐包装袋上的部分说明文字。已知:碘酸钾化学式为KIO31000g碘盐中含20mg碘,成人每天约需0.15mg碘。
【讨论交流】
【设计意图】将课堂所学知识与日常生活联系起来,让学生运用课堂所学解决生活实际中的问题。既巩固了课堂所学知识,也培养了学生学以致用的意识,同时还有利于化学学科价值的体现。
【板书设计】
有关化学式计算
1、计算物质的相对分子质量
2、计算化合物中元素的质量比
3、计算化合物中某元素的质量分数
(作者单位:江苏省南京市文昌初级中学 210000)
