伊维菌素微乳的研制及质量评价
2018-02-10朱庆贺王丽坤骆宏伟金振华史同瑞
朱庆贺,陈 曦,王丽坤,王 爽,骆宏伟,张 莹,金振华,史同瑞
(黑龙江省兽医科学研究所,黑龙江齐齐哈尔 161005)
药物递药系统是医药界的热点研究领域之一。微乳(microemulsion,ME)是一种新型递药系统,该系统是由表面活性剂、辅助表面活性剂、油和水以适当的比例乳化而成的一种均匀、低黏度、热力学稳定的透明或半透明分散体系[1-2]。微乳是由英国化学家Schulman等于1943年首先提出的。自20世纪70年代以来,人们对微乳的微观结构、形成理论、理化性质进行了较为深入的研究,并将微乳应用于工业、日用化工业等领域。至20世纪90年代,人们又对微乳作为药物的递药系统进行了研究,并逐渐引起了人们的重视。虽然微乳与传统乳状液有着许多相似之处,但两者之间也存在着本质的区别。微乳是介于乳状液和胶团溶液之间的一种过度中间状态溶液,是一种热力学稳定的体系,制备时不需要强大的外力,可以长期贮存,且离心不分层。微乳具有极高的稳定性和对溶质的高度分散性及吸附能力;微乳作为难溶性药物的载体,具有加溶作用,使不溶或难溶性药物的溶解度显著升高,从而提高药物的生物利用度及机体的吸收速率[3-4]。
伊维菌素(ivermectin,IVM)具有广谱、高效、安全等优点,是一种广谱的抗寄生虫药物,对动物体内外寄生虫,尤其是线虫和节肢动物,具有高效驱杀作用。由于伊维菌素几乎不溶于水,因此,制约了伊维菌素的应用范围。目前,伊维菌素液体制剂主要有溶液剂、口服液、注射剂、乳剂、喷剂、透皮剂和浇泼剂等[5]。由于多数伊维菌素液体制剂均使用了大量的有机溶剂,且载药量低,临床用药量大,因而常引起用药部位发生炎症和坏死,影响了该类药物的使用效果。为克服现有弊端,本研究结合微乳制备技术,研究开发了50 mg/mL伊维菌素微乳剂,旨在方便伊维菌素的临床使用,提高其应用效果。
1 材料与方法
1.1 材料
1.1.1 药品 伊维菌素,含量97.0%,武汉益华成科技发展有限公司产品;伊维菌素标准品,含量92.0%,中国食品药品检定研究院产品;蓖麻油,郑州智远化工产品有限公司产品;肉豆蔻酸异丙酯,上海高维实业有限公司产品;丙二醇、正丁醇、正戊醇,油酸、司班-80、吐温-80,天津市巴斯夫化工有限公司产品。
1.1.2 仪器 LC-20AT高效液相色谱仪,日本岛津公司产品;Winner802纳米粒度仪,济南微纳颗粒仪器股份有限公司产品;PXNDJ-2000型全自动运动黏度测定仪,上海轩澄仪器有限公司产品;ZNCL-S型恒温磁力搅拌器,上海羌强仪器设备有限公司产品;WD-A药物稳定性检查仪,天津药典标准仪器厂产品。
1.2 方法
1.2.1 配方筛选与微乳剂制备 在单因素试验基础上,将筛选的表面活性剂、辅助表面活性剂按质量比(Km)1∶2、1∶3、1∶4比例混合,配制成混合表面活性剂,再将筛选的油相分别与各配比的混合表面活性剂按质量比1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1比例混匀。称取约一定量的伊维菌素分别加入,混匀溶解,在室温环境缓慢加入超纯水,并不断搅拌,观察各配方体系的性状变化,记录体系由浑浊变至澄清时的临界加水量。分别以油、表面活性剂和助表面活性剂作为三相,利用Origin 8.0绘制不同质量比值的伪三元相图,观察乳区的大小,确定配方中最适Km值、微乳界限及乳剂配方[6-8]。
1.2.2 物理特性测定
1.2.2.1 性状与pH 外观检查50 mg/mL伊维菌素微乳剂性状,用精密pH计测定pH。
1.2.2.2 黏度与粒度测定 应用全自动运动黏度计测定黏度。测试条件:温度25 ℃,黏度系数1.20,同条件下测定3次,测得50 mg/mL伊维菌素微乳剂的运动黏度,该温度下运动黏度和同温度下液体密度之积为其动力黏度。应用纳米粒度仪,测定微乳剂粒径大小及分布。
1.2.2.3 微乳类型鉴别 采用染色法[9]鉴别。取水溶性亚甲蓝染液和油溶性苏丹红染液,分别滴入50 mg/mL伊维菌素微乳剂中,轻轻摇晃,观察比较两种染液颜色在微乳剂中的扩散速度,判断乳剂类型。
1.2.3 药物含量检测方法建立
1.2.3.1 色谱条件 流动相为甲醇∶乙腈∶水=40∶55∶5;流速1.0 mL/min;检测波长244 nm;柱温25 ℃;进样量20 μL。
1.2.3.2 溶液配制 精密称取伊维菌素标准品10 mg,置于50 mL容量瓶中,加流动相溶解后定容至刻度,制成200 μg/mL的储备溶液, 精密量取储备液5.0 mL, 置10 mL容量瓶中,加流动相稀释至刻度,摇匀,配置成100 μg/mL的标准对照品溶液。
精密量取伊维菌素微乳相当于伊维菌素10 mg,置于100 mL容量瓶中,加流动相定容至刻度,超声30 min,摇匀,经0.45 μm滤膜过滤,制成供试品溶液,进样测定。精密量取与供试品等量的空白乳剂,按照供试品溶液的制备方法制成阴性对照品溶液。
1.2.3.3 方法专属性考察 取伊维菌素标准溶液、伊维菌素微乳供试品溶液、空白基质溶液用流动相按一定比例稀释后,分别进样20 μL,测定成分峰值,记录色谱图。
1.2.3.4 标准曲线绘制 精密量取对照品储备液1.0、3.0、5.0、8.0、10 mL分别置10 mL容量瓶中,加流动相稀释至刻度,摇匀,配置成浓度分别为20、60、100 、160 、200 μg/mL的系列对照品溶液。按1.2.3.1项下色谱条件测定,以峰面积(y)对利福昔明的浓度(x,μg/mL)进行线性回归方程。
1.2.3.5 稳定性试验 取浓度为100.0 μg/mL的标准溶液,避光保存,于0、2、4、6、8、12 h后进样20 μL,分别测定峰面积并代入标准曲线方程,计算实测浓度,并计算得其RSD。
1.2.3.6 回收率试验 分别精密取适量储备液并添加配方剂量的空白微乳,超声溶解后用流动相稀释成低(L=60 μg/mL )、中(M=100 μg/mL)、高(H=160 μg/mL)3种理论浓度的溶液,每个浓度配制3份,分别测定其含量,计算其回收率。
1.2.3.7 样品含量测定 按照1.2.3.2项下供试品溶液制备方法处理样品,制备供试品溶液,按上述色谱条件测定峰面积,按外标法计算得样品中伊维菌素的含量。
1.2.4 稳定性评价
1.2.4.1 离心、灭菌、冷冻试验 取50 mg/mL伊维菌素微乳剂,加入离心管中,以10 000 r/min转速离心30 min;置高压灭菌器内,在121℃条件下高压灭菌30 min;在-20 ℃环境贮存7 d~10 d,取出置室温环境,分别观察50 mg/mL伊维菌素微乳剂性状。
1.2.4.2 光照试验 取50 mg/mL伊维菌素微乳剂样品3批,在光照度4 500 lx±500 lx条件下放置10 d,观察微乳剂性状,测定pH,以及黏度、粒度及伊维菌素含量。
1.2.4.3 加速试验 取50 mg/mL伊维菌素微乳剂样品3批,置温度40℃±2℃环境中放置6个月,每月取样,观察微乳剂性状,测定伊维菌素含量。
1.2.4.4 长期试验 取50 mg/mL伊维菌素微乳剂样品3批,置室温环境中放置24个月,分别在0、3、6、9、12、18、24个月取样检测,观察微乳剂性状,测定伊维菌素含量。
2 结果
2.1 配方筛选结果
根据伪三元相图筛选结果,当表面活性剂与辅助表面活性剂的质量比为1∶4时,形成的微乳乳区面积最大,因此,选择微乳区大、稳定性好的各组分配比作为微乳剂配方(图1)。筛选的50 mg/mL伊维菌素微乳剂各组分配比为伊维菌素5%、油6.79%、乳化剂13.58%、辅助乳化剂54.27%、超纯水20.36%。

图1 不同乳剂体系的伪三元相图
2.2 乳剂物理特性
外观50 mg/mL伊维菌素微乳剂为淡黄色、油状透明液体,微乳剂pH为6.27~6.32,运动黏度为610.50 mm2/s,动力黏度为714.28 mPa·s,乳滴粒径主要分布在1 nm~10 nm范围内,平均粒径为6.30 nm(图2)。微乳剂类型鉴别结果表明,水溶性亚甲蓝染液扩散速度较快,由此判定50 mg/mL伊维菌素微乳剂为O/W型乳剂。
2.3 伊维菌素含量检测方法
2.3.1 方法专属性考察 分别测定伊维菌素标准溶液、伊维菌素微乳供试品溶液、空白基质溶液的峰面积。如图3所示,供试品溶液和标准溶液保留时间一致,约5.3 min,组方中的辅料在此时无吸收,所以不干扰伊维菌素含量的测定。
2.3.2 标准曲线绘制 依据试验结果,得回归方程y=33 962x+26 173,R2=0.999。试验表明,伊维菌素浓度在20.0 μg/mL~200.0 μg/mL范围内呈良好的线性关系。

图2 50 mg/mL伊维菌素微乳剂粒径分布曲线图
2.3.3 稳定性试验 分别测定0、2、4、6、8、12 h标准品溶液峰面积并代入标准曲线方程,计算实测浓度,得其RSD=1.3%(表1)。
2.3.4 回收率试验 分别测定高、中、低三种浓度标准溶液含量,计算得其平均回收率为98.37%~101.70%(表2)。
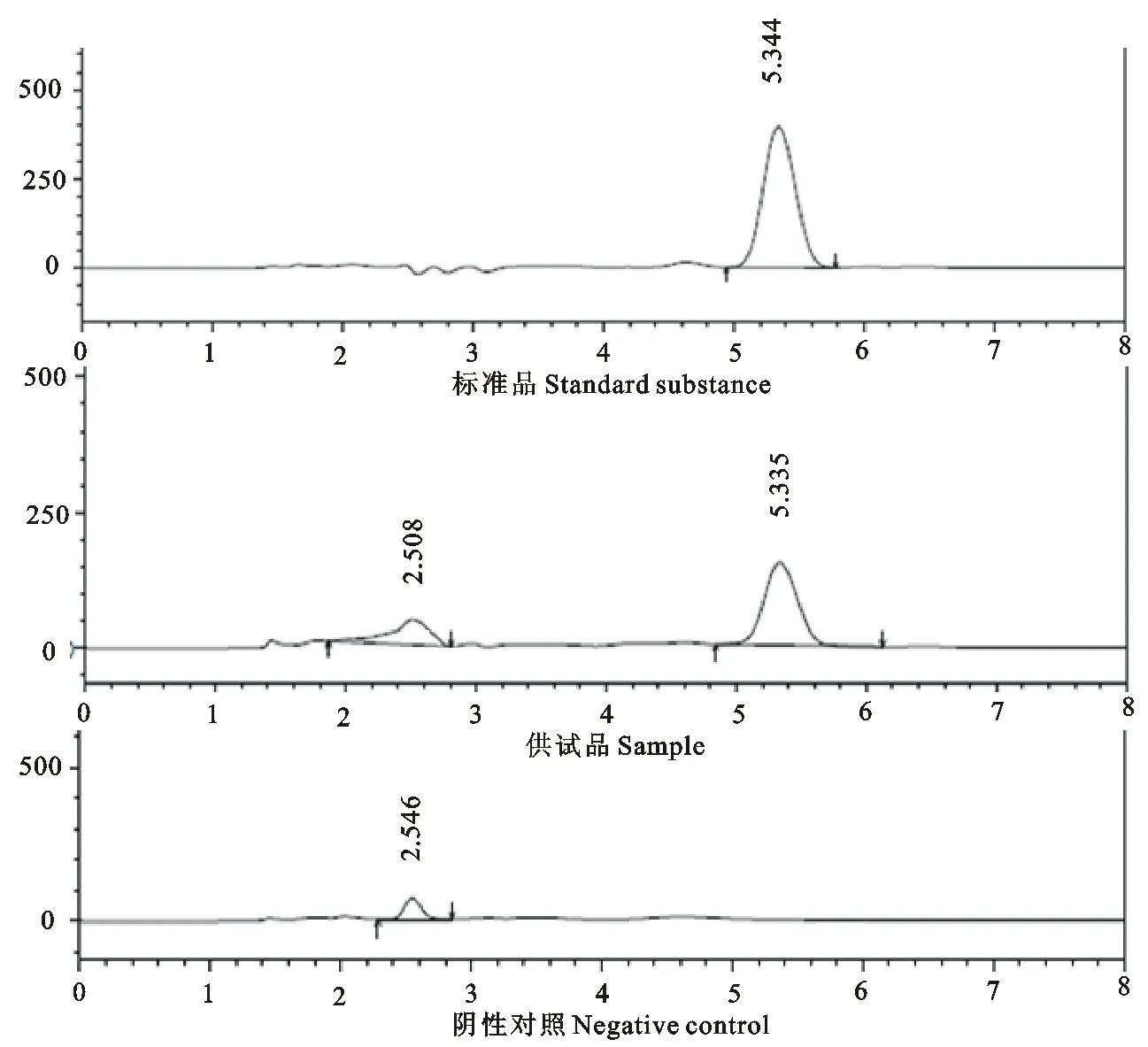
图3 伊维菌素HPLC色谱图
2.4 微乳剂稳定性
50 mg/mL伊维菌素微乳剂经10 000 r/min离心30 min,未见分层、析出等异常现象。在121℃高压灭菌30 min及冷冻保存后,外观性状均未见异常变化。光照试验结果表明,微乳剂在光照度4 500 lx±500 lx条件下放置10 d,其pH、平均粒径、运动黏度、动力黏度、药物含量均未见明显变化(表3)。加速试验和长期试验结果表明,微乳剂外观性状均未见变化,药物含量均在正常范围内,符合药物质量规定(表4和表5)。

表1 稳定性试验结果

表2 回收率试验结果
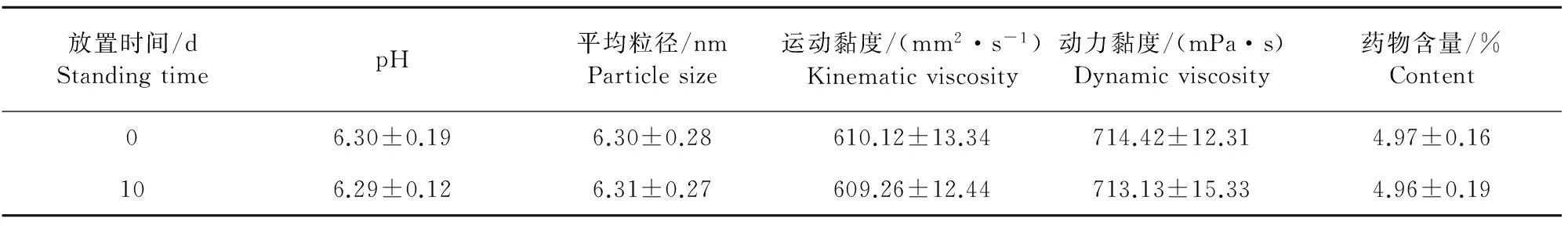
表3 伊维菌素微乳剂光照试验结果
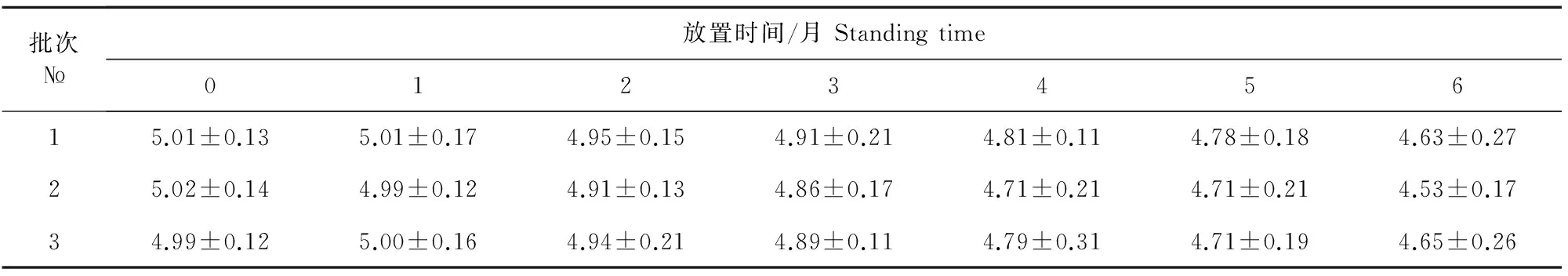
表4 加速试验中伊维菌素的含量测定结果

表5 长期试验中伊维菌素的含量测定结果
3 讨论
在制备微乳剂时,确定油相和乳化剂的种类及配比是决定乳剂稳定性的关键因素。本试验首先依据伊维菌素在不同油相中的溶解度,选择溶解度高的油相作为初选油相,然后依据亲水亲油平衡值(HLB),选择表面活性剂。根据油相对制备O/W型微乳所需的HLB值,以及O/W型微乳需用HLB值为8~18范围的表面活性剂,筛选适宜的表面活性剂和辅助表面活性剂。在确定了表面活性剂、辅助表面活性剂和油相后,通过相图选择较大微乳区的各组分配比,并确定微乳剂配方。试验证实,本试验筛选配方制备的微乳剂性状稳定。
在确定合适的微乳配方后,微乳的制备工艺较为简单。在制备伊维菌素微乳剂时,环境温度、搅拌速度和时间对微乳剂制备的影响均不明显,这与丁丹等[10]报道结果一致。笔者认为,制备稳定微乳的关键是筛选适宜的配方,除此之外,原材料的质量,以及各组分加入后搅拌的均匀度与乳剂质量具有明显关联性。本制备试验表明,如果原材料质量较差,或者搅拌不均匀,虽然在制备空白乳剂时也能形成微乳,但微乳对药物的溶解性降低,微乳剂经高压灭菌后出现分层,但摇匀后也能恢复原状。
粒径是衡量微乳形成与否的标准,粒径分布是评价微乳稳定性的重要指标。经纳米粒度仪测定,本试验制备的微乳剂平均粒径为6.30 nm,符合微乳粒径均在100 nm以下范围。微乳的显著增溶效果与其高分散性有关,O/W型微乳剂可有效提高药物的溶解度[11-12]。本试验证实,与常规10 mg/mL伊维菌素注射液制备工艺比较,微乳剂不仅可明显提高伊维菌素的溶解度,而且还简化了生产工艺,降低了生产成本。本研究采用HPLC法测定伊维菌素含量,直接用流动稀释、定容,用0.45 μm微孔滤膜过滤后进样,结果表明,微乳剂中其他辅料对伊维菌素的测定无干扰,试验说明,该方法简便易行,灵敏度高,重现性好。
目前,刘根新等[13]制备了50 mg/mL伊维菌素O/W型纳米乳注射液,汤佳莘等[14]研制了含0.3 mg/mL伊维菌素和50 mg/mL吡喹酮复方纳米乳,丁丹等[10]研制了20 mg/mL伊维菌素O/W型纳米乳透皮剂。兰州畜牧与兽药研究所研制了含水80%的伊维菌素微乳[15]。本试验研制的50 mg/mL伊维菌素微乳剂含水量为20.36%,虽然提高含水量也可制备同浓度的伊维菌素乳剂或亚微乳剂,但外观呈半透明状态,总体质量评价劣于含水20.36%的微乳剂,因此,筛选确定了本试验配方,且该配方制备工艺简便,质量优良,易于实现产业化。
[1] 陆 彬.纳米乳与亚微乳给药系统[J].中国药师,2004,7(10):759-761.
[2] Rhee Y S,Choi J G,Chi S C,et al.Transdermal delivery of ketoprofen using microemulsions[J].Int J Pharm,2001,228:161-164.
[3] 史同瑞,于万才.微乳及微乳制剂的研究[J].上海畜牧兽医通讯,2005(5):10-11.
[4] Nornoo A O,Chow D S.Cremophor-free intravenous microemulsions for paclitaxel II.Stability,invitrorelease and pharmacokinetics[J].Int J Pharm,2008,349:117-123.
[5] 刘根新,王福厚,车清明,等.伊维菌素不同制剂在兽医临床的应用[J].中国兽药杂志,2011,45(12):53-55.
[6] 汪 杨,吴 伟,阙 俐.油-吐温-醇-水体系伪三元相图在自微乳乳化制剂研究中的应用[J].中国医药工业杂志,2005,36(6):345-348.
[7] Dixit N,Kohli K,Baboota S.Nanoemulsion system for the transdermal delivery of apoorly soluble cardiovas cular drug[J].PDA J Pharmaceut Sci Technol,2008,62(1):46-55.
[8] Pons R,Carrera I,Caelles J,et al.Formation and properties of mini-emulsions formed by microemulsions dilution[J].Adv Colloid Interface Sci,2003,106:129-146.
[9] 梁文平.乳状液科学与技术基础[M].北京:科学出版社,2001:246-248.
[10] 丁 丹,盛小莉,梁孔贤,等.伊维菌素纳米乳透皮制剂的研究[J].中国畜牧兽医,2015,42(2):401-407.
[11] 姚 静,周建平,杨宇欣,等.微乳对难溶性药物增溶机理的研究[J].中国药科大学学报,2004,35(6):495-498.
[12] 王晓黎,蒋雪涛,刘皋林,等.O/W型微乳对水难溶性药物增溶作用的研究[J].第二军医大学学报,2002,23(1):84-86.
[13] 刘根新,张继瑜,吴培星,等.伊维菌素纳米乳注射液的研制与质量安全性评价[J].畜牧兽医学报,2011,42(8):1161-1167.
[14] 汤佳莘,欧阳五庆,吴小利.复方伊维菌素和吡喹酮纳米乳的制备与质量评价[J].西北农林科技大学学报:自然科学版,2014,42(2):35-40.
[15] 邢守叶,周绪正,李 冰,等.伊维菌素微乳无菌检查方法学的研究[J].中国畜牧兽医,2016,43(1):256-260.
