乙酸乙酯使含酚酞的氢氧化钠溶液褪色的原因研究
2018-02-05李伟伟李光跃刘玉畅孙晓然
李伟伟+李光跃+刘玉畅+孙晓然
摘要:乙酸乙酯可以使含酚酞的氢氧化钠溶液褪色,许多教师把此现象解释为乙酸乙酯的碱性水解。为探究该褪色的真实原因,通过设计一系列实验、对照以及理论计算、分析,证实了褪色的真正原因是乙酸乙酯萃取了溶液中的酚酞。
关键词:乙酸乙酯;氢氧化钠;酚酞;溶液褪色;实验探究
文章编号:1005–6629(2017)12–0068–03 中图分类号:G633.8 文獻标识码:B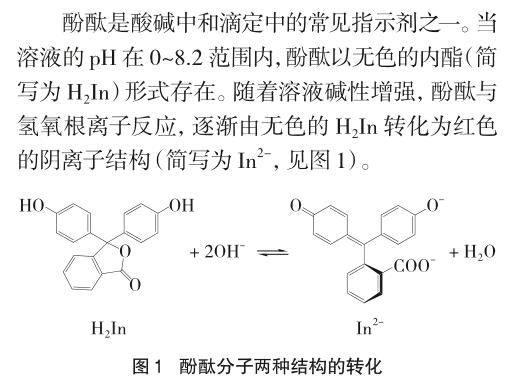
高中化学习题常涉及到“乙酸乙酯使含酚酞的氢氧化钠溶液褪色”这一实验现象。许多教师把溶液褪色的原因解释为,加入的乙酸乙酯与氢氧化钠溶液发生水解反应,生成乙酸钠和乙醇。但实际上乙酸钠水溶液显碱性,仍然可能使酚酞变红(pH>8.2,酚酞由无色变为浅红色)。所以我们认为乙酸乙酯的水解反应可能不是使含酚酞的氢氧化钠溶液褪色的原因。为此,我们进行了一系列的实验来证实此想法,并寻找褪色现象的真正原因。
1 主要试剂及仪器
使用的主要试剂包括:氢氧化钠(分析纯)、酚酞(pH指示剂)、乙酸乙酯(分析纯)、乙酸钠(分析纯)、石蜡油(分析纯)、甲苯(分析纯)、四氯化碳(分析纯)、正丁醇(分析纯)、环己酮(分析纯),石油醚(分析纯)和纯水。(其中氢氧化钠购自天津市科密欧化学试剂有限公司,纯水通过反渗透法制得,其余试剂均购自上海阿拉丁生化科技股份有限公司。)
实验中溶液的pH由HY5116型pH计(济南恒耀电子科技有限公司)测得。
2 实验设计
2.1 实验探究一:乙酸乙酯使含酚酞的氢氧化钠溶液褪色情况
(1)配制0.10mol/L的氢氧化钠溶液,滴加几滴酚酞溶液,溶液变红。
(2)取2mL上述溶液于试管中,再向溶液中加入2mL乙酸乙酯,轻轻振荡试管,不需加热,酚酞很快(<1min)褪色。
从酚酞褪色时间和反应条件来看,乙酸乙酯使酚酞褪色的原因不可能是乙酸乙酯的水解。因为过量的乙酸乙酯在不加热的条件下与氢氧化钠完全反应,需要一段较长的时间。理论上,随着反应进行,氢氧化钠浓度越来越小,碱性水解速率越来越慢,氢氧化钠不会在短时间内完全反应。
2.2 实验探究二:酚酞使0.10mol/L醋酸钠溶液变色情况
乙酸乙酯遇氢氧化钠溶液发生水解,水相中氢氧化钠剩余越少,其碱性就越小。假设氢氧化钠完全反应,此时溶液为0.10mol/L乙酸钠溶液。

2.3 实验探究三:乙酸乙酯使含酚酞的氢氧化钠溶液褪色的原因
(1)取5.0mL含酚酞的0.10mol/L氢氧化钠溶液于分液漏斗中,向分液漏斗中加入5.0mL乙酸乙酯,充分振荡后将溶液静置,分层。
(2)取少许下层水溶液,滴加几滴0.10mol/L的氢氧化钠溶液,溶液仍然保持无色;另取少许下层水溶液,滴加几滴酚酞,溶液变红。
假设乙酸乙酯使含酚酞的氢氧化钠溶液褪色仅仅是因为乙酸乙酯的水解,那么酚酞应留在水层。此时,若向水溶液中滴加氢氧化钠溶液,理论上溶液应由无色变为红色;若向水溶液中滴加酚酞,理论上溶液应该依然保持无色。而实验结果恰恰与假设相反。这再次说明酚酞已经由水层转移到酯层。换句话说,乙酸乙酯萃取了水相中的酚酞。酚酞和乙酸乙酯一样,是一种酯类化合物(见图1)。相似的结构导致酚酞在乙酸乙酯中的溶解度较大[2],所以水层中具有内酯结构的酚酞(H2In)逐渐被萃取到酯层中。水层中H2In浓度下降会导致红色的In2-转化为无色的H2In,我们就观察到了溶液褪色。谢雕等也曾经通过实验证实,在乙酸乙酯的制备实验中,酯层使含酚酞的碳酸钠溶液褪色的原因是酯层萃取了酚酞[3,4]。
2.4 实验探究四:哪些有机溶剂可使含有酚酞的氢氧化钠溶液褪色
既然乙酸乙酯因萃取酚酞使含酚酞的氢氧化钠溶液褪色,那么其他有机溶剂是否也可因萃取而使含酚酞的氢氧化钠溶液褪色呢?为此,我们选择了7种极性不同的溶剂(以相对介电常数衡量),进行了以下实验。
(1)分别配制了0.10mol/L和0.01mol/L的氢氧化钠溶液,向两溶液中分别滴加几滴酚酞,溶液均变红。
(2)分别取含酚酞的0.01mol/L氢氧化钠溶液2.0mL于8支试管中,向其中7支试管中分别加入2.0mL乙酸乙酯、石蜡油、甲苯、四氯化碳、正丁醇、环己酮、石油醚(沸程30~60℃),实验结果如表1所示。
(3)分别取含酚酞的0.10mol/L氢氧化钠溶液重复上一步实验,实验结果如表1所示。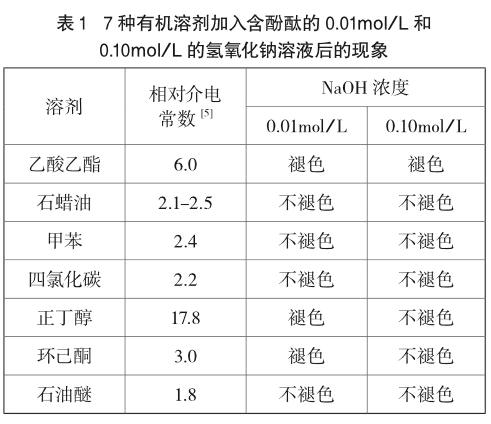
由表1可以看出,极性较大的有机溶剂(如正丁醇,环己酮)可以使含酚酞的0.01mol/L的氢氧化钠溶液褪色,而极性较小的有机溶剂或者非极性有机溶剂(如甲苯、石油醚、四氯化碳等),由于对酚酞的溶解度小,不能使含酚酞的氢氧化钠溶液褪色。这是因为酚酞的内酯结构H2In中含有酚羟基和酯基官能团,极性较大。根据“相似相溶”原理,H2In在极性有机溶剂中的溶解度大于其在非极性有机溶剂中的溶解度。H2In在正丁醇、环己酮等有机溶剂中的溶解度较大,使得水相中更多H2In被萃取到有机相,H2In浓度下降导致图1中平衡左移,最终In2-转化为无色的H2In结构,我们就观察到了溶液褪色。
由表1可以看出:氢氧化钠溶液浓度为0.10mol/L时,正丁醇和环己酮也无法使其褪色,只有乙酸乙酯可使其褪色。这是因为氢氧化钠溶液浓度大,图1中平衡右移,酚酞更多以In2-结构存在,即水相中In2-的浓度较大,而H2In浓度较小。只有有机溶剂对H2In的萃取能力足够大,才能使水相中H2In更多地被萃取到有机相中,水相中H2In浓度下降,从而使图1中的平衡左移,红色的In2-逐渐转化为无色的H2In。实验使用的有机溶剂中,只有乙酸乙酯和H2In结构相似,它对H2In的溶解度最大[6],所以,所采用的有机溶剂中,只有乙酸乙酯可使含酚酞的0.10mol/L的氢氧化钠溶液褪色。
3 结论
本文通过设计一系列实验,探究乙酸乙酯可以使含酚酞的氢氧化钠溶液褪色的原因。将过量乙酸乙酯和含酚酞的氢氧化钠溶液充分混合,无需加热氢氧化钠溶液就迅速褪色。我们配制了0.10mol/L的醋酸钠溶液,滴加酚酞,溶液变红。假如0.10mol/L的氢氧化钠溶液完全与乙酸乙酯反应,生成的0.10mol/L的醋酸钠仍可以使酚酞变红,这说明水相中已经没有酚酞,酚酞已经转移到酯层。将氢氧化钠溶液和过量乙酸乙酯溶液充分振荡并静置分液,取少量的无色下层水溶液中滴加酚酞,会观察到溶液变红;另取少量无色下层水溶液滴加氢氧化钠溶液,溶液不会变红,这同样说明原来的酚酞被乙酸乙酯萃取到了酯层。总之,乙酸乙酯之所以使含酚酞的氢氧化钠溶液褪色,是因为萃取而不是水解。除了乙酸乙酯之外,正丁醇、环己酮等极性有机溶剂也可使含酚酞的0.01mol/L氢氧化钠溶液因萃取而褪色。
参考文献:
[1]武汉大学.分析化学(第四版)[M].北京:高等教育出版社,2000:319.
[2]谢雕,唐娅.乙酸乙酯制备实验中酚酞褪色原因的探究[J].化学教学,2016,(12):64~66.
[3]余灼森.制取乙酸乙酯时使含酚酞的碳酸钠溶液褪色的原因探究[J].化学教学,2007,(9):36,72.
[4][5] Lide D. CRC Handbook of Chemistry and Physics(84th) [J]. American Journal of the Medical Sciences,2003:6~148.
[6]孙张玮,汤福隆,张泰.现代化学试剂手册(第二分册)·化学分析试剂[M].北京:化学工业出版社,1987:35.endprint
