高效液相色谱法测定碳酸饮料中苯甲酸和山梨酸的含量
2018-02-03廖鹏
廖 鹏
(成都理工大学材料与化学化工学院,四川 成都 610059)
0 引言
苯甲酸、山梨酸及其盐用作食品防腐剂,广泛应用于日常食品。苯甲酸及其钠盐具有抗菌作用。通常情况下,苯甲酸被认为是安全的。然而,苯甲酸的长期摄入也可能与哮喘,荨麻疹,代谢性酸中毒及其他不良反应有关,包括婴儿和儿童[1]。山梨酸(钾)可以有效抑制霉菌等细菌的活性,并且比杀菌更有效抑制细菌生长,有效延长食品的保存期限。随着我国食品工业的发展,在食品加工过程中对食品防腐剂需求日益增长,一些商人为追求更高的利润,甚至过量添加食品防腐剂。有资料表明过量使用苯甲酸和山梨酸可引起再生障碍性贫血,粒状细胞缺乏[2]。因此,国家严格限制其使用量。
目前,苯甲酸、山梨酸的测定方法主要有气相色谱法[3]、高效液相色谱法[4]、离子色谱法[5]、紫外分光光度法[6]等方法。高效液相色谱(HPLC)是在经典液相色谱法的基础上,引入气相色谱法,高压泵,高效固定相和高灵敏度检测仪等先进技术,具有分析速度快,分离效率高,灵敏度高,操作自动化,应用范围广等特点[7]。
1 材料与方法
1.1 主要仪器与试剂
高效液相色谱仪(LC-20A,日本岛津股份有限公司);DZKW-S-8电热恒温水浴锅(北京光明医疗仪器厂);电子分析天平(DT200,成都俊鸿达科技有限公司);甲醇(色谱纯);乙酸铵溶液(0.02 mol/L):称取 1.54 g 乙酸铵,加水至 1000 mL溶解后经 0.45 μm 滤膜过滤;稀氨水(1+1):氨水和水等体积混合;碳酸氢钠溶液(20 g/L):称取2 g碳酸氢钠(优级纯),加水至100 mL后振摇溶解;苯甲酸、山梨酸标准品;碳酸饮料样品:芬达橙味汽水(瓶装600 mL)。实验用水均为超纯水。
1.2 标准溶液的配制
苯甲酸标准溶液:准确称取0.1000 g苯甲酸,加碳酸氢钠溶液(20 g/L)5 mL,加热溶解,定容至100 mL,苯甲酸含量为1.0 mg/mL。山梨酸标准溶液配制同苯甲酸。
苯甲酸、山梨酸标准混合溶液:取苯甲酸、山梨酸标准溶液各10.0 mL至100 mL容量瓶中。溶液含苯甲酸、山梨酸标准溶液各0.1 mg/mL。经0.45 μm 滤膜过滤。
1.3 色谱条件
色谱柱为 Thermo-C18色谱柱 (4.6 mm×250 mm,5 μm),流动相为 1.54 g/L 的乙酸铵-甲醇(体积比 85:15),流速为 1.0 mL/min,检测波长为230 nm,柱温为30℃,进样量为10 μL。
1.4 样品前处理
碳酸饮料:在电子分析天平上准确称取碳酸饮料样品两份于小烧杯中,质量分别为m1=8.0100 g;m2=8.0403 g,经恒温水浴锅加温搅拌除去二氧化碳,用氨水(1+1)调节pH≈7。加水定容体积V为50 mL。经微孔过滤膜(0.45 μm)过滤后,滤液待测。
2 结果与讨论
2.1 流动相的选择
流动相会影响色谱组分的分离分析过程,是色谱分析中分离的一个非常重要的调节因素,正确地选择流动相将直接影响到组分的分离度与灵敏度[8]。本实验用甲醇—乙酸铵溶液(1.54 g/L)考察在甲醇—乙酸铵溶液不同比例下 (5∶95、10∶90、15∶85)各种物质的分离情况,发现在甲醇—乙酸铵体积比为85∶15时效果最佳,各物质间能很好地分离,分离效果较好,基线比较平稳。故本实验采用此流动相体系对样品进行测定。
2.2 柱温的选择
柱温直接影响分离效能和分析速度,柱温过高会使各组分的挥发度靠拢,保留值差别缩小,不利于分离,所以从分离的角度考虑,宜采用较低的柱温。但柱温太低,被测组分在两相中的扩散速率减小,分配不能迅速达到平衡,峰形变宽,柱效下降,并延长了分析时间。实验时考察了不同柱温下(25℃、30℃、35℃ )各峰的分离情况,结果表明,在30℃的条件下,各峰的分离效果最佳,故选择30℃为柱温。
2.3 检测波长的选择
用紫外可见光分光光度计测量苯甲酸、山梨酸在200~400 nm下的吸光度A,根据相关文献记载[9],苯甲酸、山梨酸最大吸收峰的波长为225 nm,254 nm。本实验对230 nm、240 nm、254 nm三个波长进行试验,发现在波长230 nm下苯甲酸和山梨酸均有较理想的吸收,因此本实验选用230 nm作为检测波长。在该条件下对苯甲酸和山梨酸标准溶液进行色谱分析。
2.4 色谱图
取1.2配制的苯甲酸、山梨酸标准溶液,用1.4处理好的样品1,样品2的溶液在1.3的色谱条件下进样测定,分别得色谱图如图1、图2和图3所示。
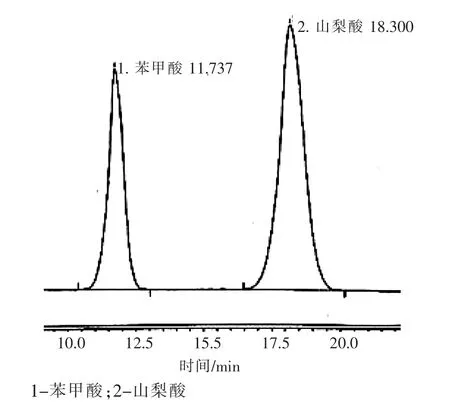
图1 苯甲酸、山梨酸的标准溶液色谱图
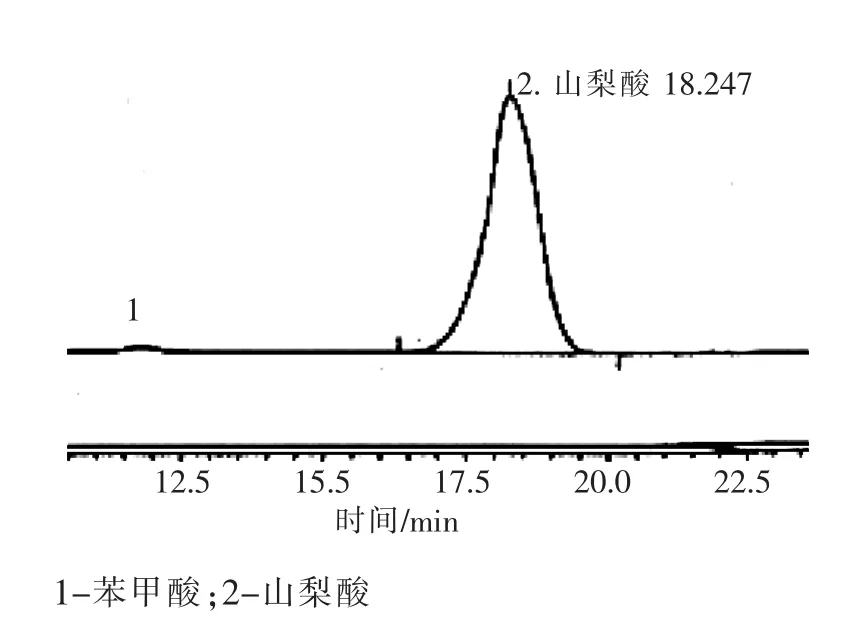
图2 样品1的色谱图
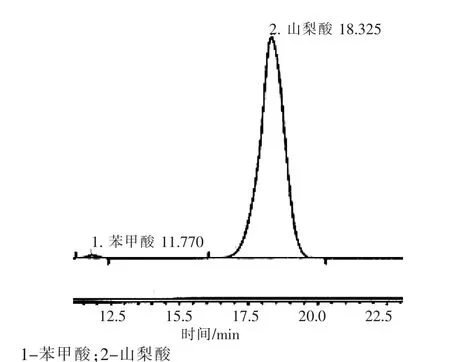
图3 样品2的色谱图
2.5 标准曲线与检出限
标准曲线的绘制:取10 mL的比色管,再分别加入苯甲酸、山梨酸的标准溶液(1.0 mg/mL)配制成浓度为 0.01 mg/mL、0.02 mg/mL、0.03 mg/mL、0.04 mg/mL、0.05 mg/mL的系列标准使用液。分别进样10 μL,依次进行测定,绘制标准工作曲线,苯甲酸的线性关系方程为Y=464.15X-2.8831,山梨酸的线性关系方程为Y=824.91X-3.5755,均能得到良好的线性关系。苯甲酸和山梨酸在0.25~100 mg/L内线性良好,相关系数分别为0.9970和0.9995。检出限均为0.5 mg/L。
2.6 测定结果计算方法
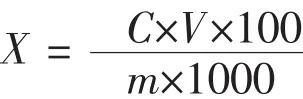
式中:X—试样中苯甲酸或山梨酸含量,g/kg;C—试样检测浓度,mg/mL;M—试样质量,g;V—试样总体积,mL。
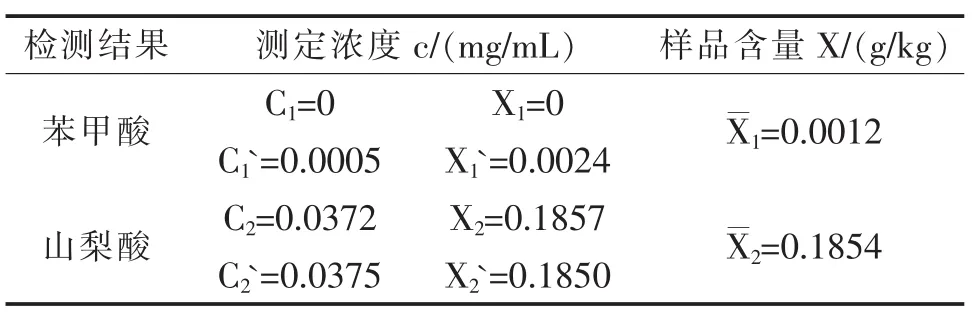
表1 样品检测结果
表1中:C1—样品1苯甲酸检测浓度,mg/mL;
C1`—样品 2苯甲酸检测浓度,mg/mL;
C2—样品1山梨酸检测浓度,mg/mL;
C2`—样品 2山梨酸检测浓度,mg/mL;
X1—样品1中苯甲酸含量,g/kg;
X1`—样品 2中苯甲酸含量,g/kg;
X2—样品1中山梨酸含量,g/kg;
X2`—样品 2中山梨酸含量,g/kg;
X1—2份样品中苯甲酸的平均含量,g/kg;
X2—2份样品中山梨酸的平均含量,g/kg;
2.7 加标回收率
按1.4预处理样品,分别加入0.02 mg/mL,0.1 mg/mL浓度的苯甲酸、山梨酸标准混合溶液,平行测定2次,测定结果见表2。
3 结论
本实验采用高效液相色谱法同时测定饮料中苯甲酸和山梨酸的含量,甲醇与乙酸铵的比例为15:85,柱温:30℃。实验结果表明各苯甲酸的加标回收率在 86.5%~105%之间,RSD<3.8%,山梨酸的加标回收率在 99%~103.4%之间,RSD<4.3%。采用不同浓度的系列混合标准溶液制作标准曲线,获得较好的线性关系。该方法检测苯甲酸和山梨酸的检出限为0.5 mg/L。回收率较好,有较高的实用价值。
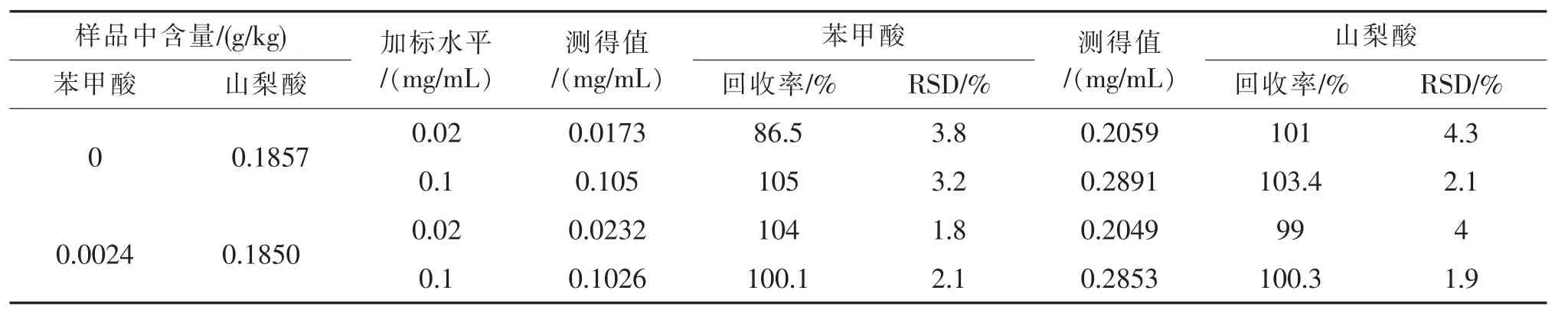
表2 苯甲酸山梨酸回收率
[1] 钱和,韩婵,刘利兵.食品中化学添加剂的功能与风险控制[J].化学进展, 2009, (11):2424-2434.
[2] 车燕妮,苏敬武,刘新荣,等.常温液相色谱法快速测定食品中安赛蜜、苯甲酸、山梨酸、糖精钠[J].预防医学文献信息, 2004, (3):309-311.
[3] 孙颖霞,翁光灿,倪炜华.气相色谱法测定果蔬汁饮料中 6种防腐剂[J].中国测试,2011,(3):37-39.
[4] 陈青川,于文莲,王静.高效液相色谱法同时测定多种食品添加剂[J].色谱,2001, (2):105-108.
[5] 马国军.离子色谱法测定饮料中7种食品添加剂[J].理化检验(化学分册), 2014, (6):766-768.
[6] 桑宏庆,蔡华珍,王大勇.紫外分光光度法同时测定饮料中山梨酸钾和苯甲酸钠[J].饮料工业,2006,(8):34-37.
[7] 蒋芝荣,郭海平,杨智敏,等.高效液相色谱在中药研究中的应用进展[J].中草药, 1996, (3):186-187.
[8] 李芸瑛,黄丽华.高效液相色谱法同时快速测定饮料中的3种食品添加剂[J].肇庆学院学报,2003,(2):31-35.
[9] 尤新.功能食品和功能性食品添加剂发展新动向[J].中国食品添加剂,2008, (S1):43-51.
