Fe-O-Al熔体—MSZ固体电解质体系中氧的传递环节研究
2018-01-18董立山王国承孙长余
董立山,王国承,马 骞,孙长余
(辽宁科技大学 材料与冶金学院,辽宁 鞍山 114051)
自从Kiukkola[1]利用固体电解质在高温状态下进行电化学研究工作以来,将固体电解质应用于高温冶金方面的研究受到关注[1-6]。其中由于MgO部分稳定的ZrO2(MSZ)固体电解质在高温时具有良好的氧离子传导功能,所以利用电化学研究冶金过程脱氧反应的方法已经得到越来越多的应用。Wook KIM[5]发现固体电解质与钢液界面的氧浓度可以通过电化学装置控制,这种方法可以测量出氧化锆固体电解质与钢液界面氧化物的电流密度,从而通过塔菲尔定理与能斯特方程计算其界面氧浓度。Dong Ju SHIN[6]的研究表明对于固体电解质与电极组成的电化学装置施加外部电压可以控制氧在钢液与MSZ固体电解质之间的传导。本文利用电化学方法控制钢液与MSZ固体电解质之间的界面氧浓度,达到控制氧传递的目的,解释脱氧过程动力学机制。先制备研究MSZ固体电解质,利用MSZ固体电解质与电极之间构建电化学装置,通过CO/CO2混合气体为MSZ与钢液界面提供氧,当达到平衡后对其施加外部电压,利用过电势来控制脱氧过程,研究氧传递过程的动力学机制。
1 MSZ固体电解质的制备与电学性质
1.1 MSZ固体电解质的制备
MSZ固体电解质主要原料以及杂质ZrO2+HfO2,MgO,Al2O3,Fe2O3,SiO2,Na2O,Cr,H2O,Ig.Loss的质量分数分别为96%,3.53%,0.05%,0.001%,0.01%,0.002%,0.006%,0.33%,1.33%。
制备过程:(1)将事先配置好的原料溶解于离子水中,形成pH为1~2的溶液,加入MgO,在搅拌的条件下,在上述的溶液中缓慢滴入氨水,形成白色沉淀物,调整溶液的pH值到9。(2)将上述白色沉淀物离心脱水,在80℃下干燥,之后在600℃下焙烧4 h,然后置于乙醇介质中球磨24~27 h,干燥后,在1 100℃下焙烧4~6 h后得到平均颗粒度为0.8~1 μm的粉体,粉体加入有机结合剂中,形成浆料,用注射成型方法形成一端封闭的坯。(3)将坯在1 200℃下脱去有机结合剂,在1 700℃下烧结5 h后,直接冷却至1 200℃,并保持1 200℃温度1~2 h。(4)直接冷却至1 000℃,并保持1 000℃温度6~14 h。(5)在室温下进行粗加工以及细加工最终制成外径8 mm,内径6 mm,高70 mm的空心圆柱状形。MSZ固体电解质实物如图1所示。

图1 MSZ实物图Fig.1 MSZ physical map
1.2 MSZ固体电解质电学性质测定
将MSZ固体电解质管底层内部以及外部高10 mm的区域均匀地涂满铂浆,将1 mm铂金丝一端与MSZ固体电解质内部涂有铂浆部分相连,另一端与电化学工作站工作电极相连;将0.5 mm铂金丝捆绑在MSZ固体电解质外部涂有铂浆位置,另一端与电化学工作站辅助电极相连,把连接好的MSZ固体电解质放入刚玉坩埚中,放入高温炉中进行加热,升温速率为5℃/min。利用电化学工作站中交流阻抗模块分别在1 100,1 200,1 300,1 400,1 500,1 600 ℃下进行测量。
由于固体电解质材料的复阻抗谱图一般由晶粒、晶界以及电极组成[7-8],其阻抗图谱如图2a,其对应的等效电路如图2b。
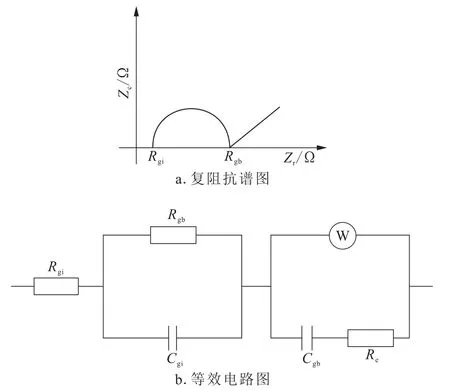
图2 固体电解质材料的典型复阻抗谱图和等效电路图Fig.2 Typical complex impedance spectra and equivalent circuit diagrams of solid electrolyte materials
利用Zsimpwin软件进行拟合计算,温度为1 100,1 200,1 300,1 400,1 500,1 600 ℃下实验数据图谱与拟合图谱如图3所示。
通过拟合得到1 100~1 600℃下晶粒、晶界电阻 Rgi、Rgb的值,实际电阻 Rg由式(1)计算,利用所涂铂浆的面积S与电阻值Rg之比得到电导率c值,S 为2.17 cm2。

晶粒电阻Rgi、晶界电阻Rgi、实际电阻Rg以及电导率σ随温度的变化情况如图4所示。在1 100~1 600℃范围内,MSZ固体电解质的电阻会有明显减小的趋势,当温度达到1 300℃时,电阻趋于稳定。而且MSZ固体电解质电阻主要由晶粒电阻所决定。MSZ固体电解质电导率逐渐增大,原因是高温状态下,MSZ固体电解质晶体结构由单斜晶型转变为萤石立方晶型,产生了大量的氧空位,随着温度的升高,氧空位会逐渐增多,晶体中的非导电离子形成刚性骨架,形成一维隧道型,二维平面型,或三维传导型的离子扩散通道,氧离子在通道中可以自由移动,使MSZ固体电解质具有很高的氧离子导电能力。当温度为1 600℃时,MSZ固体电解质的电导率为0.185 S/cm。
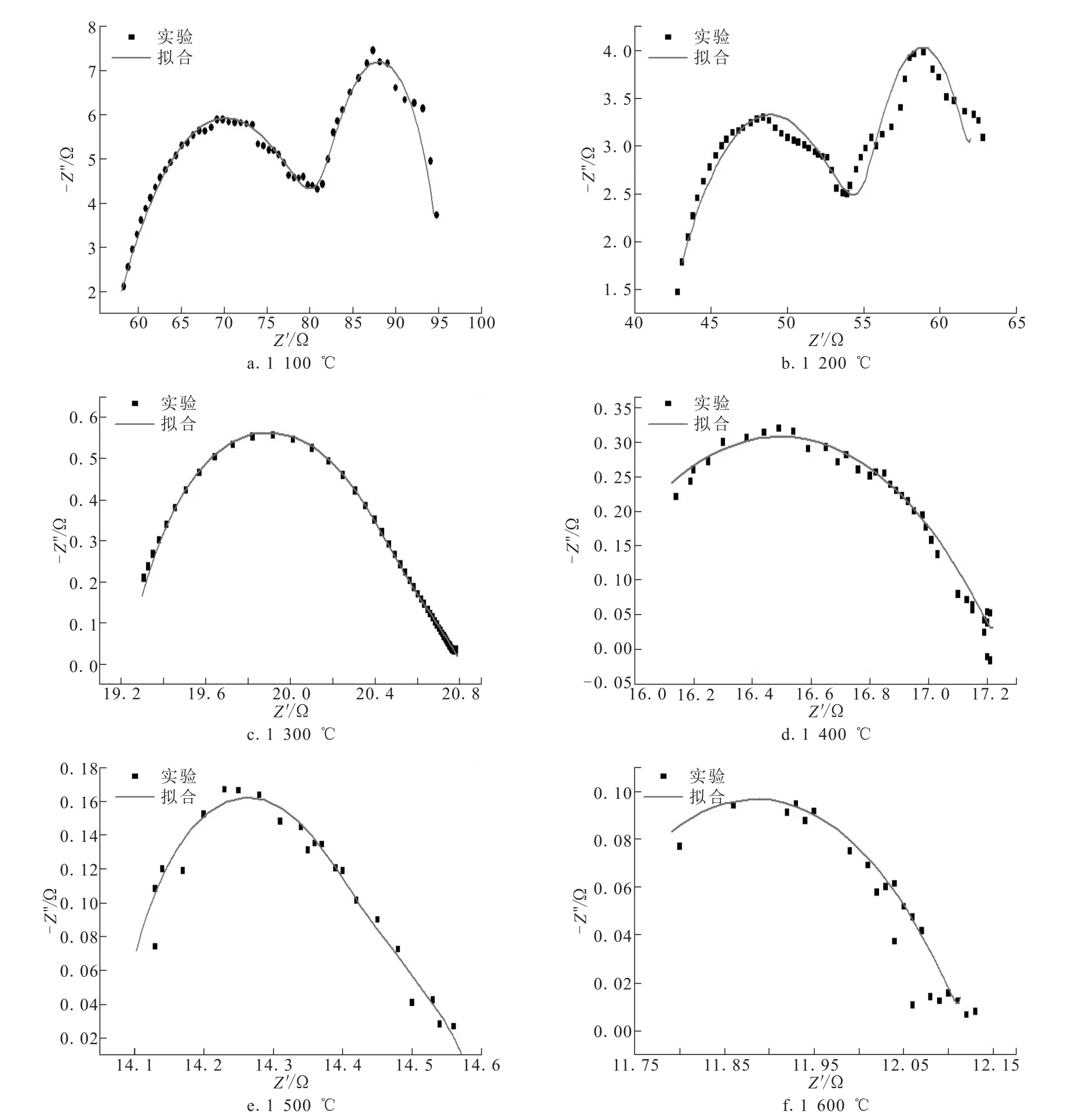
图3 不同温度下实验数据与拟合阻抗谱图Fig.3 Fitting curve under different temperature and actual curve of impedance spectra
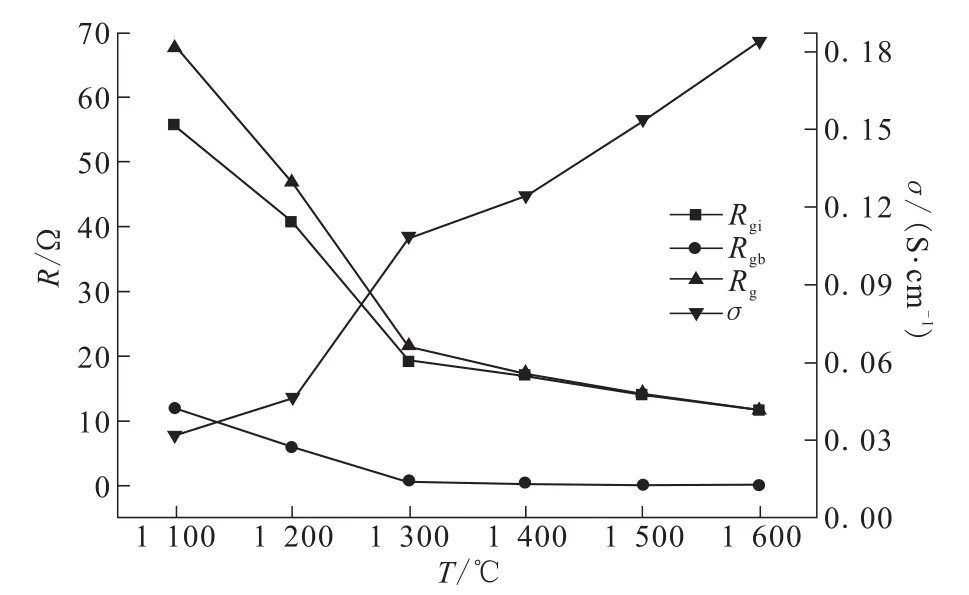
图4 Rgi、Rgb、Rg以及σ随着温度的变化Fig.4 Rgi,Rgb,Rgand σ changes with temperature
2 Fe-O-Al熔体的电化学实验
2.1 实验装置及方法
实验装置如图5所示。将装有纯度为99.99%的银以及工业纯铁的刚玉坩埚(外径70 mm,内径67 mm,高80 mm)放入电阻炉加热区,以5℃/min升温速率加热到1 600℃。以铂金丝作为阳极,钼丝为阴极,在其外部用刚玉管(外径4 mm,内径2 mm,高800 mm)保护。将钼丝插入银液中,防止钼丝在铁液中融化,原因是钼丝在铁液中溶解性好。同时将MSZ固体电解质底部10 mm范围内涂上铂浆,将铂金丝盘成圈状方便与铂浆接触。外部分别与电化学工作站的工作电极以及辅助电极相连。将氧化锆电解质插入钢液20 mm。本实验参考气体选择CO与CO2的混合气体,体积比为1:5;保护气体为高纯氩气,全程进行保护防止外界空气对实验的影响。利用参考气体使MSZ与钢液界面氧含量达到平衡值后,利用电化学工作站施加外部电压来控制氧的传递,从而达到脱氧目的。本实验铝氧配比如表1所示。
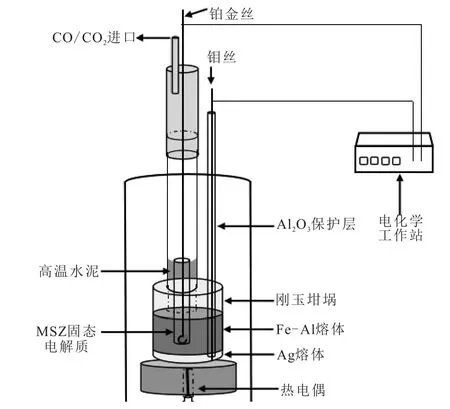
图5 电化学装置示意图Fig.5 Schematic diagram of electrochemical device

表1 电化学实验铝氧配比,%Tab.1 Electrochemical experiment Al-O ratio,%
2.2 实验结果与分析
2.2.1 Fe-O体系脱氧过程速率控制环节 为了使整个限制环节持续进行,需要提供过电势,利用公式η=Eapply-E0来确定。Eapply为外部电压,E0是开路电压即电流值为0时的电压,其中E0是通过电化学工作站中开路电压模块进行测量。根据前人的工作[9],控制界面氧化物的最主要因素是氧活度。为了确定速率控制环节,通过电化学工作站对整个电化学装置施加100~700 mV的外部电压,间隔20 mV,对含氧铁液进行脱氧反应,了解氧在整个电化学装置中的迁移情况。
当电阻炉中施加了外部电压,其反应的动力学机制可以通过塔菲尔定理利用过电势的数值来决定[10],图6为Fe-O—MSZ固体电解质体系中过电势与电流密度之间的关系图,图中展示出三大区域:一个是活度超电势区域,在这个区域内固体电解质与铁熔液界面发生电化学反应;另一个区域为欧姆区域,在这个区域内氧离子迁移穿过固体电解质;最后一个区域为浓度超电势区域,钢液中的氧向固体电解质界面移动。
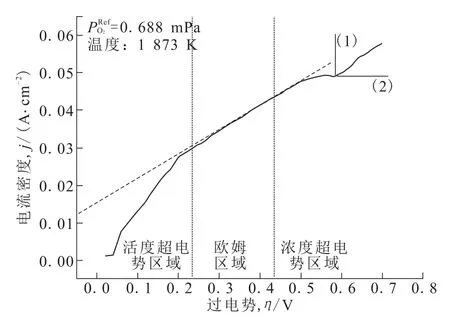
图6 铁氧体系中过电势与电流密度之间的关系Fig.6 Relationship between overpotential and current density in iron oxygen system
氧在电化学装置中的迁移通常由五部分构成[11]如图7所示。(1)氧原子从本相中向固体电解质与铁熔液界面的迁移。(2)固体电解质与参考气体在界面的化学反应。(3)氧离子迁移通过固体电解质。(4)在固体电解质与铁熔液界面的电化学反应。(5)氧原子扩散到CO/CO2参考气体区域。
本次实验只出现三个区域,主要原因是相对于其他步骤,第一步和第二步的脱氧过程达到平衡的时间非常短,故忽略不计。
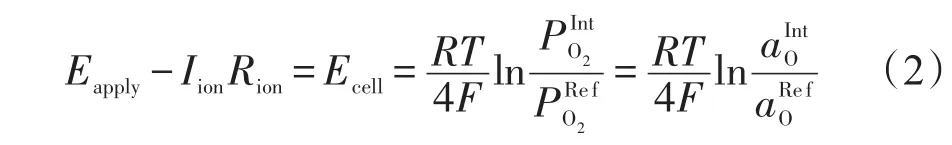
式中:F为法拉第常数,96 450 C/mol;Eapply为外部电压,V;Iion为离子电流,A;R为离子电阻,Ω。
2.2.2 Fe-O-Al体系脱氧过程速率控制环节 图8分别展示了在铝质量分数为0.003%与0.006%时Fe-O-Al电解质体系中电流密度与过电势之间的关系。区域1被定义为“活化过电压”区域,由固体电解质与铁熔液之间的界面电化学反应速率控制。化学反应为因为稳定的外部电动势,铁熔液需要克服活化位垒。在0.02~2.4 V电压范围内,随着外部电压的升高导致了更高的离子电流,此时为熔解性的氧进行传递。

区域2被定义为欧姆过电压区域,由固体电解质内氧离子的迁移和在电极材料内电子的移动受电阻控制。在此区域内遵循欧姆定理
式中:j为电流密度,mA/cm2;R为系统的电阻,包括电极电阻、连接电阻和电解质电阻。总电阻由电解质电阻决定,其他电阻可以忽略不计。在2.4~4.4 V区域进行函数拟合,得出电导率为0.164 S/cm,通过交流阻抗的方法测定的电导率为0.185 S/cm,计算值在测定值的合理误差范围内。此时部分Al2O3进行分解。
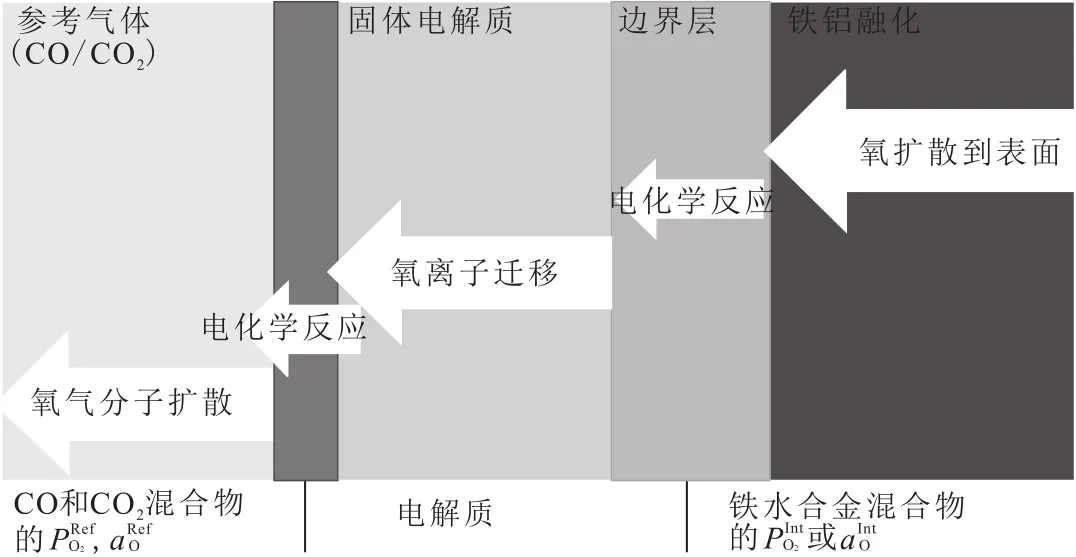
图7 电化学装置与钢液界面的反应步骤Fig.7 Reaction steps between electrochemical device and liquid steel interface
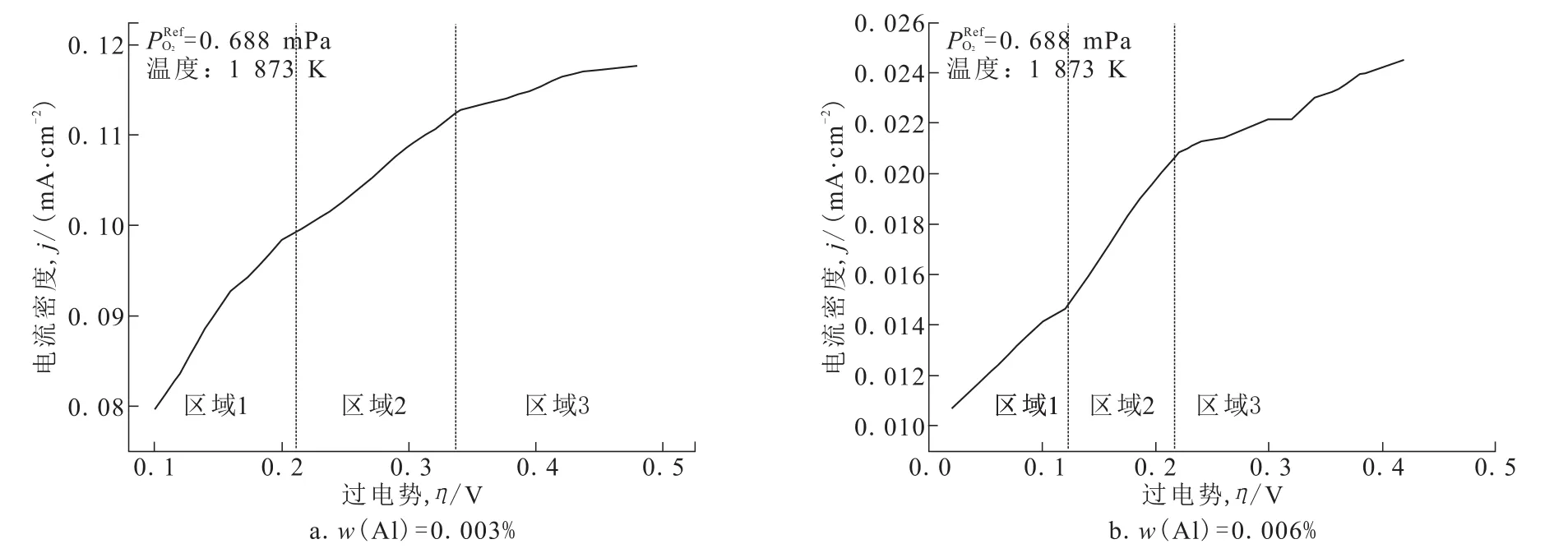
图8 铁氧铝体系中过电势与电流密度之间的关系Fig.8 Relationship between overpotential and current density in aluminum ferrite system
区域3被定义为浓度差过电势区域,由钢液中氧原子向钢液与MSZ固体电解质界面的转移速率控制。由于其转移速率非常慢,当达到临界电压时,即使对整个系统施加持续的外部电压,本相中的氧含量也不会低于临界值,因此在界面处不会有活化的氧原子发生反应,导致电流密度趋于稳定,此时Al2O3完全分解。过电势与电流密度之间的关系为

式中:α是传递系数(α=1);n是转移电子数;R是气体常数;j是当前电流密度;jL是极限电流密度。
S1、S2两组实验的临界电压与极限电流密度如表2所示。不同铝氧配比的情况下,临界电压相同,但极限电流密度不同,主要是初始氧含量不同,钢液中氧原子向钢液与MSZ固体电解质界面的转移速率之间的差异引起。

表2 临界电化学性质Tab.2 Critical electrochemical properties
3 结论
(1)采用注射成型法制造的MSZ固体电解质在高温区时,其电导率随着温度的升高有明显的增加趋势,温度为1 600℃时,其电导率为0.185 S/cm2。
(2)形成的Al2O3夹杂物可以通过施加持续的外部电压进行脱氧,当电压为0.02~0.24 V时,脱去钢液中熔解的氧;当电压为0.24~0.44 V时,部分Al2O3分解;当电压大于0.44 V时,Al2O3完全分解。
(3)在电化学装置中应用外部电压分解氧化物夹杂物涉及到了三种动力学机制,分别是激活过电压、欧姆过电压、浓度过电压。相应的限制性环节分别是电化学反应,氧离子在ZrO2电解质中的扩散,氧原子从铁溶液扩散到界面。
[1]KIUKKOLA K,WAGNER J.Measurements on galvanic cells involving solid electrolytes[J].Journal of the Electrochemical Society,1957,104(104):379-387.
[2]ODLE R R,RAPP R A.Further study of the electrochemical deoxidation of induction-stirred copper melts[J].Metallurgical Transactions B,1977 ,8(4):581-589.
[3]IWASE M,TANIDA M,MCLEAN A,et al.Electronically driven transport of oxygen from liquid iron to CO+CO2gas mixtures through stabilized zirconia[J].Metallurgical Transactions B ,1981,12(3):517-524.
[4]KIM W,MIN D J,LEE Y S,et al.Electrochemical method for controlling the interfacial oxygen in molten Fe with ZrO2based solid electrolyte[J].ISIJ International,2009,49(12):1882-1888.
[5]KIM W,SOHN I.A Phenomenological investigation on the control of oxides at the interface using an electrochemical cell[J].ISIJ International,2011,51(1):63-70.
[6]JU S D,MIN D J.Investigation on the decomposition of Al2O3using an electrochemical method[J].ISIJ International,2013,53(3):434-440.
[7]唐辉,林振汉.掺杂Yb2O3的氧化锆固体电解质材料的研究[J].稀有金属快报,2008,27(2):17-20.
[8]崔晓莉,江志裕.交流阻抗谱的表示及应用[J].上海师范大学学报(自然科学版),2001,30(4):53-61.
[9]ABELARD P,BAMUARD J F.Study of the dc and ac electrical properties of an yttria-stabilized zirconia single crystal[(ZrO2)0.88(-Y2O3)0.12][J].Physical Review B,1982,26(2):1005-1017.
[10]TAFEL J.Über die polarisation bei kathodischer was serst of fentwicklung[J].Zeitschrift Für Physikalische Chemie,1905,50(1):641-712.
[11]HASHAM Z,PAL U,CHOU K C.Deoxidation of molten steel using a short-circuited solid oxide electrochemical cell[J].Journal of the Electrochemical Society,1995,142(2):469-475.
