集中式饮用水源地邻苯二甲酸酯类物质分布特征与健康风险评估
2018-01-12马武生韦林洪王征远
马武生,韦林洪,王征远,刘 俊
1.扬州市职业大学生物与化工工程学院,江苏 扬州 225009 2.江南大学环境与土木工程学院环境生物技术研究室,江苏 无锡 214122
自20世纪初以来,邻苯二甲酸酯(PAEs)作为高分子材料助剂被广泛应用于化工行业[1-2]。2009年,全球PAEs产量已达到620万t左右,中国PAEs总消费量则达到150万t[3],主要用于聚氯乙烯(PVC)增塑剂[4]、个人护理产品、香味品、润滑剂、涂料、黏合剂、驱虫剂和农药载体的生产原料等[3]。实验研究已证明PAEs具有“三致”效应,且对人类生殖健康存在不利影响,是潜在的内分泌干扰物[5]。美国环保署(USEPA)已将邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二正丁酯(DBP)、邻苯二甲酸二正辛酯(DNOP)、邻苯二甲酸二(2-乙基己基)酯(DEHP)和邻苯二甲酸丁基苯基酯(BBP)列为优先控制污染物[6],中国也已将DMP、DBP和DEHP确定为水体优先控制污染物,并给出了地表水中DBP和DEHP的标准限值[7]。一些学者已在欧洲、美国和日本等环境水体中发现PAEs的普遍存在[8-11],中国大型河流地表水(如黄河、长江)和大型城市湖泊,也检测到高水平的DBP、DEHP[12-15]。在水生生态系统中,由于PAEs水解速度缓慢,半衰期为3~2 000 a[16],PAEs的光氧化过程也相对缓慢,半衰期为2.4~12 a[17]。故此,易造成PAEs在环境水体、土壤和生物体中的积累,对生态系统及人类健康具有潜在的危害[13, 18-19]。近年来,PAEs在环境中的水平及对人体健康的影响越来越引起人们的关注,如SCHECTER等[1]基于食物和空气中的PAEs水平计算了人们每日摄取量,GUO等[20]估算了中国人均每日PAEs摄入量,表明膳食摄入的DEHP是主要来源;STAPLES等[21]开展了PAEs对水生生物群落潜在积累的研究,得出DMP、DEP、DBP、BBP的水生生物急性毒性分别为29~337、10.3~131、0.35~6.29、0.21~5.3 mg/L。
在含有PAEs产品中,PAEs并未与PVC等成分形成共价键,故PAEs可通过产品的生产、使用、流通和最终处置向环境中释放[22],通过多种途径汇集于环境水体,使饮用水源地既是PAEs的汇,又是PAEs污染的源,并通过饮用水和食物链对人类健康产生危害。因此,对饮用水源地PAEs的分析、监控、生态和健康风险评估十分必要,具有重要的环境指示意义。研究选择某地区7处集中式地表水饮用水源地作为对象,对以下内容进行了研究:①通过对水体中PAEs的分析,获取该地区水源地PAEs的分布特征;②基于多元统计分析,对水体中PAEs的源进行解析;③基于健康风险评估模型,评估6种PAEs优先控制污染物对人类可能产生的健康风险,为该地区饮用水水源地的环境管理与保护提供科学依据。
1 实验部分
1.1 样品采集
采样点分布于某地区7个集中式饮用水源地,分别于2015年7月(丰水期)、10月(平水期)和2016年1月(枯水期)进行采样,每隔10 d采样一次,每次采集3份平行水样各1 L。采样器采用玻璃材质,盛水容器采用棕色玻璃瓶,使用前均进行环己烷清洗和采样点水体润洗。根据断面宽设置采样垂线,采样深度选择50 cm。采样后6 h内运回实验室于4 ℃冷藏保存,24 h内测定。采样过程做全程空白。
1.2 仪器和试剂
仪器:Agilent 7890 A-5975C型气相色谱质谱联用仪,配置FID检测器和DB-5MS毛细管色谱柱(30 m×250 μm×0.25 μm);C18固相萃取小柱(Agilent)。
标准物质:Phthalate Esters Mixture-8061,规格为1 000 mg/L溶于异辛烷。
其他试剂:正己烷、丙酮、甲醇、二氯甲烷等均为色谱纯,其他为分析纯,实验用水为Mili-Q超纯水。
1.3 测定方法
采用SPE-GC-MS进行测定。
固相萃取条件:依次用二氯甲烷、甲醇和超纯水各5 mL浸润C18固相吸附柱,然后量取500 mL水样进行PAEs萃取,萃取pH为2~3。洗脱:5 mL的甲醇∶超纯水(体积比为1∶19)淋洗固相吸附柱,选用10 mL二氯甲烷∶丙酮∶正己烷(体积比为4∶3∶3)洗脱目标分析物。洗脱液经无水硫酸钠脱水、旋转蒸发浓缩和二氯化碳定容后,进入GC-MS测定[23-24]。
色谱-质谱条件:进样口汽化室温度为260 ℃,柱流量为1 mL/min;60 ℃保持1 min,20 ℃/min到220 ℃保持1 min,5 ℃/min到290 ℃保持2 min;无分流进样1 μL;高纯氦气纯度为99.999%。质谱条件:EM电压为1 518 V,离子源温度为230 ℃,MS四极杆温度为150 ℃;溶剂延迟 6 min;采集模式为选择离子检测。
在选定色谱条件下,16种PAEs得到理想的分离结果(图1)。

化合物:1.DMP;2.DEP;3.邻苯二甲酸二异丁酯(DIBP);4.DBP;5.邻苯二甲酸二(2-甲氧基)乙酯(DMEP);6.邻苯二甲酸二(4-甲基-2-戊基)酯(BMPP);7.邻苯二甲酸二(2-乙氧基)乙酯(DEEP);8.邻苯二甲酸二戊酯(DPP);9.邻苯二甲酸二己酯(DHXP);10.BBP;11.邻苯二甲酸二(2-丁氧基)乙酯(DBEP);12.邻苯二甲酸二环己酯(DCHP);13.DEHP;14.邻苯二甲酸二苯酯(DPhP);15.DNOP;16.邻苯二甲酸二壬酯(DNP)。图1 16种PAEs标准品的GC-MS分离效果Fig.1 GC-MS separation effect of 16 PAEs standard products
1.4 纯溶剂相校准曲线
基于五点内标校准曲线定量PAEs。响应因子来自0.1~1 ng/μL目标分析物的校准曲线,相关系数均在0.99以上。
1.5 多元统计分析
数据结果在反映PAEs来源和类别信息上可能存在一定的相关性,常用主成分分析(PCA)和聚类分析(CA)方法对其来源进行解析。PCA以降维方式将多个变量归结为能较好反映变量主要信息的相互独立的综合因子,用于判别多源环境污染的来源[25]。CA是将所有变量(或指标)各自看成一类,选择相似程度最大的(距离系数最小或相似系数最大)两类合并为一个小类,并逐步扩大至所有的变量(或指标),最终形成一个谱系图,达到分类的目的[26-27]。研究采用PCA对水源地PAEs来源进行初步的分析,采用层次聚类分析(HCA)法对采样断面关系密切度进行分析。
1.6 健康风险评估方法
PAEs同系物中,DEHP列为B2类(人类致癌物),BBP属于C类(可能致癌物质),而DBP、DEP、DMP属于D类(非人类致癌物)。研究使用HAMIDIN等[28]和USEPA[29]提出的健康风险评估模型(HRA)评估6种PAEs优先控制污染物对人类可能产生的健康风险[28-29]。
DEHP的致癌风险(R)计算方程为

DMP、DEP、DBP、DNOP、BBP的非致癌风险(HI)计算方程为
HI=E/RfD
式中:RfD为参考剂量[DEHP、DMP、DEP、DBP、DNOP、BBP的RfD值分别为0.02、10.0、0.8、0.1、0.02、0.2 mg/(kg·d)[29-30]];SF为斜率因子[DEHP的SF值为0.014 mg/(kg·d)];E为暴露水平[mg/(kg·d)],E包括饮水暴露水平(E1)和皮肤接触暴露水平(E2),计算方法为
E2=k×C×(6τ×TE/π)0.5×Asb×EF×
式中:C为水中PAEs的质量浓度(mg/L);U为日饮用水量(2 L/d);EF为暴露频率(365 d/a);ED为暴露延时(USEPA推荐值为30 a);BW为平均体重(70 kg);AT为平均暴露时间(70 a×365 d/a);k为皮肤吸附参数(0.001 cm/h);τ为各污染物的延滞时间(假设值为1 h);TE为洗澡的时间(0.546 h);Asb为人体的表面积(16 600 cm2);FE为洗澡频率(0.3次/d);f为肠道吸收率(取值为1)。
2 结果与讨论
2.1 PAEs在集中饮用水源地的分布特征
目前,有关环境水体中PAEs的研究主要集中在列为USEPA优先控制污染物的DMP、DEP、DBP、DEHP、DBP、BBP 6种PAEs同系物。本研究分析了水体中16种PAEs同系物。结果发现,所有样品中均有DIBP、DBP、DEHP检出,而DMEP、DPP均未检出,其他PAEs同系物检出率分布为11%~89%。不同同系物在环境水体的贡献差异很大,且相同同系物在不同水源地也存在较大差异(表1和图2)。从表1和图2可以看出,DBP、DEHP在所有PAEs同系物中含量最丰富,占PAEs总量的26%~48%;第二大贡献是DIBP和DNOP,占PAEs总量的1%~20%;其他PAEs的贡献只占4%~10%。表明DBP、DEHP、DIBP、DNOP这4种类型化学品在该地区被广泛消费。

表1 饮用水源地采样点位16种PAEs浓度统计汇总
注:样本数n=9;SD为标准偏差;ND表示未检出。

注:其他PAEs为除了DNOP、DEHP、DBP、DIBP之外的同系物。图2 PAEs在水体中的分布特征Fig.2 The congener profile of phthalate esters (PAEs) in drinking water sources. Other PAEs include all congeners except for DNOP, DEHP, DBP and DIBP
SHI等[31]在江苏5个地区饮用水源地检出10种PAEs同系物,发现DIBP、DBP、DEHP含量最丰富。HE等[32]对长江江苏段6种PAEs含量研究发现,DBP、DEP、DEHP是主要的污染物质,检出率分别为100%、60%、60%。HE等[33]对巢湖湖水中6种PAEs检测发现,DBP对PAEs贡献达到65.8%。总体而言,本研究与其他研究相一致,即在该地区环境水体中,DBP、DEHP通常是最丰富的PAEs同系物,占总量的70%左右。DBP、DEHP是世界上使用最广泛的PAEs[34],这是可能原因之一。在中国,DEHP具有低成本优势而广泛用作PVC的增塑剂,占到总PAEs生产或消费量的80%[35];DBP则在食品包装、化妆品、洗发剂、防晒品和防蛀剂等中大量应用。另外,与其他PAEs相比,DEHP具有较高的辛醇-水分配系数(LogKow=7.5),由于LogKow大于4的有机化合物不易被生物降解[36],从而更容易在环境水体积累,造成DEHP检出浓度较高。
2.2 饮用水源地PAEs的含量
饮用水源地水体中PAEs含量如表1所示。由表1可知,Σ16PAEs浓度范围为0.49~8.74 μg/L。其中,Σ16PAEs最高浓度来自芒稻河二水厂断面[(3.95±2.23) μg/L]和三阳河亨达水务断面[(4.27±2.50) μg/L],这可能与该断面临近城镇居民区有关,日常生活及塑料制品垃圾造成环境水体中PAEs的累积。研究中,四水厂断面和五水厂断面Σ16PAEs浓度较低,分别为(1.70±0.89)、(1.45±0.76) μg/L,低于其他5个断面,可能因为这两处水样来自长江水体,而其他断面水体属于内河,水体中PAEs的来源、水体流量、微生物活性及其他有机物含量的不同,造成PAEs浓度及分布存在较大不同。与其他学者报道的PAEs含量相比[37-38],本研究水体中PAEs浓度处于较低水平。
研究水体中DBP、DEHP贡献最大,浓度范围分别为0.19~3.59、0.18~2.38 μg/L,对照《地表水环境质量标准》(GB 3838—2002)中DBP、DEHP的标准限值(分别为3、8 μg/L)发现,研究水体存在点位DBP超标情况,但DBP、DEHP浓度均值并未超过浓度限值,表明生态环境潜在风险较低。
不同采样时期水源地Σ16PAEs含量如图3所示。由图3可以看出,万福闸南、一水厂、二水厂、亨达水务和邵伯水厂断面丰水期Σ16PAEs浓度显著高于枯水期,其原因为万福闸南等5断面水体中PAEs主要由城镇雨水径流和大气沉降所致,尤其是在降水初期,将造成受纳水体PAEs和其他人为污染物的显著升高。而四水厂和五水厂断面则相反,呈现丰水期低于枯水期的现象,其原因是2个断面水体中PAEs更多受到沿江化工园区的影响,枯水期流量下降造成了水体PAEs浓度的升高。
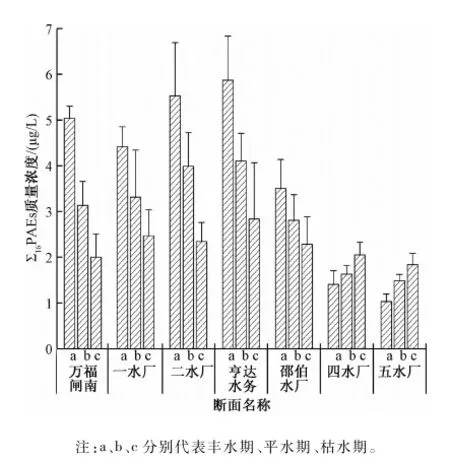
注:a、b、c分别代表丰水期、平水期、枯水期。图3 不同采样时期水源地Σ16PAEs含量Fig.3 Distribution of total 16 PAEs in different sampling sites
2.3 饮用水源地PAEs的多元统计分析
2.3.1 PCA
由于DMEP、DPP、DHXP、DPhP检出率低,故不包含PCA。其余12种PAEs共提出3个主成分,分别解释了总因子的59.5%、19.0%、12.5%,其主成分因子载荷量见图4。

图4 水源地PAEs的主成分分析(因子载荷散点图)Fig.4 Principal component analysis (PCA) of phthalate esters in water sources:Factor loading a scatter diagram
由图4可以看出,第一主成分(PC1)上,DMP、DIBP、DBP、BMPP、DEHP、DNOP、DNP都具有较大的正载荷,其中DMP、DIBP、DBP、BMPP属于低分子量的PAEs,由于LogKow较低,从而更易溶于水相,这4种PAEs可能源自化妆品和个人护理产品。而DEHP、DNOP、DNP都具有超过6个碳原子烷基链的大分子量PAEs,具有难以降解的特性,其中DEHP、DOP作为增塑剂在国内广泛使用,这3种PAEs可能源自PVC和化工溶剂。
第二主成分(PC2)由DEP、DEEP、BBP组成,他们具有较大正载荷和良好的正相关关系,可以通过某类产品添加共同的DEP、DEEP、BBP来解释。DEP可作为食品包装无毒黏合剂和香料的增塑剂,以及醇酸树脂、丁腈橡胶、氯丁橡胶的增塑剂。BBP是常用的一种增塑剂,常用于乙烯基地板、黏合剂、密封剂和工业溶剂[3]。
第三主成分(PC3)上DCHP有较大正载荷,将其来源归结于PVC、丙烯酸树脂、聚苯乙烯、硝酸纤维素等树脂材料的生产。其中一些PAEs在2个及以上主成分中占有正载荷量(如DMP、BMPP、DEEP、BBP、DEHP等)说明这些PAEs来源较复杂。
2.3.2 HCA
SPSS软件聚类分析操作如下:选用组间类平均法进行变量标准化,距离区间采用平方欧氏距离,距离越近,表明两者密切度越大,7个采样断面聚类结果如图5所示。根据采样断面的得分,并选择5为组间距离标准,得到差异明显的2个组,即万福闸南、一水厂、邵伯水厂、二水厂、亨达水务断面聚为一类,这5个断面临近城镇区,属于内河水体,PAEs来源以日常生活和农业生产为主;四水厂和五水厂断面聚为一类,采样断面位于长江,PAEs来源可能更多受到沿江化工园区的影响。

图5 基于PAEs的水源地采样断面层次聚类分析Fig.5 Dendrogram of hierarchical cluster analysis for sampling sections in water sources based on phthalate esters (PAEs)
2.4 饮用水源地PAEs健康风险评估
根据HRA模型计算出6种PAEs同系物对人类的致癌和非致癌风险值(表2和表3)。根据化学污染物可接受的R值应低于10-6,可接受的HI值小于1[30],本研究7个采样水体中DEHP的R值为1.03×10-7~1.91×10-7,其他5种PAEs的HI值为0.37×10-8~2.36×10-4,风险指数值均低于参考值,说明饮用水源地水体中PAEs不会对居民构成致癌风险或其他明显的健康风险。由于DEHP具有雌激素活性,其他PAEs对生态环境和人体健康同样具有潜在风险,PAEs通过饮水途径和洗浴过程对人群健康产生的危害仍不容忽视。为控制PAEs污染物的环境积累,可在工农业生产过程中采用低毒PAEs,提高塑料制品利用率和回收废塑料等措施。另外,还需严格控制含PAEs废水和挥发性有机物的排放,强化末端处理。
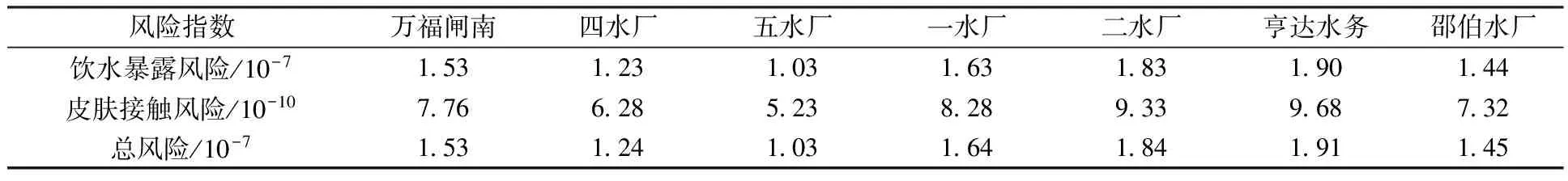
表2 含DEHP水体用于饮用和洗澡的致癌风险值
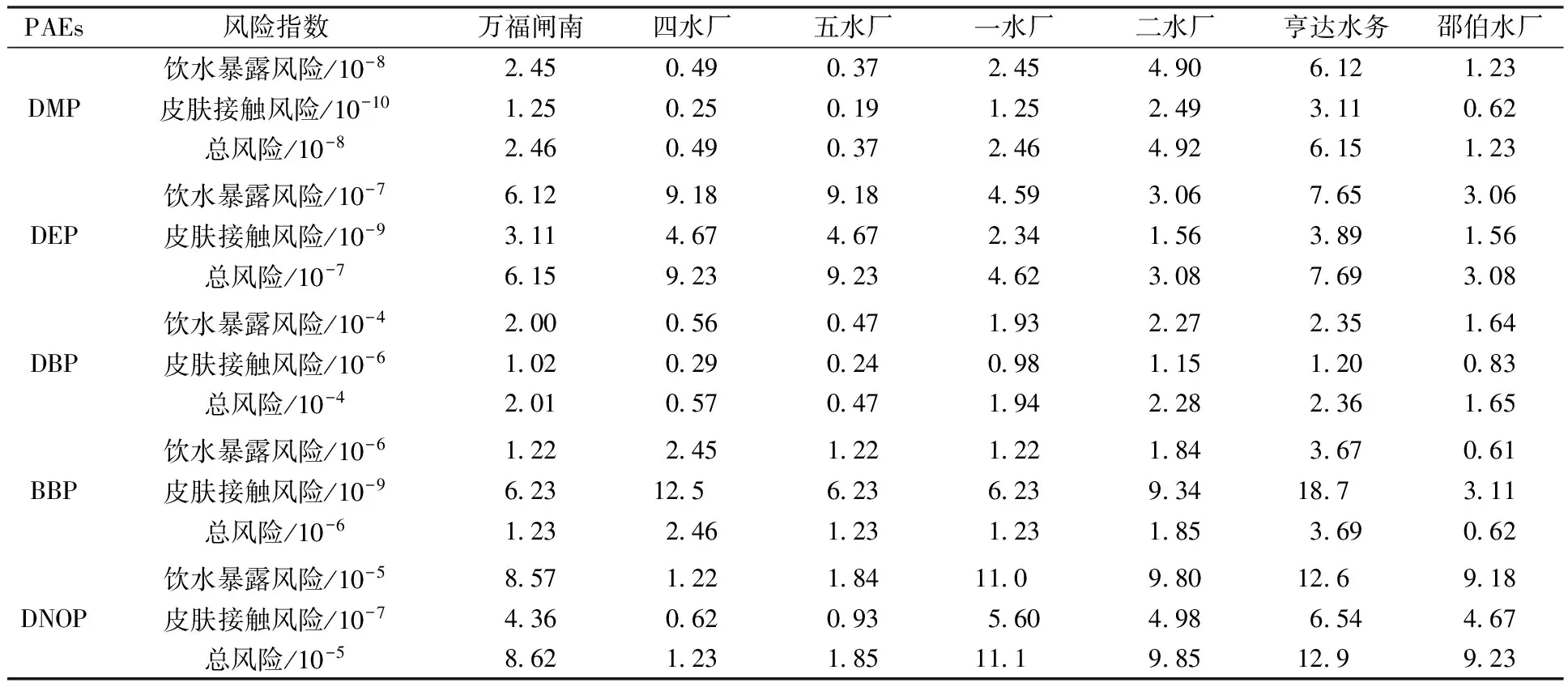
表3 含PAEs水体用于饮用和洗澡的非致癌风险值
2.5 不确定性分析
由于认知的缺乏或信息的有限性,通用场景的分析不能包含所有现实中可能发生的情形,故不确定性是决策者需要考虑的一个必要因素。饮用水源地PAEs分布特征的研究,主要根据水体不同时期采集样品进行分析所得,而研究对象水质和流量时刻变化,在样本数不够充分多的情况下,分析结果只能呈现采样时段内的水质情况,这是引起不确定性的主因。健康风险评估过程中的不确定性来源主要为模型误差引起的不确定性与参数不确定性。本研究仅采用USEPA关于PAEs对人体健康暴露风险评价方法,模型参数选择以一般性为主,未考虑人类分布的广泛性和多种污染物共存时的协同作用。另外,据报道PAEs经净化处理和煮沸后,可去除90%以上的PAEs[31],本研究也未考虑该因素的影响。因此,水体PAEs健康风险评估结果仅为初步判定。
为消减不确定性,需要增大研究对象的样本数,制定更加科学的监测方案,确定合理的人群分类、健康安全边界和评价模型等。
3 结论
1)采用SPE-GC-MS测定某地区7个地表饮用水源地中16种PAEs。结果显示,所有样品均有DIBP、DBP、DEHP检出,DMEP、DPP均未检出,其他PAEs同系物检出率范围为11%~89%。DBP、DEHP、DIBP、DNOP在所有PAEs同系物中含量丰富,表明这4种类型的化学品在该地区广泛消费。
2)芒稻河二水厂断面和三阳河亨达水务断面Σ16PAEs最高,四水厂断面和五水厂断面Σ16PAEs浓度最低,具有内河水体中PAEs浓度高于长江水体的特征。万福闸南等4个内河水体断面丰水期Σ16PAEs浓度显著高于枯水期,而四水厂和五水厂2个长江水体断面呈现枯水期高于丰水期的现象。
3)水体12种PAEs共提出3个主成分,揭示了91%的影响因子:第一主成分包括DMP、DIBP、DBP、BMPP、DEHP、DNOP、DNP,可能源自化妆品、个人护理品和PVC产品;第二主成分为DEP、DEEP、BBP;第三主成分为DCHP。基于层次聚类分析表明,7个采样断面聚为2类,即万福闸南、一水厂、邵伯水厂、二水厂和亨达水务等断面聚为一类,四水厂和五水厂断面聚为一类,分别代表了内河和长江水体。
4)饮用水源地水体的R值和HI值均远低于参考值,说明该水体中PAEs不会对居民构成致癌风险或其他明显的健康风险,但鉴于DEHP具有雌激素活性及其他PAEs对生态环境和人体健康的潜在风险,需加强PAEs使用的规范与监管,强化污染物的末端处理,以规避风险。
[1] SCHECTER A,LORBER M,GUO Y,et al.Phthalate concentrations and dietary exposure from food purchased in New York State[J].Environmental Health Perspectives,2013,121 (4):473-479.
[2] VENTRICE P,VENTRICE D,RUSSO E,et al.Phthalates:European regulation,chemistry,pharmacokinetic and related toxicity[J].Environmental Toxicology & Pharmacology,2013,36 (1):88-96.
[3] GUO Y,KANNAN K.Challenges encountered in the analysis of phthalate esters in foodstuffs and other biological matrices[J].Analytical & Bioanalytical Chemistry,2012,404 (9):2 539-2 554.
[4] LIU X,SHI J,BO T,et al.Occurrence and risk assessment of selected phthalates in drinking water from waterworks in China[J].Environmental Science & Pollution Research International,2015,22 (14):1-9.
[5] HEUDORF U,MERSCH-SUNDERMANN V,ANGERER J.Phthalates:toxicology and exposure[J].International Journal of Hygiene and Environmental Health,2007,210 (5):623-634.
[6] USEPA.EPA-440/5-80-067.Ambient water quality criteria for phthalate esters[R].Criteria and Standard Division,Washington D C:Office of Water Regulations and Standards,1980.
[7] 环境保护部科技标准司.地表水环境质量标准:GB 3838—2002[S].北京:中国环境科学出版社,2002.
[8] CLARK K,COUSINS I T,MACKAY D,et al.Observed concentrations in the environment[M].In Series Anthropogenic Compounds:Phtalate Esters,Staples,Charles A,Ed.Springer Berlin Heidelberg:Berlin,Heidelberg,2003.
[9] DARGNAT C,BLANCHARD M,CHEVREUIL M,et al.Occurrence of phthalate esters in the Seine River estuary (France)[J].Hydrological Processes,2009,23 (8):1 192-1 201.
[10] PEIJNENBURG W J G M,STRUIJS J.Occurrence of phthalate esters in the environment of the Netherlands[J].Ecotoxicology & Environmental Safety,2006,63 (2):204-215.
[11] VITALI M,GUIDOTTI M,MACILENTI G,et al.Phthalate esters in freshwaters as markers of contamination sources—a site study in Italy[J].Environment International,1997,23 (3):337-347.
[12] HUAN H,GUAN J H,CHENG S,et al.Trace analysis of persistent toxic substances in the main stream of Jiangsu section of the Yangtze River,China[J].Environmental Science & Pollution Research,2010,18 (4):638-648.
[13] FAN W,XIA X,SHA Y.Distribution of phthalic acid esters in Wuhan section of the Yangtze River,China[J].Journal of Hazardous Materials,2008,154 (1/3):317-324.
[14] YANG L H,CHENG S P,WU Z B.Anthropogenic organic contaminants in water and surface sediments of large shallow eutrophic Chaohu Lake,China[J].Fresenius Environmental Bulletin,2009,18 (11):2 048-2 054.
[15] FENG Z,WEN J,CUI K,et al.Seasonal distribution of phthalate esters in surface water of the urban lakes in the subtropical city,Guangzhou,China[J].Journal of Hazardous Materials,2009,169 (1/3):719-725.
[16] WOLFE N,STEEN W,BURNS L.Phthalate ester hydrolysis:linear free energy relationships[J].Chemosphere,1980,9 (7):403-408.
[17] HOWARD P H.Handbook of environmental degradation rates[M].London:CRC Press,1991.
[18] 张渝,张新申,杨坪,等.分散式固相萃取净化-气相色谱-质谱联用测定土壤中的邻苯二甲酸酯[J].分析化学,2009,37 (10):1 535-1 538.
ZHANG Yu,ZHANG Xinshen,YANG Ping,et al.Dispersive solid phase extraction clean-upand Gas chromatography-mass spectrometry for determination of phthalate estersin soil samples[J].Analytical Chemistry,2009,37 (10):1 535-1 538.
[19] AMIR S,MERLINA M H,HAMDI H,et al.Fate of phthalic acid esters during composting of both lagooning and activated sludges[J].Process Biochemistry,2005,40 (6):2 183-2 190.
[20] GUO Y,WU Q,KANNAN K.Phthalate metabolites in urine from China,and implications for human exposures[J].Environment International,2011,37 (5):893-898.
[21] STAPLES C,GUINN R,KRAMARZ K,et al.Assessing the chronic aquatic toxicity of phthalate ester plasticizers[J].Human and Ecological Risk Assessment:An International Journal,2011,17 (5):1 057-1 076.
[22] FROMME H,KÜCHLER T,OTTO T,et al.Occurrence of phthalates and bisphenol A and F in the environment[J].Water Research,2002,36 (6):1 429-1 438.
[23] 王凡,沙玉娟,夏星辉,等.长江武汉段水体邻苯二甲酸酯分布特征研究[J].环境科学,2008,29 (5):1 163-1 169.
WANG Fan,SHA Yujuan,XIA Xinghui,et al.Distribution characteristics of phthalic acid esters in the Wuhan section of the Yangtze River[J].Environmental Science,2008,29 (5):1 163-1 169.
[24] 董继元,王式功,尚可政.黄河兰州段邻苯二甲酸酯类有机污染物健康风险评价[J].农业环境科学学报,2010,29 (5):963-968.
DONG Jiyuan,WANG Shigong,SHANG Kezheng.Water environmental health risk assessment of phthalic acid esters in Lanzhou reach of Yellow River[J].Journal of Afro-Environment Science,2010,29 (5):963-968.
[26] FENG Z,YONG L,GUO H.Application of multivariate statistical methods to water quality assessment of the watercourses in northwestern New Territories,Hong Kong[J].Environmental Monitoring & Assessment,2007,132 (1/3):1-13.
[27] DENG J J,HUANG X F,HU J W,et al.Distribution of several microorganisms and activity of alkaline phosphatase in sediments from Baihua Lake[J].Asia-Pacific Journal of Chemical Engineering,2009,4 (5):711-716.
[28] HAMIDIN N,YU Q J,CONNELL D W.Human health risk assessment of chlorinated disinfection by-products in drinking water using a probabilistic approach[J].Water Research,2008,42 (13):3 263-3 274.
[29] USEPA.EPA 505/2-90/001.Technical support document for water quality-based toxics control[R].Washington D C:Office of Water,Reyulations and Standards,1991.
[30] USEPA.EPA/540/1-89/002.Risk assessment guidance for superfund.Human health evaluation manual[R].Washington D C:Office of Emergency and Remedial Response,1989.
[31] SHI W,HU X,ZHANG F,et al.Occurrence of thyroid hormone activities in drinking water from eastern China:contributions of phthalate esters[J].Environmental Science & Technology,2012,46 (3):1 811-1 818.
[32] HE H,HU G J,SUN C,et al.Trace analysis of persistent toxic substances in the main stream of Jiangsu section of the Yangtze River,China[J].Environmental Science and Pollution Research,2011,18 (4):638-648.
[33] HE W,QIN N,KONG X,et al.Spatio-temporal distributions and the ecological and health risks of phthalate esters (PAEs) in the surface water of a large,shallow Chinese lake[J].Science of the Total Environment,2013,461-462 (7):672-680.
[34] RIVERA-UTRILLA J,OCAMPO-PREZ R,MNDEZ-DIAZ J D,et al.Environmental impact of phthalic acid esters and their removal from water and sediments by different technologies-a review[J].Journal of Environmental Management,2012,109:164-178.
[35] 钱伯章.增塑剂的国内外发展现状(上)[J].上海化工,2011,36(2):37-39.
QAIN Bozhang.Current status of plasticizers in China and the world[J].Shanghai Chemical Indudry,2011,36 (2):37-39.
[36] MENG X Z,WANG Y,XIANG N,et al.Flow of sewage sludge-borne phthalate esters (PAEs) from human release to human intake:implication for risk assessment of sludge applied to soil[J].Science of The Total Environment,2014,476-477:242-249.
[37] 杨清华,施逸岚,史玉坤,等.2013年南通市饮用水中17种邻苯二甲酸酯类化合物含量的检测分析[J].中国卫生检验杂志,2015,25 (1):95-97.
YANG Qinghua,SHI Yilan,SHI Yukun,et al.Determination and analysis of 17 phthalic acid esters content in drinking water of Nantong in 2013[J].Chinese Journal of Health Laboratory Technology,2015,25 (1):95-97.
[38] 张彦鹏,周爱国,刘存富,等.长江流域武汉段水体中邻苯二甲酸酯含量研究[J].环境科学与技术,2011,34 (11):130-134.
ZHANG Yanpeng,ZHOU Aiguo,LIU Cunfu,et al.Phthalic acid esters in Wuhan section of Yangtze River[J].Environmental Science & Technology,2011,34 (11):130-134.
