丹皮酚羟丙基-β-环糊精包合物制备、鉴定及性能评价
2017-12-28高丽丽
高丽丽 严 孜 胡 晔
丹皮酚羟丙基-β-环糊精包合物制备、鉴定及性能评价
高丽丽1严 孜2胡 晔1
目的研究制备和鉴定丹皮酚羟丙基-β-环糊精(HP-β-CD)包合物方法,并对其进行性能评价。方法分别采用薄层色谱法、差热分析法和X-射线衍射法对丹皮酚HP-β-CD包合物进行鉴定。结果其真空干燥粉末经鉴别已形成包合物;包合物可显著增大丹皮酚溶解度,提高稳定性。结论丹皮酚HP-β-CD包合物可显著增大药物溶解度和稳定性。
丹皮酚;羟丙基-β-环糊精;包合物;X-射线衍射;差示量热扫描;包合稳定常数
丹皮酚具有显著的镇痛、抗炎和抗菌作用[1],其挥发性较强,水溶性较差,致使制剂的加工和贮存受到一定的限制。为了增加丹皮酚的溶解度,提高稳定性,并使其粉末化,以便制备各种剂型,本研究采用羟丙基-β-环糊精(HP-β-CD)对丹皮酚进行了包合研究,主要对包合物进行了鉴别及性能评价研究。
1 仪器与材料
1.1 仪器岛津UV-2550型紫外分光光度计,DZF-6050型真空干燥箱(上海新苗医疗器械制造有限公司),RE-5210型旋转蒸发仪(上海亚荣生化仪器厂),JRJ300-S型高效剪切乳化机(上海标本模型厂),SHZ-82型气浴恒温振荡器(常州国华电器有限公司)dsc、X衍射仪。
1.2 材料牡丹皮药材(购于安徽亳州,经江西中医学院褚小兰教授鉴定,符合《中国药典》2005版一部要求),丹皮酚对照品、HP-β-CD、磷酸二氢钾、无水乙醇、盐酸以及石油醚均为分析纯。
2 方法与结果
2.1 丹皮酚的制备药材粉碎浸泡2 h、加入15倍量水,采用水蒸气蒸馏法提取8 h,进行蒸馏液收集,收集后冷藏24 h、过滤、40 ℃干燥得丹皮酚针状晶体,滤液进行二次蒸馏,收集蒸馏液冷藏、过滤、干燥,将两次得到的晶体合并。
2.2 丹皮酚HP-β-CD包合物的制备饱和水溶液法制备丹皮酚HP-β-CD包合物,取HP-β-CD 25 g,加入到40 ℃的水中制成10%的HP-β-CD水溶液,在固定转速为每分钟3000 r,缓缓滴加用无水乙醇溶解的丹皮酚溶液(含丹皮酚3.52 g)10 ml,35 ℃下搅拌1 h。取出,60 ℃减压浓缩后进行真空干燥得白色粉末。
2.3 丹皮酚HP-β-CD包合物的鉴定
2.3.1 薄层色谱法取丹皮酚包合物20 mg,加适量石油醚分3次洗涤,滤过,合并滤液,挥去石油醚,残渣加无水乙醇1 ml使其溶解,作为包合物石油醚洗涤液。洗涤后的包合物挥去石油醚,加水溶解,用适量石油醚分3次萃取,合并石油醚萃取液,挥去石油醚,残渣加无水乙醇1 ml使之溶解,作为包合物提取液。另取丹皮酚对照品,加无水乙醇制成2 mg/ml的溶液,作为对照品溶液。吸取上述3种溶液各2 μl,分别点于同一硅胶G薄层板上,以乙酸乙酯-环己烷(1:3)为展开剂展开。取出,晾干,喷以5%三氯化铁(FeCl3)乙醇试液,在105 ℃加热至斑点显色清晰。

图1 丹皮酚包合物薄层鉴别(1为丹皮酚对照品,2为包合物提取液,3为包合物石油醚洗涤液)
从图1可知,丹皮酚包合物石油醚洗涤液无斑点,丹皮酚包合物提取液和丹皮酚对照品溶液斑点完全一致,均显蓝褐色斑点,说明丹皮酚已被HP-β-CD包合。
2.3.2 差示量热扫描法(DSC)鉴别测定样品的制备:将制备一定量的包合物用适量石油醚洗涤3次,再将石油醚溶液过滤,挥干滤渣得到纯净的丹皮酚HP-β-CD包合物。另取丹皮酚和HP-β-CD,制成混合物。分别对丹皮酚、HP-β-CD、两者物理混合物和包合物进行DSC鉴别。
测定条件:样品量:约2 mg;扫描温度范围:10~150 ℃;升温速度:5 ℃/min。
从图2可知,丹皮酚的熔点为50 ℃,峰形尖锐,而HP-β-CD熔程较长,从20~100 ℃,峰温为61 ℃,两者物理混合的差热曲线可以看出为两者峰形的叠加,而从包合物的峰形来看,峰钝,50 ℃时并无放热峰出现,丹皮酚特征峰消失,且峰温变为71 ℃,物性改变,形成新的物相,证明包合物形成。
2.3.3 X-射线衍射法测定样品的制备:按2.3.2项下方法制备试验样品,备用。
测定条件:Cu靶/石墨单色器,电压30 kV,电流20 mA,扫描速度0.1°/s,采样时间为1 s,扫描范围4.8~60.0°,分别将丹皮酚、HP-β-CD、丹皮酚HP-β-CD包合物、丹皮酚和HP-β-CD物理混合物进行粉末X-射线衍射,结果见图3-6。

图2 丹皮酚HP-β-CD包合物DSC鉴别(1为丹皮酚,2为丹皮酚和HP-β-CD物理混合,3为包合物,4为HP-β-CD)

图3 HP-β-CD X-射线衍射鉴别

图4 丹皮酚X-射线衍射鉴别

图5 丹皮酚HP-β-CD包合物X-射线衍射鉴别
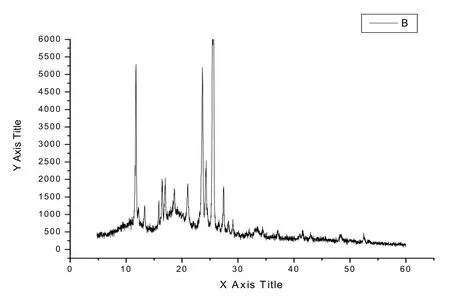
图6 丹皮酚和HP-β-CD物理混合X-射线衍射鉴别
2.4 丹皮酚HP-β-CD包合物的主要性能评价
2.4.1 包合物稳定常数测定分别称取100 mg丹皮酚,依次加入不同浓度的HP-β-CD水溶液0.00 mol/L、0.05 mol/L、0.10 mol/L、0.15 mol/L、0.20 mol/L、0.25 mol/L。将定容后的过饱和溶液分别置25 ℃空气浴震荡器震荡24 h(100次/min),静置,过滤。取适量滤液,用蒸馏水定容至一定体积,按上述方法测定274 nm的吸光度,结果见表1。
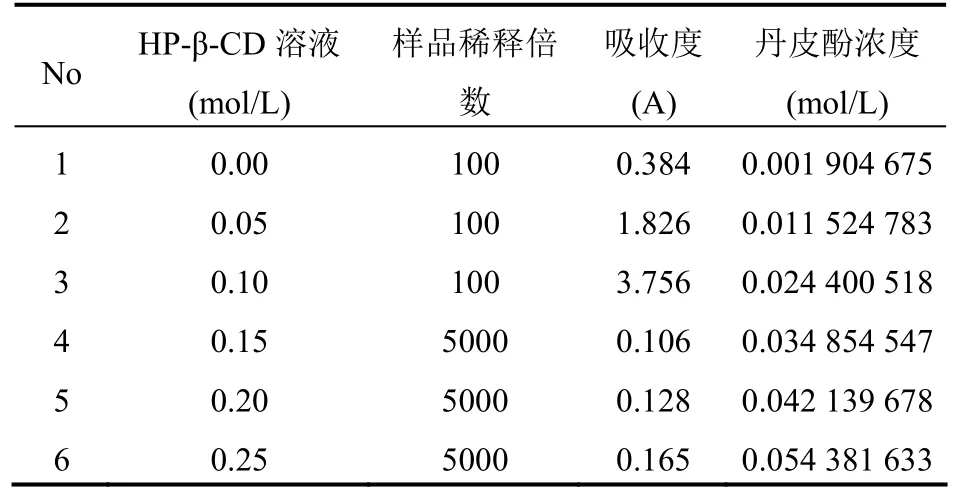
表1 丹皮酚在不同浓度HP-β-CD溶液中的溶解度

图7 丹皮酚相溶解度曲线
由图7可知回归拟合结果,y与x之间成线性关系,HP-β-CD与丹皮酚的摩尔组成比为1:1。
表观稳定常数(Kc)是衡量包合物稳定性的重要参数,Kc值越大,HP-β-CD对药物的稳定作用越强。以丹皮酚溶解度对HP-β-CD浓度线性回归,根据方程计算,公式为

将曲线方程的斜率0.2084和截距即固有溶解度S0=0.0022代入公式,求得25 ℃时丹皮酚与HP-β-CD的包合形成常数为Kc=119.67。
2.4.2 丹皮酚HP-β-CD包合物饱和溶解度的测定丹皮酚HP-β-CD包合物和丹皮酚在不同介质中的饱和溶解度比较,结果见表2。

表2 丹皮酚及包合物在各介质中的饱和溶解度
2.4.3 丹皮酚HP-β-CD包合物稳定性试验
2.4.3.1 高温试验分别称取丹皮酚及丹皮酚HP-β-CD包合物置于已恒重好的称量瓶中,放置于40 ℃恒温箱中,于第0天、第5天、第10天观察其颜色及性状变化;称定重量,计算损失率(公式如下);测定含量。若损失率大于5%,则说明其不稳定;若小于5%,则需在温度为60 ℃进行试验。结果见表3-4。

2.4.3.2 高湿试验分别称取丹皮酚及丹皮酚HP-β-CD包合物置于已恒重好的称量瓶中,放置于湿度为75%的环境中,于第0天、第5天、第10天观察其颜色及性状变化;称定重量,计算增重率(公式如下);测定含量。若增重率大于5%,说明其吸湿性较强;若增重小于5%,则需在湿度为92.5%的环境中进行试验。结果见表5-6。

2.4.3.3 光照试验分别称取丹皮酚及丹皮酚HP-β-CD包合物置于已恒重好的称量瓶中,放置于照度为4500 LX±500 LX温度25℃,恒温光照仪中,于第0天、第5天、第10天观察其颜色及性状变化;称定重量,计算增重率;测定含量。结果见表7。
3 讨论
薄层色谱法是通过丹皮酚自身结构特点,通过FeCl3对丹皮酚的酚羟基可发生络合反应,生成物显蓝褐色,而与HP-β-CD不发生反应,来对包合物进行鉴别。鉴别结果表明,包合物已经形成。本研究中X射线衍射试验结果显示,丹皮酚具有很强的衍射峰,而载体HP-β-CD为无定型粉末,几乎无衍射峰;将两者相混合,其物理混合物中药物仍然保留其特征峰,但是丹皮酚HP-β-CD包合物中药物的衍射峰也随之消失。这可能是因为丹皮酚溶解后以分子形嵌入包合材料的疏水空穴中所致。通过以上三种不同方法对制备的丹皮酚HP-β-CD包合物进行鉴别,充分证明包合物形成,且物性有所改变,形成新的物相。

表3 丹皮酚及丹皮酚HP-β-CD包合物高温试验结果(40 ℃,n=3)
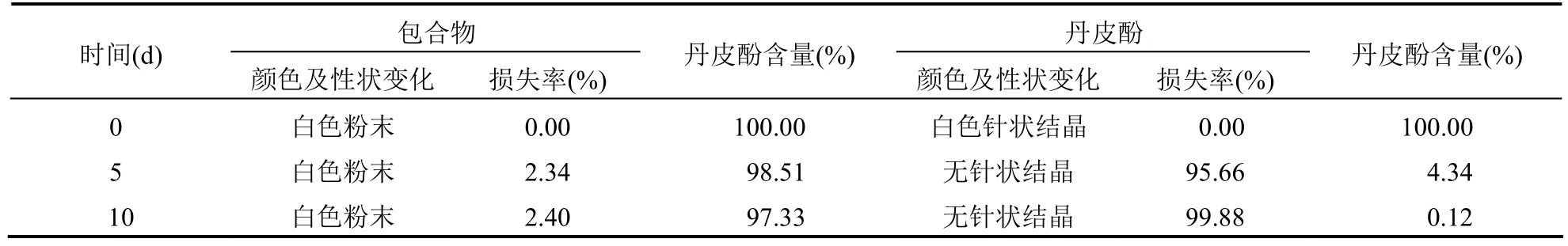
表4 丹皮酚及丹皮酚HP-β-CD包合物高温试验结果(60 ℃,n=3)

表5 丹皮酚及丹皮酚HP-β-CD包合物高湿试验结果(相对湿度70%±5%,n=3)
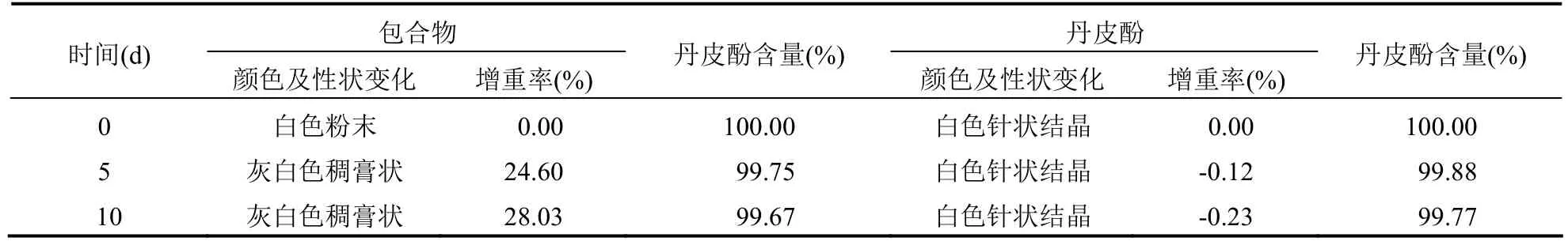
表6 丹皮酚及丹皮酚HP-β-CD包合物高湿试验结果(相对湿度90%±5%,n=3)
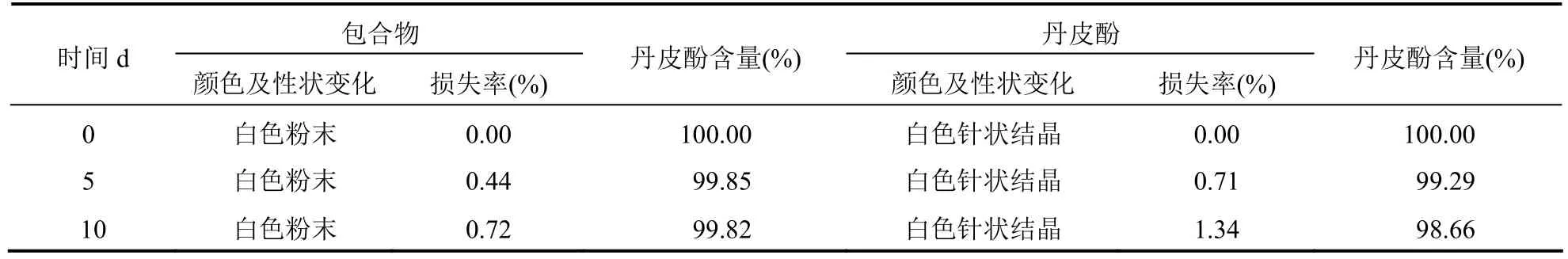
表7 丹皮酚及丹皮酚HP-β-CD包合物光照试验结果(n=3)
溶解度及稳定性试验结果表明,经过包合的丹皮酚性能有很大提高:在水、0.1 mol/L盐酸、pH 6.8磷酸盐缓冲液这三种介质中,分别增大溶解度2.7、3.2、3.0倍,原因为HP-β-CD的亲水性较好,使溶解度提高;在高温及光照条件下,丹皮酚HP-β-CD包合物的稳定性有很大提高,5 d和10 d时含量较0 d时并无明显变化,但在高湿条件下,其吸湿性有所提高,原因为HP-β-CD亲水性较好。因此,在生产和贮存过程中应注意控制湿度,做好防潮措施。
本研究对丹皮酚HP-β-CD包合物的制备工艺、鉴定方法及性能评价进行了研究。通过薄层色谱法、差示量热扫描法(DSC)鉴别和X射线衍射法这三种方法对包合物进行了鉴别,结果表明HP-β-CD可将丹皮酚包合,性质有所改变,已形成新的物相。而经过包合的丹皮酚性能有较大改善,避免了具有挥发性且溶解性差等缺点,溶解度及稳定性有很大提高。
综上所述,HP-β-CD与天然β-CD比较,经衍生化的HP-β-CD水溶性较好,并具有良好的生物相容性,几乎无溶血性,已成为替代环糊精的新型包合材料。
[1]赵俊云,杨晓敏,郭健.丹皮酚抑制SiHa细胞增殖及COX-2转录的实验研究[J].中医药学报,2016,44(1):52-54.
Preparation,identification and nature evaluation of paeonol HP-β-CD inclusion complex
Gao Lili Yan Zi Hu Ye
ObjectiveTo prepare and identify paeonol HP-β-CD inclusion complex(paeonol-HP-β-CD),as well as to appraise its nature.MethodThe inclusion complex was identified by plate chromatography,X-ray diffraction(XRD)and differential scanning calorimetry(DSC).ResultThe vacuum drying powder had been identified to be inclusion complex and its solubility and stability of paeonol was increased.ConclusionThe solubility and stability of paeonol could be increased by preparing the inclusion complex with HP-β-CD.
Paeonol; HP-β-CD;Inclusion complex;DSC;X-ray diffraction;Differential scanning calorimetry;Inclusion constant
10.12010/j.issn.1673-5846.2017.12.006
1江西省医药学校,江西南昌 330006
2江西中医药大学科技学院,江西南昌 330006
