基于蒙特卡洛方法的煤吸附水机理
2017-12-22金智新武司苑邓存宝戴凤威
金智新,武司苑,邓存宝,戴凤威
(1.辽宁工程技术大学 安全科学与工程学院,辽宁 阜新 123000; 2.山西焦煤集团有限责任公司,山西 太原 030053; 3.辽宁工程技术大学 安全工程技术研究院,辽宁 阜新 123000)
基于蒙特卡洛方法的煤吸附水机理
金智新1,2,武司苑1,3,邓存宝1,3,戴凤威1,3
(1.辽宁工程技术大学 安全科学与工程学院,辽宁 阜新 123000; 2.山西焦煤集团有限责任公司,山西 太原 030053; 3.辽宁工程技术大学 安全工程技术研究院,辽宁 阜新 123000)
为研究煤对水的吸附机理,建立煤大分子结构模型,采用巨正则系综蒙特卡洛方法,在分子尺度研究分析了压力1~100 kPa不同温度下水在煤中的吸附行为,为涉及煤水相互作用的进一步研究奠定理论基础。结果表明:水的吸附量和等量吸附热与温度负相关,与压力正相关。在大于临界压力的某一压力下,两吸附位的势能概率分布间形成高原区,说明比例相当。超过该压力,相互作用更强的氢键占主要地位,吸附量开始急剧增大,发生毛细凝聚,形成水团簇。随着压力增大,吸附继续由较弱的H2O-煤相互作用的吸附位向较强的H2O-H2O相互作用的吸附位移动,直至全部作用在由已吸附的H2O形成的第2吸附位,等量吸附热趋于平稳。得到了水在煤中吸附过程概率密度的三维分布,从而更直观全方位地认识水的吸附行为及机理。
水;煤;吸附机理;蒙特卡洛;毛细凝聚
在煤层以及采空区中,水是广泛存在的。煤中水的存在形式主要分为内在水、外在水和化合水。水这种既简单又复杂的物质在煤炭的开采与利用的许多进程中都有着很重要的影响及作用。如煤层注水润湿煤体,对于防治煤尘、防治冲击地压和瓦斯突出、抑制瓦斯解吸有重要作用[1];煤炭中的水对煤的氧化、蓄热和散热过程都有一定的影响,而煤中水分对于煤自燃到底是起阻化作用还是催化作用,还要视具体情况而定[2],其机理目前仍在研究中;近来研究较多的还有水分对于CH4和CO2的吸附以及扩散的影响[3-5],从而会影响瓦斯抽采、CO2的封存和电厂烟气防治采空区遗煤自燃等。显然,上述进程中都涉及到的一个重要问题就是煤与水的相互作用,内在水和外在水大都通过吸附作用存在于煤中,因此首先研究清楚煤对水的吸附机理,能够为上述过程的进一步研究奠定坚实的基础。
目前关于煤吸附水的研究还较少,主要采用实验以及吸附模型理论分析的方法。聂百胜和李祥春等[6-7]依据分子热力学和表面物理化学理论,分析了煤吸附水的作用力主要包括范德华力和氢键。CHARRIRE等[8]实验研究了煤对水的吸附解吸过程,用BET模型和改进的BET模型分析了水的吸附位,用单孔模型分析了水在煤中的扩散。VBOV等[9]实验研究了3种煤样对水的吸附等温线,并用吸附模型分析了吸附位,而每一种吸附模型都有其假设前提,因此有局限性。对于微观上的研究,高正阳等[10]应用密度泛函理论(DFT),以小分子片段代替褐煤模型,研究了褐煤表面与水吸附的不同构型,得到褐煤表面与水之间的弱相互作用以氢键为主。LIU等[11]用DFT和巨正则系综蒙特卡洛(Grand Canonical Monte Carlo,GCMC)方法研究了CH4/CH2/N2的吸附,但是其并没有研究水的吸附等温线,由于水的吸附等温线很难平衡,甚至是在低压下都需要很长时间,并且H2O-H2O之间的相互作用比H2O与吸附剂之间的相互作用强很多,导致H2O的吸附量比其他气体大很多。
近年来已有很多学者采用分子模拟的方法研究煤对气体的吸附[12-14],分子模拟的方法介于宏观的实验和微观的量子化学方法之间,能够用大量的微观平均值表示宏观特性,还能够研究含上千个原子的大分子体系。目前还没有采用GCMC方法系统的研究煤大分子结构模型对水的吸附机理,为了更好地理解水在煤中的吸附机制,笔者建立煤的大分子结构模型,用分子模拟方法研究在低压条件下(1~100 kPa),不同温度时(298.15,303.15,313.15,318.15 K),水的吸附量、等量吸附热、吸附能、吸附位、吸附的概率密度等,为后续研究水对于煤体的润湿和其他气体(如O2,CO2,CH4,N2)吸附的影响等相关问题奠定理论基础。
1 煤结构模型与计算方法
1.1 煤结构模型建立
煤结构十分复杂,并且不能统一,因此相应产生了许多煤结构模型。笔者在总结前人研究成果的基础上,以塔山烟煤为对照,构建的煤结构模型基本结构单元中包含单元核(芳香环、碳氧环和碳氮环),烷基侧链(甲基、乙基等),核外官能团(酚羟基、羧基、甲氧基、含硫官能团和含氮官能团)以及联结桥键(醚键等),分子式为C58H59N3O6S,C,H,O,N,S的质量分数分别为75.24%,6.38%,10.38%,4.54%,3.46%,与塔山煤样的元素分析对应的质量分数74.51%,5.42%,14.43%,3.14%,2.60%非常接近。将19个该结构单元放入空盒子中添加周期性边界条件,构建煤无定形大分子结构模型。几何优化后,为避免局部最优,进行退火动力学处理,使结构达到全局能量最小。
优化后获得的煤结构模型晶胞参数为棱长A=3.152 2 nm,B=3.186 3 nm,C=3.142 0 nm,棱间角α=90.368°,β=88.280°,γ=89.996°,微孔孔隙率为10.28%,如图1所示,在BROCHARD等[15]计算的6%~14%的范围内。
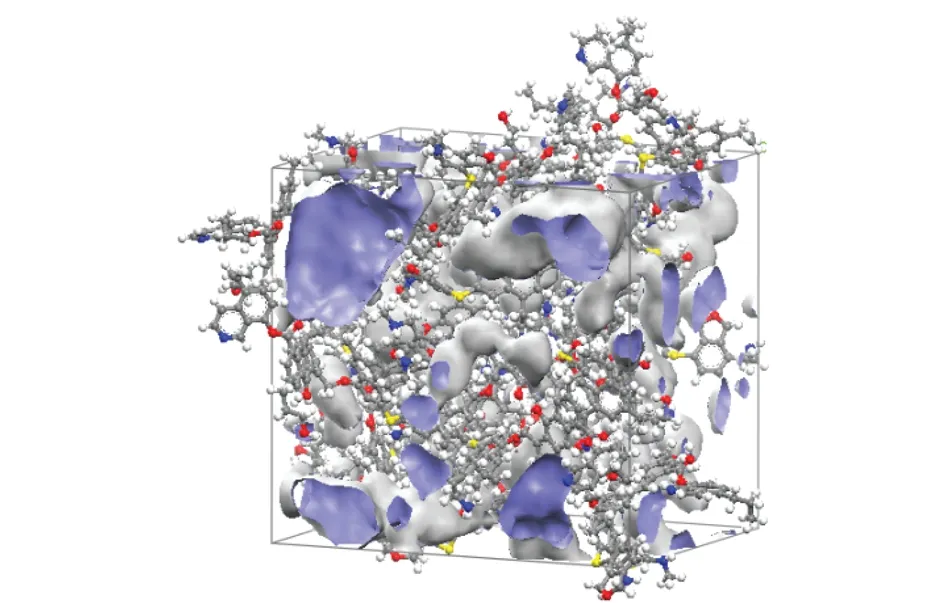
图1 煤的三维结构稳定模型及孔隙表示Fig.1 Stable 3D structure model of coal with pores
经过300~600 K退火动力学优化,密度稳定在1.128 g/cm3附近,与HU等[14]中用Dreiding力场计算的密度接近,比实际值偏小,这是由于此模型中不含矿物质元素。能量也基本达到最小并趋于稳定,如图2所示,这说明体系已达到热力学平衡状态,验证了模拟的可靠性。

图2 退火优化过程煤的密度及能量变化Fig.2 Density and energy changes of coal during annealing process
1.2 计算方法
对于水在煤中的吸附,采用GCMC方法,保持吸附质的化学势、体积和温度不变,模拟吸附过程。把吸附质分子看作刚性小分子,选择Metropolis重要性抽样算法[16]。由于水的吸附很难达到平衡,为了满足精度的要求达到平衡,并且节省计算时间,经过多次试算选取平衡步数2×107,生产步数5×107。由于水与煤和它本身存在氢键作用,因此选择可以计算氢键的Dreiding力场,在该力场中总能量(E)包括价电子能(Eval)和非成键能(Enb),范德华能(Evdw)和氢键作用能(Ehb)都包含在非成键能中。前人研究结果表明此力场适用于煤结构以及吸附的研究[17-18]。静电作用采用Ewald加和法,精度为4.184×10-4kJ/mol,范德华作用和氢键作用采用Atom based法,截断半径分别设为1.55 nm和0.45 nm。
2 结果与讨论
2.1 吸附等温线
水在4种温度下1~100 kPa的吸附等温线如图3所示。首先在相同压力下,吸附量随着温度的升高而降低,说明在计算的温度压力范围内,水在煤中的吸附是放热的,高温不利于吸附,属于物理吸附。

图3 不同温度压力下H2O的吸附量Fig.3 Adsorption amount of H2O in different temperature and pressure
图3中插入的小图为压力1~10 kPa时水的吸附量部分的放大,可见在临界压力以下,水的吸附量随着压力的增大缓慢增加,此时发生的可能为单分子层吸附,水吸附在主吸附位。随着压力继续增大超过临界压力时,在某个压力点下水的吸附量开始急剧增大。不同温度下出现的急剧增大的压力不同,298.15 K时,约在20 kPa开始吸附量急剧增大;303.15 K时,急剧增大点约为25 kPa;313.15 K时约为40 kPa;318.15 K时约为50 kPa,温度越高,该压力越大。这种吸附量的急剧增大可能是发生了毛细凝聚,形成了大量的水团簇。吸附量急剧增大之后,由于孔径的限制逐渐趋于平缓,直至填满孔隙。
2.2 等量吸附热
为了进一步研究吸附量在某压力点出现急剧增大的原因,计算了等量吸附热,如图4所示。在1~10 kPa等量吸附热受温度影响很小,温度升高,等量吸附热稍有降低,且其值都小于42 kJ/mol,属于物理吸附。在298.15,303.15 K高于10 kPa以及313.15,318.15 K高于20 kPa时,等量吸附热也出现大幅度升高,随后趋于平稳。等量吸附热的变化说明在这一过程中有吸附位的变化,大幅度升高的过程即为从主吸附位向第2吸附位吸附的过程,升高的开始就是从主吸附位转向第2吸附位的开始,升高的结束就是水分子已基本全部依赖第2吸附位在吸附。且在第2吸附位吸附所放出的热量要大于在主吸附位吸附放出的热量。
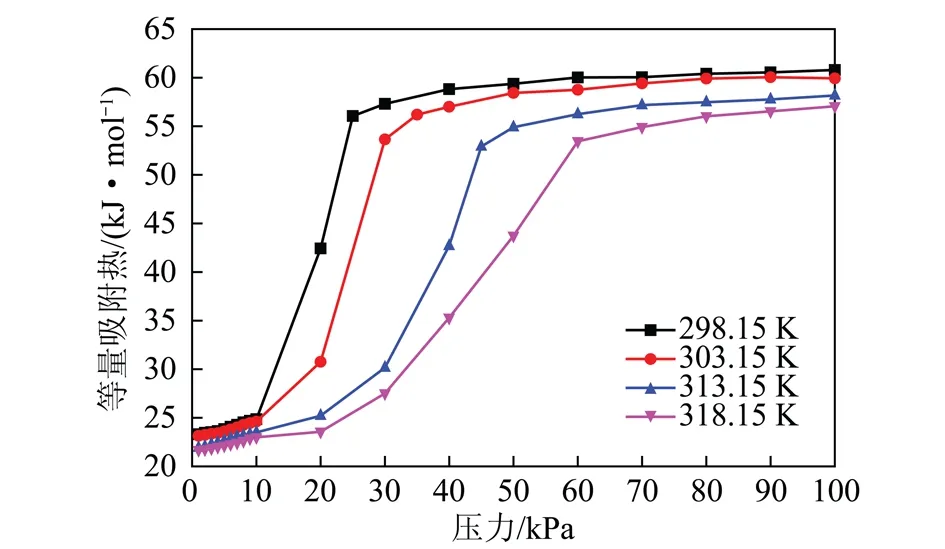
图4 不同温度压力下H2O的等量吸附热Fig.4 Isosteric heat of H2O in different temperature and pressure
不同温度下,等量吸附热开始趋于平稳的压力也不同。298.15 K时,在25 kPa左右等量吸附热即开始趋于稳定不变,303.15 K时,趋于稳定的压力点约为30 kPa,313.15 K时约为45 kPa,318.15 K时约为60 kPa。可以看到,吸附量开始急剧增大的压力基本比等量吸附热趋于平稳的压力小5~10 kPa,且大致位于等量吸附热大幅度升高的中部。可以认为,当在第2吸附位吸附的水分子占一半时,吸附量开始急剧增加。最终等量吸附热稳定于55~60 kJ/mol,超出了物理吸附的范畴,如上述吸附量分析中所提及的,推断发生了毛细凝聚,从而出现了强于H2O与煤之间相互作用的H2O-H2O之间的相互作用,形成了大量的水团簇,氢键作用强于范德华作用,因此还需要对吸附能进行计算。
2.3 吸附能
本文所指的吸附能,是吸附前后整个体系总能量的变化量。其中分子内能由于太小可忽略不计,主要考察范德华能和氢键作用能,分别如图5(a),(b)所示,可见其大小和趋势均有差别。

图5 水吸附体系的范德华能和氢键作用能Fig.5 Van der waals energy and hydrogen-bond energy in different H2O sorption systems
吸附能是吸附量和等量吸附热的综合反映。不难看出,图5(b)中氢键作用的变化趋势与图3中吸附量的变化趋势是一致的,氢键能急剧增大的压力点即为吸附量急剧增大的压力点,并且氢键作用能在数值上比范德华能大很多,因此水在煤中的吸附量主要由氢键作用控制,范德华作用占次要地位。而在发生毛细凝聚之前,氢键的优势并不明显,即在主吸附位2者共同作用。随着压力的增大,水分子之间强烈的氢键作用导致出现毛细凝聚,吸附量激增。
2.4 能量分布
除了吸附量、吸附热这些宏观的现象,蒙特卡洛模拟还能获得分子尺度的吸附位以及势能概率分布情况。图6描述了本文所研究的4个温度下,随着压力变化水的能量分布。一般情况下,势能图所表示的低相互作用能区域即为优先吸附位,通过观察不同压力下的能量分布情况,可以得知随着吸附量增加优先吸附位被占满[19]。但是如图6所示,从一开始在压力较低时,在能量较高的-20 kJ/mol处出现峰值,此处为主吸附位。随着压力的增大吸附量的增加,主吸附位吸附概率降低,表明已被填满,反而吸附位向低能量区域移动,在-60 kJ/mol左右出现峰值,为第2吸附位。吸附位没有一开始就出现在相互作用强的低能量区域,是因为该吸附位不是煤本身提供的最初就存在的吸附位,而是随着吸附的进行新形成的。也就是说,随着水在煤中吸附的进行,由于H2O-H2O之间很强的氢键相互作用,已吸附的H2O分子成为第2吸附位,形成水团簇,发生毛细凝聚。
在298.15 K时(图6(a)),从1 kPa开始,主吸附位出现峰值,随着压力增大,峰值降低,开始向较低的能量区域增加吸附位。直到压力增加到20 kPa时,在-60~-20 kJ/mol出现较为平缓的高原区域,即在该压力下,两吸附位所占比例各为一半。也是在该压力下,如上述分析,等量吸附热位于大幅度升高的中部,超过该压力即在第2吸附位所占的比例大于主吸附位时,吸附量开始急剧增大。25 kPa时,等量吸附热开始趋于平稳,在第2吸附位出现较高峰值,主吸附位已填满,主要在第2吸附位吸附,验证了上述分析的正确性。同样,在303.15 K时(图6(b)),随着压力增大主吸附位峰值下降,在27 kPa下,-60和-20 kJ/mol之间出现较为平缓的高原区域,两吸附位所占比例相当,到30 kPa时,只在第2吸附位有一较高峰值,等量吸附热趋于平稳,吸附主要在第2吸附位进行。在313.15 K时(图6(c)),在两吸附位之间出现高原区域的压力为40 kPa,该压力位于等量吸附热大幅度增大的中部,超过该压力时吸附量急剧升高,这是由于此压力下两吸附位所占比例相当。45 kPa时,等量吸附热趋于平稳,在-60 kJ/mol处有惟一较高峰值,吸附主要发生在该吸附位。在318.15 K时(图6(d)),出现高原区域的压力与等量吸附热大幅度增大的中部和吸附量急剧升高的压力一致,约为50 kPa,此时两吸附位所占比例相当。等量吸附热开始趋于平稳的压力与只在第2吸附位出现峰值的初始压力一致,约为60 kPa。每一种特征压力点都随着温度的升高而增大,这可能与水的临界压力有关,温度越高,水的临界压力越大。
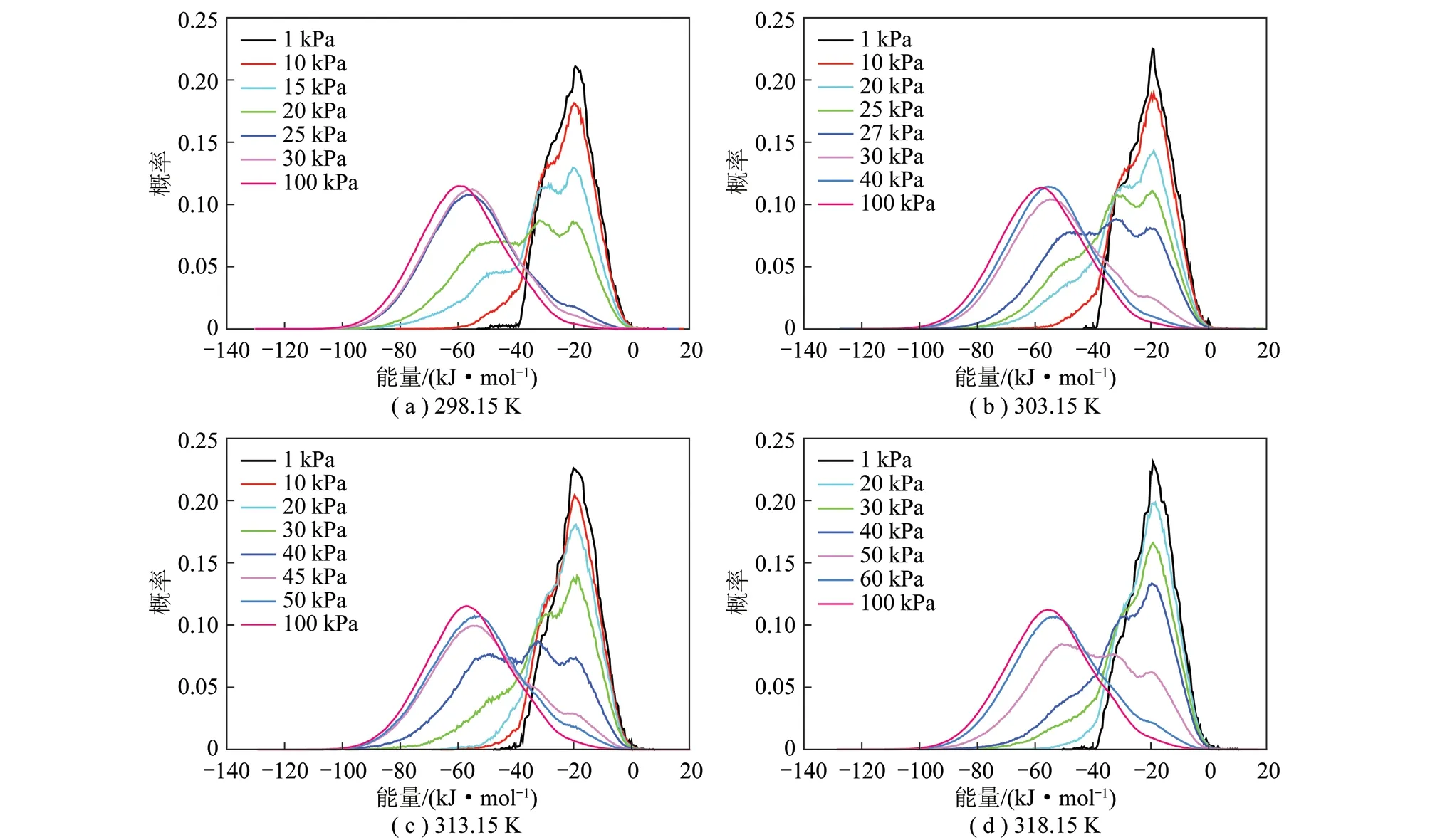
图6 随着压力变化H2O吸附的能量分布Fig.6 Energy distribution of H2O adsorption with vary pressure
2.5 概率密度场分布
为了进一步直观的了解水在煤中的吸附机理及吸附位,分析了水在煤中吸附时的概率密度场分布情况,如图7所示。没有选择分析吸附构象,是因为吸附构象只是吸附过程中任意某一随机的可能,而密度场分布则代表了在整个大量的步数过程中水在煤中
吸附位的统计平均的结果[19]。图7展示了298.15 K和318.15 K两个温度下,水在煤中随着压力变化吸附密度变化情况(选取了4个特征压力点,其余压力下没有一一列出)。在298.15 K压力10 kPa时,水零星的吸附在煤孔隙中,此时的吸附基本依赖于水分子和煤之间的相互作用力。20 kPa时,已经开始有一部分孔中有水的少量聚集,并且呈蓝色,说明密度很低。压力升到25 kPa时,有大孔中存在较大密度的水聚集,形成了水团簇。到100 kPa时,水团簇聚集的位置继续有更多的水来聚集,水的密度变得很大,因此也有很强的氢键作用。318.15 K时,水的吸附过程与298.15 K时一样,只是特征压力与上述吸附量和能量分布中的推测一致,在50 kPa时才开始出现有明显的水团簇聚集的现象,到100 kPa时,大孔中水的密度增加,几乎填满整个孔隙。

图7 H2O在煤中吸附的概率密度分布Fig.7 Probability density distribution of H2O in coal
水在煤中的密度分布的结果,结合上述对吸附量、等量吸附热、吸附能和能量分布的分析,所得到的水在煤中吸附过程的机理是一致的,它们之间互相验证,从而达到对水的吸附全面的多方位的理解认识。
3 结 论
(1)温度与吸附量负相关,压力与其正相关。且在低压时变化缓慢,在298.15,303.15,313.15和318.15 K时吸附量分别在20,25,40和50 kPa开始急剧增大,发生了毛细凝聚,形成了水团簇。
(2)温度与等量吸附热负相关,压力与其正相关。在1~10 kPa,等量吸附热变化缓慢,随后大幅度增加,最终在298.15,303.15,313.15和318.15 K时等量吸附热分别在25,30,45和60 kPa趋于平稳,基本完成了由范德华能作用的主吸附位向更强的氢键能作用的第2吸附位的转移。
(3)随着压力的增大,水在煤中的吸附位由能量较高的主吸附位(-20 kJ/mol处峰值)向能量较低的第2吸附位(-60 kJ/mol处峰值)移动,表明第2吸附位不是由煤结构提供,而是水吸附过程中形成的,即已吸附的水分子。在两吸附位之间形成高原区的压力也是等量吸附热突增的中部,两吸附位比例相当,吸附量激增。在只有第2吸附位惟一峰值的压力点,等量吸附热趋于平稳。
(4)以概率密度分布图的形式表示出不同温度压力下水在煤中的吸附,结合吸附量、等量吸附热、吸附能、吸附位等综合分析,得到更直观的全方位多方面的水在煤中的吸附机理,为今后进一步研究煤体润湿、水对于煤解吸瓦斯、封存CO2等的影响奠定了理论基础。
[1] 范家文,赵东,吴金贵,等.注水在煤层开采过程中的作用及影响[J].煤矿开采,2011,16(2):16-19.
FAN Jiawen,ZHAO Dong,WU Jingui,et al.Action and influence of water injection on coal mining[J].Coal Mining Technology,2011,16(2):16-19.
[2] 梁晓瑜,王德明.水分对煤炭自燃的影响[J].辽宁工程技术大学学报,2003,22(4):472-474.
LIANG Xiaoyu,WANG Deming.Effects of moisture on spontaneous combustion of coal[J].Journal of Liaoning Technical University,2003,22(4):472-474.
[3] 赵东,冯增朝,赵阳升.基于吸附动力学理论分析水分对煤体吸附特性的影响[J].煤炭学报,2014,39(3):518-523.
ZHAO Dong,FENG Zengchao,ZHAO Yangsheng.Effects of liquid water on coalbed methane adsorption characteristics based on the adsorption kinetic theory[J].Journal of China Coal Society,2014,39(3):518-523.
[4] GENSTERBLUM Y,MERKEL A,BUSCH A,et al.High-pressure CH4and CO2sorption isotherms as a function of coal maturity and the influence of moisture[J].International Journal of Coal Geology,2013,118(3):45-57.
[5] LI Xiaochun,FANG Zhiming.Current status and technical challenges of CO2storage in coal seams and enhanced coalbed methane recovery:an overview[J].International Journal of Coal Science & Technology,2014,1(1):93-102.
[6] 聂百胜,何学秋,王恩元,等.煤吸附水的微观机理[J].中国矿业大学学报,2004,33(4):17-21.
NIE Baisheng,HE Xueqiu,WANG Enyuan,et al.Micro-mechanism of coal adsorbing water[J].Journal of China University of Mining & Technology,2004,33(4):17-21.
[7] 李祥春,聂百胜.煤吸附水特性的研究[J].太原理工大学学报,2006,37(4):417-419.
LI Xiangchun,NIE Baisheng.Study of characteristics of coal adsorbing water[J].Journal of Taiyuan University of Technology,2006,37(4):417-419.
[10] 高正阳,吕少昆,李晋达,等.褐煤表面吸附水分子的微观机理[J].动力工程学报,2016,36(4):258-264.
GAO Zhengyang,LÜ Shaokun,LI Jinda,et al.Micro-mechanism of water molecule adsorption on Lignite surface[J].Journal of Chinese Society of Power Engineering,2016,36(4):258-264.
[11] LIU Xiaoqiang,HE Xu,QIU Nianxiang,et al.Molecular simulation of CH4,CO2,H2O and N2molecules adsorption on heterogeneous surface models of coal[J].Applied Surface Science,2016,389:894-905.
[12] ZHANG J,LIU K,CLENNELL M B,et al.Molecular simulation of CO2/CH4competitive adsorption and induced coal swelling[J].Fuel,2015,160:309-317.
[13] ZHAO Y,FENG Y,ZHANG X.Molecular simulation of CO2/CH4self and transport diffusion coefficients in coal[J].Fuel,2015,165:19-27.
[14] HU H,LI X,FANG Z,et al.Small-molecule gas sorption and diffusion in coal:Molecular simulation[J].Energy,2010,35(7):2939-2944.
[15] BROCHARD L,VANDAMME M,PELENQ R J M,et al.Adsorption induced deformation of microporous materials:Coal swelling induced by CO2-CH4competitive adsorption[J].Langmuir,2012,28(5):2659-2670.
[16] FRENKEL,SMIT.Molecular simulation-from algorithm to application[M].Beijing:Chemical Industry Press,2002.
[17] CARLSON G A.Computer simulation of the molecular structure of bituminous coal[J].Energy Fuels,1992,6(6):771-778.
[18] 相建华,曾凡桂,梁虎珍,等.CH4/CO2/H2O在煤分子结构中吸附的分子模拟[J].中国科学:地球科学,2014,44(7):1418-1428.
XIANG Jianhua,ZENG Fangui,LIANG Huzhen,et al.Molecular simulation of the CH4/CO2/H2O adsorption onto the molecular structure of coal[J].Science China:Earth Sciences,2014,44(7):1418-1428.
[19] DÜREN T,BAE Y S,SNURR R Q.Using molecular simulation to characterise metal-organic frameworks for adsorption applications.[J].Chemical Society Reviews,2009,38(5):1237-1247.
H2OadsorptionmechanismincoalbasingonMonteCarlomethod
JIN Zhixin1,2,WU Siyuan1,3,DENG Cunbao1,3,DAI Fengwei1,3
(1.CollegeofSafetyScience&Engineering,LiaoningTechnicalUniversity,Fuxin123000,China; 2.ShanxiCokingCoalGroupCo.Ltd.,Taiyuan030053,China; 3.SecurityEngineeringTechnologyResearchInstitute,LiaoningTechnicalUniversity,Fuxin123000,China)
The macromolecular coal structural model is constructed and the H2O adsorption behavior in coal is simulated using Grand Canonical Monte Carlo method at 1-100 kPa and at 298.15,303.15,313.15 and 318.15 K to investigate the H2O adsorption mechanism on molecular scale which lays a theoretical foundation for further research involving the interaction between coal and water.The results show that the adsorbed amount and isosteric heat of H2O show a negative correlation with temperature and a positive correlation with pressure.When pressure is greater than a critical pressure,there is a plateau area of potential energy probability distribution between two adsorption sites indicating equal proportion.When exceeding the pressure,the adsorbed amount increases sharply then capillary condensation occurs with water cluster because of the control of stronger hydrogen-bond interaction.With the increase of pressure,the adsorption process transfers from weaker adsorption sites provided by H2O-coal interaction to stronger adsorption sites provided by H2O-H2O interaction,until total sites are secondary adsorption sites forming from adsorbed H2O then the isosteric heat tend to be steady.The 3D probability density distribution provides a more intuitionistic comprehensive understanding to H2O adsorption behavior and mechanism in coal.
H2O;coal;adsorption mechanism;Monte Carlo;capillary condensation
金智新,武司苑,邓存宝,等.基于蒙特卡洛方法的煤吸附水机理[J].煤炭学报,2017,42(11):2968-2974.
10.13225/j.cnki.jccs.2017.0084
JIN Zhixin,WU Siyuan,DENG Cunbao,et al.H2O adsorption mechanism in coal basing on Monte Carlo method[J].Journal of China Coal Society,2017,42(11):2968-2974.doi:10.13225/j.cnki.jccs.2017.0084
TQ533
A
0253-9993(2017)11-2968-07
2017-01-14
2017-09-01责任编辑韩晋平
国家自然科学基金资助项目(51174108,51774172)
金智新(1959—),男,辽宁锦州人,中国工程院院士。Tel:0418-3351702。
武司苑(1991—),女,河北唐山人,博士研究生。Tel:0418-3351702,E-mail:wusiyuanluanx@126.com
