肾康注射液对大鼠体内厄贝沙坦药动学的影响
2017-12-19金贞姬常泽娜朱震菡杨长青延边大学附属医院药学部吉林延吉133000中国药科大学基础医学与临床药学学院南京11198
金贞姬,常泽娜,朱震菡,杨长青#(1.延边大学附属医院药学部,吉林延吉133000;.中国药科大学基础医学与临床药学学院,南京11198)
肾康注射液对大鼠体内厄贝沙坦药动学的影响
金贞姬1*,常泽娜2,朱震菡2,杨长青2#(1.延边大学附属医院药学部,吉林延吉133000;2.中国药科大学基础医学与临床药学学院,南京211198)
目的:研究肾康注射液对大鼠体内厄贝沙坦药动学的影响。方法:取18只SD大鼠随机分为对照组(生理盐水)和肾康注射液组(以生药量计为4 g/kg),每组9只,每天ip给药2次,连续给药7 d。末次给药1 h后,两组大鼠均ig厄贝沙坦25 mg/kg,分别于厄贝沙坦给药前及给药后0.25、0.5、1、2、4、8、12、24、32、48、56、72、96 h经眼底静脉丛采血0.3 mL。以联苯双酯为内标,采用高效液相色谱法测定大鼠血浆中厄贝沙坦的血药浓度,利用Phoenix WinNolin®6.1药动学软件中非房室模型拟合并计算药动学参数。结果:对照组和肾康注射液组大鼠ig厄贝沙坦后,AUC0-96h分别为(28.82±10.49)、(35.64±9.99)mg·h/L,cmax分别为(0.64±0.15)、(0.76±0.33)mg/L,tmax分别为(13.07±16.70)、(10.23±3.97)h,CLZ/F分别为(0.85±0.35)、(0.63±0.21)L/(h·kg),VZ/F分别为(38.24±24.87)、(30.99±9.75)mL/kg,组间比较差异均无统计学意义(P>0.05)。结论:肾康注射液在正常给药剂量下不影响厄贝沙坦在大鼠体内的药动学过程。
肾康注射液;厄贝沙坦;药动学;大鼠
厄贝沙坦是血管紧张素Ⅱ受体抑制药,临床上常用于原发性高血压以及2型糖尿病肾病合并高血压的治疗[1-2]。厄贝沙坦在人体内主要经肝细胞色素P4502C9酶(CYP2C9)代谢[3],原型药及代谢物经胆汁和肾排泄。肾康注射液是由大黄、丹参、黄芪、红花等4味中药组成的中药注射剂,适用于慢性肾衰竭各个阶段的治疗,呈现出良好的安全性和有效性[4],临床上常与厄贝沙坦联合用于治疗早期糖尿病肾病[5]。但是,目前尚无肾康注射液对厄贝沙坦体内药动学有无影响的研究报道。鉴于此,本研究主要考察肾康注射液对大鼠体内厄贝沙坦药动学的影响,为厄贝沙坦和肾康注射液的临床合理联用提供实验依据。
1 材料
1.1 仪器
LC-2010AHT高效液相色谱(HPLC)仪,配备LC-20AT四元高压泵、在线脱气机、SPRING(228-46460-02自动进样器、SPD-20A紫外检测器和Shimadzu Lab Solutions LC Solution工作站,购自日本Shimadzu公司;TGL-18M台式高速冷冻离心机(湖南赛特湘仪离心机仪器有限公司)。
1.2 药品与试剂
厄贝沙坦对照品(批号:100607-201202,纯度:99%)、联苯双酯对照品(内标,批号:100192-200503,纯度:99%)购自中国食品药品检定研究院;肾康注射液(西安世纪盛康药业有限公司,批号:20150521,规格:20 mL/支);厄贝沙坦片(扬子江药业集团北京海燕药业有限公司,批号:15083011,规格:75 mg/片);乙腈和甲醇为色谱纯,其余试剂均为分析纯。
1.3 动物
18只清洁级SD大鼠,♂,体质量200~220 g,购于上海杰思捷实验动物有限公司,动物生产许可证号:SCXK(沪)2008-0016。购入后大鼠分笼饲养[动物房温度为(25±2)℃],饲养期间喂以标准鼠粮,自由摄食和饮水,并在进行药动学实验前12 h禁食。本研究获得中国药科大学动物伦理委员会批准,并严格按照动物护理和处理规范操作。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液取厄贝沙坦对照品适量,用甲醇溶液制备成质量浓度为1 mg/mL的贮备液,置于4℃冰箱中,备用。临用时精密吸取上述贮备液适量,稀释成质量浓度分别为0.4、0.8、1.6、3.2、8、16 μg/mL的系列对照品溶液。
2.1.2 内标溶液取内标联苯双酯对照品适量,用甲醇溶液制备成质量浓度为8 μg/mL的内标溶液。
2.2 血浆样品的处理
取50 μL血浆至1.5 mL离心管中,加入内标溶液50 μL(8 μg/mL),再加入100 μL甲醇,涡旋混合2 min,在4℃下以10 000×g离心10 min,取上清液进样分析。
2.3 色谱条件
色谱条件是在文献[6]的基础上进行优化后得出。色谱柱:Galaksil EF-C18H(250 mm×4.6 mm,5 μm);流动相:甲醇-水(含0.1%三氟乙酸)(55∶45,V/V);流速:0.8 mL/min;检测波长:245 nm;柱温:35℃;进样量:10 μL。
2.4 专属性与系统适用性试验
取大鼠空白血浆样品、空白血浆+内标样品、ig厄贝沙坦之前血浆样品以及ig厄贝沙坦12 h后血浆样品+内标,分别按“2.2”项下方法处理后,按“2.3”项下色谱条件进样测定。结果,空白血浆中内源性物质及代谢产物均不干扰厄贝沙坦和内标的测定,厄贝沙坦与内标的色谱峰分离良好,分离度均大于1.5,保留时间分别为9.35、13.91 min,以各自的色谱峰计理论板数均大于3 000,表明该分析方法具有良好的专属性。色谱图见图1。
2.5 标椎曲线的绘制
取厄贝沙坦的0.4、0.8、1.6、3.2、8、16 μg/mL系列对照品溶液,用空白血浆制备终质量浓度分别为0.1、0.2、0.4、0.8、2.0、4.0 μg/mL的系列血浆标准溶液,按“2.2”项下方法处理后,按“2.3”项下色谱条件进样测定,记录色谱图。以厄贝沙坦的质量浓度为横坐标(x,μg/mL)、厄贝沙坦与内标峰面积的比值为纵坐标(y)进行线性回归,得回归方程为y=0.390 16x-2.49×10-3(r=0.999 0)。结果表明,厄贝沙坦在0.1~4.0 μg/mL的质量浓度范围内具有良好的线性关系,定量下限为0.1 μg/mL。
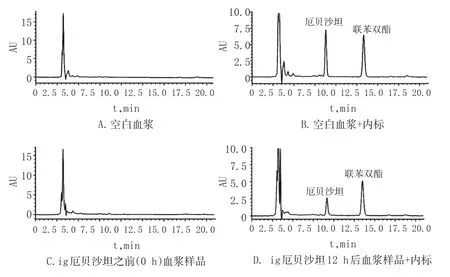
图1 高效液相色谱图Fig 1HPLC chromatograms
2.6 稳定性试验
制备低、中、高质量浓度(0.1、2.0、4.0 μg/mL)的厄贝沙坦血浆标准样品,按“2.2”项下方法处理,分别放置0、6、12 h后按“2.3”项下色谱条件进样测定,考察其稳定性。结果,低、中、高质量浓度样品的RSD分别为2.05%、1.98%、2.92%(n=3),说明处理后样品在12 h内稳定,适合自动化进样检测。
2.7 检测限
取标准曲线的最小质量浓度(0.1 μg/mL)的血浆样品,进一步稀释成0.05、0.025 μg/mL的样品溶液,按“2.2”项下方法处理后,按“2.3”项下色谱条件进样测定。每个质量浓度样品溶液连续测定5次,计算平均值和标准差(SD)。当平均值接近3倍SD时,该质量浓度即为最低检测限。结果显示,本分析方法的最低检测限为0.05 μg/mL(RSD=4.53%、RE=7%,n=5)。
2.8 精密度与准确度试验
使用空白血浆制备低、中、高质量浓度(0.1、2.0、4.0 μg/mL)的厄贝沙坦血浆标准样品,每个质量浓度平行制备3份,按“2.2”项下方法处理后,按“2.3”项下色谱条件进样测定。同日内连续测定3次,连续测定3 d,考察日内和日间精密度。制备含厄贝沙坦血浆样品,每一质量浓度进行3样本分析,分别与相应质量浓度的厄贝沙坦对照品溶液进行峰面积比较,计算相对回收率。结果,低、中、高质量浓度厄贝沙坦标准样品日内精密度试验的RSD分别为0.55%、2.38%、0.22%(n=3),日间精密度试验的RSD分别为2.41%、1.14%、1.19%(n=3);平均相对回收率分别为(98.36±2.92)%、(94.78±2.89)%、(94.21±1.76)%,RSD分别为2.97%、3.05%、1.87%(n=3),说明该试验的精密度及准确度均较好。
2.9 大鼠体内药动学研究
取18只SD大鼠适应性饲养1周后称体质量,然后随机分为对照组(生理盐水)和肾康注射液组(以生药量计为4 g/kg,按临床常用剂量换算所得),ip给予相应药物,每日2次,连续给药7 d。末次给药1 h后,两组大鼠均ig厄贝沙坦混悬液(25 mg/kg,按临床常用剂量换算所得),分别于厄贝沙坦给药前(0 h)及给药后0.25、0.5、1、2、4、8、12、24、32、48、56、72、96 h经眼底静脉丛采血0.3 mL[6],分离血浆,采用前述处理及测定方法测得各时间点厄贝沙坦血药浓度。采用Phoenix WinNonlin®6.1药动学软件中的非房室模型拟合并计算药动学参数(权重为1/C2),采用SPSS 20.0统计学软件中的t检验比较组间药动学参数的差异,P<0.05表示差异具有统计学意义。结果,大鼠体内厄贝沙坦平均药-时曲线见图2,主要药动学参数计算结果见表1。

图2 厄贝沙坦在大鼠体内的平均药-时曲线(n=9)Fig2Meanplasmaconcentration-timecurvesof irbesartan in rats in vivo(n=9)
表1 两组大鼠主要药动学参数(±s,n=9)Tab 2The main pharmacokinetic parameters of rats in 2 groups(±s,n=9)

表1 两组大鼠主要药动学参数(±s,n=9)Tab 2The main pharmacokinetic parameters of rats in 2 groups(±s,n=9)
药动学参数AUC0-96h,mg·h/L CLZ/F,L/(h·kg)VZ/F,mL/kg t1/2,h tmax,h cmax,mg/L对照组28.82±10.49 0.85±0.35 38.24±24.87 31.36±14.73 13.07±16.70 0.64±0.15肾康注射液组35.64±9.99 0.63±0.21 30.99±9.75 37.82±21.53 10.23±3.97 0.76±0.33
表1结果显示,与对照组比较,肾康注射液组大鼠体内厄贝沙坦的AUC0-∞、cmax、tmax、CLZ/F和VZ/F等药动学参数差异均无统计学意义(P>0.05),提示肾康注射液不影响厄贝沙坦的体内药动学过程。
3 讨论
体外研究结果表明,肾康注射液的单味中药或有效成分对CYP2C9酶活性具有不同程度的抑制作用,即丹参水溶性总提取物、丹参的有效成分(丹参酮Ⅰ、丹参酮ⅡA、隐丹参酮和二氢丹参酮)、大黄提取物及大黄素等对CYP2C9酶具有中等强度的抑制作用,黄芪甲苷也可显著抑制CYP2C9酶活性[7-12]。体内研究结果显示,丹参水溶性总提取物在大鼠体内抑制CYP2C9底物华法林的代谢[13];黄芪注射液在正常大鼠和糖尿病大鼠体内抑制CPY2C9的活性,降低CPY2C9底物格列美脲的清除率[14]。从这些单味中药或中药有效成分的体内外研究结果推测,肾康注射液可抑制厄贝沙坦的体内代谢。然而,本研究结果显示,与对照组比较,肾康注射液组大鼠体内厄贝沙坦的AUC0-96h、tmax、cmax、VZ/F、t1/2和CLZ/F等药动学参数差异均无统计学意义(P>0.05),表明在临床治疗剂量下肾康注射液不影响CYP2C9酶的活性,不影响厄贝沙坦的体内过程。另外,本研究中对照组中tmax的标准差大于均值,是因为2只大鼠的tmax异常大(分别为48.00、30.02 h),其具体原因有待进一步探讨。
[1]Croom KF,Curran MP,Goa KL,et al.Irbesartan:a review of its use in hypertension and in themanagementofdiabeticnephropathy[J].Drugs,2004,64(9):999-1028.
[2]吴立华,梁辑.依那普利叶酸片联合肾康注射液治疗高血压肾病的临床观察[J].中国药房,2015,26(36):5099-5101.
[3]Choi CI,Kim MJ,Chung EK,et al.CYP2C9 3 and 13 alleles significantly affect the pharmacokinetics of irbesartan in healthy Korean subjects[J].Eur J Clin Pharmacol,2012,68(2):149-154.
[4]Wu X,Guan Y,Yan J,et al.Shenkang injection suppresseskidneyfibrosisandoxidative stress via transforming growth factor-β/Smad3 signalling pathway in vivo and in vitro[J].J Pharm Pharmacol,2015,67(8):1054-1065.
[5]郝玉杰,徐雅鹏,王运红,等.肾康注射液联合厄贝沙坦对63例早期糖尿病肾病患者的疗效分析[J].中国中医基础医学杂志,2011,17(3):337-338.
[6]Bae SK,Kim MJ,Shim EJ,et al.HPLC determination of irbesartan in human plasma:its applicationtopharmacokineticstudies[J].Biomed Chromatogr,2009,23(6):568-572.
[7]叶娜,罗红丽,李容,等.丹参注射液对大鼠肝微粒体CYP450亚型酶体外抑制作用[J].中成药,2015,37(5):948-953.
[8]Hasegawa A,Kawaguchi Y,Nakasa H,et al.Effects of Kampo extracts on drug metabolism in rat liver microsomes:Rhei Rhizoma extract and Glycyrrhizae Radix extract inhibit drug oxidation[J].Jpn J Pharmacol,2002,89(2):164-170.
[9]单文雅,张玉峰,朱捷强,等.黄芪甲苷对大鼠肝微粒体酶活性影响[J].中国中药杂志,2012,37(1):85-88.
[10]Wang X,Cheung CM,Lee WY,et al.Major tanshinones of Danshen(Salvia miltiorrhiza)exhibit different modes of inhibition on human CYP1A2,CYP2C9,CYP2E1 and CYP3A4 activities in vitro[J].Phytomedicine,2010,17(11):868-875.
[11]韦炳华,陈孝,宗连柱.复方丹参滴丸对大鼠肝微粒体细胞色素b5含量的影响[J].现代食品与药品杂志,2006,16(3):21-23.
[12]王来友,李镜清,陈涛,等.大黄素的Ⅰ相代谢途径及其对细胞色素P450酶的抑制作用[J].中国临床药理学与治疗学,2014,19(3):241-245.
[13]Lo AC,Chan K,Yeung JH,et al.The effects of Danshen(Salvia miltiorrhiza)on pharmacokinetics and pharmacodynamics of warfarin in rats[J].Eur J Drug Metab Pharmacokinet,1992,17(4):257-262.
[14]刘晓峰,张帆,王惠成,等.正常大鼠和糖尿病大鼠格列美脲药动学及黄芪注射液对其的影响[J].中国新药与临床杂志,2012,31(4):227-230.
Effect of Shenkang Injection on the Irbesartan Pharmacokinetics in Rats in vivo
JIN Zhenji1,CHANG Zena2,ZHU Zhenhan2,YANG Changqing2(1.Dept.of Pharmacy,Affiliated Hospital of Yanbian University,Jilin Yanji 133000,China;2.School of Basic Medicine and Clinical Pharmacy,China Pharmaceutical University,Nanjing 211198,China)
OBJECTIVE:To study the effect of Shenkang injection on the irbesartan pharmacokinetics in rats in vivo.METHODS:18 SD rats were randomly divided into control group(normal saline)and Shenkang injection(calculated by crude drug as 4 g/kg),9 in each group,which were intraperitoneally injected twice a day,for 7 d.After 1 h of last administration,25 mg/kg irbesartan was intragastrically administrated.0.3 mL sample blood was taken in fundus venous plexus before administration of irbesartan and after 0.25,0.5,1,2,4,8,12,24,32,48,56,72,96 h of administration.Using biphenyl diester as inner standard,HPLC was adopted to determine the plasma concentration of irbesartan in plasma of rats,and pharmacokinetic parameters were calculated by using non-compartmental model in Phoenix WinNolin®6.1 pharmacokinetic software.RESULTS:After intragastrically administrated irbesartan in rats in control group and Shenkang injection group,AUC0-96hwere(28.82±10.49),(35.64±9.99)mg·h/L;cmaxwere(0.64±0.15),(0.76±0.33)mg/L;tmaxwere(13.07±16.70),(10.23±3.97)h;CLZ/Fwere(0.85±0.35),(0.63±0.21)L/(h·kg);VZ/Fwere(38.24±24.87),(30.99±9.75)mL/kg respectively,with no statistical significances(P>0.05).CONCLUSIONS:Shenkang injection will not affect the in vivo pharmacokinetics process of irbesartan in normal dose on rats.
Shenkang injection;Irbesartan;Pharmacokinetics;Rats
R969.1
A
1001-0408(2017)34-4815-03
DOI10.6039/j.issn.1001-0408.2017.34.16
*主任药师。研究方向:临床药学。电话:0433-2670822。E-mail:15526770822@163.com
#通信作者:教授,博士。研究方向:临床药学、药动学。电话:025-86185447。E-mail:ycq0315@yahoo.com
2017-05-03
2017-09-21)
(编辑:林静)
