微波灭活髓内钉固定治疗长骨骨干转移瘤的疗效观察
2017-12-01姬文晨阮之平韩学哲杨益民
李 嘉,姬文晨,阮之平,韩学哲,杨益民,戴 星,李 萌*
(1西安交通大学第一附属医院骨科,西安 710061;2西安交通大学第一附属医院肿瘤内科;*通讯作者,E-mail:drleemon@163.com)
微波灭活髓内钉固定治疗长骨骨干转移瘤的疗效观察
李 嘉1,姬文晨1,阮之平2,韩学哲1,杨益民1,戴 星1,李 萌1*
(1西安交通大学第一附属医院骨科,西安 710061;2西安交通大学第一附属医院肿瘤内科;*通讯作者,E-mail:drleemon@163.com)
目的 探讨微波原位灭活病灶刮除骨水泥填充加交锁髓内钉固定的方法治疗长骨骨干转移瘤的疗效。 方法 收集2009-01~2014-06西安交通大学第一附属医院收治的四肢长骨骨干转移瘤23例(23处),均采用微波原位灭活、病灶刮除、骨水泥填充加交锁髓内钉固定的方法治疗,其中20例伴有病理性骨折。术前术后分别采用视觉模拟评分(VAS)评价疼痛程度,Enneking评分评价肢体功能,Karnofsky评分评价生活质量。 结果 全部病例均获随访,时间4-24个月,平均16.2个月。手术顺利,无术中死亡病例,术后切口均一期愈合。局部复发1例,无感染病例。无骨水泥及髓内钉松动、断裂等情况发生。随访期间死亡14例,存活9例,总体半年生存率91.3%,1年生存率69.6%,2年生存率39.1%。术后视觉模拟评分、Enneking评分、Karnofsky评分较术前均有改善。 结论 采用瘤段微波原位灭活、病灶刮除、骨水泥填充加交锁髓内钉固定的方法治疗长骨骨干转移瘤,可以恢复患者的完全负重能力,减轻疼痛,提高生存质量,是一种有效的外科治疗方法。
骨转移瘤; 微波; 髓内钉; 外科治疗
恶性肿瘤转移到骨组织是常见的恶性病变生长形式,无论来源是癌还是肉瘤,统称为骨转移瘤。约24%的骨转移瘤发生在长管状骨,除了引起常见的骨痛症状外,还可能导致病理性骨折,使病人生活质量急剧下降,甚至丧失治疗信心[1]。随着肿瘤诊治水平的提高,近年来对骨转移瘤的治疗呈现出更为积极的态度,有效的外科治疗可以缓解疼痛、提高生活质量、改善肢体功能,还有助于改善对于原发肿瘤治疗的条件,是肿瘤综合治疗的一个重要环节。本研究对我院部分四肢长骨骨干转移瘤病人的临床资料进行分析,探讨瘤段微波原位灭活、病灶刮除、骨水泥填充加交锁髓内钉固定的方法治疗长骨骨干转移瘤的疗效。
1 资料与方法
1.1 临床资料
收集2009-01~2014-06西安交通大学第一附属医院收治的四肢长骨骨干转移瘤23例(23处),均采用微波原位灭活、病灶刮除、骨水泥填充加交锁髓内钉固定的方法治疗。
病例纳入标准:①影像学证实四肢长骨骨干骨质破坏并病理性骨折或有潜在病理性骨折风险;②全身情况可以耐受麻醉及手术治疗;③病理诊断为骨转移瘤;④不适宜行广泛切除;⑤病人有治疗意愿。
病例排除标准:①发生骨转移瘤的长骨因解剖等原因不适宜使用髓内钉固定;②既往已有截瘫、偏瘫、肢体严重畸形等导致发生骨转移瘤的肢体已丧失功能;③预期存活时间不足3个月。
其中男性16例,女性7例,年龄43-77岁,平均59岁。23例中20例伴有病理性骨折,另外3例有潜在病理性骨折风险。23例均为单处骨转移,其中15例骨转移瘤发生于股骨,3例发生于胫骨,5例发生于肱骨。原发恶性肿瘤分别为乳腺癌10例,肺癌6例,宫颈癌2例,前列腺癌2例,食管癌1例,肾癌1例,肝癌1例。
1.2 手术方法
对23例长骨骨干病理性骨折病人(包括股骨、胫骨、肱骨),术前穿刺活检明确诊断后,根据影像学制定个体化手术方案,采集CT DICOM数据通过手术计划软件制作stl文件,输入到3D打印机制作微波原位灭活个体化导板,麻醉后术中边缘外分离肿瘤,在3D打印导板引导下原位插入微波针和温度传感器(南京维京九洲医疗器械研发中心MTC-3D微波热肿瘤辅助治疗系统),控制性高温灭活肿瘤组织(设置功率70 W,维持病灶内温度60-100 ℃,持续10-15 min),灭活范围至肿瘤边缘2 cm以上。同时以冷生理盐水适时冲洗外周,保持正常组织温度低于40 ℃。微波灭活完成后,刮除微波灭活的肿瘤组织及表面焦痂,保留坚硬的骨壳,根据术前计划进行骨折复位,交锁髓内钉固定,应用骨水泥填充骨缺损区,透视确认骨折复位良好、内固定位置良好、骨缺损区被骨水泥填充完全。
1.3 术后处理及随访
术后予以预防性应用抗生素,应用低分子肝素或利伐沙班预防深静脉血栓。骨科处理完毕后,由康复科进行术后康复功能锻炼及肿瘤内科根据其原发肿瘤性质继续进行化疗或放疗,骨科定期随访。
1.4 评价指标
纳入研究的所有患者在术前及术后3个月进行疗效评价。采用视觉模拟量表(visual analogue scale, VAS)进行疼痛评价,Enneking评分评价肢体功能[2],Karnofsky评分(KPS)评价生活质量[3]。
1.5 统计学方法
采用SPSS 17.0统计软件对数据进行处理分析。计量资料均以均数±标准差表示,比较采用t检验进行统计学分析。计数资料比较采用卡方检验。P<0.05视为差异有统计学意义。
2 结果
2.1 一般情况
全部病例均获随访,时间4-24个月,平均16.2个月,随访期内无失访患者。全部患者手术均顺利,无术中死亡病例,术后均未出现伤口感染及伤口不愈合,无神经血管损伤及深部感染,无深静脉血栓形成、压疮等长期卧床相关并发症。无骨水泥及髓内钉松动、断裂等情况发生。随访期间局部转移灶复发1例。
典型病例见图1,患者,男,64岁,确诊左肺腺癌半年,摔伤导致左股骨近段病理性骨折,术中骨折端病灶病理检查证实左股骨近段转移性低分化腺癌,符合肺癌骨转移,遂予以微波原位灭活、病灶刮除、骨水泥填充加交锁髓内钉固定治疗,术后X线提示骨折对位、对线良好。
2.2 VAS疼痛评分
23例患者VAS评分术前为(7.87±1.06)分,术后第3个月为(2.26±0.81)分,差异有统计学意义(P<0.05)。
2.3 Enneking功能评分
全部患者术后3月按Enneking功能评定标准进行评价,结果显示23例患者中优7例,良10例,中3例,差3例,优良率达73.9%(17/23)。
2.4 Karnofsky生活质量评分
23例患者术后均获得良好的随访,时间4-24个月。有14例患者于随访期间死于肿瘤相关并发症,其中1-6个月内死亡2例、7-12个月死亡5例、13-24个月死亡7例,总体半年生存率91.3%(21/23),1年生存率69.6%(16/23),2年生存率39.1%(9/23)。术后3个月对23例患者行Karnofsky生活质量评分结果显示,显效8例,有效11例,无效4例,总有效率为82.6%(19/23)。
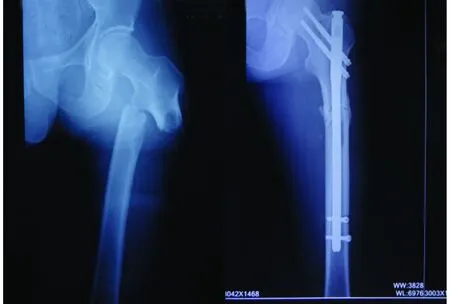
A.术前 B.术后图164岁左股骨近段转移性低分化腺癌男性患者X线表现Figure 1The X-ray findings of a typical male sixty-four-year-old patient with metastatic and poorly differentiated adenocarcinoma in left proximal femur
3 讨论
近年来,随着医疗水平的提高,恶性肿瘤患者的生存时间明显延长,出现四肢长骨骨干转移瘤合并病理性骨折在临床中亦越来越多见。骨折后的剧烈疼痛、活动障碍及生活自理能力的丧失给患者带来极大的生理及心理负担,严重降低了患者的生活质量。积极有效的外科干预可以立即缓解疼痛症状、提高生活质量、恢复肢体功能,有利于后期生活护理,是肿瘤综合治疗的一个重要环节。
目前有学者认为对于长骨骨干转移瘤,只要无手术禁忌证,且患者预期生存期大于12周,术前评估确定手术治疗可以使患者获益(术后患者可以早期开始活动或便于护理),均可考虑手术治疗[4]。对于长骨骨干转移瘤,传统的治疗方法多采用肿瘤囊内病灶刮除骨水泥填充加钢板或髓内钉内固定,然而该术式具有局部肿瘤易复发及再次骨折的缺点,一旦复发,最终只能截肢,会给患者带来极大的痛苦。
微波是一种高频电磁波,在微波产生的电磁场内,极性分子(主要为水分子)作高速的旋转运动,因震动摩擦的作用,将动能转变为热能产生高温,因而使作用范围内的肿瘤组织加热至60-100 ℃,直接对肿瘤组织进行灭活。微波灭活技术是近年来迅速发展起来的一种治疗骨肿瘤的方法,其操作简单方便、创伤小、见效快、可控性强、并发症少,为临床治疗骨肿瘤提供了一项有效治疗选择。
考虑到长骨骨干转移瘤传统的治疗方法具有局部肿瘤易复发等缺点,我们将瘤段微波原位灭活与病灶刮除骨水泥填充加髓内钉内固定相结合,以期望达到恢复肢体功能的同时有效降低局部肿瘤的复发。微波灭活已被用于肝脏、肺、肾、肾上腺及骨等多种组织肿瘤的治疗[5]。Fan等[6]首次将原位微波灭活肿瘤技术应用于治疗骨肿瘤,并证明原位微波灭活技术是一种治疗骨肿瘤的安全有效方法。微波灭活技术有以下几个优点:①保留了骨壳从而保证了骨结构的稳定性与连续性,最大限度地保存了肢体的功能;②微波通过肿瘤正中心的导线产生,使产生的高温由里及表传导,既扩大范围进行热灭活,保证了所有的肿瘤细胞都能被杀灭,减少术后局部复发的可能,又对正常组织的损伤达到最小;③除热效应外,微波还可诱导机体的抗肿瘤反应,这种效应可能由于T细胞或NK细胞介导的免疫反应所致。然而,微波灭活技术亦有一定的缺陷。微波灭活技术对手术者的经验要求较高,否则容易灭活不足或者过量。灭活不足易导致局部复发率增高,而灭活过度则易导致深部感染或损伤周围的软组织,造成神经血管损伤。因此,术者在灭活肿瘤前应充分暴露需微波灭活的部分,用湿纱布将其与周围正常组织分隔开并适时用冷生理盐水冲洗外周,避免灭活时损伤周围正常组织。为避免损伤神经血管,术者应熟悉局部解剖,将重要神经血管适当游离并用湿纱布保护。微波灭活后应充分刮除微波灭活的肿瘤组织及表面焦痂,仅保留骨皮质,避免坏死组织造成深部感染[7]。
Ruggieri等[8]报道骨盆转移瘤经局部骨转移瘤切除术术后短期复发率高达60%。Pusceddu等[9]研究表明经微波灭活治疗的骨转移瘤患者,其术后局部复发率仅为6%,且并发症少,提示原位微波灭活技术是一种安全、有效的治疗方法。吴振杰等[10]采用原位微波灭活术联合钢板内固定术治疗四肢骨干转移瘤,术后局部复发率为5%,疼痛及患肢功能较术前明显改善,且围术期及随访期内无神经血管热损伤、周围组织坏死、感染、伤口愈合不良、内固定松动、再次病理性骨折等不良并发症。本研究将瘤段微波原位灭活与病灶刮除骨水泥填充加髓内钉内固定相结合治疗长骨骨干转移瘤,结果显示23例患者中局部复发1例(4.3%),术后3个月VAS评分(2.26±0.81)较术前(7.87±1.06)明显下降,Enneking功能评分优良率达73.9%,Karnofsky生活质量评分总有效率为82.6%,且随访期无伤口感染、伤口不愈合、深静脉血栓形成、压疮、骨水泥及髓内钉松动、断裂等情况发生。
综上所述,应用瘤段微波原位灭活、病灶刮除、骨水泥填充加交锁髓内钉固定的方法治疗长骨骨干转移瘤,可以减轻患者疼痛,恢复肢体功能,提高生存质量,是一种简单、有效、并发症少、复发率低的治疗方法。
[1] Macedo F, Ladeira K, Pinho F,etal. Bone metastases: an overview[J]. Oncol Rev, 2017,11(321):43-49.
[2] Enneking WF, Dunham W, Gebhardt MC,etal. A system for the functional evaluation of reconstructive procedures after surgical treatment of tumors of the musculoskeletal system[J]. Clin Orthop Relat Res, 1993,(286):241-246.
[3] van der Linden YM, Dijkstra SP, Vonk EJ,etal. Prediction of survival in patients with metastases in the spinal column: results based on a randomized trial of radiotherapy[J]. Cancer, 2005,103(2):320-328.
[4] 王子富,尚希福.交锁髓内钉加骨水泥在股骨肿瘤中段缺损重建中的应用[J].临床骨科杂志,2013,16(1):23-25.
[5] Choi J, Raghavan M. Diagnostic imaging and image-guided therapy of skeletal metastases[J]. Cancer Control, 2012,19(2):102-112.
[6] Fan QY, Ma BA, Zhou Y,etal. Bone tumors of the extremities or pelvis treated by microwave-induced hyperthermia[J]. Clin Orthop Relat Res, 2003,406(1):165-175.
[7] 杨小明,张余,张涛,等.原位微波消融术治疗骨肿瘤的常见并发症及防治策略[J].中国修复重建外科杂志,2012,26(12):1473-1476.
[8] Ruggieri P, Mavrogenis AF, Angelini A,etal. Metastases of the pelvis: does resection improve survival [J]? Orthopedics, 2011,34(7):e236-244.
[9] Pusceddu C, Sotgia B, Fele RM,etal. Treatment of bone metastases with microwave thermal ablation[J]. J Vasc Interv Radiol,2013,24(2):229-233.
[10] 吴振杰,莫立根,刘斌,等.原位微波灭活术联合钢板内固定术治疗四肢骨干转移瘤合并病理性骨折的临床观察[J].广西医学,2017,39(4):467-469.
Theefficiencyofinsitumicrowaveablationcombinedwithintramedullaryinterlockingnailonlimbdiaphysealmetastases
LI Jia1,JI Wenchen1,RUAN Zhiping2,HAN Xuezhe1,YANG Yimin1,DAI Xing1,LI Meng1*
(1DepartmentofOrthopedics,FirstAffiliat-edHospitalofXi’anJiaotongUniversity,Xi’an710061,China;2DepartmentofMedicalOncology,FirstAffiliatedHospitalofXi’anJiaotongUniversity;*Correspondingauthor,E-mail:drleemon@163.com)
ObjectiveTo evaluate the efficiency ofinsitumicrowave ablation, clearance of focal lesion, cement infilling combined with intramedullary interlocking nail on limb diaphyseal metastases.MethodsTwenty-three patients with limb diaphyseal metastases were treated withinsitumicrowave ablation, clearance of focal lesion, cement infilling combined with intramedullary interlocking nail from January 2009 to June 2014 in the First Affiliated Hospital of Xi’an Jiaotong University. Of 23 patients, 20 patients were accompanied by pathological fractures. The visual analogue scale(VAS) score before operation and 3 months after operation were investigated. In addition, Enneking score and Karnofsky performance scale were assessed.ResultsAll of the 23 patients were followed up for 4-24 months with the average follow-up period of 16.2 months.All the operations were successful without patient death during the opera-tion and all incisions achieved primary healing. One case of local recurrence was observed and there were no complications including infection, loosening or breakage of internal fixation. During the follow-up period, 14 patients died. The postoperative 6-month,1-year and 2-year survival rates were 91.3%, 69.6% and 39.1%, respectively.The VAS score, Enneking score and Karnofsky performance scale were all improved.ConclusionInsitumicrowave ablation, clearance of focal lesion, cement infilling combined with intramedullary interlocking nail is an effective method to treat patients with limb diaphyseal metastases. It could relieve the patients’ pain and restore the limb function.
bone metastases; microwave ablation; intramedullary interlocking nail; surgery
国家临床重点专科建设资助项目
李嘉,男,1989-12生,博士,住院医师,助理研究员,E-mail:happylee-xjtu@163.com
2017-08-10
R738
A
1007-6611(2017)11-1182-04
10.13753/j.issn.1007-6611.2017.11.020
