5%咪喹莫特乳膏治疗日光性角化症一例
2017-11-28朱培秋闫慧敏赵惠娟郭独一
朱培秋 闫慧敏 赵惠娟 郭独一 姜 薇
5%咪喹莫特乳膏治疗日光性角化症一例
朱培秋 闫慧敏 赵惠娟 郭独一 姜 薇
日光性角化症(Actinic keratosis,AK)是一种癌前病变。目前其治疗方法种类较多,需结合患者病情及实际情况做出最佳选择。5%咪喹莫特乳膏新一代免疫调节剂,兼有抗病毒及抗肿瘤活性,可外用治疗日光性角化症。国内鲜有报道。本文报道一例仅外用5%咪喹莫特乳膏治疗日光性角化症的临床病例,皮损改善较为显著。
临床资料患者,女,80岁。主因右侧额部红斑反复破溃结痂2年余就诊。10年前患者右侧额部近眉尾处出现数个绿豆大红褐色丘疹,自觉轻微瘙痒。5年前皮疹渐多,周围可见明显红晕,渐融合,其上覆盖干燥性黄白色鳞屑,相互黏连,不易剥离,时有痛痒。曾经外用糖皮质激素类药膏,未见明显好转。患者高血压病史20年,口服药物血压控制可。家族中无类似情况。喜户外活动,未注意严格防晒。系统检查未见明显异常。皮肤科检查:右侧额部近眉尾处可见一直径4 cm淡红斑,边缘暗红色不规则,周边散在绿豆大红色丘疹,红斑边缘及丘疹表面覆盖干燥性黄白色鳞屑,不易剥离,可见其下灰白色组织(图1)。右额部红斑边缘处皮损组织病理示:表皮可见不典型角质形成细胞,表皮下层不典型细胞排列紊乱,呈芽蕾状突入真皮乳头层。真皮浅层可见日光弹力组织变性及少量淋巴细胞浸润,附属器及其周围角质形成细胞正常(图2)。诊断:日光性角化症。治疗:患者拒绝光动力治疗,给予5%咪喹莫特乳膏外用,隔日1次,治疗3个月。治疗1个月后皮疹变为暗红色,中心可见正常肤色(图3)。3个月后红斑完全消退,仅边缘留有色素沉着(图4)。
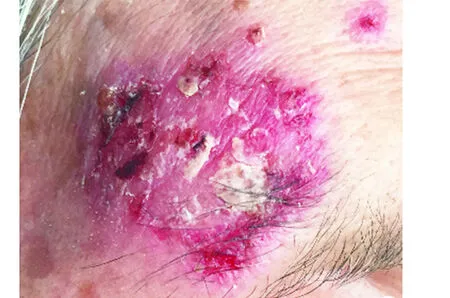
图1 治疗前皮损:境界不清淡红斑,边缘颜色较深,不规则,表面可见黏着性痂屑,不易剥离
讨论日光性角化症/病,又称光线性角化病、老年性角化病,其作为一种癌前病变,现多认为是由日光长期暴晒损伤皮肤所引起。由于全球正在进入老龄化社会,其患病率逐年增加[1]。本病可进展为皮肤鳞状上皮细胞癌,故需积极治疗[2]。
本例患者,老年女性,慢性病程,既往日光暴露史明确,曾外用糖皮质激素类药膏治疗效果差。皮损为典型光暴露部位,以淡红斑为主,颜色深浅不均匀,表面可见角化性痂屑,黏着不易剥离。组织病理检查结果符合AK特征性表现,结合临床表现及组织病理结果,日光性角化症诊断较为明确。
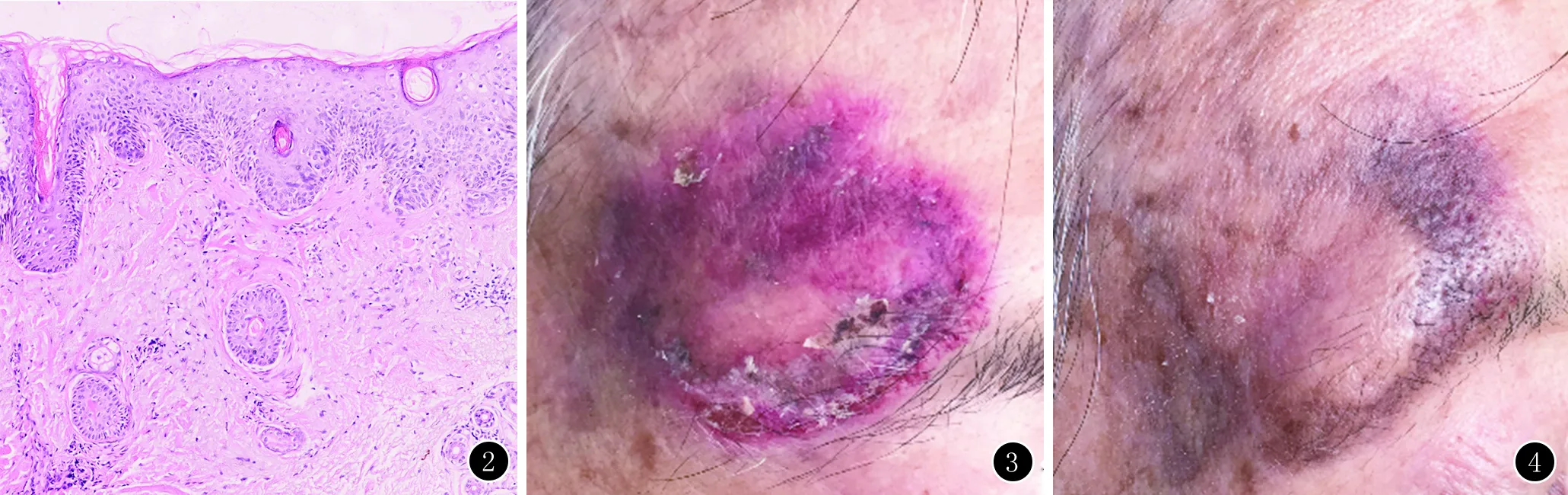
图2 表皮可见不典型角质形成细胞,表皮下层不典型细胞排列紊乱,呈芽蕾状突入真皮乳头层。真皮浅层可见日光弹力组织变性及少量淋巴细胞浸润(HE,×100)图3 治疗1个月后皮损中央可见组织愈合、黏着性痂屑明显减少图4 治疗3个月后仅见红褐色斑片及轻度色素沉着
日光性角化症的治疗方法分为两类:皮损单一、面积较小时可行冷冻术、切除术,或二者联合;皮损的范围广泛(面积大、数目多或潜在):可给予巨大戟醇甲基丁烯酸酯(ingenol mebutate,IM)、咪喹莫特乳膏、5-FU、双氯芬酸钠等药物的外用以及光动力疗法[3]。
本例患者皮损直径大约4 cm,应采用后者。光动力疗法的效果较为肯定。适用于一般情况较差、难以耐受手术的人群,而位于颜面等特殊部位或累及范围较大时也适用[4]。患者老年女性,对于疼痛的耐受度较差,拒绝接受光动力治疗。咪喹莫特是一种合成性局部免疫调节剂,兼具抗病毒、抗肿瘤活性[5]。有实验证实咪喹莫特外用于AK皮损处,可刺激局部免疫细胞分泌细胞因子及趋化因子,诱导反应性炎细胞向皮损处聚集,随后引起病变组织凋亡[6]。美国食品药品管理局已批准用5%咪喹莫特软膏来治疗日光性角化病。咪喹莫特外用的副作用常为轻中度的局部炎症性刺激反应,包括红斑、表皮剥脱、结痂、瘢痕、糜烂溃疡等,多出现在治疗早期,并在中、末期消失[7]。有研究显示,尽管上述不适可能出现,5%咪喹莫特的有效性及满意度仍较高[8]。在一项前瞻性对照研究中,入组58例,随机分为咪喹莫特治疗组和光动力治疗组,观察两种疗法的疗程耐受度及疗效满意度,结果显示两种方案之间并无明显差异[9]。本患者接受外用5%咪喹莫特乳膏(隔日一次)的治疗方案,依从性好,治疗1个月后复诊,诉患处痒、痛较前明显缓解,红斑颜色转暗,黏着性痂屑减少。外用药物后未诉明显不适,故继续当前治疗,嘱2个月后复诊,若有不适,及时就诊。治疗3个月后疗效显著,红斑及其上的黏着性痂屑消失,创面愈合,可见边缘小片状色素沉着。患者依从性好,规律用药3个月,对诊疗效果满意度高,因此认为咪喹莫特是治疗日光性角化病较好的选择,尤其适用于无法手术和光动力治疗者。
[1] Zane C, Facchinetti E, Rossi M, et al. A randomized clinical trial of photodynamic therapy with methyl aminolaevulinate vs. diclofenac 3% plus hyaluronic acid gel for the treatment of multiple actinic keratoses of the face and scalp[J]. Br J Dermatol,2014,170(5):1143-1150.
[2] Criscione V, Weinstock M, Naylor M, et al. Actinic keratoses:Natural history and risk of malignant transformation in the veterans affairs topical ttetinoin chemoprevention trial[J]. Cancer,2009,115(11):2523-2530.
[3] Ceilley R, Jorizzo J. Current issues in the management of actinic keratosis[J]. J Am Acad Dermatol,2013,68(1):28-38.
[4] 胡瑜霞,陈绍华,雷东云,等.光动力疗法治疗71例光线性角化病疗效观察[J].中国美容医学,2016,25(5):66-68.
[5] Urosevic M, Maier T, Benninghoff B, et al. Mechanisms underlying imiquimod-induced regression of basal cell carcinoma in vivo[J]. Arch Dermatol,2003,139(10):1325-1332.
[6] Torres A, Storey L, Anders M, et al. Immune-mediated changes in actinic keratosis following topical treatment with imiquimod 5% cream[J]. J Transl Med,2007,5:7.
[7] Kopera D, Kerl H. Visualization and treatment of subclinical actinic keratoses with topical imiquimod 5% cream: an observational study[J]. Biomed Res In,2014,2014:135916.
[8] Jubert-Esteve E, Del Pozo-Hernando LJ, Izquierdo-Herce N, et al. Quality of life and side effects in patients with actinic keratosis treated with ingenol mebutate: A pilot study[J]. Actas Dermo-Sifiliográficas,2015,106(8):644-650.
[9] Serra-Guillen C, Nagore E, Hueso L, et al. A randomized comparative study of tolerance and satisfaction in the treatment of actinic keratosis of the face and scalp between 5% imiquimod cream and photodynamic therapy with methyl aminolaevulinate[J]. Br J Dermatol,2011,164(2):429-433.
(收稿:2017-06-09 修回:2017-07-12)
北京大学第三临床医学院,北京,100091
