自然粒度酸化紫色土磷形态分级及其流失解析度评价
2017-11-24张洋雷平谢德体倪九派
张洋,雷平,2,谢德体,倪九派*
(1.西南大学资源环境学院,重庆 400716;2.绵阳师范学院,四川 绵阳 621000)
自然粒度酸化紫色土磷形态分级及其流失解析度评价
张洋1,雷平1,2,谢德体1,倪九派1*
(1.西南大学资源环境学院,重庆 400716;2.绵阳师范学院,四川 绵阳 621000)
土壤磷分级方法可用于土壤磷赋存形态转化的定量化研究及磷流失的解析度评价。为探讨施磷肥对酸化紫色土磷赋存形态及土壤磷流失解析度的影响,以酸化紫色土为研究对象,在榨菜生长区,设计3种磷肥处理(T1,不施磷肥;T2,常规施磷,60 kg P2O5/hm2;T3,磷肥增倍,120 kg P2O5/hm2),采用一种新的磷形态分级法,开展不同磷肥处理下径流小区土壤磷赋存形态及其流失的解析度评价。结果表明,新分级方法对土壤磷形态的提取率与Hedley分级法无显著性差异,但其对磷流失指数具有更好的表征;磷流失指数与施肥量呈正相关,且NH4F溶性磷和NaOH溶性磷对磷流失的解析度最强;增施磷肥(120 kg P2O5/hm2)显著提升土壤中游离态磷、树脂有效态磷、磷酸二钙型及磷酸八钙型等磷组分;不施磷肥显著降低磷酸二钙型、磷酸八钙型及铁(铝)结合态磷等磷形态。综上可知,自然粒度酸化土壤磷形态分级法具有可行性,其对面源污染磷流失定量化研究具有更好表征。同时,本研究证实土壤磷流失主要源于NH4F溶性磷和NaOH溶性磷,且施肥显著影响活性磷库和慢性磷库中磷形态的转化。
磷形态分级;自然粒度;酸化紫色土;磷流失指数;磷流失解析度
酸化土壤指接受一定数量交换性氢离子或铝离子,使自身碱性(盐基)离子淋失,导致pH降低的土壤[1],其产生过程主要受降雨、施肥及灌溉等因素影响[2]。据世界粮农组织(Food and Agriculture Organization of the United Nations, FAO)报道全球酸化土壤约占全球非冰川覆盖陆地面积的30%[3],而我国可耕地酸化土壤面积达6.58×107hm2,占全国可耕地总面积的51%[4]。随着土壤酸化的加速和肥料的大量施用,酸化土壤面积呈明显增加的趋势[5]。酸化土壤由于pH降低,使游离的铁、锰、铝离子溶入土壤溶液中,促进/抑制土壤中养分形态的转化,尤其改变土壤磷形态的吸附与解吸[6]。Andersson等[7]研究表明土壤酸化提高变性土中钙磷的浓度,降低其稳定性,但超过一定范围,其土壤酸溶性磷(主要为Ca10-P)稳定性增强。Baker等[8]也指出土壤磷形态转化对土壤酸化的响应具有阈值效应,在阈值范围内稳态磷与活性磷的比值不会随土壤pH而变化,低于/超过阈值均会降低其稳定性,增强/减弱土壤活性磷的固持。陈希等[9]通过研究丘陵红壤茶园根际磷转化对不同程度土壤酸化的响应,发现土壤酸化抑制根际磷素转化,降低磷矿化率和速效磷含量。酸化土壤磷形态转化受酸化进程影响而产生紊乱,传统的磷分级方法具有局限性,不能有效地描述酸化过程中土壤磷转化与循环,因而采用适当的磷分级方法来研究酸化土壤中磷形态转化及其对面源污染的贡献度对土壤酸化的响应具有重要意义。
紫色土是由紫色砂页岩发育形成的一种岩性土,盐基饱和度较高,土壤磷含量丰富,磷形态组分复杂,具有“有机磷含量高,有机-无机磷复合度高及磷素形态多样性高”等特点[10-11]。并且,近年来由于酸沉降和施肥量的增加,使紫色土酸化加重,磷在酸化紫色土中以不同的物理化学形式重组,呈现不同的地化特征[12]。因此,磷形态的定量研究是探讨酸化紫色土中磷生物地化功能的重要基础。传统的土壤磷分级体系主要分为土壤无机磷分级体系法[13-15]及土壤有机磷分级体系法[16]。但是合理的土壤磷素分级方法应该包括无机磷、易转化性、活性、慢性及稳定性有机磷的区分,这样才能有助于全面估计土壤中无机态磷和有机态磷间相互转化过程。目前国际上较为合理的磷素综合分级方法较少,主要为Hedley分级法[17]及在Hedley分级法基础上改进的Guppy分级法[18]。这两种方法对有机磷和无机磷都可进行有效的分级,但是对具有重要生态学意义的游离态磷(free phosphorus, FP)、离子交换态磷(ion exchangeable phosphorus, IEP)及有机-无机复合磷(闭蓄态磷和内团聚体磷)未能进行细分,不能准确表述酸化紫色土中磷转化及循环的信息。此外,这两种方法均需将土壤磨碎,而酸化紫色土颗粒大小不均,坚实性较强,在自然环境下不易破碎而使不同形态磷溶出。因此,在自然粒度下将酸化紫色土中不同形态磷分离,得出真正参与转化和循环的形态,是研究酸化紫色土中磷转化、循环的关键问题。本研究以酸化紫色土为研究对象,参照传统的磷分级方法[14,18],提出一种新的磷形态分级法,并采用径流小区试验验证分级方案的可靠性,同时运用层级结构方程分析确定土壤磷形态对磷流失的解析度,以期为酸化紫色土磷形态转化、地化循环及面源污染防控相关研究提供参考和借鉴。
1 材料与方法
1.1试验地概况
试验地位于重庆市涪陵区南沱镇龙王沟小流域(N 29°52′,E 107°29′),海拔240 m。该流域属于亚热带季风气候区,年均气温 22.1 ℃,月均最高气温 30 ℃,月均最低气温8 ℃,年均降水量1130 mm,≥10 ℃年积温5300 ℃,年日照时数1055 h,无霜期331 d,试验区土壤类型为酸化紫色土,质地为粉砂粘土,土壤pH 5.31,有机质16.23 g/kg,全氮1.08 g/kg,全磷0.45 g/kg,全钾14.52 g/kg,碱解氮103.44 mg/kg,有效磷31.09 mg/kg,速效钾97.28 mg/kg,田间持水量28.03%,砂粒含量6.66%,粉粒含量52.75%,粘粒含量40.59%。
1.2试验设计
试验于2015年10月至2016年3月进行,共设3个施肥处理,分别为T1(不施磷肥)、T2(常规施磷,即当地传统施磷量,P2O560 kg/hm2)、T3(磷肥增倍,即磷肥施用量是常规施磷量的2倍,P2O5120 kg/hm2),氮肥及钾肥施用量与当地传统施用量一致,分别为163 kg/hm2和120 kg/hm2。每个施肥处理包含4个小区,共计12个小区。每个小区修建如图1所示:坡度为12°,四周用水泥墙分隔,长20.00 m、宽5.00 m,高0.75 m;小区下设蓄水池(2.00 m×2.00 m×2.00 m)与小区相连,用于截留小区内的土壤径流水;蓄水池上面用石棉瓦盖住,防止降雨及其他因素干扰;小区中间铺设壤中流收集装置,该装置由储水瓶、渗漏盘、纱网、塑料导管及PVC管组成,其中储水瓶(10 L)埋在地下100 cm处,铺设纱网的渗漏盘(50 cm×40 cm)则以12°的倾角埋在地下60 cm处。此外,小区中布置滴灌系统,每个滴灌系统包含5条滴灌管(管间距1 m),每条滴灌管包含40个滴头(滴头间距50 cm),滴灌器(包含抽水泵、离心泵等设备)位于径流小区与蓄水池的交界处,用于施肥管理。各处理种植作物为榨菜(Brassicajunceavar.tumida,品种为“永安7号”),种植时间为2015年10月23日,等高横坡种植,种植密度为40000株/hm2,采用滴灌施肥,收获时间为2016年2月15日。

图1 试验小区(a)和壤中流收集装置(b)示意图Fig.1 Schematic diagram of the experiment plot (a) and leachate collection device (b) ①:滴灌带Drip tube;②:滴灌器 Drip irrigation emitter;③:分流器 Diverter;④:蓄水池 Reservoir;⑤:储水瓶 Store water bottle;⑥:PVC管 PVC tube;⑦:塑料导管 Plastic pipe;⑧:纱网 Gauze;⑨:渗漏盘 Leakage dish;:壤中流收集装置安装位置Installation location of the leachate collection device.
1.3样品采集
重庆市涪陵区气象局数据显示:2015年10月1日至2016年3月31日,研究区共产生降水77次,其中小雨(日降水量lt;10 mm/d)75次,中雨(日降水量10.0~24.9 mm/d)2次。在此期间,各试验小区产生的径流均汇入蓄水池,壤中流均通过壤中流收集装置进行收集。在榨菜收获后(即2016年2月16日)统一采集水样和土样。水样用1 L预先泡酸、清洗干净且烘干的聚乙烯塑料样品瓶盛放,样品采集后立即送至实验室,保存于4 ℃冰箱内,并于48 h内分析完毕;土样风干后进行磷形态分级测定。样品采集过程中,需要对地表径流和壤中流进行流失量测量,其中地表径流需要测量蓄水池中水样的高度,进而计算地表径流流失量;壤中流则采用抽水泵,通过PVC软管将储水瓶中的壤中流全部抽入直径为30 cm的聚乙烯塑料圆筒(20 L)中,并测量圆筒中水样的高度。
1.4分析方法
1.4.1紫色土磷形态分级 本研究紫色土磷形态采用新提出的自然粒度酸化紫色土磷形态分级法(以下简称“Ⅰ法”)和改进的Hedley分级法[17](以下简称“Ⅱ法”)进行分级比较。其中Ⅰ法的分级如图2所示,具体过程如下:称取去除根系及石粒等杂质后的风干土样5.0000 g,置于100 mL离心管中,加入50 mL去离子水,于20~25 ℃下振荡1 h,在4000 r/min下离心20 min,吸取上层清液10~15 mL,采用过硫酸钾氧化法[18]测定游离态总磷(free total phosphorus, F-TP),剩余上清液通过0.45 μm滤膜后,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定可溶性总磷(dissolved total phosphorus, D-TP)和可溶性无机磷(dissolved inorganic phosphorus, D-Pi),用差减法求得可溶性有机磷(dissolved inorganic phosphorus, D-Po)和游离态颗粒磷(free particulate phosphorus, F-PP),即:(D-Po)=(D-TP)-(D-Pi), (F-PP)=(F-TP)-(D-TP)。
上述残渣加入50 mL 0.1 mol/L的MgCl,于20~25 ℃下振荡1 h,在4000 r/min下离心10 min,吸取上清液10~15 mL,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定离子交换态总磷(ion exchangeable total phosphorus, IE-TP)和离子交换态无机磷(ion exchangeable inorganic phosphorus, IE-Pi),用差减法求得离子交换态有机磷(ion exchangeable inorganic phosphorus, IE-Po),即:(IE-Po)=(IE-TP)-(IE-Pi)。
将上述残渣用饱和NaCl溶液清洗两次后,加入2.00 g NaCl饱和阴离子交换树脂和50 mL去离子水于上述离心管中,20~25 ℃下连续振荡16 h,将悬浊液倾至装有0.18 mm筛的100 mL烧杯中,用少量水洗去土粒,使筛上仅保留树脂;用25 mL 0.7 mol/L NaCl溶液转移筛上树脂于50 mL烧杯中,将烧杯放在电热板上45 min,冷却后,将溶液过滤到50 mL容量瓶,并用0.7 mol/L NaCl溶液定容;吸取上述定溶液分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定树脂总磷(resin total phosphorus, Resin-TP)和树脂无机磷(resin inorganic phosphorus, Resin-Pi),用差减法求得树脂有机磷(resin organic phosphorus, Resin-Po),即:(Resin-Po)=(Resin-TP)-(Resin-Pi)。
将上述100 mL烧杯中的悬浊液转移至100 mL离心管中,在4000 r/min下离心20 min,弃去上清液,并向土壤残渣中加入50 mL 0.5 mol/L NaHCO3溶液,于20~25 ℃下振荡1 h,在4000 r/min下离心10 min,吸取上层清液,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定NaHCO3提取态总磷(NaHCO3extracted total phosphorus,NaHCO3-TP)和NaHCO3提取态无机磷(NaHCO3extracted inorganic phosphorus, Ca2-Pi),用差减法求得NaHCO3提取态有机磷(NaHCO3extracted organic phosphorus, NaHCO3-Po),即:(NaHCO3-Po)=(NaHCO3-TP)-(Ca2-Pi)。
将上述残渣用饱和NaCl溶液清洗两次后,加入50 mL 0.5 mol/L NH4OAC溶液,于20~25 ℃下振荡1 h,在4000 r/min下离心10 min,吸取上层清液,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定NH4OAC提取态总磷(NH4OAC extracted total phosphorus, NH4OAC-TP)和NH4OAC提取态无机磷(NH4OAC extracted inorganic phosphorus, Ca8-Pi),用差减法求得NH4OAC提取态有机磷(NH4OAC extracted organic phosphorus, NH4OAC-Po),即:(NH4OAC-Po)=(NH4OAC-TP)-(Ca8-Pi)。
将上述残渣用饱和NaCl溶液清洗两次后,加入50 mL 0.5 mol/L NH4F溶液,于20~25 ℃下振荡1 h,在4000 r/min下离心10 min,吸取上层清液,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定NH4F提取态总磷(NH4F extracted total phosphorus, NH4F-TP)和NH4F提取态无机磷(NH4F extracted inorganic phosphorus, Al-Pi),用差减法求得NH4F提取态有机磷(NH4F extracted organic phosphorus, NH4F-Po),即:(NH4F-Po)=(NH4F-TP)-(Al-Pi)。
将上述残渣用饱和NaCl溶液清洗两次后,加入50 mL 0.1 mol/L NaOH溶液,于20~25 ℃下振荡1 h,在4000 r/min下离心20 min,吸取上层清液,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定NaOH提取态总磷(NaOH extracted total phosphorus, NaOH-TP)和NaOH提取态无机磷(NaOH extracted inorganic phosphorus, Fe-Pi),用差减法求得NaOH提取态有机磷(NaOH extracted organic phosphorus, NaOH-Po),即:(NaOH-Po)=(NaOH-TP)-(Fe-Pi)。

图2 自然粒度酸化紫色土磷形态分级法Fig.2 Fractionation of phosphorus in acid-purple soil with natural size ①:过硫酸钾氧化法Potassium persulfate oxidation; ②:过0.45 μm的滤膜 Over 0.45 μm of the filter; ③:差减法 Difference subtraction; ④:钼锑抗比色法 Molybdenum antimony pit colorimetric method; ⑤:振荡、离心、过滤Oscillate, centrifuge and filter.
将上述残渣用饱和NaCl溶液清洗两次后,加入50 mL 0.3 mol/L Na3C6H5O7溶液,于20~25 ℃下振荡1 h,在4000 r/min下离心10 min,吸取上层清液,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定闭蓄态总磷(occluded total phosphorus, O-TP)和闭蓄态无机磷(occluded inorganic phosphorus, O-Pi),用差减法求得闭蓄态有机磷(occluded organic phosphorus, O-Po),即:(O-Po)=(O-TP)-(O-Pi)。
将上述土壤残渣用饱和NaCl溶液清洗两次后,加入20 mL 0.1 mol/L NaOH溶液放在超声波分散仪进行分散,分散后的土壤残渣加入30 mL 0.1 mol/L NaOH溶液, 于20~25 ℃下振荡1 h,在4000 r/min下离心10 min,吸取上层清液,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定团聚体内总磷(agglomerate total phosphorus, AI-TP)和团聚体内无机磷(agglomerate inorganic phosphorus, AI-Pi),用差减法求得团聚体内有机磷(agglomerate organic phosphorus, AI-Po),即:(AI-Po)=(AI-TP)-(AI-Pi)。
将上述残渣用饱和NaCl溶液清洗两次后,加入50 mL 0.5 mol/L 1/2 H2SO4溶液,于20~25 ℃下振荡1 h,在4000 r/min下离心10 min,吸取上层清液,分别采用过硫酸钾氧化法[18]和钼锑抗比色法[14]测定H2SO4总磷(H2SO4total phosphorus, H2SO4-TP)和H2SO4无机磷(H2SO4inorganic phosphorus, Ca10-Pi),用差减法求得H2SO4有机磷(H2SO4organic phosphorus, H2SO4-Po),即:(H2SO4-Po)=(H2SO4-TP)-(Ca10-Pi)。
将上述土壤残渣用饱和NaCl溶液清洗两次后,采用H2SO4/HClO4消解-钼锑抗比色法[14]测定残留态磷(Residual-P)。
此外,土壤中全磷采用H2SO4/HClO4消解-钼锑抗比色法[14]测定。
1.4.2水样中磷测定 水样中全磷(water total phosphorus, WTP)利用原液采用过硫酸钾氧化-钼锑抗比色法测定[18]、可溶性磷(water dissolved phosphorus, WDP)利用过滤液(原液经0.45 μm滤膜过滤)采用钼锑抗比色法测定[18],颗粒态磷(water particulate phosphorus, WPP)采用差减法求得,即WPP=WTP-WDP。
1.5地表径流、壤中流磷形态流失量及磷流失指数计算
试验各处理中地表径流和壤中流磷流失量分别采用以下方法求得:
W1i=(C1i×V1)/A1
(1)
W2i=(C2i×V2)/(A2×cosα)
(2)
式中:W1i和W2i分别表示地表径流和壤中流中磷形态流失量,C1i和C2i为地表径流和壤中流中各形态磷的浓度,V1和V2分别为蓄水池和聚乙烯塑料圆筒中水样的体积,A1和A2分别表示径流小区和渗漏盘的面积,α为渗漏盘倾斜角度。
Pindex=Pw/Ps
(3)
式中:Pindex为试验处理磷流失指数,Pw为径流或者壤中流中水样的全磷含量,Ps为试验处理土壤中全磷含量。
1.6试验数据处理
采用SPSS 21.0软件进行统计分析,用LSD法进行多重比较,用不同小写字母表示差异显著性(Plt;0.05),同时用Pearson简单相关系数法进行相关系数分析(Plt;0.05)。
2 结果与讨论
2.1土壤磷分级方法比较
本研究提出的分级体系是对自然粒度酸化紫色土磷形态区分新的尝试,因此有必要用实际土壤进行检验。检验的方法有两种:一种是将本研究提出的新方法(Ⅰ法)与国际通用的Hedley分级法(Ⅱ法)进行比较,以论证新方法的可行性;另一种是采用野外径流小区磷肥试验,探讨该方法对酸化紫色土磷形态分级的可行性和各级磷形态在磷素流失中的贡献度,解析酸化紫色土磷流失的形态源,进一步论证新方法的可靠性。
表1给出了不同处理下Ⅰ法和Ⅱ法的磷分级结果。与Ⅱ法相比,Ⅰ法将有效磷进一步区分为F-P、IE-P和Resin-P,且此3种形态磷含量之和与Ⅱ法提取的Resin-P无显著性差异。同时Ⅰ法将铁铝等金属结合态的磷细分为NH4OAC-P、NaHCO3-P和NaOH-P,且此3种形态磷含量之和与Ⅱ法提取的NaOH-P无显著性差异。此外Ⅰ法利用化学浸提法从Ⅱ法的AI-P中分离出了O-P,进一步细分了土壤中团聚体磷形态。综合比较Ⅰ法和Ⅱ法,可以发现Ⅰ法对Ⅱ法提取磷形态进行了更细致划分,且划分后的磷形态之和与Ⅱ法提取相关磷形态无显著性差异,说明Ⅰ法对磷形态的划分是成功的,具有可行性。
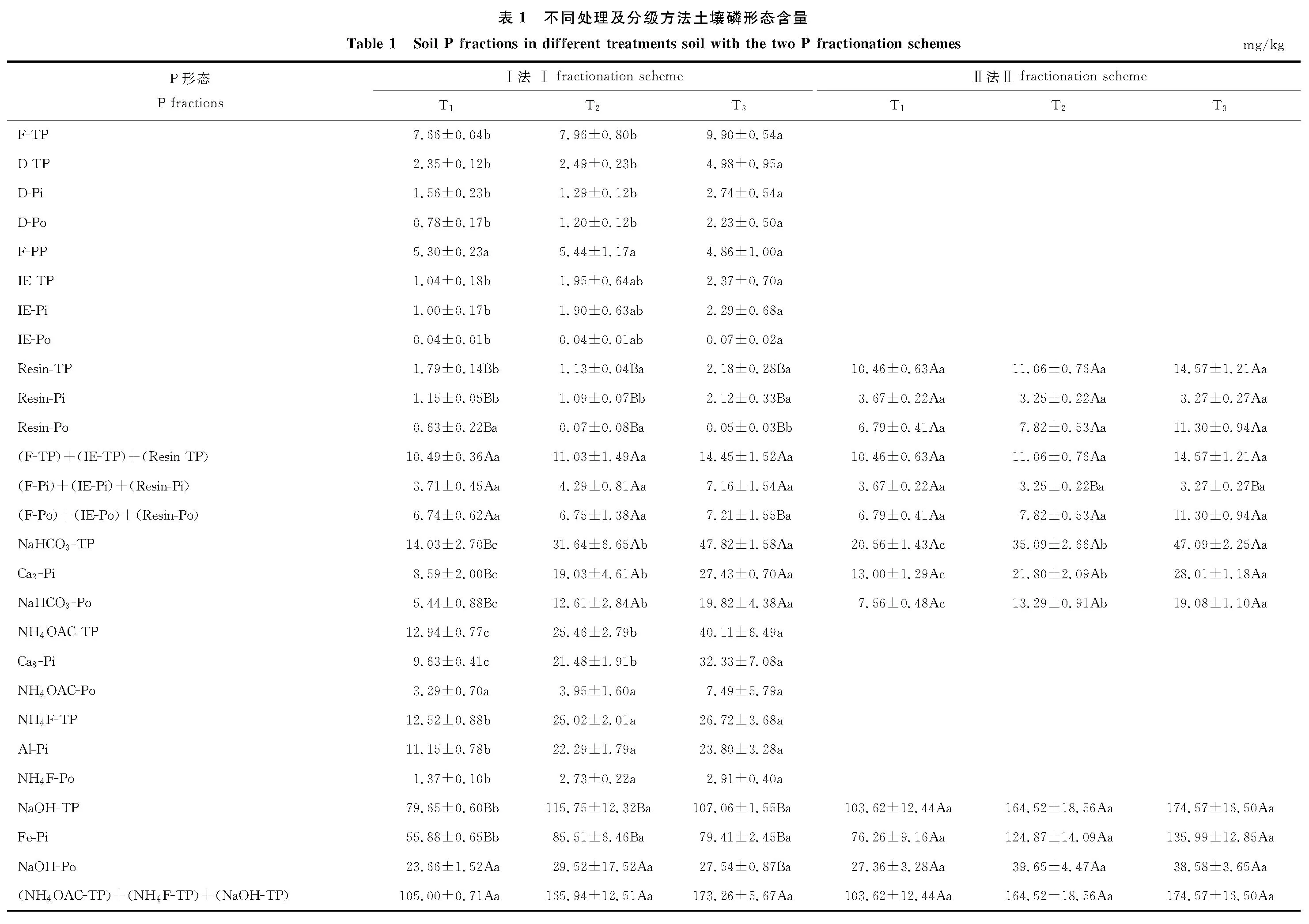
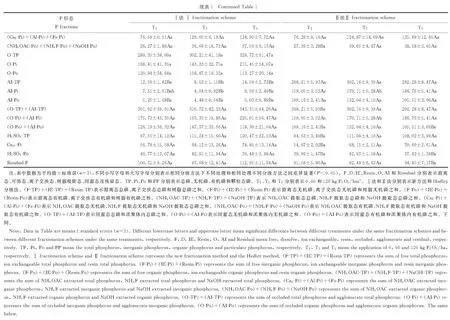
有效性磷是指能够被当季作物直接吸收利用的磷,包括速效磷和缓效磷[19]。表1表明不同施肥处理能显著影响土壤磷的有效性。增施磷肥(T3)能够显著提升土壤中D-TP、D-Pi、D-Po及F-TP等F-P及Resin-P的含量,进而增加土壤中有效磷含量。与传统施肥(T2)相比,不施磷肥(T1)不会显著降低土壤中F-P、IE-P和Resin-P含量。同时,表1可以发现磷肥处理主要影响有效性无机磷,而对有效性有机磷影响不显著。磷酸钙盐是土壤中重要的矿物态磷,在土壤缓冲体系中发挥重要作用[20],其主要分为磷酸二钙型(Ca2-P)、磷酸八钙型(Ca8-P)及磷灰石型(Ca10-P)[14]。相比传统施肥(T2),增施磷肥(T3)显著提高土壤中Ca2-P、Ca8-P,而对Ca10-P影响不显著;不施磷肥(T1)显著降低土壤中Ca2-P、Ca8-P,而对Ca10-P影响不显著,说明磷肥主要影响Ca2-P和Ca8-P的累积,而对Ca10-P影响较小,这主要因为磷肥中以Ca2-P和Ca8-P为主,施用磷肥增加了外源性Ca2-P和Ca8-P的输入,增加Ca2-P和Ca8-P的累积。磷铝石和粉红磷铁矿属于次生含磷矿物,矿物中Al和Fe彼此掺杂,固持施入土壤中磷肥形成铝结合磷酸盐(Al-P)和铁结合磷酸盐(Fe-P)[21]。表1结果显示增施磷肥(T3)对Al-P和Fe-P影响不显著,但是不施磷肥(T1)却显著降低Al-P和Fe-P含量。团聚体磷通常被胶膜包蔽,很难被植物利用,Li等[22]指出团聚体磷是土壤磷含量最多的形态,占总磷的40%~60%,但由于被胶膜包蔽,很难被植物吸收利用。Ⅰ法将团聚体磷分为O-P和AI-P,通过表1可以发现,3种处理O-P和AI-P分别占全磷45.97%,41.29%,40.44%和1.99%,1.16%,1.79%,且彼此间无显著性差异。残留态磷(Residual-P)是经物理化学方法浸提后残渣中的磷,其成分一般为土壤原生磷,不易被外界因素影响[23],表1数据也进一步证实施肥对Residual-P影响不显著。
2.2新分级方法的验证及评价
磷流失指数是磷流失量与土壤全磷量的比值,是衡量农业面源污染强度的重要指标。通过表2可以发现,磷流失指数随着施肥量的增加而提高。此外,3种施肥处理下,Ⅰ法与地表径流磷指数、壤中流磷指数及总磷流失指数均存在显著或极显著相关性,而Ⅱ法只与地表径流磷指数存在显著相关性,与壤中流磷指数和总磷流失指数相关性不显著,说明较传统的Hedley分级法(Ⅱ法),新分级方法(Ⅰ法)更能表征土壤磷流失强度,为进一步面源污染研究提供新的信息。
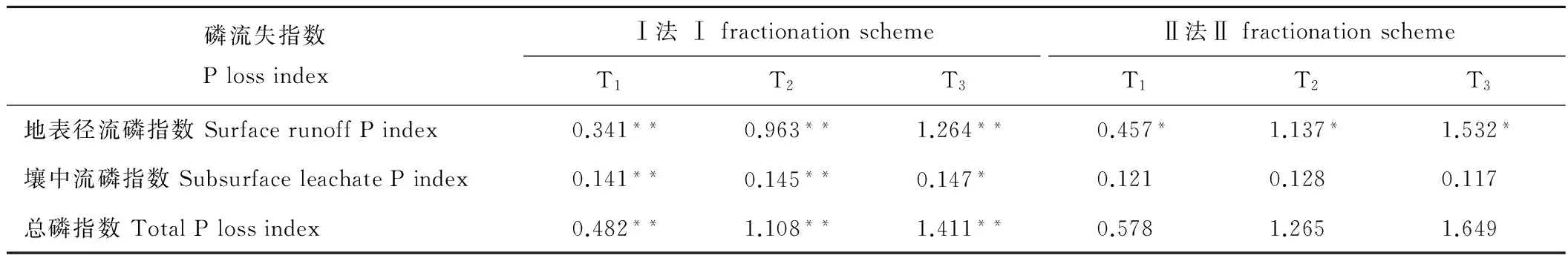
表2 不同处理下分级方法磷流失指数Table 2 P loss index in different treatments soil with the two P fractionation schemes ‰
注:*表示显著相关(Plt;0.05),**表示极显著相关(Plt;0.01)。下同。
Notes:* means significant correlation (Plt;0.05), ** means highly significant correlation (Plt;0.01). The same below.
2.3新分级体系下土壤磷形态与磷流失间的相关性分析
土壤中磷流失的途径主要包括地表径流和壤中流,为了分析磷流失与土壤磷形态间的关系,通过综合对3种处理中地表径流和壤中流中磷流失量与土壤磷形态,运用Person相关系数法进行土壤磷形态与磷流失量的相关性分析,结果表明磷流失量与土壤中F-TP、D-TP、D-Po、IE-TP、IE-Pi、IE-Po、NaHCO3-TP、Ca2-Pi、NaHCO3-Po、NH4F-TP、Al-Pi、NH4F-Po、O-TP、H2SO4-TP及Ca10-Pi等多种磷形态间具有极显著正相关性。此外,地表径流中WTP、WDP和WPP均与Resin-Po具有极显著负相关性,与Resin-Pi、NaOH-TP、Fe-Pi具有显著或极显著正相关性;壤中流中WTP、WDP、WPP与Resin-Pi、Residual-P具有显著正相关性,与Resin-Po具有显著负相关性。磷流失与土壤磷形态相关性分析比较,证明土壤磷流失是土壤中多种磷形态受降雨等外界因素干扰产生的表征集合,这与Yu等[24]研究结果一致。
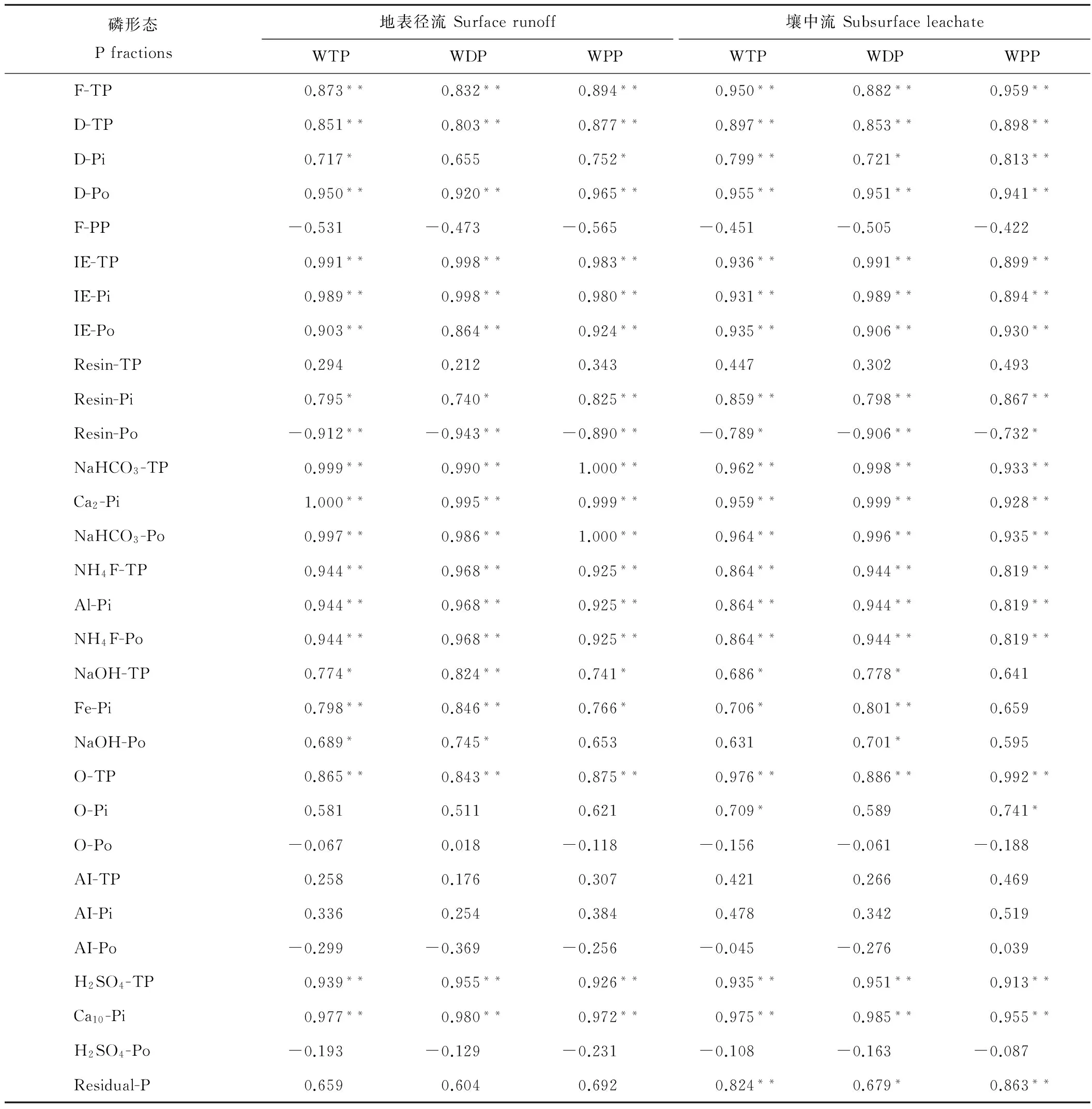
表3 新分级方法下土壤磷形态与磷流失量相关系数Table 3 The correlation coefficients between P loss and P fractions under the new P fractionation schemes
注:WTP、WDP和WPP分别表示水样中的全磷、可溶性磷及颗粒态磷。
Notes: WTP, WDP and WPP represent total phosphorus, dissolved phosphorus and particulate phosphorus in water sampling.
2.4新分级体系下土壤磷形态对磷流失的解释度分析
为了进一步比较土壤磷形态间对磷流失量的相对影响作用,确定哪一种磷形态对磷流失的解析力度更强,运用层级结构方程进行分析,具体操作步骤如下:首先将与每种处理磷流失量具有显著和极显著关系的磷形态一次性纳入结构方程中,分别对其进行结构化分析,构成若干基准模型;然后将在方程整体显著的前提下,分别将地表径流和壤中流中的WTP、WDP、WPP分层放入,然后进行逐层分析比较,最终利用结构方程模型中解析系数ζ,即R2变化的倒数(ζ=1/R2),判定土壤磷形态对磷流失的解析度,ζ越大,则解析力度越强。此外,为了简化结构方程运算,依据土壤磷活度[25],将新分级体系下的磷形态进一步综合为活性磷库(labile-P)、慢性磷库(chronic-P)、稳性磷库(stable-P)和惰性磷库(inert-P)。通过磷形态对磷流失的解析系数(图3)可以发现,地表径流对P流失量的解析力度最强,即贡献度最大,而壤中流中磷流失主要来源于颗粒态磷的贡献。此外,通过逐层对解析系数进行挖掘,可以发现对土壤磷流失解析力度最强的是NH4F-P和NaOH-P,其次是F-P和IE-P,解析力度最弱的是Residual-P,产生这种现象的原因主要与土壤中磷赋存形态的结合度和磷有效性有关,铁铝结合态磷与土壤胶体、团聚体黏合,形成颗粒态磷随径流而损失[26];F-P、IE-P及Resin-P虽然活性强,但由于有效性较高,易被作物吸收利用,在一定程度上降低了流失的风险[27];Residual-P为土壤固有“老磷”,不易对外界环境因子变化产生响应,因而对磷流失解析力度较弱[23]。

图3 新分级体系下磷形态对磷流失的解释系数(ζ)Fig.3 The interpretation coefficient of P fractions on P loss in the new fractionation system A1: D-Pi;A2:D-Po;A3:D-TP;A4:F-PP;A5:F-TP;A6:Residual-P;A7:IE-Pi;A8:IE-Po;A9:IE-TP;A10:Resin-Pi;A11:Resin-Po;A12:Resin-TP;A13:Ca2-Pi;A14:NaHCO3-Po;A15:NaHCO3-TP;A16:Al-Pi;A17:NH4F-Po;A18:NH4F-TP;A19:Fe-Pi;A20:NaOH-Po;A21:NaOH-TP;A22:O-Pi;A23:O-Po;A24:O-TP;A25:AI-Pi;A26:AI-Po;A27:AI-TP;A28:Ca10-Pi;A29:H2SO4-Po;A30:H2SO4-TP;A31:Labile-P;A32:Chronic-P;A33:Stable-P;A34:Inert-P;A35:地表径流中WDP WDP in Surface runoff;A36:地表径流中WPP WPP in surface runoff; A37:地表径流中WTP WTP in surface runoff;A38:壤中流中WDP WDP in subsurface leachate;A39:壤中流中WPP WPP in subsurface leachate;A40:壤中流中WTP WTP in subsurface leachate;A41:总P流失量Total phosphorus loss.
3 结论
与国际通用Hedley分级法一样,自然粒度酸化土壤磷形态分级法对土壤磷的提取率相对稳定,重现性好,具有可行性,并且其对面源污染磷定量化研究具有更好表征。新分级方法对土壤磷赋存形态的定量化区分及磷流失的相关性分析和结构化解析,证明土壤磷流失是土壤多种磷赋存形态的贡献集合,其流失主要源于NH4F-P和NaOH-P。此外,增施磷肥显著提升土壤有效磷、Ca2-P和Ca8-P含量,而不施磷肥显著降低Ca2-P、Ca8-P、Al-P及Fe-P含量,说明施肥显著影响活性磷库和慢性磷库中磷形态的转化,而对稳性磷库和惰性磷库中磷形态转化影响不显著。
References:
[1] Breemen N V, Driscoll C T, Mulder J. Acidic deposition and internal proton sources in acidification of soils and waters. Nature, 1984, 17(1): 241-249.
[2] Breemen N V, Verstraten J M. Soil acidification/N cycling. Studies in Environmental Science, 1991, 46: 289, 291-352.
[3] Blake L, Johnston A E, Goulding K W T. Mobilization of aluminium in soil by acid deposition and its uptake by grass cut for hay-a chemical time bomb. Soil Use and Management, 1994, 10(2): 51-55.
[4] Guo J H, Liu X J, Zhang Y,etal. Significant acidification in major Chinese croplands. Science, 2010, 327: 1008.
[5] Meng H Q, Liu J, Xu M G,etal. Evolution of pH in topsoils of typical Chinese croplands under long-term fertilization. Acta Pedologica Sinica, 2013, 50(6): 1109-1116.
孟红旗, 刘景, 徐明岗, 等. 长期施肥下我国典型农田耕层土壤的pH演变. 土壤学报, 2013, 50(6): 1109-1116.
[6] Andersson K O, Tighe M K, Guppy C N,etal. Incremental acidification reveals phosphorus release dynamics in alkaline vertic soils. Geoderma, 2015, 259: 35-44.
[7] Andersson K O, Tighe M K, Guppy C N,etal. The release of phosphorus in alkaline vertic soils as influenced by pH and by anion and cation sinks. Geoderma, 2016, 264: 17-27.
[8] Baker S R, Watmough S A, Eimers M C. Phosphorus forms and response to changes in pH in acid-sensitive soils on the Precambrian Shield. Canadian Journal of Soil Science, 2015, 95(2): 95-108.
[9] Chen X, Chen F S, Ye S Q,etal. Responses of rhizosphere nitrogen and phosphorus transformations to different acid rain intensities in a hilly red soil tea plantation. Chinese Journal of Applied Ecology, 2015, 26(1): 1-8.
陈希, 陈伏生, 叶素琼, 等. 丘陵红壤茶园根际氮磷转化对不同强度酸雨胁迫的响应. 应用生态学报, 2015, 26(1): 1-8.
[10] He Y R. The Purple Soil in China[M]. Beijing: The Science Publishing Company, 2003.
何毓蓉. 中国紫色土[M]. 北京: 中国科学出版社, 2003.
[11] Zhang F R. Soil Geography[M]. Beijing: China Agriculture Press, 2002.
张风荣. 土壤地理学[M]. 北京: 中国农业出版社, 2002.
[12] Zhang H, Yang Y K, Xie D T,etal. Effect of acid rain on leaching loss of nitrogen and phosphorus. Journal of Soil and Water Conservation, 2007, 21(1): 22-25.
张华, 杨永奎, 谢德体, 等. 酸雨对紫色土氮磷淋失的影响. 水土保持学报, 2007, 21(1): 22-25.
[13] Webber M D, Mattingly G E G. Inorganic soil phosphorus. European Journal of Soil Science, 2006, 21(1): 111-120.
[14] Gu Y C, Jiang B F. Standard test method for classification of inorganic phosphorus in calcareous soils. Soil, 1990, 22(2): 101-102.
顾益初, 蒋柏藩. 石灰性土壤无机磷分级的测定方法. 土壤, 1990, 22(2): 101-102.
[15] Jiang B F, Gu Y C. A suggested fractionation scheme of inorganic phosphorus in calcareous soils. Scientia Agricultura Sinica, 1989, 22(3): 58-66.
蒋柏藩, 顾益初. 石灰性土壤无机磷分级体系的研究. 中国农业科学, 1989, 22(3): 58-66.
[16] Bowman R A, Cole C V. An exploratory method for fractionation of organic phosphorus from grassland soils. Soil Science, 1978, 125(2): 95-101.
[17] Cross A F, Schlesinger W H. A literature review and evaluation of the Hedley fractionation: Applications to the biogeochemical cycle of soil phosphorus in natural ecosystems. Geoderma, 1995, 64(3/4): 197-214.
[18] Guppy C N, Menzies N W, Moody P W,etal. A simplified, sequential, phosphorus fractionation method. Communications in Soil Science and Plant Analysis, 2000, 31(11): 1981-1991.
[19] Batten G D. A review of phosphorus efficiency in wheat. Plant and Soil, 1992, 146(1/2): 163-168.
[20] Zhang L, Wu N, Wu Y,etal. Soil phosphorus form and fractionation scheme: A review. Chinese Journal of Applied Ecology, 2009, 20(7): 1775-1782.
张林, 吴宁, 吴彦, 等. 土壤磷素形态及其分级方法研究进展. 应用生态学报, 2009, 20(7): 1775-1782.
[21] Padhi K K. Observation of x-ray interferences on apatite and secondary phosphate minerals in Sukulu phosphatic soil, Uganda. National Metallurgical Laboratory Technical Journal, 1998, 40(2): 63-68.
[22] Li B Z, Ge T D, Xiao H A,etal. Phosphorus content as a function of soil aggregate size and paddy cultivation in highly weathered soils. Environmental Science and Pollution Research, 2016, 23(8): 7494-7503.
[23] Yerokun O A. Chemical characteristics of phosphorus in some representative benchmark soils of Zambia. Geoderma, 2008, 147(1/2): 63-68.
[24] Yu S, He Z L, Stoffella P J,etal. Surface runoff phosphorus (P) loss in relation to phosphatase activity and soil P fractions in Florida sandy soils under citrus production. Soil Biology amp; Biochemistry, 2006, 38(3): 619-628.
[25] Nziguheba G, Palm C A, Buresh R J,etal. Soil phosphorus fractions and adsorption as affected by organic and inorganic sources. Plant and Soil, 1998, 198(2): 159-168.
[26] Otani T, Ae N. The exudation of organic acids by pigeonpea roots for solubilizing iron- and aluminum-bound phosphorus. Plant Nutrition for Sustainable Food Production and Environment, 1997, 78(1): 325-326.
[27] Young E O, Ross D S. Total and labile phosphorus concentrations as influenced by riparian buffer soil properties. Journal of Environmental Quality, 2016, 45(1): 294.
Phosphorusfractionationandlossesinanacidifiedpurplesoil
ZHANG Yang1, LEI Ping1,2, XIE De-Ti1, NI Jiu-Pai1*
1.College of Resources and Environment, Southwestern University, Chongqing 400716, China; 2.Mianyang Normal College, Mianyang 621000, China
Phosphorus (P) fractionation was developed to quantitatively analyze P fraction transformation and P loss apportionment. In order to investigate the effect of P fertilization on P fractions and apportionment of P loss forms, a plot experiment with three P levels (0, 60 and 120 kg P2O5/ha) was conducted in a mustard crop grown on an acidified purple soil. Phosphorus fractions and P loss apportionment were analyzed using a new P fractionation method which is much less variable than the Hedley fractionation method and better at characterizing the P loss index. The P loss index was positively correlated with P fertilization and the main P loss source was soluble P in NH4F and NaOH. Increasing P fertilization significantly increased the free P, resin available P, Ca2-P and Ca8-P, while zero P application significantly decreased the Ca2-P, Ca8-P and iron or aluminum bound P. In conclusion, the new P fractionation method was a viable and better method for characterizing the quantitative assessment of P loss in non-point source pollution. The study also showed that soil P loss was mainly of soluble P and that P fertilization greatly influenced the transformation of P fractions in a labile and chronic phosphorus pool.
phosphorus fractionation; natural grain size; acidified purple soils; phosphorus loss index; phosphorus loss apportionment
10.11686/cyxb2017069http//cyxb.lzu.edu.cn
张洋, 雷平, 谢德体, 倪九派. 自然粒度酸化紫色土磷形态分级及其流失解析度评价. 草业学报, 2017, 26(11): 22-34.
ZHANG Yang, LEI Ping, XIE De-Ti, NI Jiu-Pai. Phosphorus fractionation and losses in an acidified purple soil. Acta Prataculturae Sinica, 2017, 26(11): 22-34.
2017-03-01;改回日期:2017-05-05
国家自然科学基金项目(41671291),中央高校基本科研业务费项目(XDJ2016E161)和重庆市研究生科研创新项目(CYB2015054)资助。
张洋(1988-),男,山东枣庄人,在读博士。E-mail:zhy2198@163.com
*通信作者Corresponding author. E-mail: nijiupai@163.com
