气肿疽延边株FliA基因真核表达载体的构建
2017-11-17张永佳李成辉
张永佳, 张 皓, 李成辉, 金 鑫
(延边大学农学院,吉林 延吉 133002)
气肿疽延边株FliA基因真核表达载体的构建
张永佳, 张 皓, 李成辉, 金 鑫*
(延边大学农学院,吉林 延吉 133002)
为构建气肿疽延边株FliA基因的真核表达载体PVAX1-FliA,根据Genbank气肿疽鞭毛基因(登录号:AB058932)的参考序列,利用Primer 5.0设计1对引物,通过PCR扩增出完整的气肿疽延边株FliA基因。将目的基因与pMD-19T载体连接转化到大肠杆菌DH5α,进行测序、PCR、双酶切鉴定阳性克隆质粒。用回收后的基因与真核表达载体PVAX-1连接,并经双酶切、测序鉴定。本试验成功构建了鞭毛基因的重组真核表达载体PVAX1-FliA,为探讨气肿疽延边株FliA基因的分子生物学特性和功能及免疫新途径提供依据。
气肿疽延边株;FliA基因;真核表达载体;构建
气肿疽梭菌(Clostridiumchauvoei)是专性厌氧菌,属细菌纲,芽孢杆菌科,梭菌属,为反刍动物细菌性传染病黑腿病的病原菌[1]。病料及幼龄培养菌革兰氏染色一般为阳性,老龄培养菌呈阴性。主要感染途径为消化道和外伤感染,病畜往往在治疗前就会死亡[2]。牛是该病的主要易感动物,感染症状为肌肉丰满部位,如股部、臀部、腰部、肩部、颈部及胸部等,发生气性水肿,呈暗红棕色到黑色,按压有捻发音,剖检局部呈黑色,肌肉干燥呈海绵状,病变肌肉与正常肌肉相间,局部骨骼肌、皮下和肌间结缔组织发生出血或坏死性炎症,并产生气体。病原菌可以芽胞形式存活于土壤中数十年,所以不易消灭[3]。气肿疽梭菌曾被认为只感染牲畜,却于2007年开始,在美国和日本出现人感染死亡的报道,这使得该病迅速成为诸多国家工作人员共同关注的焦点和研究热点[4]。
吉林省延边朝鲜族自治州敦化市、延吉市依兰镇、三道镇在2006年相继发生牛气肿疽,而延边地区一直是延边黄牛饲养比较多的地区,一旦爆发感染气肿疽,将会对延边地区乃至全国畜牧业的发展造成很大的损失[5]。延边地处长白山地区,山地面积占全州总面积的54.8%,潮湿的山谷牧场、天气炎热的多雨季节,都是气肿疽病多发的环境,所以在放牧条件下的牛很容易感染气肿疽[6]。因此,对延边地区本地流行病株的研究有重要价值。
气肿疽梭菌鞭毛的生长状态为周生,主要成分为蛋白质,由鞭毛蛋白(flagella)的亚单位组成,作为该病的重要抗原称为鞭毛抗原或H抗原,Mayumi等在1994年发表的论文结果显示,鞭毛抗原最少含有3个抗原决定簇,FliA全长1 239bp,共编码413个氨基酸。经三级结构分析得知,羧基端活性区域在第960~1 188 bp;胺基端活性区域在第81~486 bp[7-10]。
1 材料与方法
1.1材料
气肿疽延边株,由延边大学农学院预防兽医学实验室完成分离并保存;DL 2 000 DNA Marker购自Newbio industry公司;Ex Taq DNA聚合酶、pMD19-T Simple 载体、DNA纯化回收试剂盒、质粒小量提取试剂盒等均购自大连宝生物工程有限公司;其他试剂为国产分析纯。
1.2方法
1.2.1 FliA基因引物的设计与合成
应用Premier5.0软件,根据气肿疽FliA基因
序列(登录号:AB058932),设计1对特异性引物,预期的扩增全长为1 267 bp。上游引物5' 端加入BamHⅠ酶切位点(下划线部分),下游引物5' 端加入XhoⅠ酶切位点(下划线部分),由上海生工生物工程有限公司合成。
上游引物P1:5′-3′:CGGGATCCACCATGGCCATGATTATCAATCACAATATG;
下游引物P2:5′-3′:CCCTCGAGTTATCTTAATAATTGAAGAACA。
1.2.2 FliA基因的扩增与克隆
用细菌DNA抽提试剂盒对气肿疽延边株菌体DNA进行抽提。以气肿疽延边株DNA为模板进行FliA基因PCR扩增,PCR反应在50 μL体系中进行:95 ℃、5 min,95 ℃、30 s,52 ℃、30 s,72 ℃、2 min,35个循环;72 ℃、10 min。将PCR产物纯化后与pMD 19-T Simple连接,经过PCR鉴定和酶切鉴定后将正确的阳性克隆质粒送往上海生工生物技术有限公司测序。
1.2.3 重组表达载体
PVAX1-FliA的构建分别用BamHⅠ、XhoⅠ对pMD-19-T-FliA和PVAX1进行双酶切,在37 ℃环境中酶切4 h。酶切后进行1%琼脂糖凝胶电泳检测片段大小是否符合预期。用凝胶纯化回收试剂盒进行目的基因的回收。回收后用T4连接酶进行目的片段和真核表达载体的连接。将过夜连接液转入大肠杆菌DH 5α感受态细胞(100~200 μL)中,在不含Kan的LB液体培养基中震荡培养45 min,后涂布在含100 mg/L硫酸卡那霉素的LB平板上,过夜培养。经小量提取的质粒用BamHⅠ、XhoⅠ进行双酶切,将鉴定阳性的质粒送上海生工生物有限公司测定序列,质粒命名为PVAX1-FliA。
2 结果与分析
2.1FliA基因扩增
以气肿疽延边株的基因组为模板,P1、P2为引物,扩增出片段为1 267 bp的特异性产物,与预期目的条带相符(图1)。
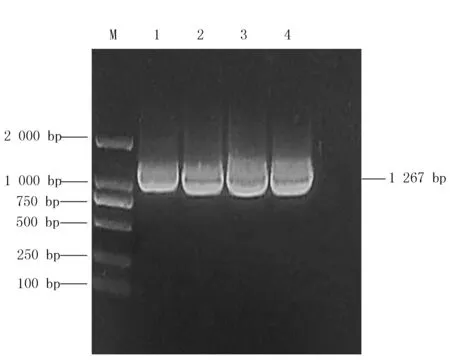
M:DL 2 000 DNA Marker;1~4:FliA基因的PCR扩增产物;5:水对照
2.2重组质粒的PCR及酶切鉴定
重组后的pMD 19-T-FliA质粒经PCR鉴定,电泳发现在1 kb左右的单一目的条带与目的基因大小一致(图2)。PCR初步鉴定阳性,用BamHⅠ、XhoⅠ进行双酶切,质粒切出2 692 bp和1 267 bp 的2条目的条带,酶切产物大小与预期相符(图3)。

M:DL 2 000 DNA Marker;1:pMD 19-T-FliA PCR鉴定产物
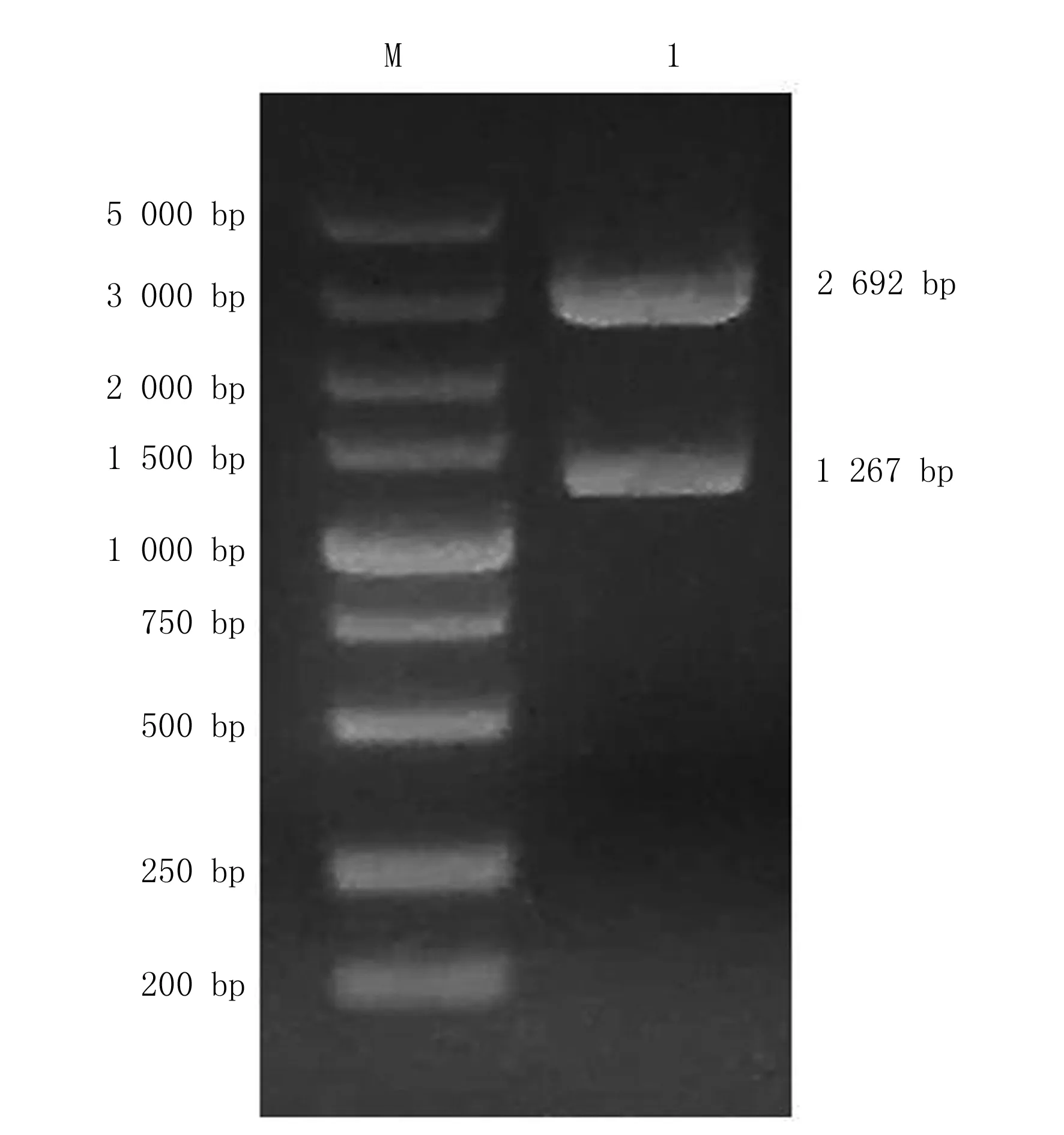
M:DL 5 000 DNA Marker;1:pMD 19-T-FliA 双酶切鉴定产物
2.3重组质粒的测序
将PCR及酶切鉴定呈阳性的质粒送上海生工生物有限公司测序,测序结果与预期相符,获得了阳性克隆质粒。
2.4重组表达载体的酶切鉴定
重组表达载体PVAX1-FliA用BamHⅠ、XhoⅠ限制性内切酶酶切结果显示,有1 267 bp和2 999 bp 2条带,与预期产物片段大小相符合,初步说明载体构建成功(图4)。

M:DL 5 000 DNA Marker;1:PVAX1-FliA 双酶切鉴定产物
2.5重组表达载体的测序
将酶切鉴定为阳性的表达载体送往上海生工有限公司进行测序,测序结果表明,成功获得阳性重组表达质粒PVAX1-FliA。测序结果与GenBank中的气肿疽梭菌ATCC 10092株中FliA基因序列进行同源性分析,一致性达97%(图5)。表明气肿疽延边株鞭毛蛋白基因真核表达载体PVAX1-FliA构建成功。


图5 FliA基因核苷酸同源性比对
3 讨论与结论
鞭毛是负责大多数细菌物种运动的细胞器。一个细菌鞭毛的基本结构可分为3部分:基体、吊钩和鞭毛丝。鞭毛丝由鞭毛蛋白重复亚基组成的。Yoshimasa Sasaki等人在气肿疽梭菌的染色体中发现至少有2个拷贝的FliA基因,发现C.chauvoeiFliA基因的上游和下游的序列(序列登录号d89073)是相同的,C.chauvoei染色体上可能存在FliA基因串联拷贝,其他梭菌属梭菌16S rDNA系统发育集群,如溶血梭菌,诺维梭菌,腐败梭菌也可能隐藏着FliA基因串联拷贝[11-13]。
唾液酸酶、鞭毛蛋白和细胞毒素是主要的气肿疽梭菌抗原。唾液酸酶(NanA),也被称为神经氨酸酶,它的分子质量大小约为81 kD,能够编码氨基酸722个,属于分子质量为50~80 kD的多肽[14-15]。此酶在细菌、真菌、病毒、原生和后生动物被发现,可以通过裂解唾液酸过程中被发现,它的活化能最低值为13.40 kJ/mol,其中,体内剩余物质在40 ℃温度下最容易被唾液酸酶裂解,该酶可作为防治黑腿病感染和反刍动物抵制病原体入侵的候选基因。鞭毛蛋白属于非常重要的保护性抗原之一,也是引起气肿疽发生和生物体感染的最重要的毒力因子之一,其分子质量为46 kD,含有多量的苏氨酸、天冬氨酸和谷氨酸,缺乏色氨酸和半胱氨酸[16-17]。气肿疽细胞毒素A是由Joachim Frey等人经全基因序列分析而得出的蛋白质毒素,其中,分子质量为33 ku的细胞毒素A蛋白都可以从气肿疽菌株分泌而来,并且只在气肿疽菌株中存在[18-19]。
本试验选用最具有代表性的抗原基因成功建立了PVAX1-FliA真核重组表达载体,为后续的真核表达及免疫原性分析奠定基础,以本地分离株作为研究对象,对延边州当地气肿疽预防工作有一定意义,为分子生物学水平上的进一步研究提供条件。
[1] 陆承平.兽医微生物学[M].北京:中国农业出版社,2007:197-198.
[2] 丁宜宝.兽用疫苗学[M].北京:中国农业出版社,2008:468-470.
[3] 陈溥言.兽医传染病学[M].北京:中国农业出版社,2006:302-304.
[4] 陈发喜,蔡扩军,范玉娟,等.家畜气肿疽的研究进展[J].草食家畜,2015(3):6-10.
[5] 张皓,田金华,金鑫,等.气肿疽梭菌鞭毛基因克隆载体的构建[J].延边大学农学学报,2015,37(2):91-95.
[6] 朱月,袁树先,于洪艳.牛肝菌水溶性多糖提取的正交试验[J].赤峰学院学报(自然科学版),2008(10):22-24.
[7] Tamura Y,Kijima M,Ohishi K,et al.Antigenic analysis of Clostridium chauvoei flagella with protective and non-protective monoclonal antibodies[J].J Gen Micro-bio,1992,138:537-542.
[8] 邢明勋,李连峰,贾生美.牛前胃疾病的诊疗[J].赤峰学院学报(自然科学版),2009(06):62-63.
[9] 张雪寒,何孔旺,赵攀登,等.肠出血性大肠杆菌O157∶H7鞭毛可变区基因片段的克隆、表达与免疫原性[J].江苏农业学报,2011,27(5):1021-1025.
[10] Zdobnov E M,Apweiler R.An integration platformfor the signature-recognition methods[J].Inter Pro Bioinformatics,2001,17:847-848.
[11] Arnold K,Bordoli L,Kopp J,et al.The SWISS-MODEL Work-space:A wed-based environment for protein structure homology modelling[J].Bioin formatics,2006,22:195-201.
[12] Chandler H M,Gulasekharam J.The protective antigen of a highly immuno genic strain of clostridium chauvoei including an evaluation of its flagella as a protective antigen[J].Journal of General Microbiology,1974,84(1):128-134.
[13] Tamura Y,Kijima-Tanaka M,Aoki A,et al.Reversible expres-sion of motility and flagella in Clostridium chauvoei and their relationship to virulence[J].Microbiology,1995,141(3):605-610.
[14] 周金玲,吴丹丹,周玉龙,等.气肿疽梭菌HLJ-1株分离鉴定及系统进化分析[J].黑龙江八一农垦大学学报,2016(6):83-88.
[15] 云巾宴,任春宇,车达,等.气肿疽梭菌PCR检测方法的建立[J].江苏农业科学,2015,43(10):53-55.
[16] 李香春,金鑫,朴春宇,等.利用SOE-PCR与TD-PCR技术对气肿疽梭菌FliA(C)-NanA融合基因扩增方法的构建[J].安徽农业科学,2013(24):9921-9923.
[17] 王志慧,徐剑华,李鹏.籽鹅FSH真核表达载体的构建及表达[J].黑龙江八一农垦大学学报,2015(04):39-41.
[18] 李晓婷,宋佰芬,崔玉东.鸡白介素18与鸡γ干扰素基因融合表达载体构建[J].黑龙江八一农垦大学学报,2017(01):49-53.
[19] 宋佰芬,李迎春,邹珊,等.牛干扰素-γ基因的克隆与真核表达载体的构建[J]. 黑龙江八一农垦大学学报,2010(01):53-57.
ConstructionofeukaryoticexpressionvectorsoftheFliAgenefromClostridiumChauvoeiofYanbianStrain
ZHANG Youjia, ZHANG Hao, LI Chenghui, JIN Xin*
(AgriculturalCollegeofYanbianUniversity,YanjiJilin133002,China)
In order to construct the eukaryotic expression vector PVAX1-FliA, the complete FliA gene fromC.Chauvoeiof Yanbian Strain were amplified by PCR. A pair of primers designed by Primer 5.0 according to reference sequence standards (the accession number:AB058932) ofC.Chaucoeiflagella. The purpose gene was connected with pMD19-T vector, and then transformed intoE.coliDH5α. The positive clones were confirmed by sequencing, PCR and restriction enzyme digestion. The FliA gene was connected with PVAX1 vector, and then the recombination plasma DNA was identified by restriction enzyme digestion and sequencing. The PVAX1-FliA recombinant eukaryotic expression vector was constructed in this study. The reseach can provide evidence for features, functions of molecular biology and new ways of immunization for the study the FliA gene fromC.Chauvoeiof Yanbian Strain.
ClostridiumChauvoeiof Yanbian Strain;flagellin gene;eukaryotic expression vector;construction
2017-03-02
吉林省教育厅资助项目(吉教科合字[2014]第6号)
张永佳(1992—),女,吉林延吉人,在读硕士,研究方向为动物传染病学。金鑫为通信作者,
E-mail:jinxin@ybu.edu.cn
1004-7999(2017)03-0050-05
10.13478/j.cnki.jasyu.2017.03.009
S858
A
