对-三联苯化合物的合成与光谱性能的研究
2017-11-08余文浩王延铭刘金彦郭志刚李松波
冀 虹, 余文浩, 王延铭, 刘金彦, 郭志刚, 李松波*
(1. 内蒙古科技大学 化学与化工学院, 内蒙古 包头 014010; 2. 四川师范大学 化学与材料科学学院, 四川 成都 610066)
对-三联苯化合物的合成与光谱性能的研究
冀 虹1, 余文浩2, 王延铭1, 刘金彦1, 郭志刚1, 李松波1*
(1. 内蒙古科技大学 化学与化工学院, 内蒙古 包头 014010; 2. 四川师范大学 化学与材料科学学院, 四川 成都 610066)
通过以PdCl2-EDTA为催化剂的Suzuki偶联反应,成功合成具有不同取代基及对称性的对-三联苯化合物,利用核磁共振氢谱(1H NMR)和红外光谱(IR)对目标化合物的结构进行表征,利用熔点仪、差示扫描量热仪(DSC)、热重分析仪(TGA)、紫外光谱(UV)和荧光光谱(PL)对目标化合物的光谱性能进行研究.结果表明,对-三联苯化合物具有良好的热稳定性.在对-三联苯上引入—OMe、—COOMe和—CHO基团后,会使对-三联苯的最大吸收峰波长和最大发射峰波长向长波方向移动,对-三联苯化合物结构的对称性对紫外吸收峰有影响,对荧光发射峰无影响.
对-三联苯; Suzuki偶联反应; 紫外吸收; 荧光发射
对-三联苯化合物具有3个苯环相连的较大共轭体系线性刚性结构,其在紫外光的照射下能产生荧光[1],广泛应用于有机闪烁剂、激光染料、聚合物蓝光材料等方面[2-4].对-三联苯化合物还具有良好的光、化学稳定性,各向异性、黏度与双折射等物理常数可调等优点,是一类良好的液晶材料,被大量应用于液晶终端显示器件(LCD)和制备发光二极管(LED)中[5-11],因此对-三联苯化合物得到研究者的广泛关注[12-14].
为进一步研究分子结构对对-三联苯化合物紫外吸收和荧光发射性能的影响,在对-三联苯上分别引入—OMe、—COOMe和—CHO基团.通过紫外吸收和荧光发射性能表征,来讨论不同取代基及分子对称性,对化合物光谱性能的影响,同时在对-三联苯上引入—OMe、—COOMe和—CHO基团所得到的对-三联苯化合物,是合成液晶及聚合物蓝光材料的重要中间体,为进一步合成具有良好性能的三联苯液晶及聚合物蓝光材料奠定了基础.
本文改变以往Suzuki偶联反应常用的[Pd(PPh3)4]催化剂[15],利用原料价格低、制备简单且易保存的催化剂PdCl2-EDTA[16],将1,4-二溴苯或4-溴联苯分别与具有不同取代基的苯硼酸衍生物发生Suzuki偶联反应,合成了9个不同取代基及对称性的对-三联苯化合物,合成路线如图1所示.
1 实验
1.1仪器和试剂
1.1.1仪器 核磁共振氢谱使用美国Bruker公司生产的AvanceⅢ-500核磁共振仪测定(CDCl3为溶剂,Me4Si作内标),红外光谱使用美国PE公司生产的RX-1型红外光谱仪测定(KBr压片),目标化合物的熔点(除a-3、4、5外)使用南京桑力电子设备厂生产的SLRD-I型数字熔点测定仪测得,目标化合物a-3、4、5的熔点使用美国TA公司生产的TA-DSC Discover分析仪测得,目标化合物的热重使用美国TA公司生产的TA-TGA Discover分析仪测得,紫外光谱使用澳大利亚GBC公司生产的Cintra 1010型紫外-可见分光光度计测得,荧光光谱用日本日立公司生产的F-2500型荧光分光光度计测得.
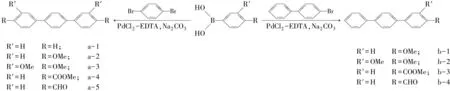
图1对-三联苯化合物的合成路线
Fig.1Synthesisrouteofp-terphenylcompounds
1.1.2试剂 1,4-二溴苯购于武汉长成化成科技发展有限公司. 4-溴联苯购于上海晶纯生化科技股份有限公司.苯硼酸、4-甲氧基苯硼酸、3,4-二甲氧基苯硼酸、4-甲氧羰基苯硼酸、4-甲酰基苯硼酸购于苏州苏凯路化学科技有限公司.氯化钯购于中国国药集团化学试剂有限公司.乙二胺四乙酸二钠(EDTA二钠盐)购于天津市东河区红岩试剂厂.无水碳酸钠、无水乙醇、二氯甲烷(CH2Cl2)、石油醚(60~90 ℃)、乙酸乙酯购于天津市风船化学试剂科技有限公司.1,4-二氧六环购于天津市光复精细化工研究所.其中溶剂1,4-二氧六环在使用前蒸馏,其他试剂在使用前均未进一步纯化.
1.2催化剂PdCl2-EDTA的制备参照文献[16]的合成方法,向25 mL的圆底烧瓶中加入PdCl2(44.3 mg,0.25 mmol),再加入2.5 mL蒸馏水稀释成0.1 mol/L的溶液后,加入EDTA二钠盐(0.25 mmol)和Na2CO3(0.5 mmol), 混合液在室温下搅拌至溶液为红棕色,pH值为8~9, 室温放置待用.
1.3目标化合物的制备
1.3.1a系列目标化合物的制备 以化合物a-3(3,3’,4,4’-四甲氧基-对-三联苯)的制备为例,在氩气保护下,向50 mL的两口瓶依次加入0.50 mmol 1,4-二溴苯,1.05 mmol 3,4-二甲氧基苯硼酸,1 mL 2 mol/L的Na2CO3溶液,10 mL 1,4-二氧六环,2 mL无水乙醇及0.01 mL 0.1 mol/L的PdCl2-EDTA溶液,85 ℃加热回流反应8 h.冷却,旋蒸,柱层析(洗脱剂:CH2Cl2的体积分数96.8%,乙酸乙酯的体积分数3.2%),无水乙醇重结晶,得66 mg白色片状晶体,产率38%,m.p.206.4℃(DSC测得).
a-1(对-三联苯):138 mg白色片状晶体,产率60%.m.p.210~211 ℃(文献值212~213℃[17]);UV-vis(CH2Cl2)λmax:279 nm;1H NMR(CDCl3,500 MHz)δ:7.37(t,J=7.5 Hz,H,ArH),7.47(t,J=7.5 Hz,2H,ArH),7.65(d,J=7.5 Hz,2H,ArH),7.68(s,2H,ArH);IR(KBr)ν:838、745、687 cm-1.
a-2(4,4’-二甲氧基-对-三联苯):72 mg白色片状晶体,产率25 %.m.p.272~273 ℃(文献值273~274.5℃[17]);UV-vis(CH2Cl2)λmax:296 nm;1H NMR(CDCl3,500 MHz)δ:3.86(s,3H,CH3),7.00(d,J=8.5 Hz,2H,ArH),7.57(d,J=9 Hz,2H,ArH),7.61(s,2H,ArH);IR(KBr)ν:2 956、2 917、1 607、1 491、1 291、1 251、1 188、811 cm-1.
a-3(3,3’,4,4’-四甲氧基-对-三联苯):66 mg白色片状晶体,产率38 %.m.p.206.4 ℃(DSC测得);UV-vis(CH2Cl2)λmax:306 nm;1H NMR(CDCl3,500 MHz)δ:3.94(s,3H,CH3),3.97(s,3H,CH3),6.97(d,J=8 Hz,H,ArH),7.15(d,J=2 Hz,H,ArH),7.19(dd,J=8 Hz,2 Hz,H,ArH),7.62(s,2H,ArH);IR(KBr)ν:2 974、2 929、1 600、1 499、1 279、1 252、1 223、1 172、1 152、834、802、766 cm-1.
a-4(4,4’-二甲氧羰基-对-三联苯):90 mg白色片状晶体,产率26 %.m.p.>260.6 ℃;UV-vis(CH2Cl2)λmax:304 nm;1H NMR(CDCl3,500 MHz)δ:3.96(s,3H,CH3),7.72(d,J=8 Hz,2H,ArH),7.74(s,2H,ArH),8.14(d,J=8 Hz,2H,ArH);IR(KBr)ν:2 957、2 366、2 346、1 719、1 426、1 299、1 276、1 194、1 148、1 111、830、766、694 cm-1.
a-5(4,4’-二甲酰基-对-三联苯):73.4 mg白色粉末,产率26 %.m.p.212.1 ℃(DSC测得);UV-vis(CH2Cl2)λmax:322 nm;1H NMR(CDCl3,500 MHz)δ:7.78(s,2H,ArH),7.82(d,J=8 Hz,2H,ArH),8.00(d,J=8 Hz,2H,ArH),10.09(s,H,CHO);IR(KBr)ν:2 922、2 851、2 751、1 676、1 604、844、804、700 cm-1.
1.3.2b系列目标化合物的制备 (以化合物b-2(3,4-二甲氧基-对-三联苯)的制备为例)在氩气保护下,向50 mL的两口瓶,依次加入1.00 mmol 4-溴联苯,1.05 mmol 3,4-二甲氧基苯硼酸,1 mL 2 mol/L的Na2CO3溶液,15 mL 1,4-二氧六环,3 mL无水乙醇及0.01 mL 0.1 mol/L的PdCl2-EDTA溶液,85oC加热回流反应8 h.冷却,旋蒸,柱层析(洗脱剂: CH2Cl2的体积分数75%,石油醚的体积分数25%),无水乙醇重结晶,得232 mg白色片状晶体,产率80 %,m.p.152~153 ℃.
b-1(4-甲氧基-对-三联苯):154.3 mg白色粉末,产率63 %.m.p.218~219 ℃; UV-vis (CH2Cl2)λmax: 289 nm;1H NMR (CDCl3,500 MHz)δ: 3.87 (s,3H,CH3),7.00 (d,J=7.5 Hz,2H,ArH),7.36 (t,J= 7 Hz,H,ArH),7.46 (t,J=7.5Hz,2H,ArH),7.58 (d,J=8.5 Hz,2H,ArH),7.64~7.67 (m,6H,ArH);IR (KBr) ν:2 921、1 601、1 474、1 286、1 255、1 219、1 179、825、764 cm-1.
b-2(3,4-二甲氧基-对-三联苯):232 mg白色片状晶体,产率80 %.m.p.152~153 ℃;UV-vis (CH2Cl2)λmax: 300 nm;1H NMR (CDCl3,500 MHz)δ: 3.94 (s,3H,CH3),3.97 (s,3H,CH3),6.97(d,J=8.5 Hz,H,ArH),7.16 (d,J=2 Hz,H,ArH),7.20 (dd,J=8.5 Hz,2.5 Hz,H,ArH),7.36 (t,J=7 Hz,H,ArH),7.46 (t,J=7.5 Hz,2H,ArH),7.63~7.67 (m,6H,ArH);IR (KBr) ν: 2 966、2 934、2 839、1 589、1 509、1 485、1 460、1 300、1 271、1 249、1 151、838、810、767 cm-1.
b-3(4-甲氧羰基-对-三联苯):63 mg白色片状晶体,产率22 %.m.p.217~218 ℃;UV-vis(CH2Cl2)λmax:299 nm;1H NMR(CDCl3,500 MHz)δ:3.95(s,3H,CH3),7.38(t,J=7.5 Hz,H,ArH),7.48(t,J=7.5 Hz,2H,ArH),7.65(d,J=7.5 Hz,2H,ArH),7.72(d,J=7.5 Hz,6H,ArH),8.13(d,J=8 Hz,2H,ArH);IR(KBr)ν:2 946、1 718、1 601、1 279、1 227、1 194、1 144、1 113、834、761、691cm-1.
b-4(4-甲酰基-对-三联苯):117 mg白色粉末,产率45 %.m.p.186~187 ℃;UV-vis(CH2Cl2)λmax:309 nm;1H NMR(CDCl3,500 MHz)δ:7.39(t,J=7 Hz,H,ArH),7.48(t,J=7.5 Hz,2H,ArH),7.66(d,J=7.5 Hz,2H,ArH),7.73(s,4H,ArH),7.82(d,J=8 Hz,2H,ArH),7.98(d,J=8 Hz,2H,ArH),10.08(s,H,CHO);IR(KBr)ν:2 920、2 831、2 739、1 702、1 601、820、763、688 cm-1.
2 结果与讨论
2.1目标化合物的合成本文的目标化合物是通过1,4-二溴苯或4-溴联苯在PdCl2-EDTA的催化下, 分别与具有不同取代基的苯硼酸衍生物发生Suzuki偶联反应制得.在Suzuki偶联反应中比较常用的催化剂是[Pd(PPh3)4],而使用该催化剂反应后处理过程繁琐,且[Pd(PPh3)4]的制备和保存条件比较苛刻.本文所用的PdC12-EDTA催化剂配制过程简单,原料价格低,且在空气中可长时间保存不变质.发现反应温度、溶剂,以及反应时间对反应结果有影响,反应须在氩气保护下进行,且必须加热,室温下不反应,溶剂选用新蒸二氧六环,加热反应时间不宜过长,一般8 h左右,反应收率在22%~80%.对PdCl2-EDTA催化下的Suzuki偶联反应的条件进行优化,合成目标化合物的产率会有提高.
2.2目标化合物的结构表征本文所合成的化合物结构经IR和1H NMR确认.其中化合物a-4、a-5和b-3、b-4的核磁共振氢谱如图2所示.化合物a-4与b-3的氢谱相似,在δ为3.96附近有一个单峰,是与羰基相连的甲氧基上氢(—OCH3)的特征峰;δ为7.72和δ为8.14附近各有一个双重峰,是三联苯上芳氢(ArH)的特征吸收峰.不同的是,化合物a-4由于2个酯键对称结构取代的影响,三联苯上芳氢(ArH)在δ为7.74处裂分为单峰,化合物b-3由于一个酯键非对称结构取代的影响,三联苯上芳氢(ArH)在δ为7.65处裂分为双重峰,在δ为7.38和δ为7.48处分别裂分为三重峰.化合物a-5与b-4的氢谱相似,在δ为10.09附近处有一个单峰,是醛基上氢(—CHO)的特征峰;δ为7.78附近有一个单峰,δ为7.82和δ为8.00附近各有一个双重峰,均是三联苯上芳氢(ArH)的特征吸收峰.不同的是,化合物b-4由于一个醛基非对称结构取代的影响,三联苯上芳氢(ArH)在δ为7.66处裂分为双重峰,在δ为7.39和δ为7.48处分别裂分为三重峰.

图 2 部分目标化合物的核磁共振氢谱
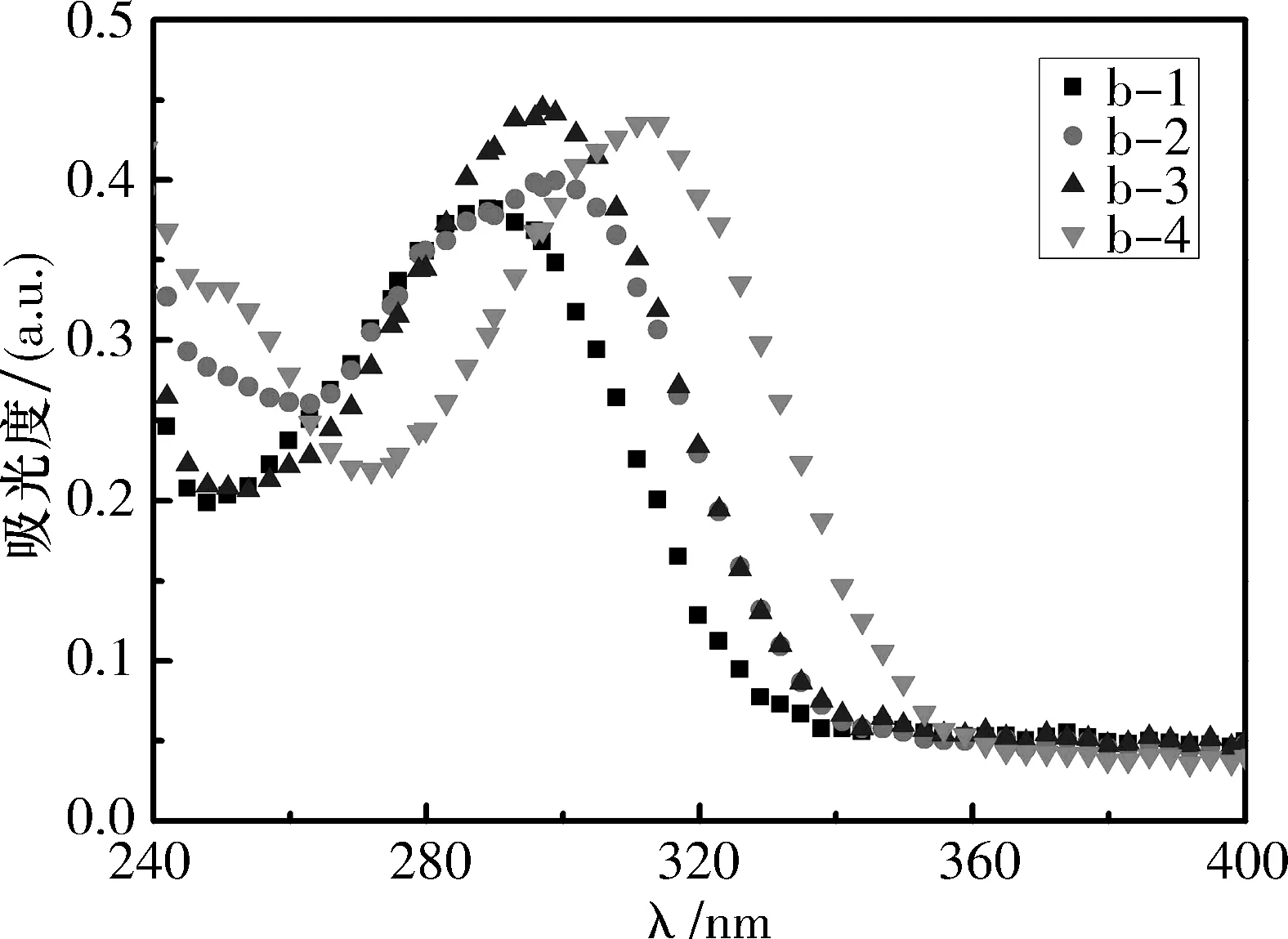
2.3目标化合物的紫外吸收和荧光发射性能目标化合物在溶剂CH2Cl2中的紫外吸收光谱如图3、4所示,目标化合物在279~322 nm之间有吸收峰,这是由于三联苯共轭结构π→π*跃迁所引起的.其中对-三联苯a-1的最大吸收峰波长为279 nm,其他含有取代基的对-三联苯化合物的最大吸收峰波长在289~322 nm之间,相对于对-三联苯a-1而言,其他化合物a-2~a-5,b-1~b-4的最大吸收波长均向长波方向移动,这是由于—OMe、—COOMe、—CHO与苯环形成的共轭效应所致.分子中的共轭体系由于大π键的形成,使各能级间能量差减小,跃迁所需能量降低,因此吸收峰向长波方向移动[18].
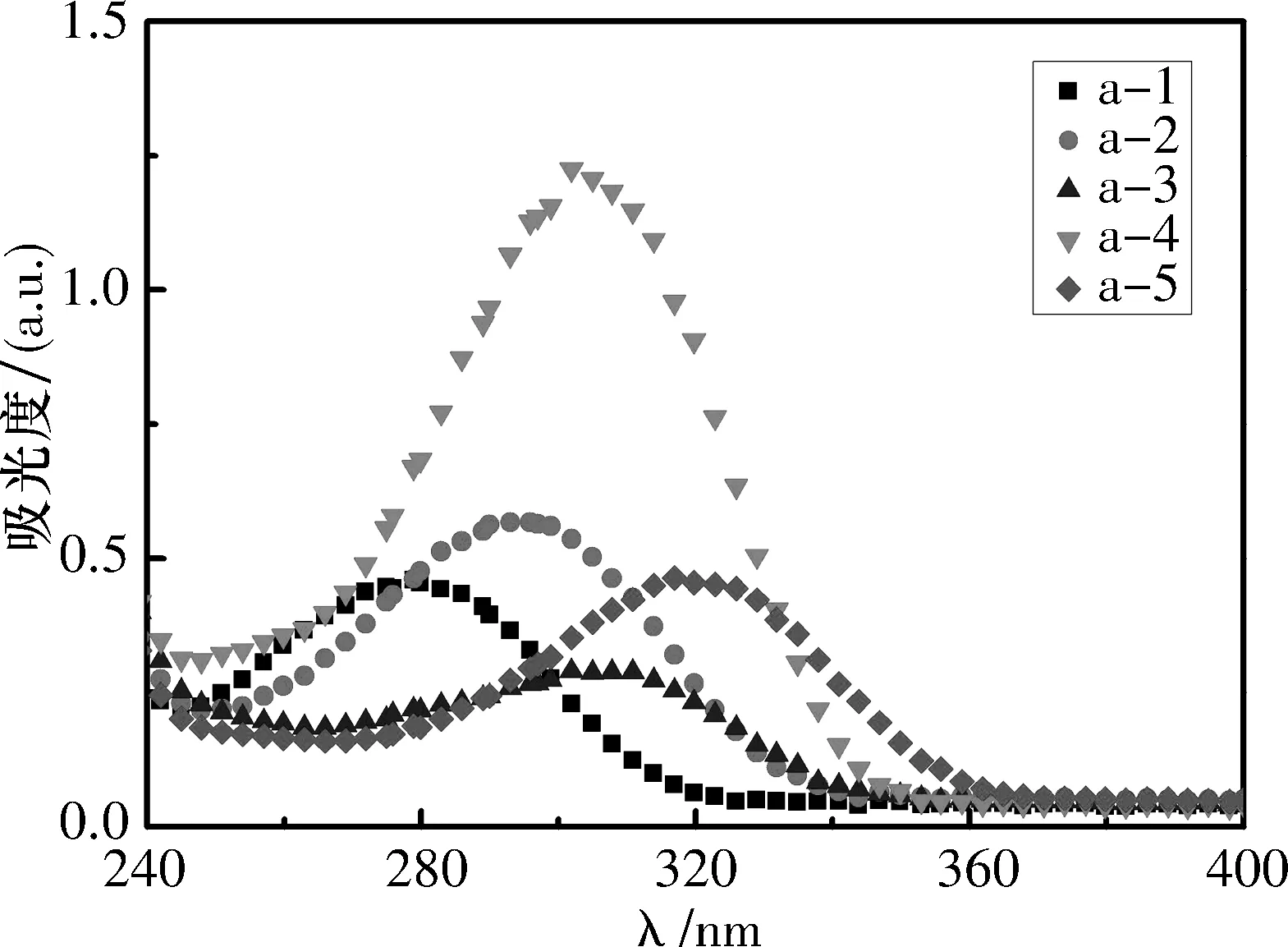
溶剂:CH2Cl2,c(B)=1×10-5 mol/L
对-三联苯具有3个苯环相连的共轭体系结构,其在紫外光的照射下能产生荧光,是一种具有高发光性能的生色团.本文利用荧光光谱仪,研究了目标化合物在溶剂CH2Cl2中的荧光性能,其荧光发射光谱如图5、6所示.
溶剂:CH2Cl2,c(B)=1×10-5 mol/L
图5、6中化合物a-2、a-3和b-1、b-2的最大发射峰波长较对-三联苯a-1的最大发射峰波长向长波方向移动,这是由于给电子取代基—OMe氧上的n电子的电子云几乎与苯环上的π轨道平行,共享了苯环的共轭π电子结构,扩大了共轭双键体系,因而被—OMe取代的对-三联苯化合物a-2、a-3和b-1、b-2的最大发射峰波长比未被取代的对-三联苯a-1的最大发射峰波长长[19].
同时,由图5可知,化合物a-4的最大发射峰波长,较对-三联苯a-1的最大发射峰波长向长波方向移动,这是由于化合物a-4的4和4’位上各有一个取代基—COOMe,虽然羰基氧上的n电子的电子云不与苯环上的π电子云共平面,但是与羰基相连的—OMe氧上的n电子云与羰基碳上的p轨道平行,电子云可重叠,参与了苯环的π键共轭,因此扩大了三联苯的共轭体系,使得化合物a-4的发射峰波长向长波方向移动[19-20].
由图5和6测试结果显示,化合物a-5和b-4分别在λex=297 nm和λex=308 nm,狭缝宽度为2.5 nm的测试条件下,荧光强度极弱,甚至不发光,原因是对-三联苯a-1的4或4’位上的氢被得电子取代基—CHO取代,羰基氧上的n电子云不与苯环上的π电子云共平面,不能与苯环共享和扩大其共轭π键,—CHO中的n电子跃迁到π*键的跃迁即n→π*跃迁属于警戒跃迁,最低单线激发态S1为n和π1*型,S1→T1的系间跨越程度增加,S1→S0放出光子的数量大大减少,致使荧光强度减弱[19].
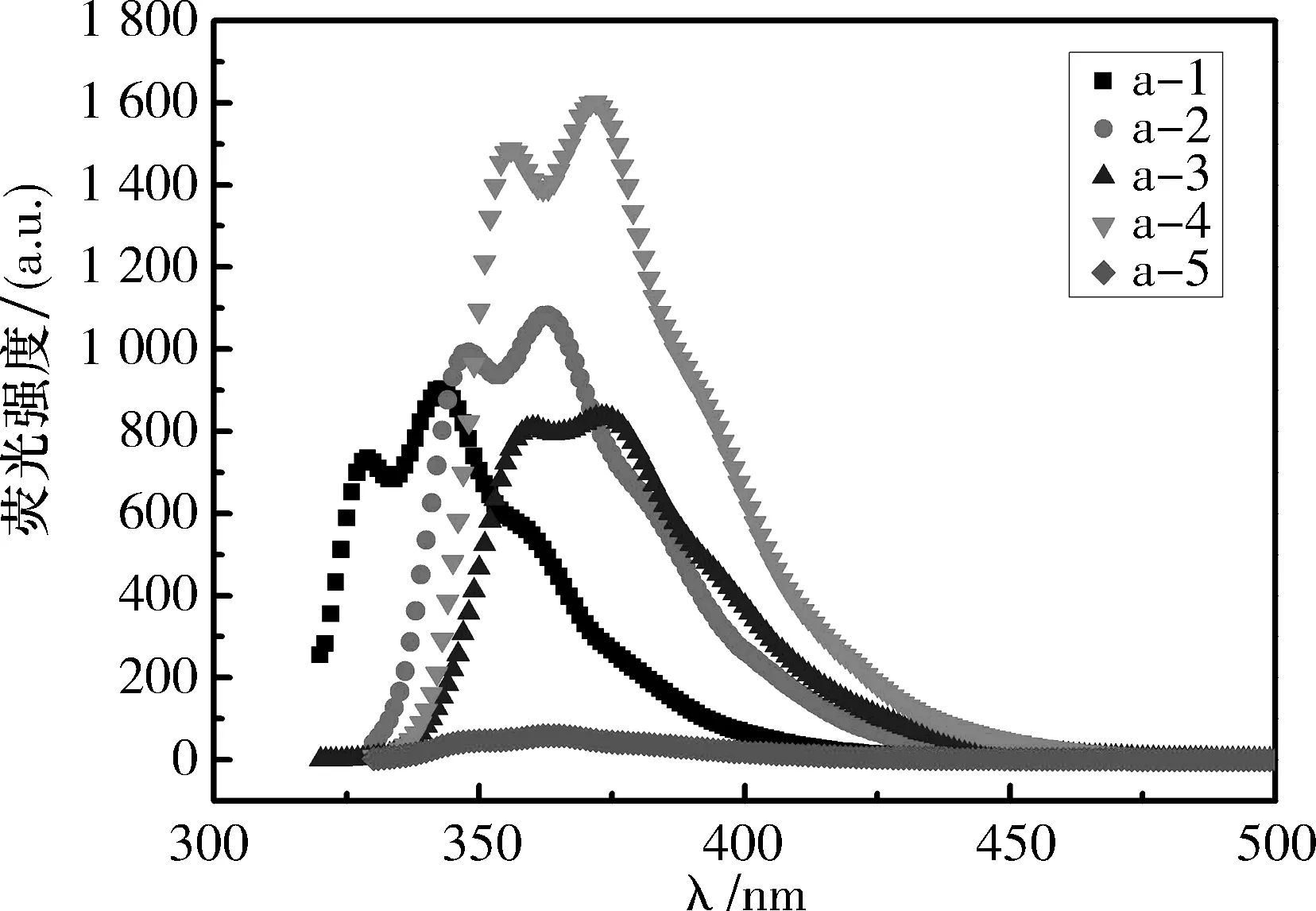
溶剂:CH2Cl2,c(B)=1×10-5mol/L,狭缝宽度:2.5 nm
图5a系列目标化合物的荧光发射光谱
Fig.5Fluorescenceemissionspectrumsofaseriestargetcompounds
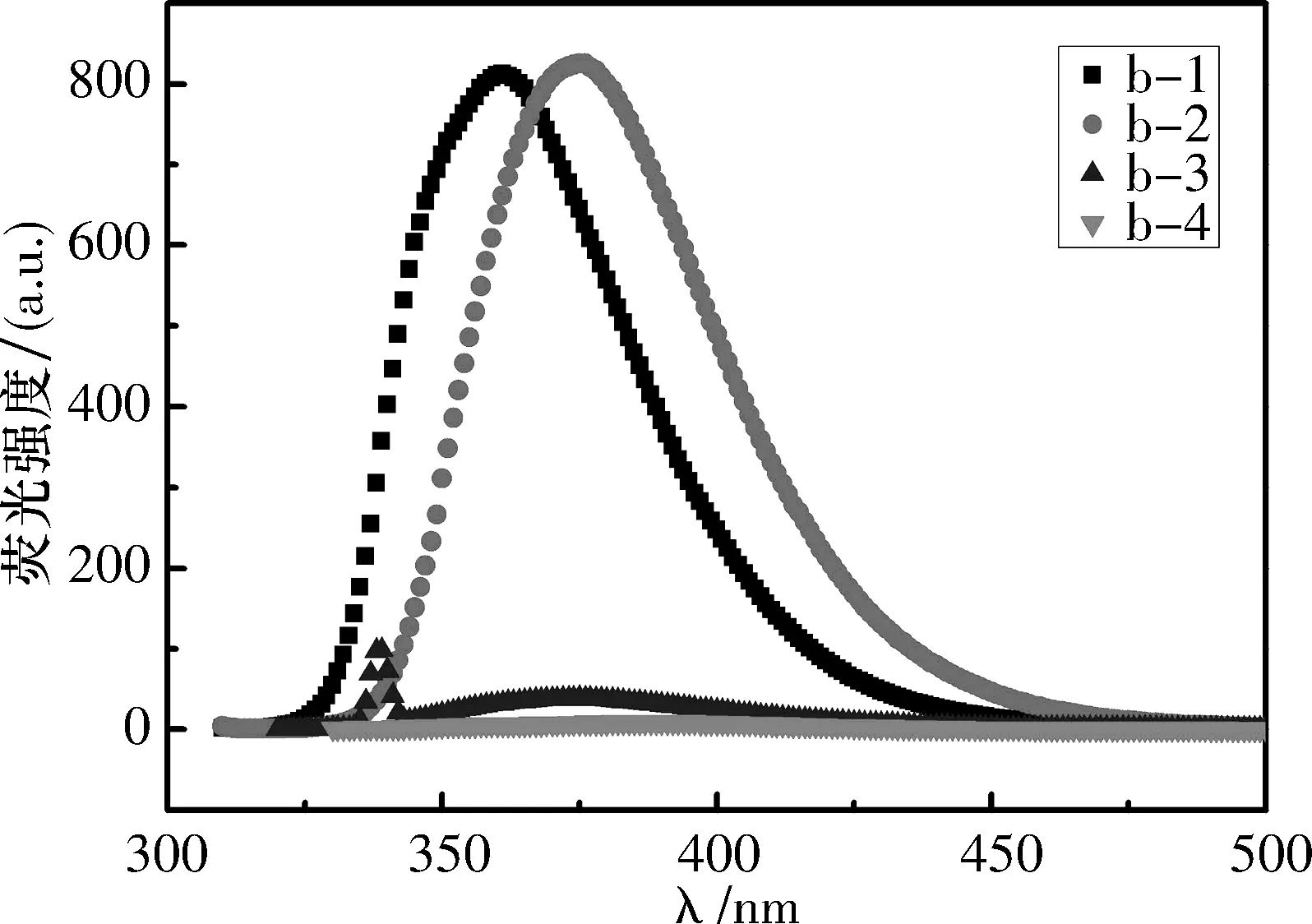
溶剂:CH2Cl2,c(B)=1×10-5 mol/L,狭缝宽度:2.5 nm
固定激发波长为336 nm,仪器狭缝宽度为2.5 nm,研究了不同浓度1×10-3、1×10-4和1×10-5mol/L下化合物b-3在溶剂CH2Cl2中的荧光性能,不同浓度化合物b-3的荧光发射光谱如图7所示.测试结果表明,化合物b-3的CH2Cl2溶液浓度为1×10-3mol/L时,荧光发射强度最大,同时可知,不同浓度下,化合物b-3的最大发射波长均为372 nm,证实了浓度对化合物的最大发射峰波长无影响.
目标化合物的光谱性质列于表1,如表1数据显示,化合物a-2~a-5比b-1~b-4的最大吸收峰波长明显向长波方向移动,这是由于对称取代的三联苯化合物比非对称取代的三联苯化合物具有较大的共轭体系结构,吸收峰向长波方向移动.

溶剂:CH2Cl2,λex=336 nm,狭缝宽度:2.5 nm,1) 1×10-3 mol/L,2)1×10-4 mol/L,3)1×10-5 mol/L
而化合物a-2~a-5与b-1~b-4的最大发射峰波长几乎相同,证明文中所合成的对-三联苯化合物的对称性对荧光发射峰波长无影响.

表1 目标化合物的光谱性质
注:*表示溶剂:CH2Cl2, c(B)= 1×10-5mol/L;**表示溶剂:CH2Cl2, c(B)= 1×10-4mol/L.
2.4目标化合物的热稳定性图8是部分目标化合物热失重(TGA)曲线图, 从图中可以看出化合物a-3、a-4、a-5的分解温度均在200 ℃以上, 进一步证实了对-三联苯化合物具有良好的热稳定性.结合DSC测试结果,化合物a-4在加热至260 ℃时未熔化便开始分解, 所以没有测得具体的熔点值.

图8部分目标化合物的TGA曲线图
Fig.8TGAtracesofseveraltargetcompounds
3 结论
本文通过PdCl2-EDTA催化下Suzuki偶联反应成功合成了具有不同取代基及对称性的对-三联苯化合物.通过对其紫外吸收光谱和荧光发射光谱研究发现, 在对-三联苯上引入—OMe、—COOMe和—CHO基团后, 会使对-三联苯的最大吸收峰波长和最大发射峰波长向长波方向移动;对-三联苯化合物结构的对称性对紫外吸收峰波长有影响, 对称取代的三联苯化合物比非对称取代的三联苯化合物最大吸收峰波长向长波方向移动, 而对-三联苯化合物结构的对称性对荧光发射峰波长无影响;本文所合成的目标化合物是合成液晶及聚合物蓝光材料的重要中间体, 为进一步合成具有良好性能的三联苯液晶及聚合物蓝光材料奠定了基础.
致谢内蒙古科技大学创新基金资助项目(2014QDL030)对本文给予了资助,谨致谢意.
[1] 王记江,侯向阳,高楼军,等. 基于三联苯-2,2’,4,4’-四羧酸的二维双层锌(Ⅱ)配位聚合物的水热合成、晶体结构及荧光性质[J]. 无机化学学报,2014,30(2):379-383.
[2] 姜永才,吴世康. 对-三联苯液体闪烁剂荧光发光特性的研究[J]. 核电子学与探测技术,1984,4(3):151-154.
[3] WANG J L, HAROLD S F, LARRY D C. Synthsis and mutagenic properties of 4,4’-diamino-p-terphenyl and 4,4’-diamino-p-quaterphenyl[J]. Color Technol,2007,123(1):34-38.
[4] JOHN A M, GERASIMOS M T. Synthesis and characterization of soluble blue-fluorescent polyamides and polyimides containing substitutedp-terphenyl as well as long aliphatic segments in the main chain[J]. Jolym Sci Part A:Polym Chem,1999,37(18):3646-3656.
[5] CHEN B, UTE B, GERHARD P, et al. Carbohydrate rod conjugates:ternary rod-coil molecules forming complex liquid crystal structures[J]. J Am Chem Soc,2005,127(47):16578-16591.
[6] CHEN L, CHEN Y W, YAO K, et al. A novel type of optically active helical liquid crystalline polymers:synthesis and characterization of poly(p-phenylene)s containing terphenyl mesogen with different terminal groups[J]. J Polym Sci Part A:Polym Chem,2009,47(18):4723-4735.
[7] ZHOU W Q, XU J K, DU Y K, et al. Electrochemical polymerization ofp-terphenyl in mixed electrolyte of boron trifluoride diethyl etherate and CH2Cl2[J]. Appl Polym Sci,2010,117(5):2688-2694.
[8] 谌烈,陈义旺,姚凯, 等. 新型光学活性含氰基三联苯液晶聚噻吩合成与分子构象[J]. 物理化学学报,2010,26(4):971-980.
[9] TIEN H L, CHAIN S H. Synthesis of fluorinated terphenyl liquid crystals with 3-propylcyclopentane end group[J]. Liq Cryst,2014,41(9):1235-1245.
[10] ZOHRA N K, ROBERT A L, SHAHZAD N. Development of novel chiral dopants to be used in ferroelectric liquid crystal system[J]. J Mol Liq,2013,180(160C):74-88.
[11] 余文浩,向琴,董坤,等. 巯基-端烯/炔点击反应合成棒状液晶化合物[J]. 四川师范大学学报(自然科学版),2015,38(1):101-108.
[12] CHANG M Y, CHIEH K C, WU M H. One-pot synthesis of functionalizedp-terphenyl derivatives[J]. Tetrahedron,2013,69(37):7916-7924.
[13] ANDREW P R, FOOK S T, ERIC L C. A temperature dependent X-ray study of the order-disorder enantiotropic phase transition ofp-terphenyl[J]. J Chem Crystallogr,2013,43(1):14-25.
[14] 石巍,俞婷婷,崔冬梅. 三联苯类化合物合成方法的研究进展[J]. 有机化学,2015,35(2):362-372.
[15] NORIO M, AKIRA S. Palladium-catalyzed cross-coupling reactiongs of organoboron compounds[J]. Cheminform,1995,27 (11):2457-2483.
[16] DMITRII N K, NIKOLAY A B. Pd-EDTA as an efficient catalyst for Suzuki-Miyaura reactiongs in water[J]. Cheminform,2005,36(50):5751-5754.
[17] HAROLD H, KATSUMASA H, et al. Synthetically useful aryl-aryl bond formation via grignard generation and trapping of arynes a one-step synthesis ofp-terphenyl and unsymmetrical biaryls[J]. J Org Chem,1985,50(17):3104-3110.
[18] 刘约权. 现代仪器分析[M]. 2版. 北京:高等教育出版社,2006:66-67.
[19] 许金钩, 王尊本. 荧光分析法[M]. 3版. 北京:科学出版社,2006:25-27.
[20] 曹宣辉. 试论共轭效应 [J]. 内江师专学报,1989(6):53-58.
Synthesis and Spectral Properties of p-Terphenyl Compounds
JI Hong1, YU Wenhao2, WANG Yanming1, LIU Jinyan1, GUO Zhigang1, LI Songbo1
(1.SchoolofChemistryandChemicalEngineering,InnerMongoliaUniversityofScienceandTechnology,Baotou014010,InnerMongolia;2.CollegeofChemistryandMaterialsScience,SichuanNormalUniversity,Chengdu610066,Sichuan)
p-Terphenyl compounds are successfully prepared via Suzuki coupling reaction which uses PdCl2-EDTA as catalyst. Structures of target compounds are characterized by nuclear magnetic resonance (1H NMR) and infrared spectroscopy (IR), properties of target compounds are evaluated with differential scanning calorimetry(DSC), ultraviolet spectroscopy (UV) and photoluminescence (PL). The results show that p-Terphenyl compounds have good thermal stability. Compared with p-terphenyl , the maximum ultraviolet absorption peak and fluorescence emission peak wavelengths of p-terphenyl compounds which contain —OMe, —COOMe and —CHO are red shift. The symmetry properties of p-terphenyl compounds have great influence on the ultraviolet absorption peaks, while no influence on fluorescence emission peaks.
p-terphenyl; Suzuki coupling reaction; ultraviolet absorption; fluorescence emission
2016-05-18
国家自然科学基金(21463016)和内蒙古自然科学基金(2013MS0209)
*通信作者简介:李松波(1972—),男,教授,主要从事发光材料方向的研究,E-mail: lisongbo@imust.cn
O433
A
1001-8395(2017)05-0686-07
10.3969/j.issn.1001-8395.2017.05.021
(编辑 陶志宁)
