离子交换树脂D001对罗丹明B的吸附特性
2017-10-31刘保锋
刘保锋,洪 军,王 丽,童 晨
(中国地质大学 环境学院纳米矿物材料及应用教育部工程研究中心,湖北 武汉 430074)
离子交换树脂D001对罗丹明B的吸附特性
刘保锋,洪 军,王 丽,童 晨
(中国地质大学 环境学院纳米矿物材料及应用教育部工程研究中心,湖北 武汉 430074)
采用强酸性阳离子交换树脂D001作为吸附剂吸附脱除水溶液中的罗丹明B(RhB)。SEM和FTIR表征结果显示:D001树脂表面存在孔隙,可增加树脂的比表面积;树脂表面的磺酸基团可通过与阳离子染料RhB络合而将其吸附。实验结果表明:Langmuir等温吸附模型能更好地描述树脂对RhB的吸附规律,升高温度有利于树脂吸附RhB;吸附过程符合Lagergren准一级动力学方程,初始RhB质量浓度为20 mg/L时吸附活化能为7.06 kJ/mol;树脂对RhB的吸附是一个自发的、吸热的、熵推动的过程;颗粒扩散为吸附过程的控制步骤;树脂具有良好的重复使用性能。
阳离子交换树脂;罗丹明B;吸附热力学;吸附动力学
罗丹明B(RhB)是一种碱性染料,广泛应用于印刷、纺织、化妆品、食品等行业。RhB是难生物降解的有机物,且具有潜在的毒性、致突变性和致癌性,对水质和水中动植物产生的危害较大[1-3]。
离子交换树脂物理化学性质稳定,具有比表面积大、机械强度高、易再生等优点,可于水溶液中富集和分离有机物,因此被广泛用于染料废水处理[4]。其中,D001树脂是在大孔结构的苯乙烯-二乙烯苯共聚体的基础上通过连接磺酸基(—SO3H)制备而成的。该树脂稳定性高,具有较大的比表面积,是较为理想的吸附剂。但采用D001树脂吸附染料的研究较少,且相关吸附特性的研究也不够深入,不能很好的阐述吸附过程及机理。
本工作采用强酸性阳离子交换树脂D001作为吸附剂吸附脱除水溶液中的RhB,利用SEM和FTIR技术对树脂进行了表征,研究了D001树脂吸附RhB过程的吸附动力学、热力学和机理,以期为固液吸附研究和染料废水处理提供理论支持。
1 实验部分
1.1 试剂、材料和仪器
RhB、NaOH、盐酸:分析纯;实验用水均为二次蒸馏水。
D001树脂:购于浙江争光实业股份有限公司,强酸性阳离子交换树脂,其结构式见图1。
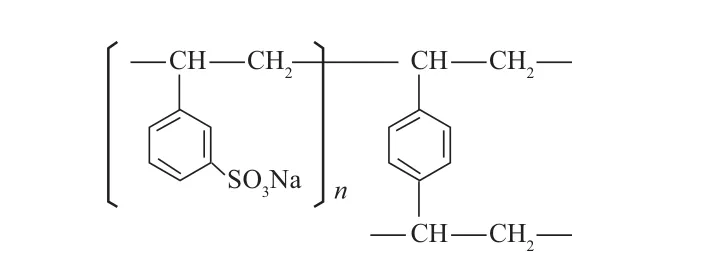
图1 D001树脂的结构式
UV2800型紫外-可见分光光度计:尤尼克(上海)仪器有限公司;HH-S型水浴锅:巩义市予华仪器有限责任公司;RS-8801型空气泵:中山市日胜电器制品有限公司;DHG-9101-2SA型烘箱:上海三发科学仪器有限公司;SI-234型电子天平:丹佛仪器(北京)有限公司;Quanta 450 FEG型场发射环境扫描电子显微镜:美国FEI公司;Nicolet 6700型傅里叶变换红外光谱仪:美国赛默飞世尔有限公司。
1.2 树脂的预处理
分别用1 mol/L的盐酸和NaOH溶液浸泡树脂24 h,再用蒸馏水清洗至中性。重复上述操作一次,以保证树脂中的杂质被交换出来。最后,置于50℃烘箱中烘干24 h,密封避光保存。
1.3 实验方法
吸附实验:配制5,10,15,20,25 mg/L的RhB溶液,分别移取200 mL于250 mL锥形瓶中,加入0.01 g预处理好的树脂。将锥形瓶置于25 ℃水浴锅中曝气搅拌,吸附72 h。其他条件不变,分别在35,45,55 ℃下进行上述实验。每隔一段时间取样,离心后取上清液待测。
重复使用实验:移取200 mL 5 mg/L的RhB溶液于250 mL锥形瓶中,加入0.01 g预处理好的树脂,在25 ℃水浴锅中曝气搅拌24 h。将树脂分离出来,分别用酸、碱清洗后干燥,再投入到新的溶液体系中进行吸附。
1.4 分析方法
采用紫外-可见光分光光度计在波长554 nm处测定水样的吸光度值,由工作曲线得到RhB的质量浓度,进而计算出树脂对RhB的吸附量。
分别采用SEM和FTIR技术对预处理后的树脂进行微观形貌观察和官能团分析。
2 结果与讨论
2.1 树脂的表征结果
2.1.1 SEM照片
D001树脂的SEM照片见图2。由图2可见,树脂表面存在许多小孔,这些孔隙的存在增加了树脂的比表面积,有利于RhB的吸附。

图2 D001树脂的SEM照片
2.1.2 FTIR谱图
试样的FTIR谱图见图3。
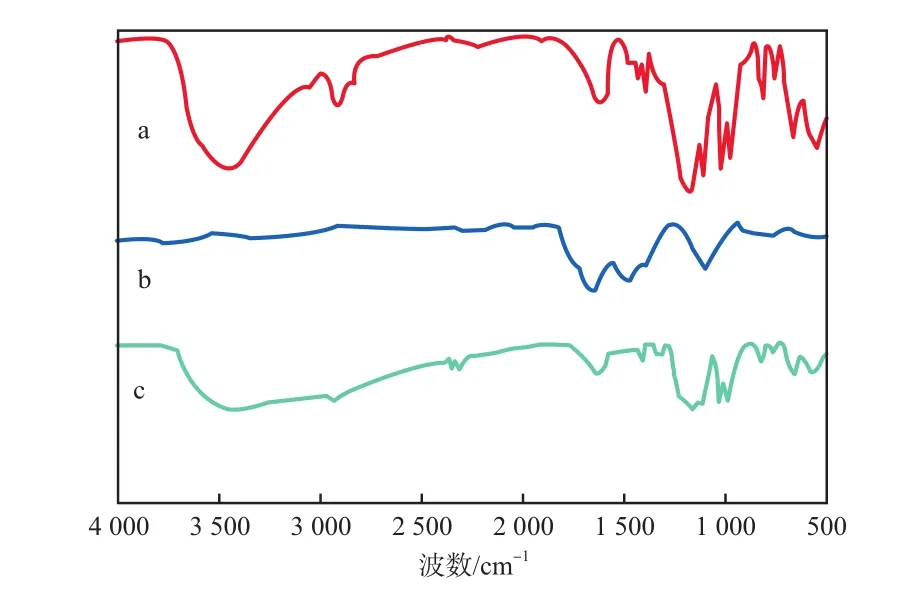
图3 试样的FTIR谱图
由图3a可见,3 443 cm-1处的吸收峰归属于羟基的伸缩振动[5];1 644,1 497,1 453,1 414 cm-1处的吸收峰是苯环的特征峰[6];1 183 cm-1和1 040 cm-1处的吸收峰分别归属于磺酸基团的非对称和对称伸缩振动[7]。由图3b可见,1 613,1 426,1 109 cm-1处的吸收峰分别归属于RhB分子苯环骨架、C—CH3和Ar—N键的伸缩振动[8]。由图3c可见,树脂吸附后出现RhB的特征吸收峰,且吸附前1 183 cm-1处的峰吸附后分裂成1 217 cm-1和1 163 cm-1处的两个峰,这是因为RhB阳离子与树脂上的磺酸基团发生了反应,导致S=O的振动吸收峰分裂,这说明RhB可通过与磺酸基团络合而负载到树脂表面上。此外,因罗丹明B具有一定的疏水性,故分子间的范德瓦耳斯力和疏水作用对树脂吸附罗丹明B也有一定的贡献。
2.2 吸附等温线
D001树脂对RhB的吸附等温线见图4。
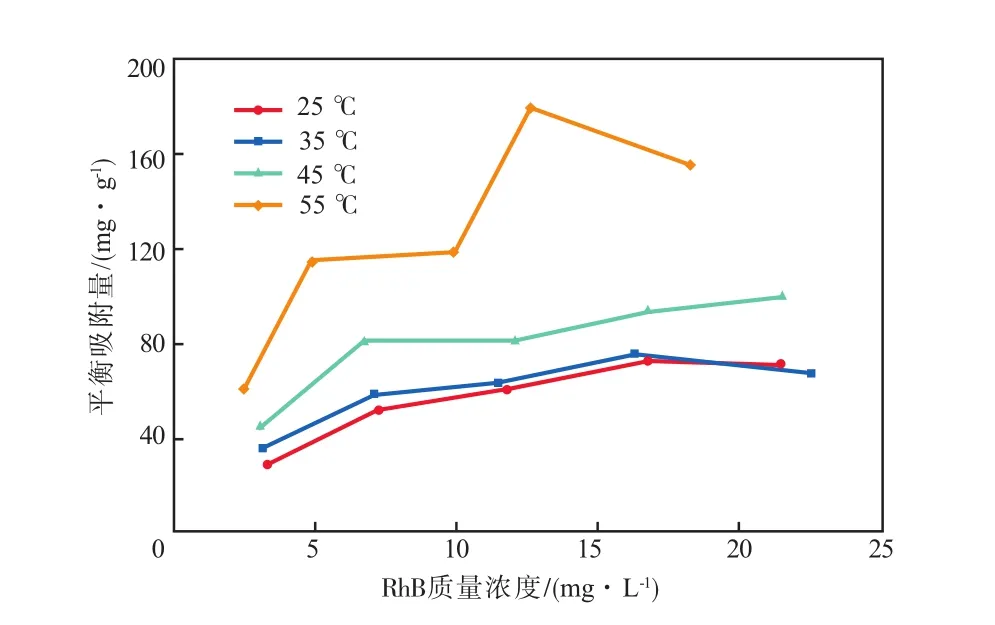
图4 D001树脂对RhB的吸附等温线
由图4可见:在同一温度下随着RhB质量浓度的增加,树脂对RhB的平衡吸附量也逐渐增加,但最终平衡吸附量会趋于平稳甚至有所降低,说明树脂吸附RhB已经达到饱和;温度升高时,树脂对RhB的平衡吸附量也逐渐升高,尤其是在温度为55℃时,平衡吸附量增加得更为明显,说明升高温度有助于树脂吸附RhB;55 ℃时吸附曲线出现陡然上升可能是在高浓度染料条件下,吸附过程的传质动力得到了极大的提高,使得RhB向树脂内部孔隙不断扩散并与其内部吸附位点结合,从而极大的增加了树脂的平衡吸附量;在RhB浓度过高时,55 ℃吸附曲线陡然下降可能是因为随着吸附进行,溶液中的水分逐渐蒸发,使得吸附平衡时染料浓度上升更多所致。
分别采用Langmuir和Freundlich等温吸附模型(分别见式(1)和式(2))[9]对图4的实验数据进行拟合,拟合结果见表1。由表1可见:在同条件下,Langmuir等温吸附方程的R2比Freundlich等温吸附方程的更高,说明Langmuir等温吸附方程更能反应树脂对RhB的吸附过程,由此推测RhB是呈单分子层状态吸附于树脂表面;KL和树脂的饱和吸附量均随温度的升高而增大,说明温度升高有利于树脂吸附RhB。

式中:ρe为吸附平衡时的RhB质量浓度,mg/L;qe为平衡吸附量,mg/g;qsat为饱和吸附量,mg/g;KL为Langmuir吸附常数,L/mg;n和KF为Freundlich吸附常数。
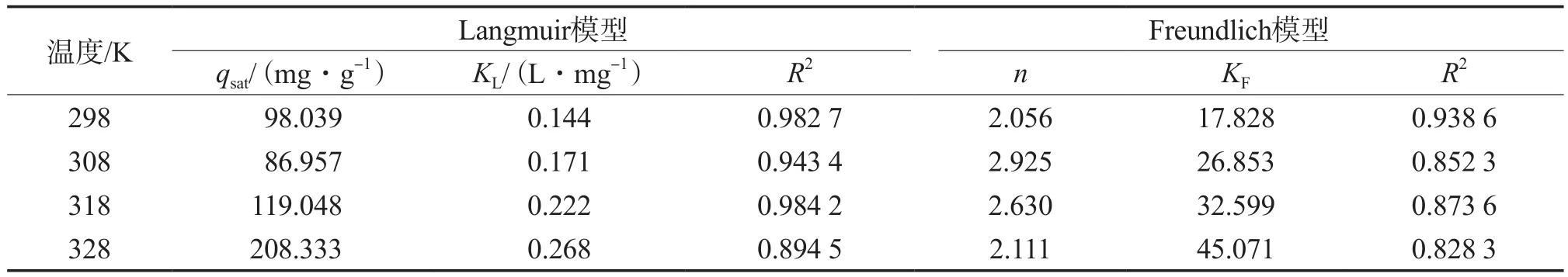
表1 等温吸附方程的拟合结果
2.3 吸附动力学
在初始RhB质量浓度为20 mg/L时,D001树脂吸附量随吸附时间的变化见图5。
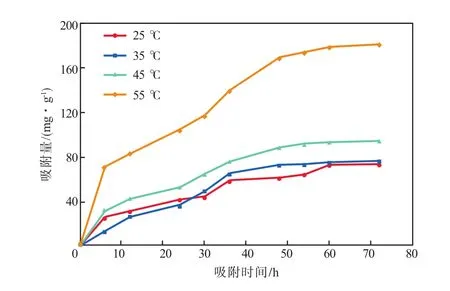
图5 D001树脂吸附量随吸附时间的变化
由图5可见:不同温度下吸附72 h时,吸附量基本均不再变化,说明吸附趋于平衡;温度对树脂吸附量的影响较大,树脂的吸附量随温度的升高而逐渐增大,尤其是在温度为55 ℃时,吸附量的增加尤为明显。
分别采用Lagergren准一级动力学方程(见式(3))和准二级动力学方程(见式(4))[10]对图5的实验数据进行拟合,拟合结果见表2。由表2可见,按准一级动力学方程拟合的R2整体比按准二级动力学方程拟合的更高,说明准一级动力学模型能更好地描述树脂对RhB的吸附过程。

式中:t为吸附时间,h;qt为t时刻的吸附量,mg/g;k1为准一级吸附速率常数,h-1;k2为准二级吸附速率常数,g/(mg·h)。
以lnk1对1/T作图,得到直线拟合方程(R2=0.921 1)为:lnk1=-8.49.49(1/T)+0.04。根据Arrhenius方程(见式(5)),得到吸附活化能为7.06 kJ/mol。

式中:Ea为吸附活化能,J/mol;R为摩尔气体常数,8.314 J/(mol·K);T为吸附温度,K;A为指前因子。
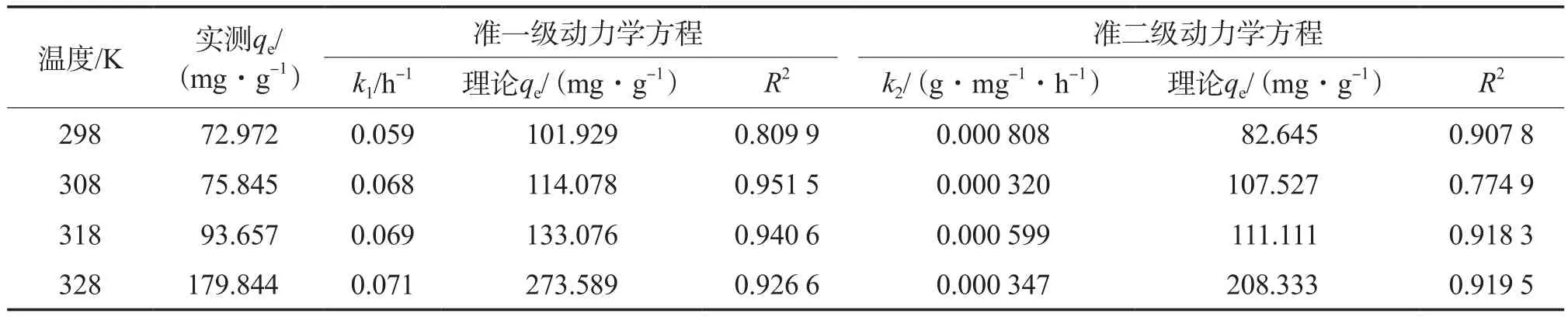
表2 动力学方程的拟合结果
2.4 吸附热力学
D001树脂对RhB的吸附量随温度的升高而增加,说明该吸附反应为吸热反应。吸热反应中的热力学函数可通过式(6)[11]以及Van Hoff方程(见式(7))计算。

式中:ΔG为吸附自由能变,J/mol;Kd为吸附平衡常数,Kd=qe/ρe,L/g;ΔH为吸附焓变,J/mol;ΔS为吸附熵变,J/(mol·K)。
根据在不同温度条件下树脂吸附处理5 mg/L RhB溶液的实验结果,计算出吸附平衡常数Kd。由式(6)得到298,308,318,328 K下的ΔG分别为-5.411,-6.271,-7.113,-8.744 kJ/mol,均为负值,说明树脂吸附RhB是一个自发的过程。随着温度的升高,ΔG逐渐减小,说明温度的提升有利于吸附的进行。按式(7)进行拟合得到ΔH为26.749 kJ/mol,ΔS为0.107 kJ/(mol·K),R2为0.954 4。吸附体系的ΔH>0,说明吸附过程是一个吸热过程。吸附体系的ΔS>0,说明RhB在树脂上的吸附是熵推动过程。根据吸附交换理论[12],对于固液体系,溶质分子的吸附是熵减少的过程,溶剂的脱附是熵增加的过程,两者的总和就是吸附过程的熵变,它取决于溶质和溶剂在固体表面作用的强弱和分子体积。由于RhB的分子体积远大于水分子,故吸附过程的熵变大于零。
2.5 控速机理的判定
离子交换过程受液膜扩散、颗粒扩散和化学反应3个步骤控制,而其中速度最慢的一步就是控制离子交换速率的主要控制步骤。液膜扩散、颗粒扩散和化学反应控制方程的表达式分别见式(8)~(10)。
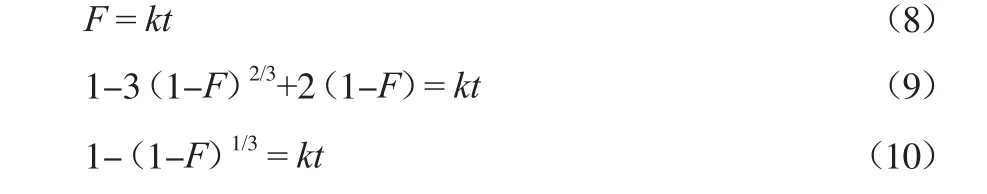
式中:F为离子交换度,F = qt/qe;k为扩散系数,h-1。
在25 ℃下将树脂吸附处理15 mg/L RhB溶液的实验数据,按照3个速率控制方程分别进行拟合,结果见图6。由图6可见,颗粒扩散和化学反应的控制方程的拟合曲线均具有较好的线性关系,说明颗粒扩散和化学反应两个步骤一起影响树脂吸附过程的反应速率。但是因为一般化学反应都很快,很难成为控速步骤[13],所以颗粒扩散是D001树脂对RhB吸附的控制步骤。
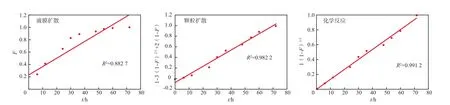
图6 速率控制方程的拟合曲线
2.6 树脂重复使用
D001树脂的重复使用性能见图7。由图7可见,树脂连续使用3次后,对RhB染料的吸附量有一定的下降,可能是因为树脂在清洗过程中内部的染料分子难以完全清洗干净所致,但下降幅度不大,说明树脂具有良好的重复使用性能。
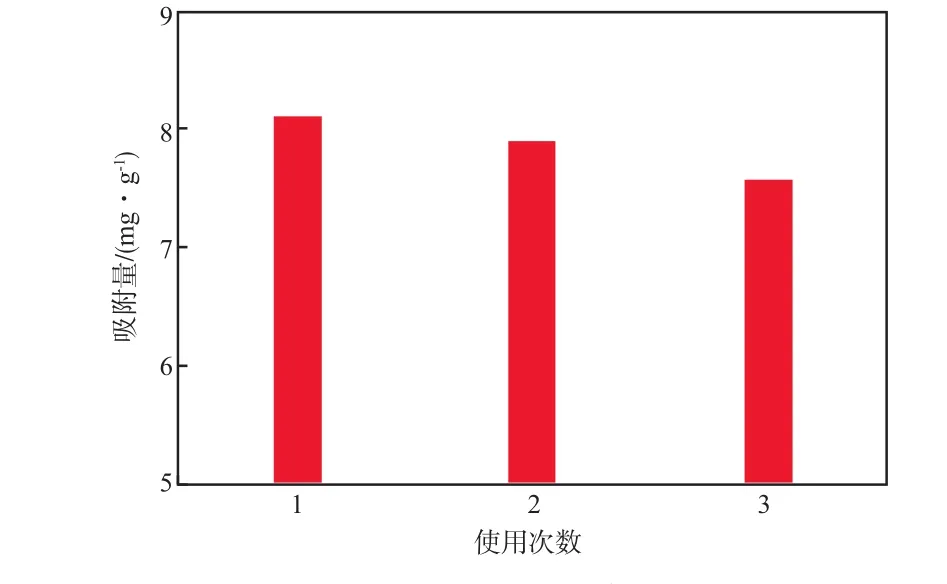
图7 D001树脂的重复使用性能
3 结论
a)D001树脂表面存在孔隙,可增加树脂的比表面积,有利于RhB的吸附。树脂表面的磺酸基团可通过与阳离子染料RhB络合而将其吸附。
b)Langmuir等温吸附模型能更好地描述树脂对RhB的吸附规律,说明RhB在树脂表面呈单分子层吸附状态。升高温度有利于树脂吸附RhB。
c)吸附过程符合Lagergren准一级动力学方程,初始RhB质量浓度为20 mg/L时吸附活化能为7.06 kJ/mol。
d)树脂对RhB的吸附是一个自发的、吸热的、熵推动的过程。
e)颗粒扩散为吸附过程的控制步骤。
f)树脂具有良好的重复使用性能。
[1] 李丽华,马明明,任庆军,等. 羧基化改性有序介孔碳对罗丹明B的吸附[J]. 化工环保,2016,36(2):157 - 162.
[2] 谢焕玲. 高级氧化技术处理有机废水的研究进展[J].重庆理工大学学报:自然科学,2013,27(6):41 -43.
[3] 张卫梅,李巧玲. TiO2中空微球的制备及其对罗丹明B的光催化降解[J]. 化工环保,2015,35(6):630 -633.
[4] 李红艳,李亚新,李尚明. 离子交换技术在重金属工业废水处理中的应用[J]. 水处理技术,2008,34(2):12 - 15,20.
[5] Viswanathan N,Meenakshi S. Effect of metal ion loaded in a resin towards fluoride retention[J]. J Fluorine Chem,2008,129(7):645 - 653.
[6] Han Zhenbang,Dong Yongchun,Dong Siming.Copper-iron bimetal modified PAN fiber complexes as novel heterogeneous Fenton catalysts for degradation of organic dye under visible light irradiation[J]. J Hazard Mater,2011,189(1/2):241 - 248.
[7] Viswanathan N,Meenakshi S. Role of metal ion incorporation in ion exchange resin on the selectivity of fl uoride[J].J Hazard Mater,2009,162(2/3):920 - 930.
[8] 刘栓,杨昌英,陈登霞,等. (光)助电-Fenton降解有机染料罗丹明B[J]. 三峡大学学报:自然科学版,2009,31(6):84 - 88.
[9] 马聪,王潘,朱春雷,等. 离子交换树脂吸附锰(Ⅱ)的热力学和动力学研究[J]. 中国锰业,2010,28(2):43 - 46,53.
[10] Wang Yuxian,Sun Hongqi,Duan Xiaoguang,et al.A new magnetic nano zero-valent iron encapsulated in carbon spheres for oxidative degradation of phenol[J].Appl Catal,B,2015,172/173:73 - 81.
[11] 刘福强,陈金龙,李爱民,等. 超高交联吸附树脂对苯甲酸的吸附研究[J]. 离子交换与吸附,2002,18(6):522 - 528.
[12] 沈学优,卢瑛莹,朱利中. 对硝基苯酚在水/有机膨润土界面上的吸附行为:热力学特征及机理[J]. 中国环境科学,2003,23(4):367 - 370.
[13] 唐嘉英,李鑫,应汉杰. 离子交换树脂吸附TP5的热力学和动力学研究[J]. 南京工业大学学报:自然科学版,2006,28(5):79 - 83.
Adsorption capability of ion exchange resin D001 to Rhodamine B
Liu Baofeng,Hong Jun,Wang Li,Tong Cheng
(Engineering Research Center of Nano-Geomaterials of Ministry of Education,School of Environmental Studies,China University of Geosciences,Wuhan Hubei 430074,China)
Strong-acid cation exchange resin D001 was used as adsorbent for removal of Rhodamine B(RhB)from aqueous solution. The characterization results by SEM and FTIR showed that:The pores structure on the resin surface contribute to increase the specific surface area of the resin;Sulfonic acid groups on the resin surface could adsorb RhB by complexing with the cation dye. The experimental results showed that:The adsorption isotherm of the resin followed Langmuir model better,the increase of temperature favored adsorption reaction;The adsorption kinetics followed the pseudo- fi rst order equation,the adsorption activation energy was 7.06 kJ/mol when the initial mass concentration of RhB was 20 mg/L;The adsorption process was a spontaneous,endothermic and entropy driving reaction;The ratedetermining step was particle diffusion;The resin had good reusability.
cation ion exchange resin;Rhodamine B;adsorption thermodynamics;adsorption kinetics
X791
A
1006-1878(2017)05-0543-05
10.3969/j.issn.1006-1878.2017.05.009
2017 - 02 - 27;
2017 - 06 - 04。
刘保锋(1990—),男,江西省吉安市人,硕士生,电话 134762292920,电邮 cugliubaofeng@163.com。联系人:洪军,电话 18817138857,电邮 hongjun@cug.edu.cn。
(编辑 魏京华)
