急性Stanford A型主动脉夹层术后急性肾损伤的肾叶间动脉血流动力学改变
2017-10-23武海波范占明
秦 淮,武海波,程 颐,范占明
(1.首都医科大学附属北京安贞医院超声科,2.心外科,3.影像科,北京 100029)
急性StanfordA型主动脉夹层术后急性肾损伤的肾叶间动脉血流动力学改变
秦 淮1,武海波2,程 颐1,范占明3*
(1.首都医科大学附属北京安贞医院超声科,2.心外科,3.影像科,北京 100029)
目的探讨急性Stanford A型主动脉夹层术后急性肾损伤(AKI)的超声血流动力学指标改变情况。方法收集40例接受手术治疗的急性Stanford A型主动脉夹层患者,分别在手术前1天、术后即刻(进入重症监护室)、手术后6、24、48 h测量双肾叶间动脉收缩期峰值流速(PSV)、舒张期最小流速(EDV)、搏动指数(PI)、阻力指数(RI),同时记录血肌酐(sCr)水平和尿量。以AKIN为标准将患者分为AKI组和无AKI组,比较两组间差异。结果40例患者中,AKI组27例,无AKI组13例。无AKI组与AKI组患者术后6、24 h肾叶间动脉EDV、PI、RI差异有统计学意义(P均<0.05)。肾叶间动脉EDV与sCr呈负相关(r=-0.508,P=0.001),PI、RI与SCr呈正相关(r=0.411、0.443,P=0.009、0.005)。结论通过肾叶间动脉EDV、PI、RI可早期预测AKI发生,术后6、24 h是超声测量肾叶间动脉血流动力学指标预测肾损伤的最佳时间。
急性肾损伤;动脉瘤,夹层;超声检查
近年来手术后急性肾损伤(acute kidney injury,AKI)受到临床医师的重视。目前AKI的相关研究聚焦于可早期诊断的生物学标志物,以期通过早期发现、早期诊断,而获得较早的干预,尽早恢复肾功能,减低肾替代治疗的风险。急性Stanford A型主动脉夹层患者的手术过程中所需体外循环时间较长,且常需要经历较长时间的深低温循环停止(deep hypothermic circulatory arrest, DHCA),因此术后AKI发生率较高[1-2]。目前临床通用的AKI诊断标准均基于肌酐(Serum creatinine, SCr)与尿量的变化,但SCr与尿量受血容量等多种因素影响,具有一定的局限性[3-4]。本研究通过对Stanford A型主动脉夹层术前、术后不同时点的肾叶间动脉血流动力学检测,分析血流动力学指标改变与AKI的关系,旨在寻找出预测AKI的超声血流动力学指标。
1 资料与方法
1.1 一般资料 连续收集2016年4月—7月在我院接受手术治疗的急性Stanford A型主动脉夹层患者41例。排除1例心律失常患者,共40例纳入本研究,男34例、女6例。急性Stanford A型主动脉夹层的外科手术方式为全主动脉弓替换+支架型人工血管植入术(孙氏手术),手术中需进行DHCA和选择性脑灌注(selective cerebral perfusion, SCP),手术后患者立即入住重症监护室(intensive care unit, ICU)。
1.2 仪器与方法 采用GE Vivid E9超声诊断仪及3~5 MHz脉冲波多普勒探头[5]。分别在手术前1天、术后即刻(T0,进入ICU)、术后6 h(T6)、术后24 h(T24)、术后48 h(T48)进行超声检查。二维超声显示肾脏后,在肾门纵向切面,以彩色多普勒成像定位肾叶间动脉,于肾柱两侧叶间动脉的中间部分取样,采用脉冲多普勒测量肾叶间动脉收缩期峰值流速 (peak systolic velocity, PSV)、舒张期最小流速 (end diastolic velocity, EDV)、搏动指数(pulsative index, PI)、阻力指数 (resistive index, RI),血流与声束的夹角<30°(图1)。同时记录SCr,术后48 h内每隔6 h测量尿量。所有数据均为3次测量的平均值。所有指标计算均为双侧肾脏的平均值。
根据AKIN分类标准[6][SCr增加0.3 mg/dL(即26.4μmol/ L)或从基线增加150%~200%,或尿量<0.5 ml/(kg·h)超过6 h,诊断为AKI]将患者分AKI组和无AKI组。记录以下指标:性别、年龄、体质量指数(body mass index, BMI)、有无高血压、糖尿病、马凡综合征,吸烟、饮酒情况及平均动脉压(mean arterial pressure, MAP)。记录手术细节情况,如手术时长、体外循环(cardiopulmonarybypass, CPB)持续时间、主动脉夹钳DHCA时间及术中尿量。到达ICU后,记录MAP、心率(heart rate, HR)、CO2分压(PaCO2)、射血分数(ejection fraction, EF)、肾替代治疗(continuous renal replacement therapy, CRRT)及住院时长和入住监护室时长。

图1 患者男,37岁,肾叶间动脉CDFI和血管频谱图 A.术前肾功能正常; B.术后6 h发生急性肾损伤
1.3 统计学分析 采用SPSS 20.0统计分析软件。数据以±s或百分比表示。采用两独立样本t检验或χ2检验比较两组患者一般资料及超声指标。相关性分析采用Pearson相关性检验。P<0.05为差异有统计学意义。
2 结果
40例患者中,AKI组27例,无AKI组13例。AKI组患者术中尿量少于无AKI组(P=0.018);术后AKI组MAP低于无AKI组(P=0.011);AKI组监护室时长多于无AKI组(P=0.034),见表1。两组肾叶间动脉血流PSV、EDV、PI、RI比较见表2,术后6、24 h无AKI组与AKI组患者肾叶间动脉EDV、PI、RI差异有统计学意义(P均<0.05)。肾叶间动脉PSV与SCr无相关性(r=-0.310,P=0.055),EDV与SCr呈负相关(r=-0.508、P=0.001);PI、RI与SCr呈正相关(r=0.411、0.443,P=0.009、0.005)。
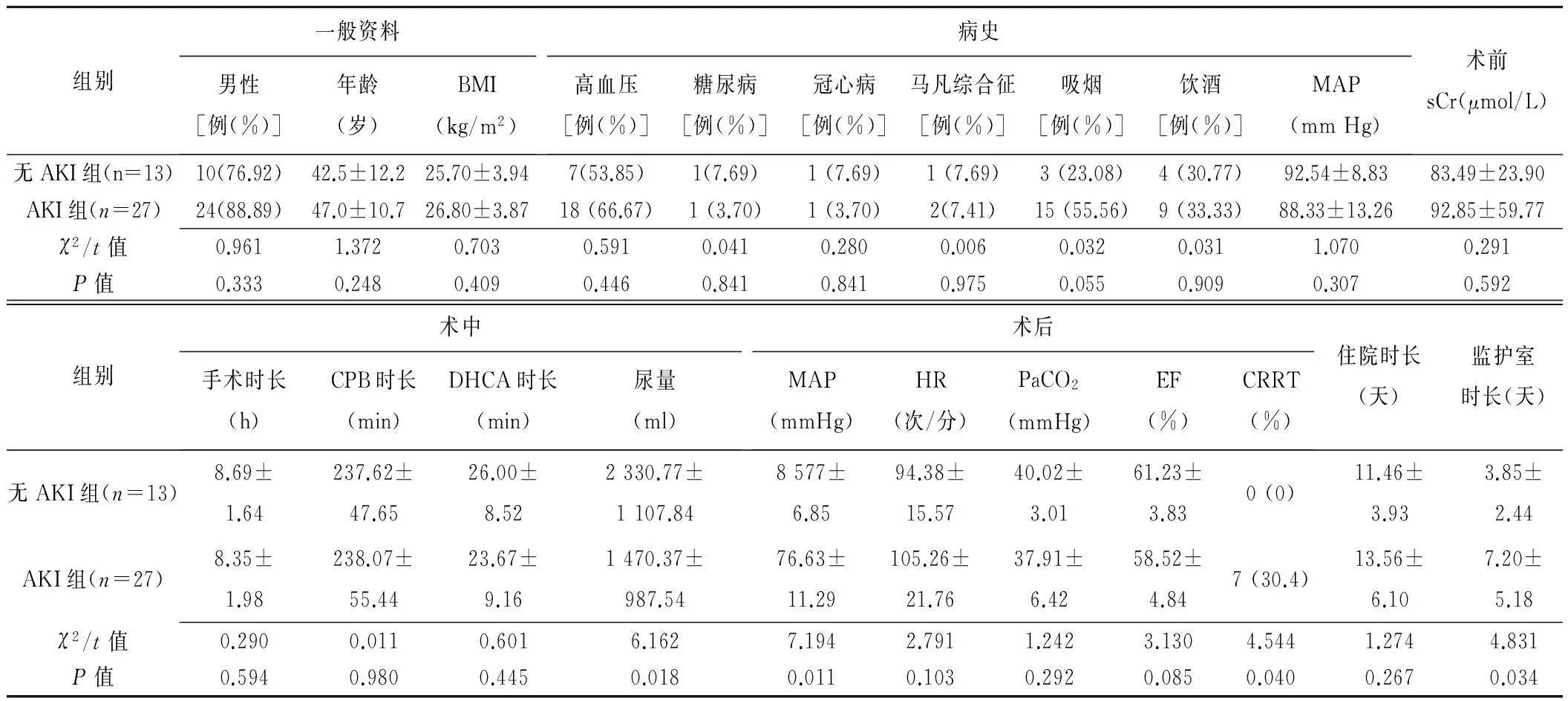
表1 AKI 和 无AKI 组患者的一般资料及术中、术后指标比较
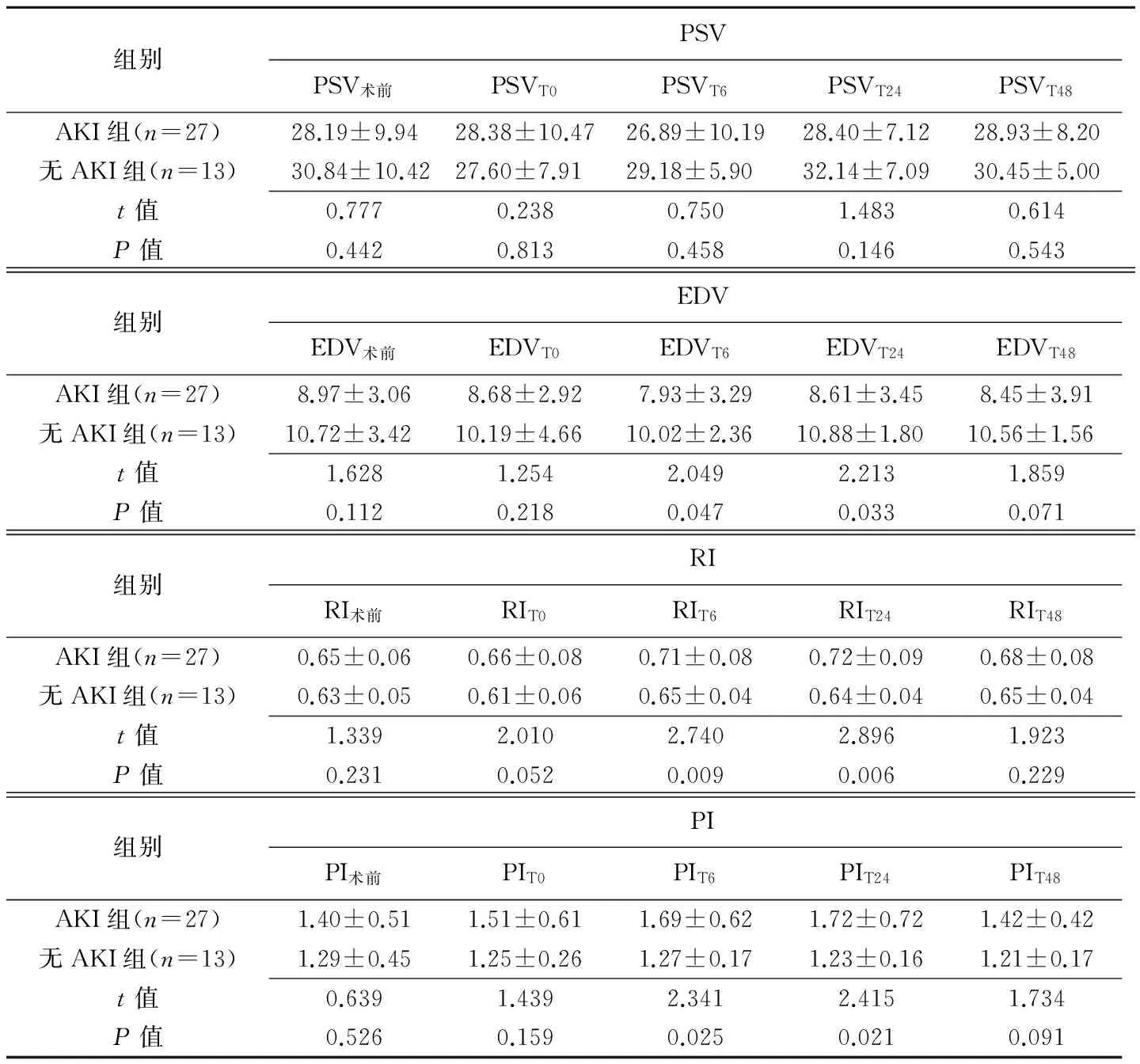
表2 AKI组与无AKI组的不同时点叶间动脉PSV、EDV、PI、RI比较(cm/s)
3 讨论
本研究结果显示AKI和无AKI两组患者术前基本资料差异无统计学意义, AKI组术中尿量少于无AKI组,术中尿量的减少可能是AKI发生的预兆,术后AKI组MAP低于无AKI组,差异有统计学意义。研究[7]表明,术后MAP<60 mmHg 超过1 h,导致心输出量急剧下降,肾脏灌注压下降,肾脏皮质缺血缺氧,即可导致AKI。
肾叶间动脉PSV、EDV主要反映肾血流的供应程度。本研究中,PSV在两组间差异无统计学意义,而EDV在术后6 h、24 h两组间差异均有统计学意义,AKI组明显低于无AKI组,提示EDV对于AKI预测较PSV更敏感。当心输出量降低、肾脏血供减少时,多普勒频谱显示舒张期血流速度明显降低[8]。急性Stanford A型主动脉夹层手术影响肾功能的重要原因是心输出血量减少和在手术过程中较长时间的肾脏血流低灌注状态,而术后假腔相对低供血灌注也是影响因素之一。Pearson相关分析表明肾叶间动脉PSV与肾功能指标SCr无相关性,EDV与SCr呈负相关,因此认为肾叶间动脉的EDV是预测AKI发生的敏感指标,这与以往研究结果一致[9]。
肾叶间动脉PI=(PSV-EDV)/MV,RI= (PSV-EDV)/PSV,MV为平均流速(mean velocity),此指标反映动脉某一横断面的顺应性和血流阻力。Cicoira等[10]通过对慢性肾功能衰竭患者随访6个月发现肾血流PI是肾功能下降的独立预测指标。尽管AKI的特征是由于管状损伤导致的肾小球滤过率减少,其本质上意味着血液动力学调节潜在的损害。这可能是因为AKI早期肾输出血管发生收缩、输入血管扩张,为保护肾血流和肾小球滤过率,在低血流量条件下,肾滤过压、滤过分数提高,从而起到保护肾功能作用;而在血流量严重降低的情况下,肾内血流代偿失衡,从而出现肾功能不全。通常,AKI的反应是肾血管阻力的持续增加[11],RI是AKI的显著标记。本研究中,AKI患者PI、RI在术后6 h、24 h均显著增高,Pearson相关分析表明肾叶间动脉PI、RI均与肾功能指标SCr呈正相关,因而PI、RI是早期预测AKI发生的可靠指标。
本研究中,AKI组患者肾叶间动脉EDV、PI、RI均在术后6 h及24 h与无AKI组差异有统计学意义,且与SCr具有相关性,因此认为术后6 h、24 h是超声测量肾叶间动脉血流动力学指标预测肾损伤的最佳时间。
总之,多普勒超声能够快速成像,且可灵活移动,同时具有无创、操作简单的特点,相比其他影像学检查如CT、MRI,更适合监护室床边操作。且超声可以短期重复评估肾血流,因此超声多普勒检查是一种重要的临床诊断肾功能损害的工具,同时也是早期检测AKI的准确、敏感的方法[12]。
[1] Hobson CE, Yavas S, Segal MS, et al. Acute kidney injury is associated with increased long-term mortality after cardiothoracic surgery. Circulation, 2009,119(18):2444-2453.
[2] Kim MY, Jang HR, Huh W, et al. Incidence, risk factors, and prediction of acute kidney injury after off-pump coronary artery bypass grafting. Ren Fail, 2011,33(3):316-322.
[3] Bagshaw SM, Gibney RT. Conventional markers of kidney function. Crit Care Med, 2008,36(4 Suppl):S152-S158.
[4] Carvounis CP, Guro-Razuman S. Significance of the fractional excretion of urea in the differential diagnosis of acute renal failure. Kidney Int, 2002,62(6):2223-2229.
[5] Marty P, Szatjnic S, Ferre F, et al. Doppler renal resistive index for early detection of acute kidney injury after major orthopaedic surgery: A prospective observational study. Eur J Anaesthesiol, 2015,32(1):37-43.
[6] Mehta RL, Kellum JA, Shah SV, et al. Acute kidney injury network: Report of an initiative to improve outcomes in acute kidney injury. Crit Care, 2007,11(2):R31.
[7] Fischer UM, Weissenberger WK, Warters RD, et al. Impact of cardiopulmonary bypass management on postcardiac surgery renal function. Perfusion, 2002,17(6):401-406.
[8] 孙卓贵,刘立静.糖尿病肾病的彩色多普勒超声诊断价值.中国超声诊断杂志,2005,6(11):868-869.
[9] 李明星,刘慧,付勇,等.CDFI检测肾血流PSV、EDV改变与CPB术后AKI相关性研究.中国临床医学影像杂志,2013,24(11):784-787.
[10] Cicoira M, Conte L, Rossi A, et al. Renal arterial pulsatility predicts progression of chronic kidney disease in chronic heart failure patients. Int J Cardiol, 2013,167(6):3050-3051.
[11] Tublin ME, Bude RO, Platt JF. Review. The resistive index in renal Doppler sonography: Where do we stand? AJR Am J Roentgenol, 2003,180(4):885-892.
[12] Darmon M, Schortgen F, Vargas F, et al. Diagnostic accuracy of Doppler renal resistive index for reversibility of acute kidney injury in critically ill patients. Intensive Care Med, 2011,37(1):68-76.
消息
《中国介入影像与治疗学》网站的域名为www.cjiit.com,作者投稿请登录本刊网站(www.cjiit.com)主页,点击左上角“作者登录”进入,第一次投稿需完成作者注册;专家审稿请点击“审稿登录”进入。
为了便于广大作者、读者查阅本刊文献,本站提供从2004年起的过刊和现刊的全文检索。
ChangesofrenalinterloburarteryhemodynamicsinacuterenalinjuryafteroperationofacuteStanfordAaorticdissection
QINHuai1,WUHaibo2,CHENGYi1,FANZhanming3*
(1.DepartmentofUltrasond, 2.DepartmentofCardiacSurgery, 3.DepartmentofMedicalImaging,BeijingAnzhenHospital,CapitalMedicalUniversity,Beijing100029,China)
ObjectiveTo explore the changes of hemodynamics in acute kidney injury (AKI) after acute severe Stanford type A aortic dissection.MethodsForty patients with acute Stanford A type aortic dissection were enrolled. Arterial peak systolic velocity (PSV), end diastolic velocity (EDV), pulsative index (PI), resistive index (RI), Serum creatinine (SCr) and urine volume were recorded and measured 1 day before operation, immediately after operation (enter the intensive care unit), 6 h after operation, 24 h after operation and 48 h after operation. Patients were divided into AKI group and non-AKI group taking AKIN as a standard.ResultsTwenty-seven patients were in AKI group and 13 were in non-AKI group. The EDV, PI and RI had significantly differences between AKI group and non-AKI group at 6 h, 24 h after operation. Correlation analysis showed that EDV negatively correlated with SCr (r=-0.508,P=0.001), while PI, RI positively correlated with SCr (r=0.411, 0.443,P=0.009, 0.005).ConclusionEDV, PI and RI in the interlobular arteries can be used to predict AKI early in the interosseous arteries, and the optimal time for ultrasonic measurement of renal arterial hemodynamics to predict is at 6 h and 24 h after operation.
Acute renal injury; Aneurysm, dissecting; Ultrasonography
R691.5; R445.1
A
1672-8475(2017)10-0623-04
秦淮(1976—),女,山西霍州人,博士,副主任医师。研究方向:血管疾病超声及肾损伤超声。E-mail: qxbkwy@163.com
范占明,首都医科大学附属北京安贞医院影像科,100029。E-mail: fanzm120@tom.com
2017-06-02
2017-09-14
10.13929/j.1672-8475.201706003
