富锂材料Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)的制备及性能研究
2017-10-17彭庆文刘兴江
彭庆文,刘兴江
(中国电子科技集团公司第十八研究所化学与物理电源重点实验室,天津300384)
富锂材料Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)的制备及性能研究
彭庆文,刘兴江
(中国电子科技集团公司第十八研究所化学与物理电源重点实验室,天津300384)
锂离子电池富锂层状正极材料因具有超高的比容量,引起了极大的关注。依据材料相图进行富锂材料的设计、制备及性能研究。采用醋酸盐燃烧法制备了锂离子电池富锂层状正极材料Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1),应用原子吸收光谱(AAS)和电感耦合等离子体发射光谱(ICP-OES)对材料进行了成分分析,采用X射线多晶衍射(XRD)、扫描电子显微镜(SEM)对材料进行了结构和形貌分析,并对材料的电化学性能进行了测试分析。研究表明所制备的五种富锂正极材料均为层状α-NaFeO2结构,随着x数值的逐渐减小,富锂材料Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)的首次放电比容量逐渐增大,循环性能逐渐提高。
锂离子电池;富锂材料;Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2
Abstract:Lithium-rich layered cathode material had drawn much attention due to its extraordinarily high capacity.Lithium-rich material was designed according to phase diagram.Lithium-rich layered cathode material Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)was prepared by acetate combustion method.The Li,Ni,Co and Mn contents in the samples were determined by atomic absorption spectrum(AAS)and inductive coupled plasma optical emission spectrometry(ICP-OES).X-ray diffraction(XRD)and scanning electron microscopy(SEM)were carried out to analyze the structure and morphology of Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1).The electrochemical properties of the samples were also studied.The research results show that all the five lithium-rich layered materials are α-NaFeO2structure.The charge-discharge tests of Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)show that the first discharge capacity and the cycleability are improved with the value ofxdecreasing.
Key words:lithium-ion battery;lithium-rich materials;Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2
锂离子电池具有质量轻、能量高、功率大、充放电效率高、无记忆效应、自放电小、使用寿命长、工作温度范围宽等特点,问世以来,发展迅速,应用广泛。目前锂离子电池在3C数码类消费电子产品及纯电动车(EV)、混合动力车(HEV)等领域,占有绝对的主导地位。而随着消费类电子产品日益强大的功能需求及电动车对长续驶里程的渴求越来越强烈,作为它们能量之源的锂离子电池急需提高自身的比能量,而锂离子电池比能量的高低主要取决于其正极材料比容量的大小。目前已经商业化应用的锂离子电池正极材料钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、磷酸铁锂(LiFePO4)以及三元材料(NMC)等的比容量均小于200mAh/g,因此为了满足未来纯电动车及混合动力车的发展要求,需要研究开发具有更高比容量的新型锂离子电池正极材料。近年来,锂离子电池富锂层状正极材料因具有超高的比容量[1-3]而广受关注。这种富锂层状正极材料可以用通式 Li1+xM1-xO2(M=Ni,Co,Mn)来表示,具有大于 200mAh/g的比容量。
本文从构建的锂离子电池正极材料相图出发,进行富锂层状正极材料的设计,应用醋酸盐燃烧法合成制备富锂正极材料 Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1),并对这些材料的相关性能进行了研究。
1 材料设计
富锂正极材料 Li1+xM1-xO2(M=Ni,Co,Mn) 也可以用xLi2MnO3·(1-x)LiMO2(M=Ni,Co,Mn)来表示,即可以把富锂正极材料看作是Li2MnO3与LiMO2形成的固溶体材料。由于相图具有简洁、直观的优点,应用到锂电正极材料的设计上,可让研究人员更好地理解材料的构成及相关性能的变化。在前期研究工作中我们建立了Li2MnO3-LiMnO2-LiNiO2-LiCoO2四元相图,如图1所示,研究了锂离子电池富锂正极材料三角相图,如图1中红 (Li1.2Ni0.2Mn0.6O2)、绿 (Li1.2Ni0.4Mn0.4O2)、蓝(Li1.2Co0.4Mn0.4O2)三点组成的三角相图,如图2中底边的五种富锂正极材料 Li1.2(Ni0.4Mn0.4)x(Co0.4Mn0.4)1-xO2(0≤x≤1)[4]的相关性能。本文按照设计的比例合成制备三角相图中Li1.2Ni0.2Mn0.6O2和Li1.2Ni0.4Mn0.4O2所在的左边线的五种固溶体材料 Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(x=0、0.25、0.5、0.75、1)。

图1 LiNiO2-LiCoO2-LiMnO2-Li2MnO3四元空间立体相图
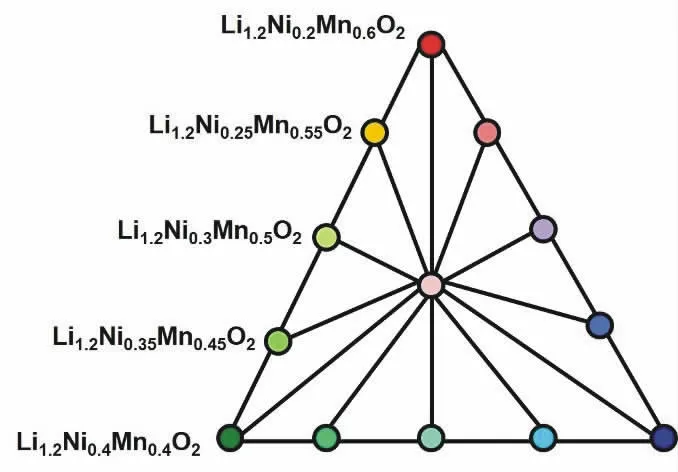
图2 富锂三角相图中左边五种材料的分布
2 实验
2.1 样品的合成
实验采用二水合乙酸锂、四水合乙酸镍和四水合乙酸锰为起始原材料,制备合成目标材料样品Li1.2(Ni0.4Mn0.4)x-(Ni0.2Mn0.6)1-xO2(x=0、0.25、0.5、0.75、1)。首先按照设计的比例分别称取三种原材料进行混合,混合均匀后在空气气氛下使用马弗炉450℃下恒温降解3 h,停止加热,随炉温自然冷却后将燃烧后的粉体材料加入到玛瑙球磨罐中,加入适量酒精湿法球磨1 h,然后在鼓风干燥箱中干燥,将干燥后的粉体材料转至马弗炉中,于900℃下恒温煅烧8 h,停止加热,随炉温自然冷却后经研磨、过筛得到五种富锂正极材料样品。
2.2 材料的表征
采用Thermo SOLLAAR M6型原子吸收光谱仪 (AAS)分析测定五种富锂正极材料样品中金属元素Li的含量,应用Thermo ICAP6300型电感耦合等离子体发射光谱仪(ICP-OES)分析测定五种材料样品中金属元素Ni和Mn的含量。采用日本理学D/MAX-2500型辐射衍射仪(XRD)测试分析五种材料样品的晶体结构[CuKα辐射,管流100 mA,管压40 kV,扫描范围 (2θ)10°~80°]。应用日立S-4800扫描电子显微镜(SEM)观察分析五种材料样品形貌及颗粒大小。
2.3 电化学性能测试
将五种富锂正极材料样品作为正极材料,分别组装成CR2430型扣式电池进行电化学性能的测试研究。按照质量比85∶10∶5的比例分别称取正极活性材料、导电剂(SP)、粘结剂(PVDF),混合均匀成为正极浆料,然后将浆料均匀涂布在铝箔上,经干燥、辊压、冲片得到正极极片,选用金属锂作为负极,Celgard2300作为隔膜,1mol/L的LiPF6/(EC+DEC+DMC)(体积比为1∶1∶1)作为电解液,在高纯氩气氛围的手套箱中组装完成测试用扣式电池。应用Arbin Instruments BT2000充放电仪作为本实验的充放电设备,测试环境温度为25℃,充放电制度采用恒流充放电,电流为20 mA/cm2,电压范围为2~4.8 V。
3 结果与讨论
3.1 XRD物相结构分析
图3是所合成的五种富锂正极材料样品Li1.2(Ni0.4Mn0.4)x-(Ni0.2Mn0.6)1-xO2(0≤x≤1)(x=0、0.25、0.5、0.75、1)的XRD曲线。从图3的衍射图谱分析可以知道,实验制备合成的五种材料样品均具有α-NaFeO2层状结构,属于R-3m空间群。每种样品的XRD衍射图谱均具有尖锐的衍射峰,无杂质峰,为规整固溶体材料。图3中每种样品的(006)/(102)和(108)/(110)这两组衍射峰均呈现明显分离,这一现象表明每种样品的层状结构规整度高。图3中五种样品的XRD曲线上在20°~28°区间都可以观察到一些锯齿峰,而这些锯齿峰出现的位置及形貌与Li2MnO3的衍射峰相近[5]。Li2MnO3属单斜晶系,C2/m空间群,为层状岩盐结构,在其晶体结构中八面体金属离子层和氧离子层交叠排列。其八面体金属离子层的晶格点被Li和[Li1/3Mn2/3](Li+和Mn4+的摩尔比为1∶2)分别占据,由于过渡金属层间阳离子Li+和Mn4+的混排效应而引起超晶格结构,致使其XRD衍射图谱上在20°~28°范围内出现了锯齿峰。如果金属离子层中的[Li1/3Mn2/3]被Ni2+离子取代,就会导致Li和Mn元素之间原有1∶2的摩尔比例失衡,另外由于Li+离子与Ni2+离子的电荷之差小于Li+离子与Mn4+离子的电荷之差,因此XRD图谱上的超晶格结构峰将随着Ni含量的增加而逐渐变得平缓。图3显示五种实验所得样品或多或少的都存在超晶格结构峰,随着x数值从0到1的增大,对应着样品中Ni含量的增加,XRD曲线的超晶格结构峰也由尖锐逐渐变得平缓,这一实验结果正好验证了上述理论分析。
3.2 SEM形貌分析
图4是实验制备的锂离子电池富锂正极材料Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2当x=0 时,即 Li1.2Ni0.2Mn0.6O2的SEM形貌图,从电镜图中可以看到样品材料是由尺寸为1 μm左右的微晶颗粒团聚而成的二次颗粒组成的,这些二次颗粒的粒径约 5~10 μm。其他四种富锂材料 Li1.2Ni0.25Mn0.55O2、Li1.2Ni0.3Mn0.5O2、Li1.2Ni0.35Mn0.45O2、Li1.2Ni0.4Mn0.4O2的SEM形貌图与Li1.2Ni0.2Mn0.6O2的相似,此处不再分别列出。
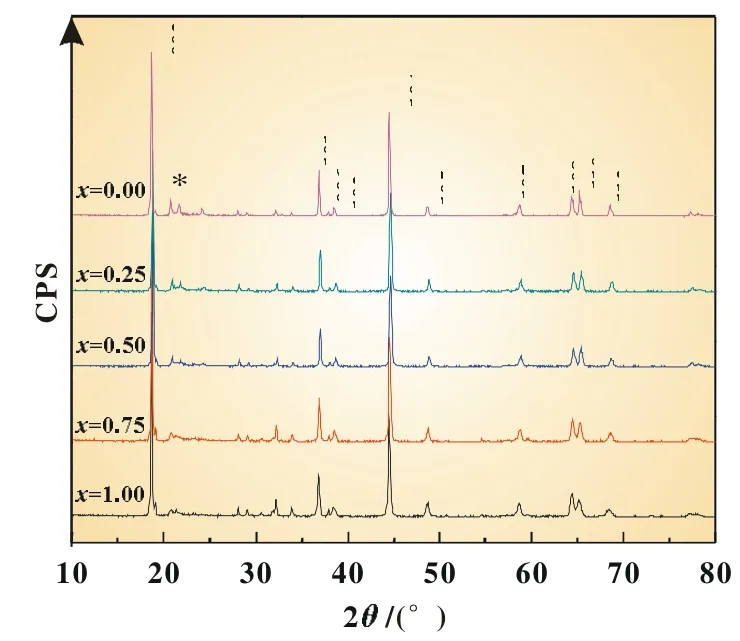
图3 Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)的XRD曲线

图4 Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(x=0)的SEM形貌图
3.3 电化学性能
图5是所得样品材料Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(x=0)即Li1.2Ni0.2Mn0.6O2的前2次充放电曲线,其它4种富锂正极材料样品的前2次充放电曲线与Li1.2Ni0.2Mn0.6O2的形状上是一样的,不再分别给出。从图5中可见Li1.2Ni0.2Mn0.6O2样品材料的首次充电曲线在达到4.5 V之前一直是平滑上升的,与之对应的是Ni2+逐渐被氧化为Ni4+[6]。当电压大于4.5 V之后,首次充放电曲线上出现了一个较长的电压平台,但却没有与之对应的放电平台出现在其放电曲线上,而且这个4.5 V充电平台在后续循环充电过程中消失了。这主要是因为4.5 V这个富锂正极材料的特征充电平台是其电化学活化过程,确切地说是电化学惰性的Li2MnO3向电化学活性的MnO2的转变过程。在这一充电过程中,晶格中O2-伴随着Li+一起脱出,并形成Li2O,而生成的MnO2不仅参与后续的充放电过程,还可以起到稳定晶格结构的作用。O2-和Li+一起从富锂正极材料体相中脱出后会留下空位,此时位于材料表面的金属离子为了实现电荷平衡就会迁移到体相中去占据空位,导致原空位消失,从而致使在放电过程中原来脱出的Li+由于没有足够的空位而不能全部嵌回到富锂正极材料中去,这就形成了较大的首次不可逆容量损失,首次充放电效率较低。此外,注意到图5中的首次充电曲线和第二次充电曲线之间有较大的落差,即存在较大的电压降,比如选取均充电至50mAh/g的容量时,首次充电曲线对应的电压是4.16 V,而第二次充电曲线对应的电压就变为3.77 V。图6是五种富锂正极材料样品的前50次循环性能曲线,从图6中可见随着x数值的变小,Li1.2-(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)对应的样品材料的首次放电比容量从143mAh/g增大到245mAh/g,循环性能也得到了显著改善。五种材料样品的第50次循环的容量保持率由46%增大到90%,见图7所示。

图5 Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(x=0)的前2次充放电曲线

图6 Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)的循环曲线

图7 Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)第50次循环容量保持率
4 结论
本文制备合成了位于锂离子电池富锂正极材料Li1.2Ni0.2Mn0.6O2、Li1.2Ni0.4Mn0.4O2和 Li1.2Co0.4Mn0.4O2三种材料构成的三角相图左边线的五种富锂正极材料Li1.2(Ni0.4Mn0.4)x-(Ni0.2Mn0.6)1-xO2(x=0、0.25、0.5、0.75、1),并对其相关性能进行了研究。研究表明所获得的五种富锂材料样品均为规整的固溶体材料,随着通式中x数值的变小,Li1.2(Ni0.4Mn0.4)x-(Ni0.2Mn0.6)1-xO2材料的首次放电比容量及循环性能均得到提高改善,尤其是Li1.2Ni0.2Mn0.6O2材料首次放电比容量达到245mAh/g,50次循环的容量保持率为90%,是一种很有前景的锂离子电池富锂正极材料。
[1]THACKERAY M M,KANG S H,JOHNSON C S,et al.Li2MnO3-stabilized LiMO2(M=Mn,Ni,Co)electrodes for lithium-ion batteries[J].Journal of Materials Chemistry,2007,17:3112-3125.
[2]JIN S J,PARK K S,CHO M H,et al.Effect of composition change of metals in transition metal sites on electrochemical behavior of layered[Co1-2x(Li1/3Mn2/3)x(Ni1/2Mn1/2)x]O2solid solutions[J].Solid State Ionics,2006,177:105-112.
[3]ZHANG L Q,TAKADA K,OHTA N,et al.Synthesis of(1-2x)Li-Ni1/2Mn1/2O2·xLi[Li1/3Mn2/3]O2·xLiCoO2(0≤x≤0.5)electrode materials and comparative study on cooling rate[J].Journal of Power Sources,2005,146:598-601.
[4]彭庆文,卢志威,任丽彬,等.Li1.2(Ni0.4Mn0.4)x(Co0.4Mn0.4)1-xO2(0≤x≤1)系列富锂材料的制备及性能研究[J].电源技术,2013,37(3):354-357.
[5]HONG Y S,PARK Y J,RYU K S,et al.Charge/discharge behavior of Li[Ni0.20Li0.20Mn0.60]O2and Li[Co0.20Li0.27Mn0.53]O2cathode materials in lithium secondary batteries[J].Solid State Ionics,2005,176(11/12):1035-1042.
[6]PENG Q W,TANG Z Y,ZHANG L Q,et al.Synthesis of layered Li1.2+x[Ni0.25Mn0.75]0.8-xO2materials(0≤x≤4/55)via a new simple microwave heating method and their electrochemical properties[J].Materials Research Bulletin,2009,44:2147-2151.
Synthesis and characterization of lithium-rich Li1.2(Ni0.4Mn0.4)x(Ni0.2Mn0.6)1-xO2(0≤x≤1)
PENG Qing-wen,LIU Xing-jiang
(Science and Technology on Power Sources Laboratory,Tianjin Institute of Power Sources,Tianjin 300384,China)
TM 912.9
A
1002-087X(2017)09-1248-03
2017-03-12
彭庆文(1982—),男,河北省人,高级工程师,博士,主要研究方向为锂电池及相关材料。
