还原型谷胱甘肽治疗妊娠期肝功能异常63例
2017-10-17张秋英马金春
张秋英 马金春
湖北省黄石市爱康医院消化内科 (湖北 黄石, 43500)
还原型谷胱甘肽治疗妊娠期肝功能异常63例
张秋英 马金春△
湖北省黄石市爱康医院消化内科 (湖北 黄石, 43500)
妊娠期发生的肝功能损害(异常),统称为妊娠期肝病,有报道妊娠期肝病的发病率约为3%~5%[1]。
妊娠期合并肝功能损害,临床用药不仅考虑其疗效,而且更应该注意孕妇及胎儿安全性。还原型谷胱甘肽(GSH)是人类细胞质中自然合成的一种肽,由谷氨酸、半胱氨酸和甘氨酸组成,广泛分布于机体各器官内,主要起维持细胞生物功能的作用,无明显生殖毒性。现将笔者应用该药治疗妊娠期肝功能异常63例情况报告如下。
1.资料和方法
1.1 一般资料 收集2012年1月至2015年1月在本院门诊及住院的妊娠期肝功能异常患者124例,孕早期15例,包括2例甲状腺功能亢进患有,服药维持甲状腺功能正常;孕中期89例;孕晚期20例,孕中晚期病例均无其他基础疾病。按照就诊先后顺序根据随机数字表分为治疗组63例,年龄19~38岁,平均25.8岁;对照组61例,年龄20~40岁,平均26.5岁。两组患者病情、病程、年龄、妊娠周数等比较,差异无统计学意义(P>0.05),具有可比性。
1.2 诊断及排除标准 根据陈灏珠主编《实用内科学》及王淑贞主编《实用妇产科学》诊断标准:凡妊娠期间出现胆红素和/或转氨酶、胆汁酸异常升高者均视为肝功能异常[1,2]。肝功能损害(异常)诊断:①B超确认患者妊娠,且胎儿无畸形;②ALT和(或)AST水平在正常值上限(ULN)3~10倍之内,不超过10倍。血清总胆红素、凝血功能在正常范围。③腹部彩超检查肝、胆、脾、胰均未见其他异常。并需排除以下情况①妊娠急性脂肪肝。②艾滋病毒阳性、梅毒阳性。③各种原因导致的急、慢性重型肝炎,肝硬化。④恶性肿瘤以及其他严重性疾病或感染性疾病。
1.3 治疗方法 妊娠期患者属于特殊人群,治疗前首先就治疗方案与患者充分沟通并知情同意。治疗组患者给予还原型谷胱甘肽注射液(重庆药友制药有限责任公司)1.2g/次,静脉滴注,1次/d;对照组患者予肌酐注射液0.6g/次,静脉滴注,1次/d,其他基础治疗均相同。均以4W为1个疗程,共治疗1个疗程,4W后肝功能未恢复正常者,继续治疗,但不纳入统计范围。1.4 观察指标及方法 观察孕妇血清生化指标ALT、AST;肝功能复常率孕妇不良反应及胎儿出生的情况。两组患者均于治疗后1w、2w、4w时复查肝功能。治疗1w时复查肝功能若提示ALT或和AST上升30%以上或有重症趋势,则联合其他护肝降酶药物治疗,此病例作为无疗效病例提前终止研究,按脱落病例处理,其他情况的患者则继续治疗。合并慢性乙型肝炎的患者按《慢性乙型肝炎防治指南》诊治。所有患者,均应查明肝功能损害的病因,采取标本兼治。两组患者均建议低脂饮食,注意卧床休息。
1.5 疗效判定 显效:临床症状消失,ALT、AST降至正常水平。有效:临床症状有改善,ALT、AST下降至治疗前的50%,但未恢复正常。无效:治疗后肝功能指标无明显变化,或改善未达到上述显效及有效的标准。
1.6 统计学方法 计量资料采用均数±标准差表示,进行重复测量数据方差分析,每个分组每个时间点均值的两两比较采用重复测量数据多重比较配对的t检验法,基线数据间比较用独立样本的t检验,计数资料用率表示,组间比较用χ2检验。均通过SPSS17.0统计软件完成。统计检验为双侧检验,P<0.05为差异具有显著性意义。
2.结果
2.1 两组患者临床症状变化 两组患者治疗后临床症状均有改善。特别是乏力、易疲劳、饮食情况较治疗前均有不同程度的改善。
2.2 两组患者血清生化学指标变化情况 见表1。
表1 两组患者肝功能结果比较
2.3 两组患者疗效情况 见表2
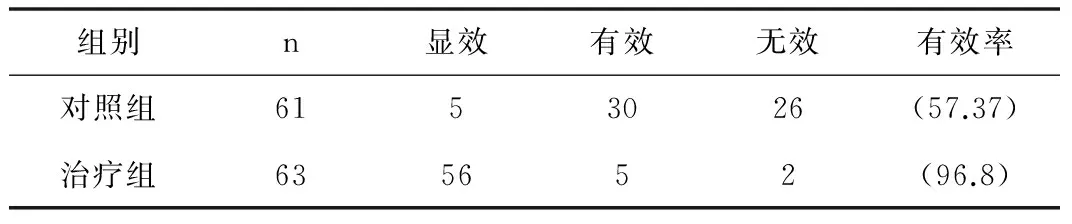
表2 两组患者疗效比较 [n(%)]
2.4 两组孕妇的新生儿安全指标情况 见表3。
妊娠期间,患者胎心监护检查均具有反应性,胎心、胎动良好。新生儿出生质量,身长、早产率、Apgar评分(1min)等方面均在正常新生儿范围内,且两组新生儿出生时上述安全指标差异无统计学意义(P>0.05)。

表3 两组孕妇的新生儿安全指标比较
2.5 不良反应 治疗期间,两组均未发生明显副反应。
3.讨论
妊娠期合并肝功能损害是临床常见疾病,可发生在妊娠早、中、晚期。患者往往由于肝功能受损,凝血因子合成减少,产前、产时、产后出血机会增加,蛋白质合成减少,对胎儿产生不良影响,严重者甚至危及母婴生命,病死率也高于非孕期[1]。笔者观察肝功能损害的妊娠患者早期15例,中期89例,晚期20例。其中妊娠中期最多,发生原因可能与在中期孕妇进食量增大,三大物质代谢加强,类固醇增多以及激素分泌紊乱加重肝脏负担有关。
目前临床上常用的护肝降酶的药物种类繁多,治疗机制各不相同,均未标明妊娠期用药的安全性。但临床实际中,医生在妊娠期用药还必须考虑对胎儿的安全性,药物选择非常有限。GSH是体内存在的生物活性肽,肝细胞代谢及三羧酸循环过程中多个关键酶类的辅酶,能够促进肝细胞的代谢、合成过程,能够减轻肝细胞的能量代谢障碍[3]。外源性谷胱甘肽有利于提高肝细胞内谷胱甘肽的含量,促进肝细胞的修复,同时其还原作用能够防止过氧化物在细胞内蓄积引起肝细胞继发性损伤,发挥对肝细胞的保护作用[4]。还有研究表明,抗氧化剂谷胱甘肽在子宫基层影响巨噬细胞诱导性氧自由基的产生可以预防早产和死胎[5]。
本研究结果提示GSH适用于妊娠期合并肝功能损害的患者,既能有效恢复妊娠患者肝功能,又可以不影响胎儿发育。但本研究纳入病例有限,且缺乏长期随访资料,GSH治疗妊娠合并肝功能损害的确切疗效及安全性有待进一步积累更多、更科学的临床资料予以验证。对于妊娠期合并肝功能损害的患者选择护肝药物时,仍需谨慎评估风险与效益,需充分告知患者与家属,并签写知情同意书后再使用。
[1] 姚光弼.临床肝脏病学[M].上海:上海科学技术出版社,2011:593.
[2] 王淑贞.实用妇产科学[M].北京:人民卫生出版社,1993:326.
[3] 张汉平,李卫平,孟宪栋.还原型谷胱甘肽治疗药物性肝损害的临床疗效分析[J],河北医药,2010,32(2):3007-3008.
[4] 李志荃,张龙跃.甘草酸二胺联合还原型谷胱甘肽治疗病毒性肝炎80例疗效观察[J],中国基层医药,2009,15(1):100-101.
[5] Hadi T,Bardou M,Mace G,etal. Glutathione prevents preterm parturition and fetal death by targeting macrophage-induced reactive oxygen species production in the myometrium [J].FASEB J, 2015, 29(6):2653-2666.
2016-09-13,编辑:肖明中)
10.3969/j.issn.1005-0264.2017.01.022
△通信作者,E-mail:13581296598@163,com
