3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑的合成及光谱性质研究
2017-10-16李俊芬
李俊芬, 樊 鸽, 董 川
(1.山西大学化学化工学院,山西太原 030006;2.山西大学环境科学与工程研究中心,山西太原 030006)
近年来,对具有共轭结构的电荷转移化合物的光物理行为进行研究一直比较热门[1 - 3]。咔唑是有机含氮杂环化合物,具有类似共轭烯烃的结构。由于咔唑不仅具有比较好的电子传输性能和优良的光电性质,且易于引入各种功能基团进行修饰从而获得新功能材料,因此常常作为合成有机光电功能性化合物的原料[4 - 5]。2-甲基蒽醌富含电子且具有共轭烯烃结构,也常在合成染料、感光剂和光电材料方面有重要应用价值[6 - 7]。
双荧光现象是指化合物在极性溶剂中的荧光光谱呈现两个荧光带。该理论的实验基础是二甲基氨基苯腈(DMABA)及其衍生物的光物理性质的研究[8]。甲基取代物不同,DMABA在不同极性的溶剂中的荧光现象就不同,如邻位甲基取代物有一个荧光带,间位取代物存在两个荧光带。这种现象的产生还与其分子结构有关,对于邻位甲基取代的分子,由于甲基与甲基之间存在空间位阻效应,分子中电子给体二甲胺基和电子受体氰基苯基团之间趋向于垂直,形成扭曲的分子内电荷转移(TICT)态,原来的光诱导电荷转移(ICT)态荧光被淬灭,因此分子表现出单一的荧光带,而对于间位的甲基取代物,由于其空间位阻效应很小,分子受甲基的影响也不大,出现了ICT与TICT双重荧光现象[9]。
本文利用N-乙基咔唑作为电子给体,2-甲基蒽醌作为电子受体,合成了一种A-π-D-π-A分子内电荷转移型化合物3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑,并利用荧光光谱、核磁共振谱对该化合物的光物理及光化学性质进行了研究。该化合物的发光行为强烈地依赖于溶剂的极性,在强极性溶剂乙腈中出现了双荧光现象。电荷从咔唑基上的N原子转移到了两端蒽醌的羰基上,可以作为一种良好的光电材料。
1 实验部分
1.1 仪器与试剂
DRX-300超导核磁共振仪(德国,Bruker公司);F-4500荧光光度计(日本,Hitachi公司);SHZ-Ⅲ循环水式多用真空泵(杭州瑞佳精密科学仪器有限公司);SZCL-2型数显智能控温磁力搅拌器(巩义市予华仪器有限责任公司);X-5显微熔点测定仪(巩义市予华仪器有限责任公司)。
咔唑(化学纯,天津市光复精细化工研究所);2-甲基蒽醌(色谱纯)、四氢吡咯(化学纯,TCI化成工业发展有限公司);N,N-二甲基甲酰胺(分析纯,天津市星月化工有限公司);吡啶(分析纯,天津市光复科技发展有限公司);冰HAc、H3PO4、HCl (分析纯,北京化工厂);实验所用其它试剂均为分析纯(购自天津市福晨化学试剂厂)。
1.2 实验步骤
1.2.1N-乙基咔唑的合成[10 - 11]向250 mL的三口烧瓶中加入10 g咔唑和120 mL丙酮,用控温磁力搅拌器,设定温度为40 ℃,搅拌使咔唑充分溶解。向烧瓶中缓慢加入16 mL(约18.8 g)硫酸二乙酯,反应25 min后,冷却到室温,用恒压滴液漏斗向溶液中加入30 g NaOH和25 mL蒸馏水配成的浓度为54.5%的溶液,开启搅拌开关,转速设为800 r/min,反应20 min后,将其倒入装有约700 mL水的烧杯中,静置,有大量米白色絮状的物质析出,抽滤,干燥,用无水乙醇重结晶,得到白色的细针状晶体18.1 g,产率为76.3%,熔点为72~74 ℃。1H NMR(300 MHz,CDCl3),δ:8.1~7.1 (7H,Ar-H);4.3~4.2(2H,-CH2);1.4~1.3(3H,-CH3)。
1.2.2N-乙基咔唑-3,6-二甲醛的合成[12 - 13]在150 mL的圆底烧瓶中加入无水MgSO4干燥过的19 mL N,N-二甲基甲酰胺,将其置于冰水浴中,用恒压滴液漏斗将25 mL三氯氧磷缓慢滴加到圆底烧瓶中,再将5.0 g N-乙基咔唑溶解在8 mL用无水MgSO4干燥过的N,N-二甲基甲酰胺中,缓慢加入到圆底烧瓶中。把烧瓶转移到控温磁力搅拌器上,设定温度为100 ℃,反应约30 h后,停止加热和搅拌,冷却至室温。将溶液倒入大量水中,剧烈搅拌约2 h后,缓慢加入30 g NaOH溶液,再用NaHCO3调节pH到8左右,用400 mL二氯甲烷萃取,萃取液用蒸馏水洗至澄清,有机相用无水Na2SO4干燥,最后加入200~300目的适量硅胶,旋干,柱色谱分离提纯(展开剂:二氯甲烷∶乙酸乙酯=20∶1),最后得到黄色粉末状固体3.2 g,产率为49.7%,熔点为168~170 ℃。1H NMR(300 MHz,CDCl3),δ:10.139(2H,-CHO);8.6~7.2(6H,咔唑);4.4(2H,-CH2);1.4~1.5(3H,-CH3)。
1.2.33,6-二(蒽醌-2-乙烯基)-N-乙基咔唑的合成[14 - 15]将0.9 g 2-甲基蒽醌以及25 mL吡啶加入到200 mL的三口烧瓶中。N-乙基咔唑-3,6-二甲醛0.5 g,用15 mL吡啶搅拌至完全溶解,转移到20 mL的恒压滴液漏斗中,半小时内滴到三口烧瓶中,再滴加1 mL四氢吡咯,加上冷凝回流管,在90 ℃下反应38 h。向烧瓶中加入少量无水Na2SO4,静置后,把上清液转移到150 mL的单口烧瓶中,加入适量硅胶,旋干,柱色谱分离提纯(展开剂:石油醚∶乙酸乙酯=1∶3),最后得红棕色粉末状固体0.39 g,产率为32.4%,熔点为 188~190 ℃。1H NMR(300 MHz,CDCl3),δ:7.1(4H,-CH=CH-); 8.5~7.2 (20H,咔唑和蒽醌);4.4(2H,-CH2);1.41~1.38(3H,-CH3)。各步合成路线见图1。
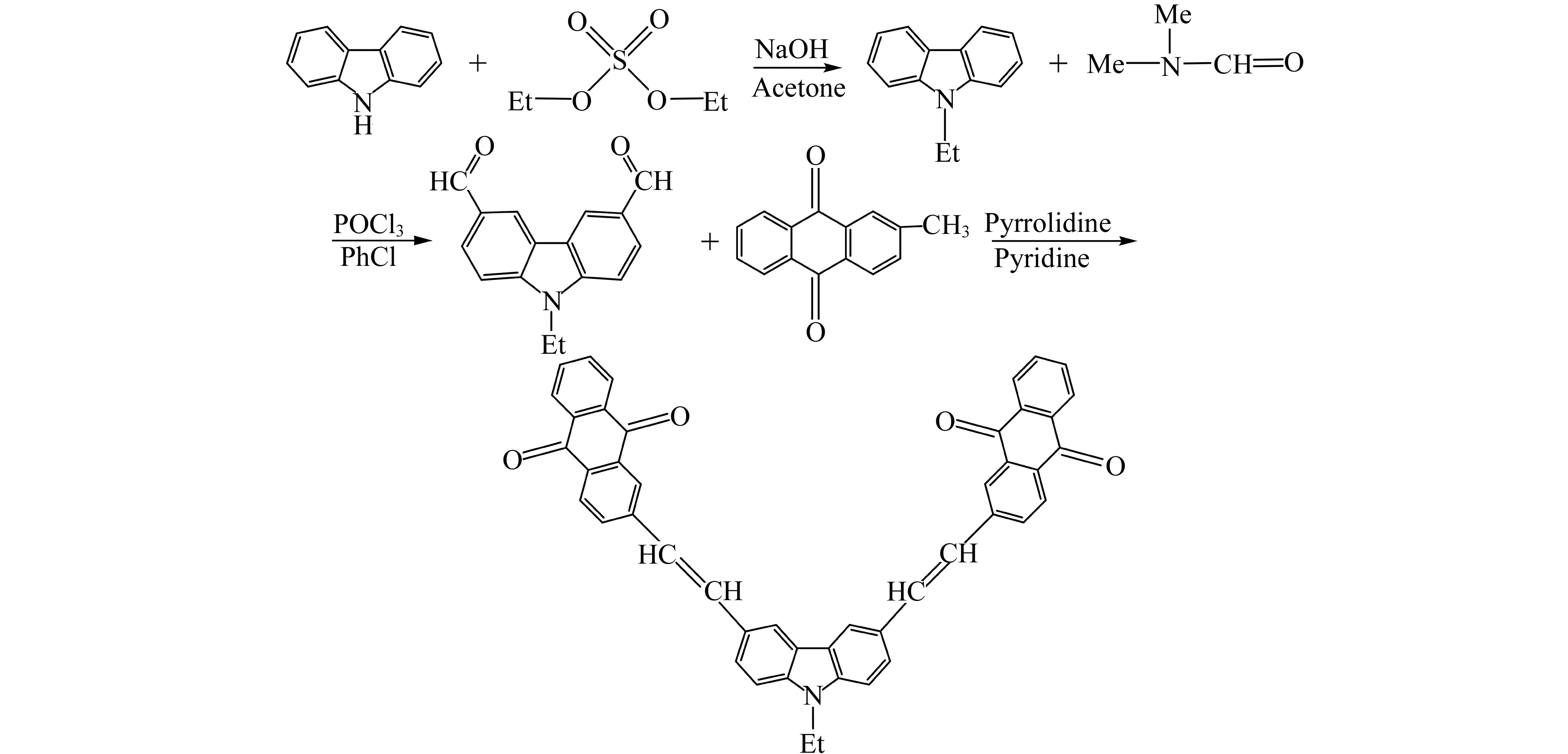
图1 3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑的合成路线Fig.1 Synthetic route of 3,6-bis(anthraquinone-2-vinyl)-N-ethyl-carbazole
2 结果与讨论
2.1 原料与产物的荧光光谱比较
原料N-乙基咔唑-3,6-二甲醛(1)和产物3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑(2)的激发光谱和发射光谱分别见图2a和2b。由图2可见,原料的最大激发峰在320 nm左右,最大发射峰在451 nm左右;产物的最大激发峰在368 nm左右,最大发射峰在530 nm左右,二者的Stokes位移分别是131 nm和162 nm;产物荧光光谱较原料出现了明显的红移。由于在原料N-乙基咔唑-3,6-二甲醛分子的左右两端分别键合了两个富电子取代基蒽醌,产物共轭体系大大增强,因此其荧光发射峰产生了更大的Stokes位移[16]。
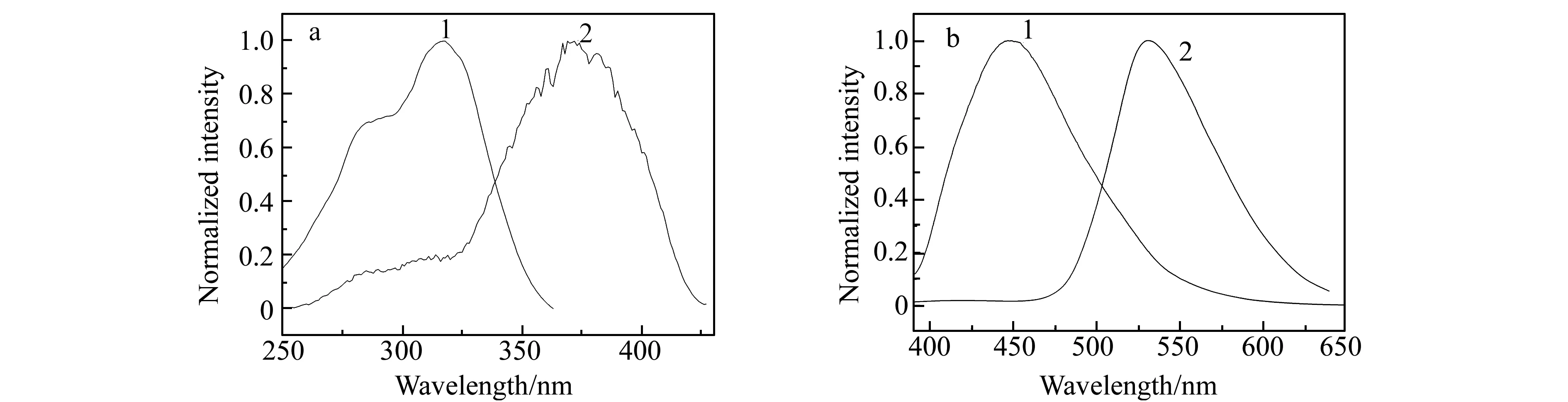
图2 原料(1)和产物(2)在二甲基亚砜中的归一化荧光激发光谱(2a)和发射光谱(2b)Fig.2 Normalized fluorescence excitation spectra(2a)and emission spectra(2b) of the raw material (1) and the product (2) in DMSOThe excitation and emission slits are 5 nm,the scanning speed is 1 200 nm/min,the excitation wavelengths are 320 nm and 368 nm respectively,and the concentrations are both 5.0×10-6 mol/L.
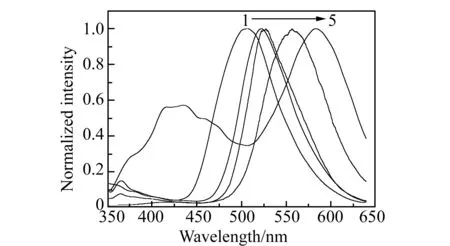
图3 3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑 (5.0×10-6 mol/L) 在不同溶剂中的归一化荧光光谱Fig.3 Normalized fluorescence spectra of 3,6-bis(anthraquinone-2-vinyl)-N-ethyl-carbazole (5.0×10-6 mol/L) in different solventsSolvents:1-5:Cyclohexane;Benzene;Ethyl acetate;Dichloromethane;Acetonitrile.The excitation and emission slits are 5 nm,the scanning speed is 1 200 nm/min,the excitation wavelength is 321.0 nm.
为了研究3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑的溶剂化效应,考察了其在不同溶剂中的荧光光谱。试剂浓度均为5.0×10-6mol/L,激发和发射狭缝均为5 nm,扫描速度为1 200 nm/min,激发波长均为321.0 nm。结果见图3。由图3可见,3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑的荧光发射光谱对外部环境的变化比较灵敏,随溶剂极性的增大,荧光光谱的最大发射峰有明显红移,最大发射波长随溶剂极性参数增加,从505 nm红移到583 nm,并且在强极性溶剂乙腈中出现了两个荧光带,即所谓双荧光现象。
由化合物的结构可见,3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑分子中既有电子给体又有电子受体,属于强极性分子。在非极性溶剂中,其荧光发射谱属于光诱导电荷转移(ICT,B带),Stokes位移也小。虽然电子给体(N-乙基咔唑)和电子受体(蒽醌)本身具有很好的平面性,但是彼此和共轭烯键以单键连接,两端端基可以旋转,因此在极性溶剂中,容易出现扭曲的分子内电荷转移(TICT,A带),其极性比ICT态大,因此在极性溶剂中,TICT态更能稳定存在,荧光主要来自TICT态的发射[17]。极性溶剂中的荧光发射谱带包含了平面激发态的ICT和TICT两部分。
2.2 溶剂效应
3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑在不同极性溶剂中的荧光光谱参数见表1。由表可见,随着溶剂极性的增大,吸收光谱位置变化不大,而荧光最大发射波长随溶剂极性参数增加从505 nm红移到583 nm。
以溶剂极性参数ET(30)[18]对最大吸收和最大发射位置(υa,υf)作图(图4),可以看出溶剂极性强弱对化合物的荧光发射光谱的影响。
Lippert-Mataga方程能更好地解释溶剂极性对溶质荧光光谱偏移的影响:

表1 3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑在不同溶剂中的吸收和荧光光谱参数
Note:υaandυfare the wave numbers of maximum absorption and emission,respectively.
(1)
(2)
其中,υa和υf分别是吸收和发射的波数(cm-1),h是Plank常数,c是光速,a是荧光团所在的溶剂笼的半径,对于长条形的分子,a通常估计为它最长轴的40%;μE、μG分别为荧光分子在基态和激发态的偶极矩,△f称为溶剂的定向极化率,是介电常数ε和折射率n的函数。
以溶剂的定向极化率(△f)对Stokes位移作图,得到了化合物在5种不同溶剂中的Lippert-Mataga的曲线,如图5 所示。
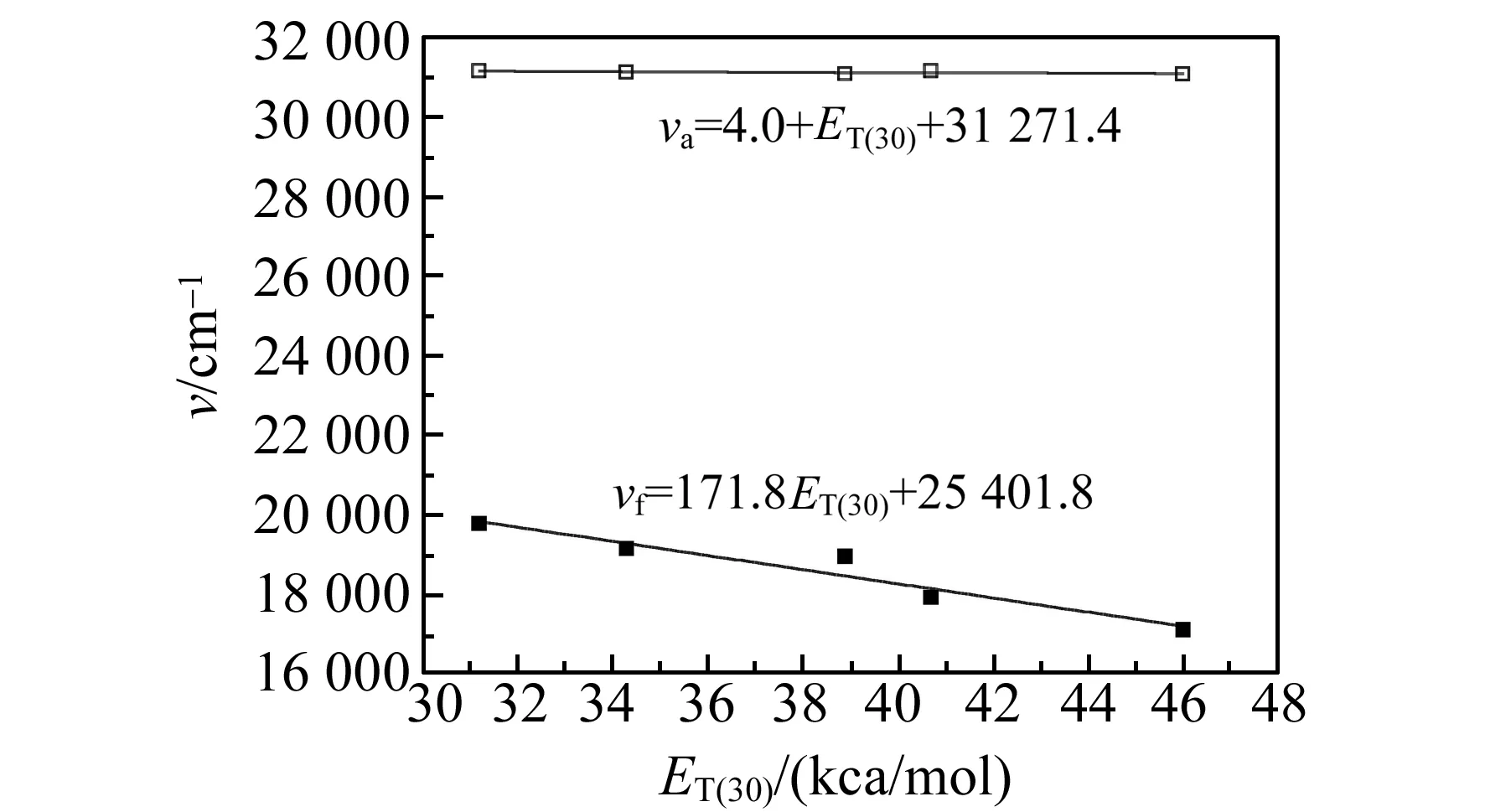
图4 最大吸收和发射与溶剂极性参数ET(30)的关系Fig.4 Relationship of maximum absorption and emission with solvent polarity parameter ET (30)

图5 定向极化率△f与化合物的最大激发和发射波数差△υ关系曲线Fig.5 Relationship of directional polarization △f with the difference of the wave number of maximum excitation and emission1.cyclohexane,2.benzene,3.ethyl acetate,4.dichloromethane,5.acetonitrile.

图6 3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑的平面分子内电荷转移示意图Fig.6 Intramolecular charge transfer mechanism of 3,6-bis(anthraquinone-2-vinyl)-N-ethyl-carbazole
由图可见,化合物在乙酸乙酯中的Stokes位移严重偏离线性,这暗示着溶剂极性不是影响光谱位移的唯一因素,溶质与溶剂分子间存在的特殊的溶剂效应,包括氢键、酸碱效应和电荷转移的相互作用等,它们都可能导致Lippert-Mataga方程的非线性。3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑可能与乙酸乙酯发生分子间电荷转移,使得化合物的发射光谱复杂化。
根据Lippert-Mataga方程直线的斜率,可以计算出激发态与基态之间的偶极矩(△μ):
(3)
根据能量最小化原理,经优化过的分子的直径为1.25 nm。由图中曲线斜率可以估算出化合物的偶极差为3.014 D,由此可以说明在光激发下,3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑发生了分子内电荷转移[19]。N-乙基咔唑具有强的给电子能力,蒽醌具有强的吸电子能力,电荷可以从咔唑基团转移至两端的蒽醌基团,如图6所示。
3 结论
本文合成了3,6-二(蒽醌-2-乙烯基)-N-乙基咔唑,考察了化合物的光物理行为和性质。在光诱导作用下,随着溶剂极性增大,其最大荧光发射峰红移,发生了分子内电荷转移(TICT)并产生双荧光(TICT引发的异常荧光),该化合物在光电材料领域具有潜在的应用价值。
