超高效液相色谱法测定炎可宁胶囊中4组分含量
2017-09-29张建华
张建华,苏 晶 ,陈 卓
(1.沈阳药科大学基于靶点的药物设计与研究教育部重点实验室,辽宁 沈阳 110016; 2.重庆市食品药品检验检测研究院·重庆市药物过程与质量控制工程技术研究中心,重庆 401121; 3.重庆医科大学药学院,重庆 4000161)
超高效液相色谱法测定炎可宁胶囊中4组分含量
张建华1,苏 晶2,陈 卓3
(1.沈阳药科大学基于靶点的药物设计与研究教育部重点实验室,辽宁 沈阳 110016; 2.重庆市食品药品检验检测研究院·重庆市药物过程与质量控制工程技术研究中心,重庆 401121; 3.重庆医科大学药学院,重庆 4000161)
目的建立同时测定炎可宁胶囊中盐酸黄柏碱、黄芩苷、大黄素和大黄酚含量的超高效液相色谱(UPLC)法。方法 色谱柱为Water ACWUITY UPLC BEH C18柱(100 mm ×2.1 mm,1.7 m),流动相为乙腈(A) -0.05 mol/L 的磷酸二氢钾溶液(KOH 调pH =5.0,B),梯度洗脱,流速为 0.3 mL/min,柱温 35℃,检测波长 244 nm。结果 盐酸黄柏碱、黄芩苷、大黄素和大黄酚进样量分别在0.049 30 ~ 0.086 276 g(r= 999 0),0.032 450 ~ 0.648 995 g(r= 999 9),0.004 979 ~ 0.995 88 g(r= 999 9),0.002 486 ~ 0.428 280 g(r=999 8)范围内与峰面积线性关系良好,平均加样回收率分别为 95.44%,95.20%,99.61%和95.60%。各组分基线分离,各阴性样品无干扰,无其他组分峰影响。结论 该法可以作为炎可宁胶囊的一种多成分同时分析和质量控制方法。
炎可宁胶囊;超高效液相色谱;盐酸黄柏碱;黄芩苷;大黄素;大黄酚
炎可宁胶囊为常用药,炎可宁糖衣片载于《卫生部药品标准·中药成方制剂(第七册)》,功能与主治均为清热泻火、消炎止痢[1]。炎可宁胶囊生产企业众多,各生产企业的注册标准多为自行申请的标准,检测项目不一。参考文献[2-6]针对制剂中的各味药材,本研究中建立了同时测定其含量的超高效液相色谱(UPLC)法,方法操作简便,既节约时间又节约了试剂,对炎可宁胶囊质量的整体控制具有重要意义和应用价值,可以作为其一种多成分同时分析和质量控制的方法。
1 仪器与试药
Waters ACQUITY 超高效液相色谱仪(美国Waters);AX205 型电子天平(瑞士 Mettler Toledo,0.01 mg);BP221S 型电子天平(德国 Sartorius,0.1 mg);KQ-500B型超声波清洗器。
炎可宁胶囊(A公司,批号分别为20160502,20160503;B 公司,批号分别为 160352,160422;C 公司,批号分别为 1507003,1607007;D公司,批号分别为ZEA1602,ZEA1601)。甲醇、乙腈为色谱纯(安徽时联特种溶剂股份有限公司);水为实验室自制纯化水;样品前处理所用甲醇、乙醇、磷酸等其他试剂均为分析纯(重庆川东化工<集团>有限公司)。盐酸黄柏碱、黄芩苷、大黄素和大黄酚均购于中国食品药品检定研究院,批号分别为 111895-201504,110715-201318,110756-201512,110796-201017,含量分别以 94.9% ,93.3% ,98.7%和99.6%计算。
2 方法与结果
2.1 色谱条件[7-10]
色谱柱:Waters ACQUITYUPLC®BEHC18柱(100 mm ×2.1 mm,1.7 μm);流动相:以乙腈为流动相 A,以0.05 mol/L 的磷酸二氢钾溶液(用氢氧化钾调 pH =5.0)为流动相B,进行梯度洗脱,见表1;检测波长:244 nm;流速:0.3 mL /min;柱温:35 ℃。

表1 流动相梯度洗脱程序
2.2 溶液制备
对照品溶液:称取盐酸黄柏碱对照品0.009 58 mg,精密称定,置100 mL容量瓶,加70%甲醇溶解并稀释至刻度,摇匀,作为盐酸黄柏碱对照品贮备液。同法,分别称取黄芩苷对照品 0.010 23 mg、大黄素对照品0.010 68 mg、大黄酚对照品 0.010 75 mg,精密称定,置100 mL容量瓶,加70%甲醇溶解并稀释至刻度,摇匀,作为黄芩苷、大黄素和大黄酚对照品贮备液。分别精密量取盐酸黄柏碱对照品溶液、黄芩苷对照品溶液、大黄素对照品溶液和大黄酚对照品溶液 1,3,1,1 mL,置100 mL容量瓶,加70%甲醇溶解并稀释至刻度,摇匀,作为混合对照品溶液。
供试品溶液:取供试品20粒,取出内容物,研细混匀,取约0.15 g,精密称定,置锥形瓶中,精密加入70%甲醇50 mL,称定质量,超声(功率240 W,频率45 kHz)处理30 min,取出冷却至室温,用70%甲醇补足质量,摇匀,用微孔滤膜滤过,取续滤液,即得。
阴性对照品溶液:取按处方比例及制备工艺,分别制备缺黄柏的阴性样品、缺黄芩的阴性样品和缺大黄的阴性样品,按炎可宁片[1]制法项下制备,再按上述供试品溶液制备方法制备溶液,即得。
2.3 方法学考察
专属性考察:分别精密吸取对照品、供试品及阴性对照品溶液各1 μL,进样,记录色谱图。阴性对照品溶液色谱中,在与大盐酸黄柏碱、黄芩苷、大黄素和大黄酚对照品保留时间处无吸收峰,说明阴性样品无干扰。色谱图见图1。
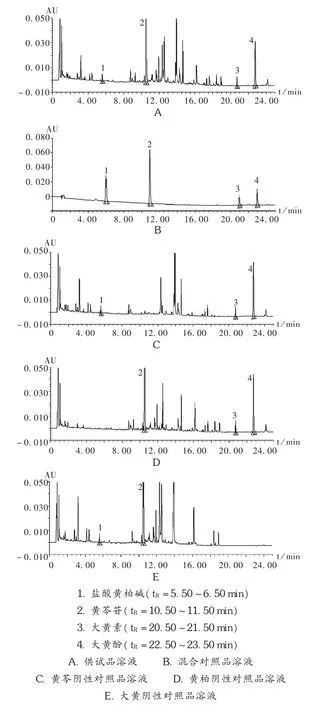
图1 专属性考察液相色谱图
线性关系考察:精密量取盐酸黄柏碱对照品贮备液,逐级稀释,分别配制成质量浓度 4.930,12.325,24.650,49.301,73.951,86.276 μg /mL 的溶液;精密量取黄芩苷对照品贮备液,逐级稀释,分别配制成质量浓度32.450,81.124,162.249,324.497,486.746,648.995 μg /mL 的溶液;精密量取大黄素对照品贮备液,逐级稀释,分别配制成质量浓度 4.979,12.449,24.897,49.794,74.691,99.588 μg/mL的溶液;精密量取大黄酚对照品贮备液,逐级稀释,分别配制成质量浓度 2.486,53.535,107.070,214.140,321.120,428.280 μg /mL 的溶液;分别进样1 μL 溶液,测定峰面积。以进样量为横坐标(X,μg)、峰面积为纵坐标(Y)绘制标准曲线,得盐酸黄柏碱、黄芩苷、大黄素、大黄酚的回归方程。结果见表2。
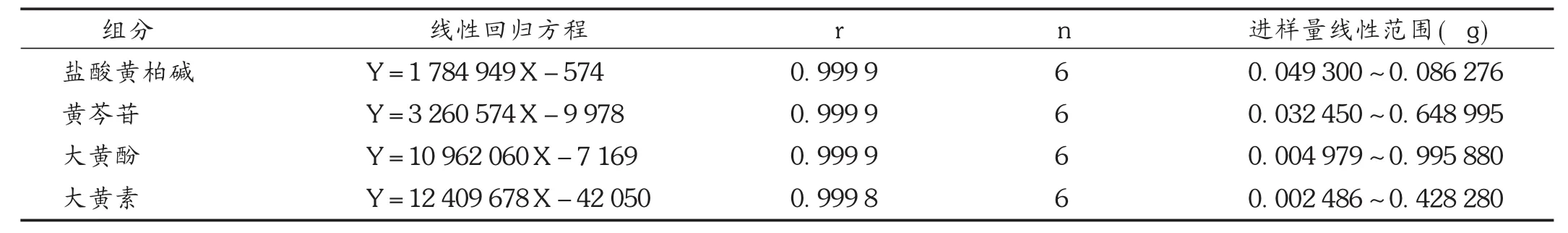
表2 线性关系考察结果
精密度试验:将含有盐酸黄柏碱对照品9.58 μg/mL,黄芩苷对照品 10.23μg/mL,大黄素对照品 10.68μg/mL,大黄酚对照品10.75 μg/mL的混合溶液连续进样6针,每次1 μL,测定峰面积。结果盐酸黄柏碱、黄芩苷、大黄素和大黄酚峰面积的 RSD分别为 0.85%,0.28%,0.80%和 0.82%(n=6),表明仪器精密度良好。
稳定性试验:取盐酸黄柏碱、黄芩苷、大黄素、大黄酚标准品物质,按照2.2项下对照品溶液制备方法配置成对照品的混合溶液,在 0,2,4,8,12,24 h 时分别进样 2 次,每次精密进样1 μL。结果盐酸黄柏碱、黄芩苷、大黄素和大黄酚峰面积的 RSD分别为 0.86%,0.31%,0.90%和0.79%(n=6),表明对照品溶液在24 h内稳定。
重复性试验:取同一批次样品混合均匀,按2.2项下供试品溶液制备方法制备6份供试品溶液,分别依法测定。结果盐酸黄柏碱、黄芩苷、大黄素和大黄酚的含量的 RSD 分别为 1.04%,1.93%,2.49%,1.29%(n =6),表明该方法重复性较好。
加样回收试验:分别精密量取盐酸黄柏碱(0.0801g/L)、大黄素(0.133 0 g /L)、大黄酚(0.124 3 g /L)对照品的70% 甲醇溶液各 3,0.12,0.5 mL,另取黄芩苷 5.00 ~6.00 mg,精密称定,置6个锥形瓶中,挥干溶剂,再精密量取已知盐酸黄柏碱、黄芩苷、大黄素、大黄酚含量的样品6份,分别加入上述锥形瓶中,按2.2项下供试品溶液制备的方法制备溶液,测定含量,并计算加样回收率。结果见表3。
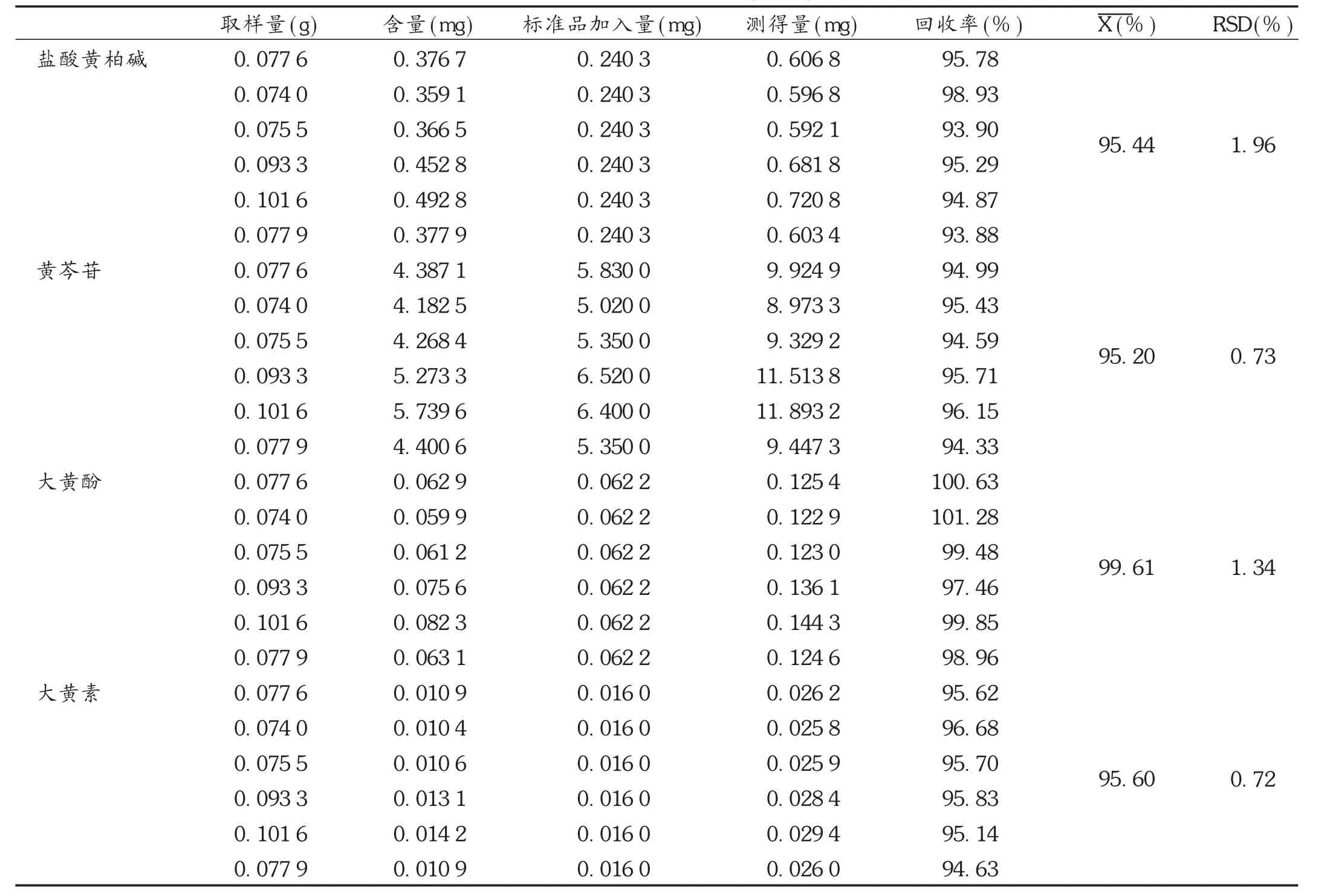
表3 加样回收试验结果(n=6)
2.4 样品含量测定
使用所得方法测定样品,结果见表4。结果表明,所采用的超高效液相色谱法对炎可宁胶囊中盐酸黄柏碱、黄芩苷、大黄素、大黄酚的含量进行测定,选择不同厂家生产的8个批次炎可宁胶囊进行考察,结果发现不同批次的炎可宁胶囊中,各个组分差异的含量明显。

表4 8批样品含量测定结果(mg/g)
3 讨论
3.1 提取方法考察
本试验中分别考察了取样量 0.10,0.15,0.50 g,加入提取溶剂量分别为25,50,100 mL,所用提取溶剂分别为体积分数60%,70%,80%和90%甲醇、体积分数60%,70%,80%和90%乙醇、0.1%HCl水溶液9个溶剂系统,并考察了超声提取20,40,60 min、加热回流提取30 min和60 min和索氏提取法7个提取方案。结果表明,采用体积分数70%甲醇50 mL,超声(功率240 W,频率45 kHz)处理30 min,各组分的提取效率较高,且省时、节省溶剂,因此最终采用该提取方法。
3.2 流动相考察
本试验中分别考察了甲醇-水、乙腈-水、甲醇-磷酸水(pH = 5.0)、乙腈 -磷酸水(pH =5.0)、乙腈 -磷酸缓冲盐水溶液(以 0.05 mol/L KH2PO4,KOH 调 pH =5.0)和甲醇 -磷酸缓冲盐水溶液(以 0.05 mol/L KH2PO4,KOH调pH=5.0)6个流动相系统,结果表明,采用乙腈-磷酸缓冲盐水溶液(以 0.05 mol/L KH2PO4,KOH 调 pH =5.0))流动相系统,各峰的分离度较好,且基线平稳,因此最终采用乙腈-磷酸缓冲盐水溶液流动相系统。
3.3 检测波长考察
分别对盐酸黄柏碱、黄芩苷、大黄素、大黄酚4种对照品用Waters的PDA检测器进行紫外区200~400 nm波长扫描,在244 nm波长下,炎可宁胶囊中所有含量较高的化合物峰形良好,峰高接近,且在该波长下,4种成分的色谱图基线平稳,分离度好。综合比较后,选择244 nm作为本试验的检测波长。
3.4 应用价值
采用超高效液相色谱法对炎可宁胶囊中盐酸黄柏碱、黄芩苷、大黄素、大黄酚的含量进行测定,选择不同厂家生产的8个批次炎可宁胶囊进行考察,结果不同批次的炎可宁胶囊中盐酸黄柏碱、黄芩苷、大黄素、大黄酚的含量差异明显。根据制剂处方[1],黄柏使用水提醇沉工艺得到浸膏入药;但制法中静置时间、条件等工艺各生产厂家参数不一,导致各生产厂家得到的胶囊中黄柏碱含量存在差异的情况发生。同时,黄芩苷的测得结果差异也较大,可能是因为投入的药材质量不符合规定或者黄芩投药量偏少,或者非法添加黄芩苷单体化合等原因造成的。本次选取的炎可宁胶囊收集于国内不同地区,因此本研究所建立的含量测定方法,能较好地反映出炎可宁胶囊本身的质量情况,并对全国各地区生产的炎可宁胶囊质量一致性有一定的控制意义。
[1]WS3-B-1368-93,卫生部药品标准·中药成方制剂(第七册)[S].
[2]黄燕萍.HPLC测定炎可宁片中盐酸小檗碱、黄芩苷和汉黄芩素的含量[J].中国实验方剂学杂志,2012,18(20):97-99.
[3]高洪琳,刘小兵,肇鑫宇,等.RP-HPLC法同时测定炎可宁片中6种成分的含量[J].沈阳药科大学学报,2014,31(11):885-890.
[4]周 新,陈会明,白 桦,等.HPLC与UPLC色谱条件转换方法研究[J].分析试验室,2008,27(4):56-58.
[5]刘少华,金 郁,周大勇,等.超高效液相色谱(UPLC)用于丹参药材水溶性成分指纹图谱研究[J].世界科学技术-中医药现代化,2007,9(6):46-50.
[6]王文琼.超高液相在药物分析领域中的应用[J].中国医药导报,2012,9(11):13-14.
[7]汪杨丽,苏 晶.HPLC测定八正胶囊中的大黄素与大黄酚[J].华西药学杂志,2014,29(2):201-203.
[8]母小东,苏 晶,汪杨丽.HPLC测定八正片中大黄素及大黄酚含量[J].食品与药品,2014,16(3):203-207.
[9]周静安.RP-HPLC法测定炎可宁片中黄芩苷的含量研究[J].中华中医药学刊,2005,23(2):353-354.
[10]尹永芹,严优芍,沈志滨,等.炎可宁片中大黄5种蒽醌类成分的含量测定[J].中国实验方剂学杂志,2010,16(6):122-124.
Simultaneous Determination of Four Components in Yankening Capsules by UPLC
Zhang Jianhua1,Su Jing2,Chen Zhuo3
(1.Key Laboratory of Structure-Based Drug Design and Discovery Ministry of Education,Shenyang Pharmaceutical University,Shenyang,Liaoning,China 110016; 2.Chongqing Institute for Food and Drug Control,Chongqing Engineering Center for Pharmaceutical Process and Quality Control,Chongqing,China 401121; 3.College of Medicine,Chongqing Medical University,Chongqing,China 400016)
ObjectiveTo establish an UPLC method for the content determination of phellodendrine chloride,baicalin,emodin and chrysophanol of Yankening Capsules at the same time.Methods The water ACQUITY UPLC BEH C18column(100 mm ×2.1 mm,1.7 μm)was adopted with acetonitrile(A)-0.05 mol/L KH2PO4(adjusted pH = 5.0 by KOH,B)as mobile phase in gradient elution,the flow rate was 0.3 mL /min,the column temperature was 35 ℃ ,the detection wavelength was set at 244 nm.Results The linear ranges of phellodendrine chloride,baicalin,emodin and chrysophanol were 0.049 30-0.086 276 μg(r= 0.999 0),0.032 450-0.648 995 μg(r= 0.999 9),0.004 979-0.995 88 μg(r= 0.999 9),0.002 486-0.428 280 μg(r= 0.999 8),respectively.The average percentages of recovery were 95.44%,95.20%,99.61% and 95.60%,respectively.The baseline was separated in each group,the negative sample had no interference,and the target peaks showed good conditions.Conclusion This method can be used for the simultaneous analysis and the quality control of Yankening Capsules.
Yankening Capsules;UPLC;phellodendrine chloride;baicalin;emodin;chrysophanol
R284.1;R286.0
A
1006-4931(2017)17-0017-04
10.3969 /j.issn.1006-4931.2017.17.005
国家十二五重大专项“中药质量安全检测和风险控制技术平台”[2014ZX09304307-002]。
张建华(1991-),男,硕士研究生,主要从事天然药物化学成分的研究,(电话)024-23986475(电子信箱)wshhzsdo07280@ 163.com。
苏晶(1980-),男,副主任中药师,主要从事中药质量控制技术的研究,(电话)023-86072753(电子信箱)4267434@qq.com。
2017-04-10)
