冠心病支架置入术后接受非心脏外科手术围术期抗栓治疗策略
2017-09-18崔军凯余阳周文君柳梅
崔军凯 余阳 周文君 柳梅
冠心病支架置入术后接受非心脏外科手术围术期抗栓治疗策略
崔军凯 余阳 周文君 柳梅
目的 比较三种抗栓策略对药物洗脱支架(DES)置入术1年内需接受非心脏外科手术患者的主要不良心血管事件和出血发生率。方法 回顾性分析因冠心病行DES置入术且正行双联抗血小板药物治疗(氯吡格雷和阿司匹林)并于置入1年内需行非心脏外科手术的患者42例,根据抗栓策略分为三组。替罗非班组和低分子肝素组患者均于术前5~7 d停用双联抗血小板药物治疗。替罗非班组30 min内以0.4 μg/(kg⋅min)静脉输注替罗非班,30 min后调整速度为0.1 μg/(kg⋅min),继而以0.1 μg/(kg⋅min)的速度维持,肌酐清除率下降的患者减量;低分子肝素组给予低分子肝素钠(克塞)4000 AxaIU皮下注射,每日1次;阿司匹林组仅继续使用阿司匹林75 mg,每日1次。三组患者术后根据分组继续使用替罗非班、低分子肝素钠或阿司匹林直至重新恢复双联抗血小板治疗。比较三组患者围术期主要不良心血管事件和出血发生率。结果 替罗非班组和低分子肝素组主要不良心血管事件发生率明显低于阿司匹林组,阿司匹林组有1例支架内血栓形成。三组出血发生率比较,差异无统计学意义(P>0.05)。替罗非班组和低分子肝素组围术期均无患者出现心绞痛或心肌梗死,低分子肝素组有1例患者心电图出现ST-T改变,但无自觉症状,考虑与糖尿病导致的心脏交感神经变性有关。阿司匹林组有3例出现心电图ST-T改变,其中2例为心绞痛发作,1例发生急性ST段抬高型心肌梗死,行急诊经皮冠状动脉介入治疗,诊断为前降支支架内血栓形成,给予血栓抽吸等处理后好转。三组患者均无心血管相关性死亡。三组患者围术期出血量比较,差异无统计学意义(P>0.05)。替罗非班组有1例股骨头置换术后出现伤口渗血,皮下瘀斑,未特殊处理,自行好转。低分子肝素组1例消化道出血,表现为黑便,未见呕血,给予药物治疗后好转。结论 替罗非班和低分子肝素可作为中断双联抗血小板药物治疗期间的“过渡治疗”,可安全有效地用于DES置入术后需接受外科手术的患者。
支架置入术;抗血小板药物治疗;外科手术;围术期
冠状动脉粥样硬化性心脏病(冠心病,coronary atherosclerotic heart disease,CHD)是常见的心血管疾病,其主要治疗方式包括药物治疗、经皮冠状动脉介入治疗(PCI)和冠状动脉旁路移植术(CABG)[1]。据统计,90% PCI患者需要行冠状动脉支架置入术[2],为防止支架内血栓形成,置入支架患者均应接受一定时间的双联抗血小板药物治疗[3]。双联抗血小板药物治疗期间,部分患者可能会经历非心脏外科手术治疗,抗血小板药物存在引起围术期出血的风险,但停用抗血小板药物治疗又有发生支架内血栓形成的风险,严重时可能会引起心肌梗死、心力衰竭、恶性心律失常、甚至死亡[4]。本研究拟探讨冠心病患者支架置入术后如何在非心脏外科手术围术期抗血小板药物治疗,并分析不同抗血小板药物治疗策略对主要不良心血管事件(MACE)发生率的影响。
1 对象与方法
1.1 研究对象
2014年1月至2016年1月入住江汉大学附属医院需接受外科手术,并且在术前1年内接受过冠状动脉支架置入术,仍需长期抗血小板药物治疗的患者。入选标准:(1)年龄<75岁;(2)术前正接受双联抗血小板药物治疗(氯吡格雷和阿司匹林);(3)患者和家属知情并同意纳入研究。排除标准:(1)终末期心功能衰竭,或根据心功能状况不适宜接受外科手术者;(2)外科疾病本身有严重的出血或出血倾向;(3)严重贫血;(4)有严重的其他器官功能衰竭。共入选42例患者,接受外科手术包括:胆囊切除术、阑尾切除术、乳腺癌根治术、胃大部分切除术、肺癌切除术、股骨头置换术、肠癌根治术、骨折固定术。根据围术期抗血小板药物治疗策略分为三组。替罗非班组(17例)和低分子肝素组(16例)均于术前停用双联抗血小板药物治疗,替罗非班组接受替罗非班抗血小板药物治疗,低分子肝素组患者接受低分子肝素钠抗凝治疗,阿司匹林组(9例)停用氯吡格雷,继续使用阿司匹林抗血小板药物治疗。
1.2 研究方法
三组患者均长期使用阿司匹林和氯吡格雷双联抗血小板药物治疗预防血栓形成,围术期抗血小板药物治疗分别采用以下策略。三组患者均在外科手术前5~7 d停用氯吡格雷,三组的围术期抗血小板治疗策略如下:(1)阿司匹林组:阿司匹林组继续给予阿司匹林100 mg、每日1次。(2)替罗非班组:停用阿司匹林及氯吡格雷,给予静脉输注血小板糖蛋白Ⅱb/Ⅲa受体拮抗药(替罗非班)。肌酐清除率正常(80~120 ml/min)的患者前30 min输注速度为0.4 μg/(kg⋅min),继而以0.1 μg/(kg⋅min)速度维持;肌酐清除率升高或者在30~80 ml/min之间的无需调整剂量;肌酐清除率<30 ml/min的患者,替罗非班用量减半[前30 min速度为0.2 μg/(kg⋅min),继而以0.05 μg/(kg⋅min)速度维持]。术前4~6 h停止输入。(3)低分子肝素组:皮下注射低分子肝素钠(克塞),剂量为4000 AxaIU,每天1次。三组患者术后根据情况尽早开始使用氯吡格雷,最早可至术后2 h,负荷剂量300 mg,然后以75 mg、每日1次维持,如果不能尽早开始使用氯吡格雷,则继续给予替罗非班或低分子肝素钠,持续至与氯吡格雷重叠6 h。如无出血风险,尽早恢复阿司匹林100 mg、每日1次。
1.3 观察指标
比较三组患者围术期(入院至术后30 d)心血管相关并发症和出血发生率。MACE包括心血管相关性死亡,再发心肌梗死、心绞痛及靶血管血运重建。心血管相关性死亡包括由恶性心律失常、心力衰竭、心肌梗死等引起的死亡。心肌梗死诊断包括缺血性胸痛症状、心电图改变(新出现的ST-T改变或新出现的左束支传导阻滞、病理性Q波)和心肌酶学改变[心肌生物标志物升高和(或)降低,至少有一次数值超过参考值上限的 99 百分位值]。心绞痛定义为有相关的心前区疼痛或放射痛,心电图检查可见以R波为主的导联中,出现ST段压低,T波平坦或倒置(变异型心绞痛者则有关导联ST段抬高),发作后数分钟内逐渐恢复。靶血管血运重建包括PCI和CABG。 出血事件包括与抗血小板药物相关的消化道出血、伤口渗血、皮下出血、脑出血、气道出血等[5]。
1.4 统计学方法
所有数据应用SPSS 19.0统计软件进行处理。计量资料以均数±标准差表示,组间比较采用t检验。计数资料以百分率表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 三组患者临床资料比较
三组患者在年龄、性别、合并高血压病、糖尿病、高脂血症的比例、支架平均数目、支架置入时间、置入部位、支架置入术后至外科手术时间、术中出血等情况比较,差异均无统计学意义(均P>0.05,表1)。
2.2 三组患者MACE和出血发生率比较
替罗非班组和低分子肝素组在围术期内均无MACE发生,阿司匹林组有3例发生MACE。三组患者围术期出血发生率比较,差异无统计学意义(P>0.05,表 2)。
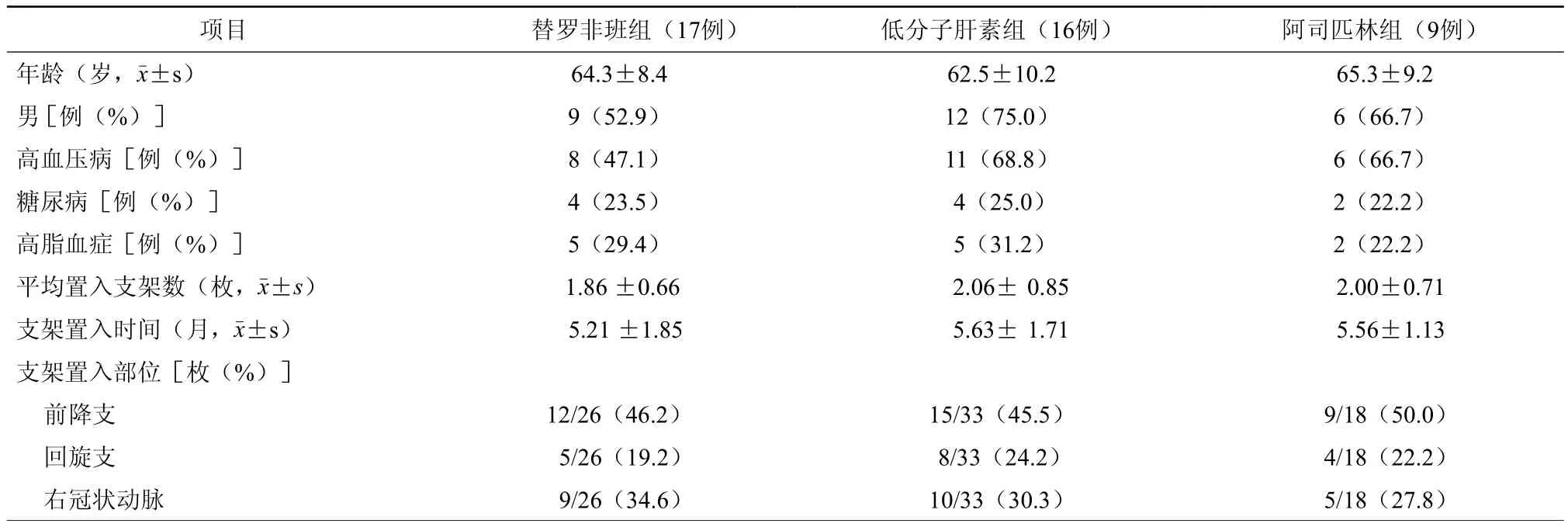
表1 三组患者临床资料比较
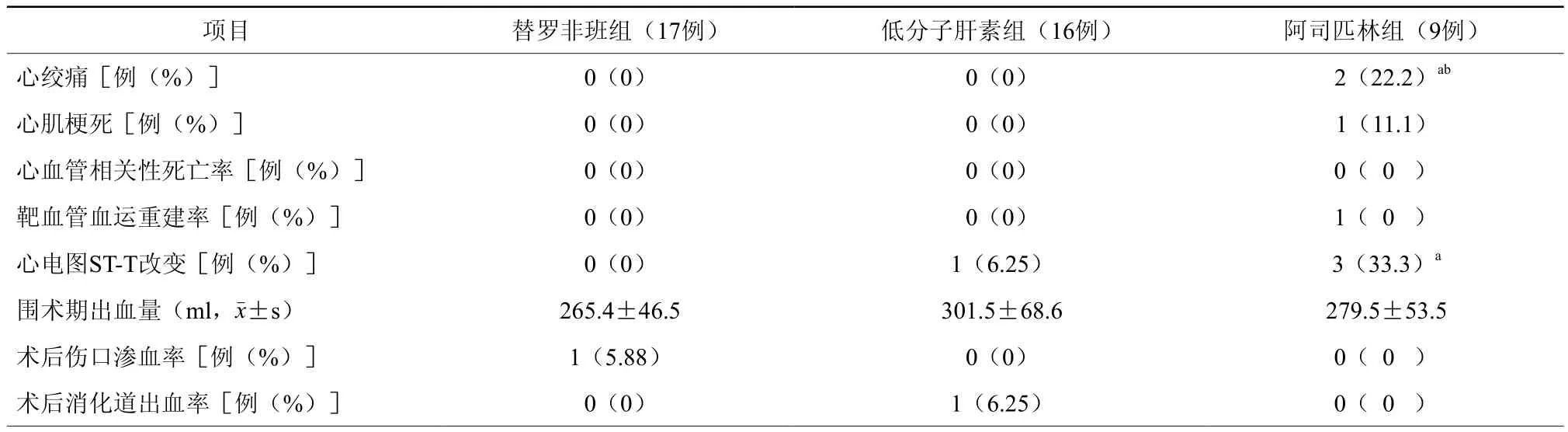
表2 三组患者主要心血管事件发生率和出血事件比较
替罗非班组和低分子肝素组围术期均无患者出现心绞痛或心肌梗死,低分子肝素组有1例患者心电图出现ST-T改变,但无自觉症状,考虑与糖尿病导致的心脏交感神经变性有关。阿司匹林组有3例出现心电图ST-T改变,其中2例为心绞痛发作,1例发生急性ST段抬高型心肌梗死,行急诊PCI,诊断为前降支(LAD)支架内血栓形成,给予血栓抽吸等处理后好转。三组患者均无心血管相关性死亡。三组患者围术期出血量比较,差异无统计学意义(P>0.05)。替罗非班组有1例股骨头置换术后出现伤口渗血,皮下瘀斑,未特殊处理,自行好转。低分子肝素组1例消化道出血,表现为黑便,未见呕血,给予药物(奥美拉唑注射液、铝镁加混悬液、云南白药等)治疗后好转。
3 讨论
在欧洲和北美,每年约有200万患者接受PCI术,术后1年内,5%~20%患者因各种原因需要接受非心脏外科手术[6]。非心脏外科手术围术期心血管并发症的问题已引起广泛关注。据统计,每年约有1000万患者发生围术期心血管并发症,比如非致死性心肌梗死、非致死性心源性休克、心源性死亡,该数据尚有逐年上升的趋势[7]。有研究表明,置入药物洗脱支架(DES)患者接受非心脏外科手术后1周内为心血管并发症发生的高峰期,主要原因是抗血小板药物治疗的中止或减弱[8]。置入DES后通常建议接受6周~12个月的双联抗血小板药物治疗(阿司匹林和氯吡格雷),在此期间,如需接受其他外科手术,为避免出血风险,一般要求提前5~7 d停用氯吡格雷,但外科手术会引起交感神经系统的激活、增加血小板活化、血管痉挛、促凝血因子合成增多,炎症因子增加等,导致机体处于高凝状态[9]。对于临床医师来说,需要在预防MACE发生和防止出血事件之间寻找平衡,因此,抗血小板 “过渡治疗”至关重要。目前,临床实践尚无统一的最佳外科手术围术期抗血小板药物治疗策略,多数指南缺乏1A及1B级别证据,并在策略上会有所不同,但仍有几点共识:(1)如果条件允许,应尽可能将外科手术延迟至裸金属支架(BMS)置入后4~12周,DES置入后6~12个月。(2)围术期宜继续使用水杨酸类药物(阿司匹林);如果可能,MACE和支架内血栓形成高风险患者考虑继续双联抗血小板药物治疗,除非有外科出血高危患者。(3)目前关于中断抗血小板药物治疗的时间和术后重新启动双联抗血小板药物治疗的时间尚无统一定义。(4)“过渡治疗”时药物选择也存在很大差异[10]。但总体来说,包括以下几种策略。①普通肝素:普通肝素常用于围术期静脉血栓栓塞的预防,但并无抗血小板特性,有研究表示其并不能预防支架内血栓形成[11]。且普通肝素停用后会产生反跳现象导致血栓形成和血小板活性增加。②低分子肝素:与普通肝素相比,低分子肝素抗凝作用更强,出血并发症少,生物利用度高,半衰期长,对凝血因子影响小,其抗血栓形成的机制与抗凝血酶及其复合物结合,抑制Xa因子和凝血酶。Tanaka等[8]回顾性分析了210例择期行非心脏外科手术的DES置入术后患者,均在中断抗血小板药物治疗期间采用低分子肝素“过渡治疗”,置入DES(2.1±1.3)枚。外科术后30 d内患者均无MACE(包括心源性死亡、支架内血栓形成和非致死性心肌梗死)发生,有4例(1.9%)在外科术后30 d内因出血需要再次手术。③血小板糖蛋白Ⅱb/Ⅲa受体拮抗药:血小板糖蛋白Ⅱb/Ⅲa受体拮抗药通过阻断血小板聚集的终末途径,发挥强效抗血小板聚集作用,半衰期短,仅为2 h,停用6 h后血小板功能即可恢复正常90%,出血时间延长≤1.5倍。替罗非班是非肽类血小板糖蛋白Ⅱb/Ⅲa受体拮抗药,其通过精氨酸-甘氨酸-门冬氨酸序列占据非肽类血小板糖蛋白Ⅱb/Ⅲa的交联位点,竞争性地抑制纤维蛋白原或血管性假血友病相关因子介导的血小板聚集,阻止血栓形成。其起效快,半衰期短,静脉输注5 min对血小板的抑制作用达96%,停药4 h内50%血小板功能恢复,因此,通常用作非心脏外科手术围术期 “过渡治疗”抗血小板药物[12]。已有研究报道,替罗非班为术前4 h停用,严重肾功能不全患者术前8 h停用[13]。Savonitto等[14]纳入30例支架内血栓形成高风险并在DES置入后12个月(平均4个月)内需接受非心脏外科手术或眼科手术患者。外科手术前5 d停用氯吡格雷,并在24 h后给予替罗非班,持续到外科手术前4 h,在外科手术后2 h继续使用替罗非班,直到重新开始使用口服氯吡格雷;是否使用阿司匹林由外科医师决定。
本研究结果表明,替罗非班和低分子肝素可作为DES置入术后需接受非心脏手术患者的围术期抗血小板“过渡治疗”。替罗非班和低分子肝素均可以显著降低围术期MACE发生率,且不增加出血发生率。冠心病患者接受非心脏外科手术围术期MACE发生率明显高于其他患者,除了选择适宜的围术期抗血小板药物治疗策略外,临床医师尚需要提前识别高危患者。因此,完善术前评估系统也十分重要。
[ 1 ] 刘桂勇. 冠状动脉支架植入术后行非心脏手术时抗凝治疗的研究. 湖南中医药大学学报,2010,30(10):43-45.
[ 2 ] Spaulding C, Henry P, Teiger E, et al. Sirolimus-eluting versus uncoated stents in acute myocardial infarction. N Engl J Med, 2006, 355(11): 1093-1104.
[ 3 ] 李解贵,周卫建,吴欣军,等. 冠脉支架术后非心脏手术围手术期抗凝治疗分析.湖南师范大学学报(医学版),2014,11(3):47-49.
[ 4 ] 郁正亚. 非心脏手术患者围术期抗血小板药物的使用. 中华临床医师杂志(电子版),2011,5(5):1371-1374.
[ 5 ] 罗新林,刘强,王丽丽,等,延期支架置入对高血栓负荷ST段抬高急性心肌梗死预后的影响. 中国介入心脏病学杂志, 2014, 22(11):697-701.
[ 6 ] Wąsowicz M, Syed S, Wijeysundera DN, et al. Effectiveness of platelet inhibition on major adverse cardiac events in noncardiac surgery after percutaneous coronary intervention: a prospective cohort study. Br J Anaesth, 2016,116(4):493-500.
[ 7 ] Devereaux PJ, Chan M, Eikelboom J. Major Vascular Complications in Patients Undergoing Non-Cardiac Surgery: Magnitude of the Problem, Risk Prediction, Surveillance, and Prevention. Evidence-Based Cardiology, Third Edition. 2010:47-62.
[ 8 ] Tanaka A, Sakakibara M, Ishii H, et al. The risk of adverse cardiac events following minor surgery under discontinuation of all antiplatelet therapy in patients with prior drug-eluting stent implantation. Int J Cardiol, 2014,172(1):e125- e126.
[ 9 ] 吕慧,秦永文. 支架术后患者非心脏手术的围术期抗血小板药物治疗. 国际心血管病杂志,2011,38(6):350-353.
[10] Darvish-Kazem S, Gandhi M, Marcucci M, et al. Perioperative management of antiplatelet therapy in patients with a coronary stent who need noncardiac surgery: a systematic review of clinical practice guidelines. Chest, 2013 ,144(6):1848-1856.
[11] Collet J P, Montalescot G. Premature withdrawal and alternative therapies to dual oral antiplatelet therapy. Eur Heart J Suppl, 2006, 8(suppl_G):G46-G52.
[12] 夏经钢,尹春琳,曲杨,等.替罗非班应用在药物涂层支架植入术后老年患者实行非心脏手术的可行性和安全性. 实用医学杂志,2011,27(23):4213-4215.
[13] 钱翠平, 彭稳中, 张予,等. Meta分析:冠状动脉内应用替罗非班用于急性冠状动脉综合征经皮冠状动脉介入治疗的疗效. 中国介入心脏病学杂志, 2014,22(4):237-245.
[14] Savonitto S, D'Urbano M, Caracciolo M, et al. Urgent surgery in patients with a recently implanted coronary drug-eluting stent: a phase II study of 'bridging' antiplatelet therapy with tirofiban during temporary withdrawal of clopidogrel. Br J Anaesth, 2010,104(3):285-291.
Bridging antiplatelet strategies during temporary withdrawal of antiplatelet therapy for non-cardiac surgery after drug-eluting stent implantation
CUI Jun-kai, YU Yang, ZHOU Wen-jun, LIU Mei.
Department of General Surgery, Affiliated Hospital of Jianghan University, Wuhan 430056, China
YU Yang, Email: yuyang7003@yahoo.com
Objective To compare the rates of major adverse cardiovascular events(MACE) and bleeding events of three different antiplatelet strategies during temporary withdrawal of antiplatelet therapy for non-cardiac surgery within 1 year after drug-eluting stent (DES)implantation. Methods Retrospectively analyzed 42 patients who had accepted non-cardiac surgery and required temporary withdrawal of antiplatelet therapy within 1 year after drug-eluting stent implantation. The patients were divided into three groups according to the bridging antiplatelet strategies they
. All patients discontinued clopidogrel 5 to 7 days before the non-cardiac surgery. The tirofiban group wastreated with intravenous tirofiban 0.4ug/kg·min in the first 30 min followed 0.1μg/(kg·min). The dosage was reduced by half for patients whose Creatinine clearance were less than 30 ml/min.The low molecular weight heparin group was treated with subcutaneous enoxaparin (Clexane 4000 AxaIU, once per day) .The asprin group was given only oral asprin(100 mg, once per day) . Tirofiban and low molecular weight heparin were continued until clopidogrel was resured. Perioperative cardiovascular events and serious bleeding were recorded. Results The rates of major adverse cardiac events in the tirofiban and the low molecular weight heparin group were lower than the aspirin group. Acute myocardial infarction caused by confirmed in-stent thrombosis was diagnosed in one patient in the aspirin group. One case of asymptomatic ST-T changes was found in the low molecular weight the aspirin group. 3 cases in the aspirin group presented ST-T changes on ECG and among them 1 case was STEMI due to LAD thrombosis requiring primary and 2 other cases were agina pectoris.There were no significant differences in bleeding events among the three groups. Conclusions Potential for the perioperative management with tirofiban or low molecular weight heparin is safe and feasible for patients who had recently undergone DES implantation and required noncardiac surgery with the interruption of antiplatelet therapies.
Stent implantation;Antiplatelet;Surgery;Perioperation
R541.4
2017-05-24)
10. 3969/j. issn. 1004-8812. 2017. 08. 006
430056 湖北武汉,江汉大学附属医院肝胆外科(崔军凯、余阳、周文君);武汉市第一医院重症监护室(柳梅)
余阳,Email: yuyang7003@yahoo.com
