1, 1′, 3, 3′-四(二苯膦基)二茂铁的合成研究
2017-09-16马金焕
马金焕
(鲁南制药集团股份有限公司 国家手性制药工程技术研究中心,山东 临沂 276006)
1, 1′, 3, 3′-四(二苯膦基)二茂铁的合成研究
马金焕
(鲁南制药集团股份有限公司 国家手性制药工程技术研究中心,山东 临沂 276006)
优化了1, 1′, 3, 3′-四(二苯膦基)二茂铁(3)的合成工艺,起始原料为二苯膦基环戊二烯锂(1)。二苯膦基环戊二烯锂(1)先与二苯基氯化磷在甲苯中发生取代反应,继而用正丁基锂拔氢得到1, 3-双(二苯膦基)环戊二烯锂(2)的溶液。所得2的溶液直接与氯化亚铁回流反应得到1, 1′, 3, 3′-四(二苯膦基)二茂铁(3),总收率75%。优化后的工艺操作简便,收率更高,适合工业化生产。
二苯基氯化磷;1, 3-双(二苯膦基)环戊二烯基锂;1, 1′, 3, 3′-四(二苯膦基)二茂铁
含二茂铁结构的膦配体在金属催化的有机反应中扮演着非常重要的角色,受到了科学家们的广泛关注[1-2]。由于二茂铁结构易修饰和改进,并且此类膦配体对氧气和水不敏感,多种多样的二茂铁类双膦化合物被合成出来[3-5]。1, 1′,3, 3′-四(二苯膦基)二茂铁作为一种结构对称的化合物,在金属催化领域有较好的应用前景。但是,目前仅有一例关于此化合物合成的报道[6]。此方法以二苯膦基环戊二烯锂为起始物,与二苯基氯化磷在甲苯中低温反应得到1, 3-双(二苯膦基)环戊二烯,继续加入正丁基锂拔氢得到1,3-双(二苯膦基)环戊二烯锂。接着与氯化亚铁反应得到目标产物1, 1′,3, 3′-四(二苯膦基)二茂铁。利用这种方法制备1, 3-双二苯基膦环戊二烯锂(2)时,需要减压蒸出甲苯,得到的残余物是非常粘稠的玻璃态化合物,很难从反应瓶中取出。在下一步制备1, 1′,3, 3′-四(二苯膦基)二茂铁时,不仅需要滤出粘性不溶物,还要柱层析分离才能得到纯品,方法比较繁琐。本研究利用新蒸的二苯基氯化磷与二苯膦基环戊二烯锂1:1反应,并用1当量的正丁基锂拔氢,制得纯度较高的1, 3-双二苯膦基环戊二烯锂的甲苯溶液。该溶液无需分离提纯,与氯化亚铁回流反应,然后用正己烷-二氯甲烷重结晶得到1, 1′,3, 3′-四(二苯膦基)二茂铁。合成路线见图1。
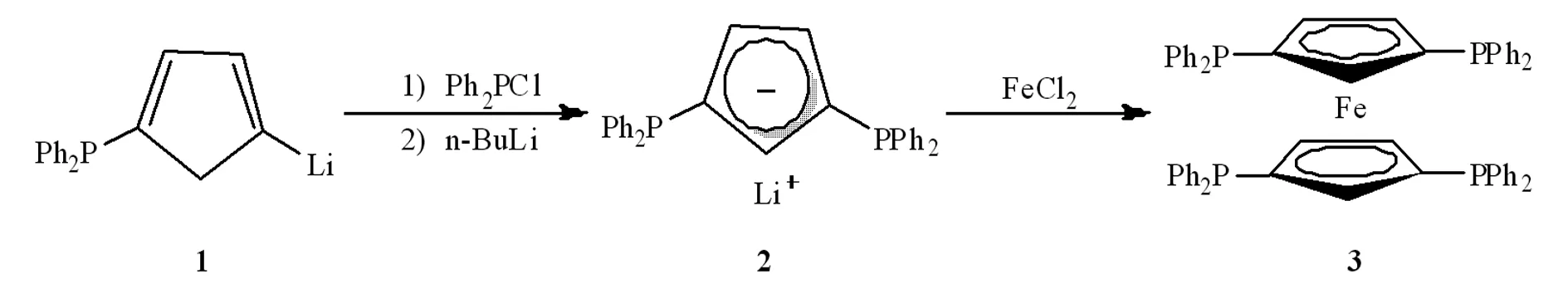
图1 1, 1′, 3, 3′-四(二苯膦基)二茂铁(3)的合成路线
Fig.1 Synthesis of 1, 1′, 3, 3′-tetrakis(diphenylphosphino)-ferrocene (3)
1 实验部分
1.1 主要试剂及仪器
二苯基氯化磷,氯化亚铁(含量≥99.9%),甲苯,四氢呋喃,二氯甲烷,正己烷均为分析纯试剂。正丁基锂的含量为1.6 mol/L,所有溶剂在使用前均经无水处理,甲苯,正己烷,四氢呋喃用钠回流干燥;二氯甲烷用氢化钙回流12 h除水。二苯膦基环戊二烯锂采用文献方法制备[7],所有溶剂在处理时都使用氮气保护,并在使用前经氮气鼓泡15min除氧。
华鲁HL-15-35 78-1磁力加热搅拌器,SGW X-4型数字显微熔点仪,Bruker Avance 400型核磁共振仪, Elementar Vario EL Cube型元素分析仪, Finnigan LCQ Advantage型质谱仪(赛默飞世尔)。
1.2 操作步骤
1.2.1 1, 3-双(二苯膦基)环戊二烯锂的制备
将溶有25.6g(0.1 mol)二苯基膦基环戊二烯锂的200 mL无水甲苯用液氮-丙酮浴冷至-78℃,滴加17.9 mL(0.1 mol)新蒸的二苯基氯化磷。滴完,自然升温至室温,并在室温搅拌2h。离心,将所得橙色清夜重新冷却至-78℃,缓慢加入62.5 mL(0.1 mol)正丁基锂(1.6 M in hexane),加完后自然升温至室温,并在室温搅拌10h,滤除少量不溶物后备用。
1.2.2 1, 1′, 3, 3′-四(二苯膦基)二茂铁的制备
将6.3 g(0.05 mol)无水 FeCl2加入200 mL无水四氢呋喃中,搅匀后溶液颜色变成粉红色。缓慢加入上述1, 3-双(二苯膦基)环戊二烯锂的甲苯溶液,加完后加热至85℃回流反应5h,冷至室温,离心除去不溶物。减压抽干溶剂,将残余物溶在50 mL二氯甲烷中,搅拌下滴加300 mL正己烷,逐渐有橙色固体析出,滴完后继续搅拌2 h,抽滤,滤饼用正己烷洗涤,真空干燥得到34.6 g橙红色固体,收率75%,mp 179~180°C。1H NMR (400 MHz, DMSO-d6,TMS),δ:5.88~5.90 (m,4H,Cp),6.06~6.09 (m,2H,Cp),7.12~7.35 (m,40H, Ph)。31P{1H} NMR (162 MHz,DMSO-d6,85% H3PO4),δ:-19.4 (s)。 Anal Calcd for C58H46FeP4: C,75.50;H,5.02。Found:C,75.39;H,4.98。ESI-MS (m/z):923 [M+]。
2 结果讨论
2.1 1, 3-双(二苯膦基)环戊二烯锂的制备
首先,我们对溶剂的种类进行了优化。由于原料和产物的碱性较强,而且反应中用到强碱正丁基锂,我们主要优化了非质子化溶剂,如乙醚,四氢呋喃,正己烷,甲苯等。尝试在正己烷中反应时,几乎没有得到目标产物。在乙醚和四氢呋喃中反应时收率偏低,副产物很多。此外,溶剂甲苯的用量也是非常重要的。在当前投料量的情况下,甲苯的用量不能少于200mL。如果少于200mL,滴加正丁基锂的正己烷溶液时,会导致相当多的产物析出,导致收率偏低。
其次,二苯基氯化磷的纯度同样对反应有较大影响。纯度过低时会导致1, 3-双(二苯膦基)环戊二烯基锂的残留,对下一步的反应非常不利。所以一定要用新蒸的二苯基氯化磷,以保证1, 3-双(二苯膦基)环戊二烯基锂与二苯基氯化磷的摩尔比为1∶1。
2.2 1, 1′, 3, 3′-四(二苯膦基)二茂铁的制备
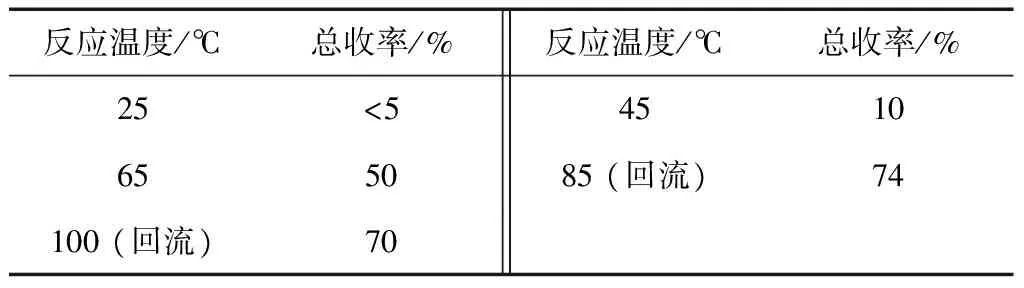
表1 不同反应温度对收率的影响
在此步反应中,溶剂四氢呋喃对反应的顺利进行起着关键作用。若是没有四氢呋喃的参与,本步骤的反应几乎不发生。我们首先对反应温度进行了优化,在固定反应时间为7 h时,85℃回流时能够得到最佳的效果(表1)。在25℃时,绝大多数原料都没有参与反应。此后随着温度的升高收率逐渐增加,但是超过85℃达到100℃时,由于混合溶剂中的四氢呋喃和正己烷沸点都比较低,回流剧烈,溶剂损失严重,造成收率的下降。
在确定最优反应温度的基础上,我们对反应时间进行了优化。回流5h时能达到最佳效果,继续回流时对收率的影响不大(表2)。

表2 不同反应时间对收率的影响
3 结论
以二苯膦基环戊二烯锂为原料,先与二苯基氯化磷发生取代反应,继而用正丁基锂拔氢得到1, 3-双(二苯膦基)环戊二烯基锂。所得产物不经进一步处理直接与氯化亚铁在85℃回流反应5h得到1, 1′, 3, 3′-四(二苯膦基)二茂铁,总收率75%。与文献报道的方法相比,该方法不需要提纯1, 3-双(二苯膦基)环戊二烯基锂,而且避免了柱层析方法提纯1, 1′,3, 3′-四(二苯膦基)二茂铁。处理更方便,收率更高,适合大规模生产。
[1] Hierso J, Smaliy R, Amardeil R,et al. New concepts in multidentate ligand chemistry: effects of multidentarity on catalytic and spectroscopic properties of ferrocenyl polyphosphines[J]. Chemical Society Reviews, 2007, 36: 1754-1769.
[2] 宋庆宝,东 宇. 二茂铁手性膦配体研究的一些新进展[J]. 有机化学, 2007, 27(1): 66-71.
[3] Tong R, Zhao Y, Wang L,et al. Recent research progress in the synthesis and properties of burning rate catalysts based on ferrocene-containing polymers and derivatives[J]. Journal of Organometallic Chemistry, 2014, 755: 16-32.
[4] Sarhan A E. Synthesis and applications of tetrathiafulvalenes and ferrocene-tetrathiafulvalenes and related compounds[J]. Tetrahedron, 2005, 61(16): 3889-3932.
[5] Moyano A, Rios R. En route to new chiral ferrocene derivatives: dead ends, detours, and avenues [J]. Synlett, 2009:1863-1886.
[6] Broussier R, Bentabet E, Mellet P, et al. New 1, 1- or 1, 2- or 1, 3-bis(diphenylphosphino)-ferrocenes [J]. Journal of Organometallic Chemistry, 2000, 598: 365-373.
[7] Casey C, Bullock R, Fultz W,et al. Heterobimetallic compounds linked by heterodifunctional ligands: synthesis and x-ray crystal structure of (CO)4MnMo(CO)3(η5-C5H4PPh2)[J]. Organometallics, 1982, 1: 1591-1596.
(本文文献格式:马金焕.1, 1′, 3, 3′-四(二苯膦基)二茂铁的合成研究[J].山东化工,2017,46(7):18-19.)
Synthesis of 1, 1′, 3, 3′-tetrakis(diphenylphosphino)-ferrocene
MaJinhuan
(Lunan Pharmaceutical Group, National Engineering and Technology Research Center of Chirality Pharmaceutical, Linyi 276006,China)
This manuscript describes an optimized process for the synthesis of 1, 1′, 3, 3′-tetrakis(diphenylphosphino)-ferrocene (3) using diphenylphosphinocyclopentadienyllithium (1) as starting material,which firstly reacted with chlorodiphenylphosphine via substitution reaction in toluene and then n-BuLi to give the solution of 1, 3-diphenylphosphinocyclopentadienyllithium (2) which could be used in the subsequent reaction without further purification. The solution of 1, 3-diphenylphosphinocyclopentadienyllithium (2) reacted with iron dichloride under refluxing at 85℃leading to 1, 1′, 3, 3′-tetrakis(diphenylphosphino)-ferrocene (3) in 75% yield。The optimized process is simpler, higher yielding and suitable for industrial production.
chlorodiphenylphosphine; 1, 3-diphenylphosphinocyclopentadienyllithium; 1, 1′, 3, 3′-tetrakis(diphenylphosphino)-ferrocene
2017-02-23
马金焕(1983—),女, 山东济宁人, 本科, 主要从事药学相关工作。
O627.8
A
1008-021X(2017)07-0018-02
