微纳米空心结构金属氧化物作为锂离子电池负极材料的研究进展
2017-09-16麻亚挺刘鹏飞蔡余新谢清水彭栋梁
麻亚挺,黄 健,刘 翔,刘鹏飞,蔡余新,谢清水,彭栋梁
微纳米空心结构金属氧化物作为锂离子电池负极材料的研究进展
麻亚挺,黄 健,刘 翔,刘鹏飞,蔡余新,谢清水,彭栋梁
(厦门大学材料学院,福建厦门 361005)
电动汽车和智能电网的快速发展对锂离子电池提出了更高的要求,即在拥有高能量密度和高功率密度的同时,兼有快速充放电和较高的安全性能。电极材料是电池性能的关键,金属氧化物因为拥有较高的比容量和安全性能,已经成为有希望替代传统商用石墨负极的新型电极材料。然而,金属氧化物负极的循环结构稳定性较差、电导率低,由此导致差的循环及倍率性能,极大地阻碍了其商业化应用。近年来,拥有微纳米空心结构的金属氧化物显示出了优异的电化学性能。本文介绍了制备空心结构金属氧化物的常用方法,讨论了各种方法的优缺点,并列举了常见空心结构金属氧化物作为锂离子电池负极时的性能表现,最后对空心结构金属氧化物未来的发展方向和发展前景予以展望。
微纳米空心结构;金属氧化物;锂离子电池;负极材料
进入21世纪以来,因为经济的发展和社会对环境保护的重视,人们更加迫切的需要对清洁能源进行大规模应用,从而减轻由化石燃料带来的温室气体排放和环境污染问题。在这个过程中,高效的储能系统是清洁能源应用的关键。在众多的新型储能系统中,锂离子电池因为拥有能量密度高、循环寿命长、输出电压高、自放电率低和无记忆效应等优势,被广泛地应用于手机、笔记本电脑等移动消费电子领域。然而,随着电动汽车、混合动力汽车和智能电网的发展,现在商业化的锂离子电池受制于自身的材料局限,其性能还远不能满足这些新兴领域对高比能量密度、高比功能密度、快速充放电和安全性的要求[1-3]。因此,在锂离子电池的正负极材料、电解液、隔膜等方面都有许多急需解决的难题。
电极材料是决定锂离子电池性能的关键因 素[4]。其中负极材料作为锂离子电池的关键材料之一,其性能的优劣直接影响着整个锂离子电池系统的综合性能。现阶段,传统碳材料因其循环性能优异、来源广泛和价格低廉等优势,已经成为最广泛使用的商用负极材料。然而传统碳材料的理论质量比容量相对较低(约372 mA·h/g),并且低的嵌锂电位容易产生锂枝晶,导致锂离子电池能量密度不高并存在安全隐患,难以满足下一代高性能锂离子电池的要求。因此,研究者急需发展一种能量密度高、安全性能好的替代负极材料。
自从2002年POIZOT等[5]在杂志上报道了金属氧化物作为锂离子负极材料的研究之后,金属氧化物负极因为其极高的比容量和优异的安全性能逐渐引起了研究者的重视。本综述首先简短地总结了金属氧化物材料的特点,分析其作为锂离子电池负极材料的优点和缺点,并介绍一些优化其电化学性能的方法。本文主要聚焦于具有空心结构的金属氧化物负极材料,因为它们在拥有纳米材料普遍的优点的同时,也显示出了空心结构作为锂离子电池负极材料的特殊优势。本文中提到的空心结构主要包括了空心球、多层壳空心球、蛋黄壳结构、纳米管和空心纳米立方块等。此外,本文将分章节讨论一些常见金属氧化物空心结构的制备及其作为锂离子电池负极材料的电化学性能,最后对空心结构金属氧化物负极材料未来的发展方向和发展前景予以展望。
1 金属氧化物负极材料
1.1 锂储存机理的分类
如图1所示,金属氧化物的种类繁多,目前研究中涉及的上百种负极材料按照储锂机理可以分为3类:合金/去合金化机制、转化反应机制和脱/嵌锂机制[6]。
(1)合金/去合金化机制(alloying/dealloying meachanism)合金/去合金化机制主要包括两个过程:在第一个过程中,金属氧化物不可逆地形成金属纳米颗粒,并分散在氧化锂的基体中;在第二个过程中,这些金属纳米颗粒在充电时将会与锂离子反应形成一系列的Li-M合金,并在随后的放电过程中发生可逆的去合金化反应,通过可逆的合金/去合金化反应提供电池容量。包括Ge、Sn、Sb、In和Pb基金属氧化物在内的许多金属氧化物都是基于此储锂机制[7],其化学反应方程式如下:
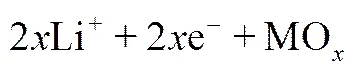
(2)
(2)转化反应机制(conversion reaction mecha- nism)在转化反应机制中,储锂机制包括氧化锂的可逆生成和分解,以及尺寸范围在1~10 nm的金属颗粒的可逆还原和氧化。一般来说氧化锂是化学惰性的,很难被分解。但是纳米金属可以催化氧化锂分解。因此,金属纳米颗粒的形成促进了这类金属氧化物作为负极材料的电化学反应,并获得大的可逆容量和稳定的可逆循环。基于转化反应机制的电化学反应如下:
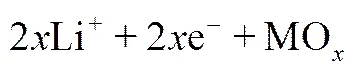
式中,M代表Cr、Mn、Fe、Co、Ni和Cu等金属元素。
(3)嵌/脱锂机制(insertion/extraction mechanism)锂离子可以在具有层状结构的金属氧化物的层状晶格之间可逆地嵌入/脱出,同时不破坏晶格的完整性。这类金属氧化物在反应过程中体积变化较小,结构稳定,确保了循环的稳定性。基于嵌/脱锂机制的MoO2、MoO3、WO3和TiO2等金属氧化物与锂离子反应时的电化学反应如下:

包括MoO2、MoO3、WO3和TiO2在内的多种金属氧化物都遵循嵌/脱锂机制。
1.2 金属氧化物作为锂离子电池负极材料的优缺点
理想的锂离子电池负极材料需要具备以下几个条件:①能够和锂离子进行可逆反应,并且嵌锂的电位尽可能接近金属锂;②有较高的比容量;③拥有良好的离子及电子导电性,保证在离子迁移和电子传递过程中的阻抗尽量小;④良好的结构稳定性,从而得到优异的循环性能;⑤来源广泛、价格低廉、环境友好。依据以上对理想负极材料的要求,可以看出相较于现在的商用石墨负极材料,金属氧化物负极材料最大的优点在于它们的高比容量和安全特性。如表1所示,常见金属氧化物负极的理论容量是传统石墨负极材料的2倍以上。现阶段,低的离子、电子传导率和较差的循环稳定性是阻碍金属氧化物负极材料工业化应用的主要原因。如对于合金/去合金化机制的SnO2材料,在合金化和去合金化过程中会产生巨大的体积变化(约300%)。这个过程会增加电极内部应力,导致活性物质粉化并从集流体上脱落,降低了循环寿命[8]。与合金/去合金化机制负极材料的情况类似,基于转化反应机制和脱/嵌锂机制的负极材料也会因为巨大的体积变化而降低材料的循环性能。此外,低的电子传输效率增加了电极极化,降低了锂离子电池的功率密度。

表1 常见金属氧化物负极材料的理论比容量
1.3 构筑空心结构金属氧化物
为了解决金属氧化物作为锂离子电池负极材料所存在的问题,从而改善其电化学性能,目前的优化手段主要集中在以下两个方面:一方面是设计金属氧化物与其它功能材料的纳米复合物,如与无定形碳[9]、碳纳米管[10]、石墨烯[11]和导电聚合物[12]等材料复合。这些被用作复合材料的导电基体不仅能够作为金属氧化物巨大体积膨胀的物理缓冲,还能提高电极材料整体的导电性;另一方面是制备多种结构的纳米材料,如空心结构[13]、介孔结构[14]、纳米线阵列[15]和薄膜结构[16]等。
材料的纳米化设计为金属氧化物在锂离子电池中的研究和应用打开了一扇大门[17-24]。与普通块状材料相比,纳米材料用在锂离子电池中能够表现出明显优势:①纳米尺度的粒子缩短了锂离子和电子的扩散路径,提高了锂离子和电子的传输速率;②纳米材料能够带来一些块状材料不能发生的新的储锂反应;③电极材料的纳米化增加了电极材料和电解液的接触面积,提高了界面锂离子的流通量。相较于其它纳米结构的金属氧化物,空心结构金属氧化物作为锂离子电池负极材料时表现出了许多特有的优势[25-26],可以归结为以下几点:①空心结构能够有效缓冲金属氧化物在充电过程中的巨大体积膨胀,从而缓解容量衰退;②空心结构拥有更高的比表面积,并且其中的孔洞能够提供额外的储锂位置,有利于提高电极材料的比容量;③空心结构拥有较薄的壳层,有利于提高锂离子的传输速率,从而提升其倍率性能。
2 空心结构金属氧化物的制备
鉴于空心结构金属氧化物表现出的优异性能,研究者们设计了一系列不同的制备方法和相应的改进工艺。这些方法总体上可以分为两类:模板法和免模板法。下文详细介绍这两种方法。
2.1 模板法
模板法是制备空心结构金属氧化物最普遍和有效的方法,其总体线路就是将纳米材料吸附在多种可以去除的模板之上。基于模板的不同,可以将模板法分为硬模板法和软模板法两种。
(1)硬模板法 硬模板法是制备空心结构金属氧化物的常用方法。如图2所示,硬模板法主要包括以下4个步骤:①硬模板的制备;②对硬模板进行表面处理,从而得到理想的表面结构;③通过合适的方法在硬模板表面包覆目标产物或者前驱体,然后处理得到致密的壳层;④利用合适的方法选择性去除硬模板得到最后的空心结构。常用的硬模板有聚苯乙烯(PS)球、碳基材料、金属氧化物和二氧化硅球等。由于硬模板种类的多样性,可以得到多种金属氧化物的空心结构。下文介绍一些例子来说明硬模板法制备金属氧化物空心结构的具体过程。
PS球因为制备方法简单、粒径大小和表面官能团可控等优点,已经成为制备空心结构金属氧化物的常用模板之一。PS球模板制备空心结构一般包括两个步骤:首先通过沉淀或者直接反应等方式将金属盐前驱体包覆在PS球表面,最后通过煅烧或者溶解处理得到相应的空心纳米结构。YANG等[27]首先报道了用硫酸硫化的PS球作为模板制备无机物空心结构。然后他们还用特殊空心PS球模板制备了双层壳结构的TiO2空心球[28-29]。经过硫酸处理后的PS球得到了磺化,使得表面的亲水性加强,更加容易吸收包括金属离子、金属氧化物前驱体和有机前驱体在内的功能化组分。类似地,DING等[30]利用磺酸基团(—SO3H)功能化过的PS空心球为模板,制备了表面为纳米片结构的NiO空心球。金属盐前驱体不仅可以吸附在PS球的表面形成致密的金属前驱体层,而且还能通过微小孔道渗透进入PS球的内层,在内部官能团的帮助下形成较厚的壳层。ZENG等[31]利用二氧化钛溶胶渗透进入经过处理的PS球形成二氧化钛-聚合物的纳米复合物,然后通过煅烧得到多层壳的二氧化钛空心结构。
碳基材料包括碳球、碳纤维和碳纳米管等,这些材料都可以用作制备空心结构金属氧化物的模板。碳微球和碳纤维拥有多孔和亲水的特性,能够更好地与金属氧化物前驱体溶液混合,然后通过煅烧去除模板后制备得到相应的空心结构金属氧化物。因为碳基模板表面本身就存在许多官能团,所以免去了表面活化和激活的步骤,与其它模板相比极大地减少了反应步骤和制备时间。WANG等[32]利用碳微球作为模板,在溶液中吸附金属离子后煅烧得到了一系列空心结构的铁酸盐,并且通过控制金属盐的浓度有效调控壳层的厚度。他们还利用碳球模板精确控制得到了多层壳空心结构的氧化锌微米球。在碳微球吸附金属离子之后,利用煅烧温度、时间和速率作为变量,不仅能够控制空心球壳层的数量,还能调控内部壳层的间隙,得到一系列复杂内部结构的氧化锌空心球[33]。在此基础上,WANG等充分利用碳球模板的吸附特性,通过改变金属离子、溶剂配比、溶液pH值等实验条件,精确控制得到了具有不同内部结构的Fe2O3[34]、Mn2O3[35]、Co3O4[36]、TiO2[37]和SnO2[38]空心球。
阳极氧化氧化铝(AAO)是制备金属氧化物空心管的最常用模板之一。AAO通过金属铝在酸性溶液中电化学氧化制备,拥有规整的一维多孔通道。通过调控温度、浓度和电流密度等实验参数能够得到具有不同孔洞直径的AAO模板。AAO模板用来制备金属氧化物空心结构有以下两方面的优势:首先它们拥有高密度的规则孔洞,并且能在至少700 ℃以下保持化学稳定;其次是可以通过多种方法去除模板,可以根据目标产物的特点合理选择酸或碱刻蚀的方法溶解模板。WANG等[39]报道了一种利用AAO模板制备的SnO2纳米管。制备时首先在AAO模板的一维孔道中制备胶体状的SnO2纳米颗粒,然后通过热处理让胶体产生化学联结,最后利用氢氧化钠刻蚀去除模板。制备得到的SnO2纳米管具有均一的多孔形貌,直径在180~230 nm之间。除此之外,Cu2O也可以被用作模板来制备其它空心结构金属氧化物纳米结构。Cu2O模板的优势在于可以制备出多种形貌的模板,如球型、立方块、正八面体等对称结构,最终得到多种形貌的空心结构。此外,Cu2O的化学活性较强,可以简单地利用酸或碱刻蚀去除。LOU等[40]在文献中报道了利用Cu2O立方块作为模板制备空心结构SnO2立方块的方法。该课题组还用类似的方法制备了多种形貌的Cu2O@Fe2O3、Cu@Fe3O4、Fe2O3和Fe3O4等空心结构金属氧化物[41]。
SiO2模板具有毒性低、比表面积高、孔洞体积大和孔洞尺寸可调节的特点,是作为空心结构制备基体的理想原料。制备步骤包括利用合适的无机前驱体在SiO2模板上形成致密的壳层,然后通过氢氟酸或氢氧化钠去除SiO2模板。DING等[42]利用介孔SiO2“纳米反应器”制备了分散均一和结构稳定的SnO2空心球。制备过程首先让SnCl2溶液扩散进入SiO2“纳米反应器”的介孔壳层中,热处理后SnCl2会原位生成SnO2,得到双壳层的SnO2@SiO2空心结构。最后通过氢氟酸刻蚀外面的SiO2壳层得到SnO2空心球。在另外一个报道中,LOU等[43]通过在橄榄状SiO2模板表面沉积多晶的SnO2,制备了双层壳结构的SnO2纳米蚕茧状结构。
牺牲模板是一类制备金属氧化物空心结构的特殊硬模板,其区别于传统硬模板的主要特点是让前驱体参与空心结构的制备过程。但是与传统的硬模板法相类似,牺牲模板决定了空心结构的最终形貌。FEI等[44]利用MnCO3纳米球和纳米立方块作为牺牲模板,制备了形貌均一的MnO2空心球和空心立方块。制备的过程包括3个步骤:首先制备球形和立方块形状的MnCO3前驱体,然后通过控制加入KMnO4的量来调控MnO2壳层的厚度,最后利用盐酸去除内部的MnCO3得到最后的MnO2空心结构。WANG等[45]通过可控的溶解单个金属盐,发展了一种利用牺牲模板法制备空心结构金属氧化物的通用方法,并基于这种方法制备了Fe、Co、Ni和Mn基空心结构金属氧化物。
除了牺牲模板法,硬模板法的制备步骤一般包括制备模板,然后在模板表面包覆纳米材料,最后去除模板。硬模板法的优点可以概括为以下几点:①硬模板法是制备空心结构的普遍方法,空心结构的直径等参数可以通过调控模板的大小实现;②能够得到形貌均一、分散性良好的产品。但是另一方面,模板法的缺点也非常明显,即制备过程比较繁琐,在去除模板的过程中导致结构和形貌的坍塌,并且无法大规模制备产品,价格昂贵。因此需要寻找更加简单廉价的途径来制备空心结构金属氧化物。
(2)软模板法 软模板法制备金属氧化物空心结构包含3个步骤:首先利用微乳液、表面活性剂和气泡等形成软模板,然后在模板的表面形成目标产物前驱体的壳层,最后处理得到空心结构金属氧化物。与硬模板法相比,软模板法能够更加简单地去除模板。但是,软模板存在形貌不稳定和结构不稳定等缺点,因此很难控制最终金属氧化物空心结构的大小、均一性和微观形貌。尽管如此,基于软模板法研究者们还是制备得到了一系列的金属氧化物空心结构,如Fe2O3、Cu2O和Co3O4等。
LOU等[46]利用准乳液模板法制备了形貌均一的Fe2O3空心球。在合成过程中,他们首先将丙三醇分散在水中形成油水混合微乳液滴,然后让含铁元素前驱体在这些微乳液滴表面进行自组装,接着通过水热处理将前驱体转化为Fe2O3晶体。因为内部的微乳液滴模板能够通过溶剂简单地去除,制备的Fe2O3空心结构拥有良好的结构稳定性。XU等[47]利用CTAB单层和多层囊泡作为软模板制备了单层和多层的Cu2O空心球。如图3所示,作者通过简单控制CTAB的浓度得到了单层、双层、三层和四层Cu2O空心球。通过类似的合成方法,WANG 等[48]在PVP软模板的帮助下拓展制备了单层、双层和三层的Co3O4空心球。这些空心球的形貌均一、分散性良好。此外,通过这种PVP软模板的方法还可以大规模制备Co3O4空心结构样品。除此之外,ZENG等[49]还利用水热的方法制备了纺锤型和球型的Fe2O3空心结构。他们认为水热过程中,尿素分解产生的二氧化碳气泡能够作为软模板引导生成空心结构金属氧化物。
2.2 免模板法
模板法制备空心结构金属氧化物有着结构可控的特点,但是在去除模板的过程中往往需要采用繁琐的煅烧和化学刻蚀手段,容易导致空心结构的破坏和产物化学结构及成分的变化。因此,寻找能够可控且大规模制备金属氧化物空心结构的方法具有重要意义。目前为止,研究者已经发展了包括利用柯肯德尔效应(Kirkendall effect)和奥斯特瓦尔德熟化(Ostwald ripening process)在内的许多新方法来制备空心结构金属氧化物。这个部分主要介绍基于这两种手段的新方法。
(1)奥斯特瓦尔德熟化效应 在温度较高的反应系统中,大的团簇或颗粒会逐渐长大,而小的团簇或者颗粒会逐渐减小直到完全溶解,这个现象被称为奥斯特瓦尔德熟化。该过程的驱动力就是表面能的减小。奥斯特瓦尔德熟化反应已经成为制备空心结构金属氧化物的重要方法。LOU等[50]利用溶剂热手段,通过奥斯特瓦尔德熟化的方法制备了SnO2空心球。球的大小能够通过改变前驱体的浓度进行调节。CHEN等[51]通过溶剂热的方法制备了平均直径为700 nm的多孔Fe3O4空心球。制备得到的空心球形貌均一、分散良好,并且通过一系列以时间为变量的实验,他们观察了产物形貌结构的演变过程。本课题组XIE等[52]利用简单的水浴法制备了多种空心结构的柠檬酸锌微米球,然后在空气中煅烧得到相应结构的ZnO空心微米球。如图4所示,在室温熟化过程中,随着熟化时间的增加,柠檬酸锌微米球逐渐从实心向蛋黄壳及空心结构转变。此外,将不同空心结构的柠檬酸锌微米球在惰性气氛下煅烧,可以得到相应结构的ZnO-C纳米复合物[53]。柠檬酸锌中的羧酸根带负电,在水溶液中能够很好地吸附带正电的金属离子。利用这个原理,XIE等[54-59]通过改变金属离子的种类和浓度,得到了一系列的空心结构氧化锌基复合微米球。对比软/硬模板法,奥斯特瓦尔德熟化在制备空心结构金属氧化物的过程中存在明显的优点:它不仅可以避免硬模板法在去除模板的过程中遇到的问题,还能制备软模板法较难得到的均一分散的形貌。然而,由于缺乏直接的证据,通过奥斯特瓦尔德熟化方法制备空心结构金属氧化物的具体机理还有待进一步研究。
(2)柯肯德尔效应 该效应源于对两种不同扩散速率金属在扩散过程中会出现缺陷的解释,现在已经成为制备空心结构材料的重要方法。一般来说,基于此方法制备空心结构氧化物的机理如下:在温度升高的过程中,金属纳米粒子暴露在氧气环境中,向外扩散的金属阳离子相比向内扩散的氧阴离子具有更高的扩散速率,在此过程中产生了相应的空穴,通过空穴的积累获得相应的空心结构。这种方法同样适用于其它金属化合物,如金属硫化物和金属硒化物等。YIN等[60]利用柯肯德尔效应制备了一系列的钴基空心结构,如CoO、CoS和CoSe。HUANG等[61]在常温下将具有磁性的铁纳米粒子在水溶液中进行简单的熟化,得到了一维链状的Fe3O4空心结构。XIA等[62]利用溶剂热制备了空心的Co3O4纳米阵列,其机理是基于轴向错位和柯肯德尔效应的协同作用。SONG等[63]报道了一种内部孔洞可控的多孔NiO纳米管,其制备方法也是基于柯肯德尔效应和相变过程中的体积变化之间的相互作用。如图5所示,WU等[64]制备了SnO2-C的纳米复合空心结构,通过不同时间下产物的形貌分析,证实了纳米尺度的柯肯德尔现象在Sn球转化为SnO2-CP复合空心球的过程中起到至关重要的作用。
3 空心结构金属氧化物的储锂特性
3.1 二氧化钛
二氧化钛作为负极材料具有合适的工作电压、高的安全性和较小的体积变化等优点。但该材料的导电性和倍率性能较差。将材料在纳米尺度上进行结构优化是解决该问题的一个有效方法[65]。LOU等[66]利用α-Fe2O3模板合成了空心结构的TiO2,并测试了其电化学性能。在0.2 C的测试电流密度下循环35次,容量保持在172 mA·h/g,即使在2 C高倍率电流密度下充放电循环,比容量依然达到112 mA·h/g,表现出优异的倍率性能。WANG等[67]利用氧化亚铜为模板制备了纳米笼结构的TiO2,在1 C的电流密度下,循环200次容量保持在140 mA·h/g,具有良好的循环稳定性。YU等[68]合成了金红石型亚微米级空心TiO2,在5 C的电流密度下,循环500次,容量保持在141 mA·h/g。此外该材料还表现出优异的倍率性能,在经过30 C的电流密度循环10次后,当测试电流密度回到1 C时,比容量迅速回升到210 mA·h/g。ZHANG等[69]利用碳球模板合成了高度结晶颗粒组成的中空TiO2纳米球。该材料在1 C的电流密度下,循环300次容量保持在147.6 mA·h/g;在40 C的电流密度下,容量为60.8 mA·h/g;当测试电流密度回到1 C时,容量迅速回升到158.2 mA·h/g。如图6所示,DING等[70]利用PS空心球作为模板合成了纳米片组成的空心TiO2纳米球。相对于原来的小颗粒组成,这种纳米片层状能暴露出更多的(001)晶面。而(001)晶面的暴露对该材料的倍率性能起到至关重要的作用。该材料在1 C的测试电流密度下循环200次,比容量保持在148 mA·h/g。
3.2 锡基氧化物
近年来,锡氧化物由于高的比容量受到广泛的关注,被认为是极具应用潜力的负极材料[8]。但研究发现锡氧化物在充放电过程中存在较大的体积变化,会导致电池性能急剧下降。针对这一问题,目前解决思路主要集中在纳米结构的构建,而模板法制备空心结构是目前比较常用的方法[71-74]。早在2000年,ZHONG等[75]就用PS球模板法制备了空心球状结构的TiO2和SnO2。WANG等[76]利用碳球模板合成了SnO2中空纳米球,并测试了其电化学性能。在0.2 C的电流密度下,首次放电容量为456 mA·h/g,循环60圈后依然保持91.4%的比容量。SUN等[77]采用胶体多糖为模板合成了包括SnO2在内的多种金属氧化物空心纳米球,然而碳模板在煅烧时放出的大量二氧化碳使得空心结构遭到破坏。LOU等[78]利用Si纳米球为模板合成出了SnO2空心纳米球,通过再次水热沉积成功制得双壳层SnO2空心纳米球结构。WANG等[40]用CuO为模板合成了SnO2空心纳米立方块结构,在0.2 C的电流密度下,首次放电和充电比容量分别为2242 mA·h/g和 1041 mA·h/g;循环40圈后其可逆比容量仍保持在570 mA·h/g。LOU等[50]提出了一种合成SnO2空心纳米球的免模板法,该方法基于奥斯特瓦尔德熟化机制,通过控制混合物极性和反应剂溶度可以控制SnO2的大小和纳米结构。
相对于单一过渡族金属氧化物,混合金属氧化物由于存在协同效应显示出更好的电化学性能[79]。本课题组利用自模板法合成了中空结构ZnSnO3-C立方块,如图7所示,其壳层厚度在200 nm左右,外层均匀包覆着厚度为10 nm左右的碳层。该材料首次放电比容量高达2255 mA·h/g,在100 mA/g的电流密度下循环50圈比容量为703 mA·h/g[80]。在此基础上我们还通过反复刻蚀的方法制备了双层壳结构的ZnSnO3,进一步提高了电化学性能[81]。此外,制备石墨烯包覆的电极材料也是提高其性能的一种常用的改性方法。WANG等[82]制备了一种橄榄石状的还原氧化石墨烯包覆ZnSnO3复合材料。在100 mA/g的电流密度下,首次放电容量1691 mA·h/g,100次循环过后容量保持在713 mA·h/g。此外,该课题组还合成了还原氧化石墨烯包覆空心ZnSnO3的复合材料[83],在100 mA/g的电流密度下循环100次,容量为745.4 m·Ah/g,并表现出优异的倍率性能,在1200 mA/g的电流密度下比容量依然保持在552.6 mA·h/g左右。
3.3 钴、镍基氧化物
2000年TARASCON课题组[5]利用纳米Co3O4代替石墨等传统负极材料实现了较高的比容量。尽管微/纳米Co3O4的最佳比容量已经提高到了1450 mA·h/g,但是差的循环稳定性和低的倍率性能限制了材料的实际应用。通过设计空心微纳米结构Co3O4能够有效缓解体积膨胀,缩短离子与电子的传输路径,从而改善材料的电化学性能。WANG 等[36]以碳微球为模板通过精确控制合成条件实现了高纯度Co3O4多层空心结构的批量制备。如图8所示,通过改变实验温度和溶剂类型,有效调控了碳球对金属离子的吸附程度,最终实现空心结构层数的有效调控。电化学性能测试发现,在50 mA/g的电流密度下,三层和四层壳结构的Co3O4首次放电容量分别为2063.7 mA·h/g和1626.2 mA·h/g,循环30圈后还能保持在1615.8 mA·h/g和1011.5 mA·h/g,当电流密度增加到2 A/g时,具有三层壳结构的Co3O4的比容量依旧维持在1117.3 mA·h/g以上。值得注意的是,当电流再次减小到50 mA/g时,容量还能恢复到1505 mA·h/g。相比其它的模板法,通过金属有机框架(MOF)得到的金属氧化物由于具有稳定的形貌和大的孔隙率,作为负极材料表现出很大的优势。2015年TIAN等[84]通过MOF的热分解制得Co3O4多孔四面体空心结构,分别在50 mA/g和200 mA/g的电流密度下进行充放电测试,经过60圈循环后,放电容量对应为1196 mA·h/g和1052 mA·h/g,库仑效率稳定在98%。倍率性能测试表明,在0.8 A/g电流密度下循环,可逆容量维持在606 mA·h/g;当电流减小到50 mA/g时,可逆容量还能达到1125 mA·h/g。SHAO等[85]用MOF法制备了一种十四面体空心结构Co3O4,与一般的空心结构不同,它的内部有一个多孔的球形核心,核心与外壳之间是中空的。电化学测试表明,在100 mA/g的电流密度下,首圈可逆容量为1118 mA·h/g,但是随着循环的进行,由于电极材料多层结构的活化先后不同,容量有一个波动,循环60圈后达到最高值(1550 mA·h/g),100圈循环后比容量维持在1335 mA·h/g;倍率性能测试表明,在2 A/g的电流密度下循环时可逆容量为650 mA·h/g,高于一般纳米结构四氧化三钴的比容量。2014年,WU等[86]利用MOF法合成了一批各向异性的菱形十二面体空心结构Co3O4,探究了煅烧条件对孔洞的形成以及形貌保持的影响。电化学储锂测试显示,在100 mA/g的充放电流下,首圈可逆容量为921 mA·h/g,库 仑效率为70%,100圈循环后放电容量衰减至 780 mA·h/g,库仑效率稳定在98%。虽然循环可逆容量偏低,但倍率性能优异,在5 A/g电流密度下测试,放电容量能够维持在800 mA·h/g以上。
此外,YAO等[48]用PVP软模板法制备了由定向排列的纳米片构成的Co3O4多层壳结构。分别对单层、双层和三层壳结构的Co3O4样品组装成半电池进行测试,在178 mA/g的电流密度下,3层壳结构的首圈可逆容量最高,约为1030 mA·h/g,循环50圈后,可逆容量降到611 mA·h/g。对双层壳结构进行进一步循环测试表明,在电流密度为250 mA/g充放电时首圈和50圈的可逆容量分别为750.1 mA·h/g和731 mA·h/g,而2 C(1 C=890 mA/g)的倍率性能测试显示可逆容量为500.8 mA·h/g。YAN等[87]在2012年用自模板法制备了Co3O4纳米立方块,探明在550 ℃温度热处理时立方块的形貌和性能最优,50 mA/g的电流密度下循环30圈后的放电容量为970 mA·h/g。除了常见的空心球结构,LOU等[88]利用自模板法制备了空心管状结构Co3O4,50 mA/g电流下进行半电池测试,首圈可逆容量为950 mA·h/g,30圈后性能稳定在918 mA·h/g,然而循环80圈后比容量下降到400 mA·h/g左右。为了进一步提高Co3O4的导电性,SUN等[89]利用静电吸附的方法制备了石墨烯包覆Co3O4空心结构,在1 A/g的电流密度下循环500圈后,容量稳定在600 mA·h/g左右并且没有下降的趋势。
与钴基氧化物类似,NiO的比容量高,安全性好,并且成本低,也是研究热点材料之一。但是NiO电极材料也存在诸多问题,如脱嵌锂的过程中体积效应大,易造成材料粉化。因此必须对NiO进行改性设计。YOSHIO等[90]在2014年利用胶束软模板法制备了直径在28 nm左右的NiO空心球,在0.3 C电流下电化学性能测试表明首圈放电容量为 1223 mA·h/g,循环50圈后可逆容量为392 mA·h/g,优于一般的NiO纳米管结构电极。对循环后的电极材料进行透射电镜观察,发现有小部分的颗粒发生了变形和破裂。考虑到模板法很难实现大规模生产,XIE等[91]通过两步法首先制备草酸盐前驱体,接着在空气中煅烧得到了空心结构的NiO微米球。电化学性能测试显示在200 mA/g的电流下,首圈可逆容量为975.1 mA·h/g,但是不可逆容量损失达到了37.8%,循环30圈后可逆容量为380 mA·h/g。ZHONG等[92]利用喷雾热解的手段制得了纳米晶NiO空心球,同时探究了CMC和PVDF作为黏结剂的区别。在100 mA/g的电流密度下,以PVDF为黏结剂的首圈可逆容量为747 mA·h/g,但是不可逆容量损失达到了43%;而以CMC为黏结剂的电极材料虽然首圈可逆容量只有698 mA·h/g,但是循环40圈后的放电容量还有547 mA·h/g,相比之下,NiO(以PVDF为黏结剂)只有157 mA·h/g。此外,LIU等[93]还利用生物模板法得到了空心结构的NiO纳米管,在200 mA/g电流密度下进行充放电测试,首圈放电容量为1072 mA·h/g,库仑效率只有58.2%,循环100圈后,可逆容量保持在600 mA·h/g左右,循环性能表现优异;而在500 mA/g和1000 mA/g电流下分别循环100圈后放电容量还能维持在550 mA·h/g和500 mA·h/g左右,库仑效率在98%以上,显示出极好的倍率性能。
3.4 铁、铜基氧化物
铁、铜基氧化物以其高理论容量(1000 mA·h/g)、无毒性、低加工成本及安全性好等优点受到了人们的格外重视[94]。基于转化反应的铁氧化物也存在很多亟待解决的问题:充电时锂离子从Li2O母体中的脱出是热力学不稳定的;铁基氧化物在充放电过程中较大的体积变化会造成其循环稳定性的降低;铁基氧化物较低的电导率会导致其在高倍率下的性能快速退化[95]。目前,解决以上问题的主要手段是通过调节电极材料的形貌、结构、孔隙率以及微米和纳米结构的复合以提高电极材料在电化学过程中的结构稳定性,其中空心结构,如空心球、空心纳米管等受到了特别关注。
XU等[34]通过碳球模板法制备了多壳层的α-Fe2O3空心球,通过控制合成条件,能够调控空心球的壳层厚度、壳层数目以及壳层的孔隙率。经过优化,壳层较薄、孔隙率较高、且具有三层同心壳层的空心球的容量最高,稳定性最好。在50 mA/g的充放电电流下,其容量高达1702 mA·h/g。该材料优良的电化学性能源于3个方面:较大的比表面积;多壳层提供了更多的储锂位置;壳层上的孔隙不仅有利于锂离子和电子迁移,而且还能够缓冲充放电过程中体积变化引入的内部应力。WANG等[46]通过准模板法合成了α-Fe2O3空心球。在200 mA/g的电流密度下,该材料的稳定容量为750 mA·h/g,经过100次的充放电测试后其容量为710 mA·h/g,展现了较高的容量保持率。CHAUDHARI等[96]通过静电纺丝法制备了一维空心纳米纤维状α-Fe2O3,相互连接的空心结构提高了α-Fe2O3纳米纤维的比表面积,在60 mA/g电流密度下的可逆容量高达 1293 mA·h/g。CHO等通过静电纺丝法制备了α-Fe2O3纳米棒-碳复合的纳米纤维,其中纳米棒由空心球组成。空心纳米球能够有效缓解循环过程中的应力,与碳复合的特殊结构提高了材料的结构稳定性和导电性。在1 A/g的电流下,该材料经过300次循环后的放电容量为812 mA·h/g,而同样条件下的空心α-Fe2O3纳米纤维的容量只有285 mA·h/g。除此之外,ZHOU[97]用喷雾热解法制备α-Fe2O3多壳层空心球,该方法制备简单,具有可扩展性。
虽然α-Fe2O3具有以上优点,但是其导电性较差,倍率性能需要进一步提高。为此,人们发展了导电性更好的Fe3O4空心结构。CHEN等[51]基于定向自组装和奥斯特瓦尔德熟化原理制备了具有多孔结构的空心Fe3O4,在100 mA/g电流下,循环50圈后,其可逆容量为500 mA·h/g。与碳复合时,相同条件下的容量提高到了700 mA·h/g。这是Fe3O4具有较高的理论容量、纳米尺寸化的粒子、独特的空心结构和能够提高电导率和结构稳定性的碳包覆层协同作用的结果。LOU等[98]使用一种简单的溶剂热法制备了由纳米片组成的Fe3O4空心纳米球,溶剂为乙二醇,添加剂为乙二胺。如图9所示,随着反应时间的增加,产物的形貌逐渐从实心向空心转变。在200 mA/g的电流下,经过100次循环后,其可逆比容量为580 mA·h/g,展现了优异的电化学性能。为了进一步提高倍率性能,很多课题组转向了碳复合Fe3O4材料。如CHEN等[99]通过一锅溶剂热法制备了直径为750 nm的尖晶石结构的空心Fe3O4/C复合结构。这种结构的可逆比容量高达984 mA·h/g。此外,该材料还具有优良的倍率性能,在5 C充放电电流下,经过70圈循环后,其比容量为460 mA·h/g。除石墨外,LU等[100]基于自组装原理制备了石墨烯包覆的空心Fe3O4球。该复合材料的可逆比容量为900 mA·h/g,经过50圈循环后,容量几乎没有衰减。经过90圈的不同倍率下的充 放电过程后,其在100 mA/g电流下的比容量为 832 mA·h/g,展现了优异的循环稳定性。
受铁基氧化物材料作为负极材料的诸多优点的启发,研究人员还研发了铜基负极材料。作为负极材料,铜基氧化物理论容量较高(CuO为670 mA·h/g)、价格低、来源丰富、环境友好、热力学稳定性和化学稳定性高,因而受到了研究人员的重视[101]。RYU等[102]使用CTAB多壁囊泡作为软模板合成了多壳层空心CuO球。多壳层的空心结构能够缓冲CuO负极材料在充放电过程中的应力,同时还能保护CuO不被电解液侵蚀。此外,多壳层结构还能提高电极材料与电解液的接触,缩短电子和锂离子扩散距离,因此该材料具有较好的循环稳定性。YAN等[103]基于奥斯特瓦尔德熟化原理,通过控制反应时间,制备了CuO固体球、CuO空心球和CuO/Cu2O空心球。其中CuO空心球的电化学性能最好,经过30圈循环后,其保留容量为598 mA·h/g。LI等[104]基于柯肯达尔效应制备了三维树突状空心CuO微/纳米结构。经过优化,外部为纳米管,内部为致密膜的空心结构具有最好的电化学性能,在0.5 C电流下循环50次后,其平均库仑效率为97%,容量保持率为57.9 %。LIU等[105]通过谷氨酰胺辅助法制备了绒球状CuO空心微球。在0.1 C电流下循环50次后,其保留容量为683.7 mA·h/g。CHEN等[106]通过水热法合成了高孔隙率的蒲公英状空心CuO微球。0.2 C电流下,经过50次循环后,保留容量超过600 mA·h/g。CHEN等[107]基于柯肯德尔效应制备了空心CuO纳米粒子/石墨烯复合结构,该材料在50 mA/g电流下的比容量为640 mA·h/g,其容 量保持率为96%;在1 A/g的电流下循环时其 可逆容量为485 mA·h/g,500次循环后保留容量为281 mA·h/g。
3.5 锰、锌基氧化物
锰基氧化物是一种新型的锂离子电池负极替代材料[108]。相对于其它金属氧化物负极材料,锰基氧化物具有相对高的理论比容量和低的充电电压等优势。同时,锰元素在地壳中的储量十分丰富,且毒性较低,对环境相对友好。锰基氧化物的储能是通过转化反应来实现,即可逆的氧化还原反应。二元锰基氧化物包括MnO、Mn3O4、Mn2O3和MnO2。2000年,TARASCON等[5]即开始对包括MnO、Mn3O4、Mn2O3和MnO2在内的锰基氧化物进行了研究。YUE等[109]利用碳球作为模板制备了空心结构的MnO、Mn3O4和MnO2中空结构纳米球,多孔的表面以及纳米尺度的颗粒对锰基氧化物的储锂性能有了很大的提高,3种材料在100 mA/g电流下循环60圈后,其比容量分别有840 mA·h/g,1165 mA·h/g和1515 mA·h/g;在电流增加至500 mA/g循环150圈后,可逆比容量仍有637 mA·h/g、820 mA·h/g和1050 mA·h/g。JIAN等[110]利用气凝胶模板法制备了Mn3O4中空纳米球,在200 mA/g电流下循环140圈后,其可逆比容量值为980 mA·h/g,在10 A/g的大电流下仍能保留300 mA·h/g的比容量。SEKHAR等[111]采用简单的水热法通过奥斯特瓦尔德熟化制备了Mn2O3中空微米球,在100 mA/g的电流密度下循环100圈后,其比容量保留在610 mA·h/g左右。QIAO等[112]测试了实心、中空以及蛋黄核壳结构的Mn2O3微米球的电化学性能,研究发现中空以及蛋黄结构的Mn2O3负极材料具有比实心Mn2O3更优异的循环性能和倍率性能。LIN等[113]发现三层壳结构的Mn2O3中空纳米立方块具有优异的储锂性能,在500 mA/g电流密度下循环100圈后,仍有533 mA·h/g的比容量保留。LI等[114]通过奥斯瓦尔德熟化,在没有表面活性剂和模板的条件下制备了中空海胆状的MnO2,在270 mA/g电流密度下循环40圈后,其可逆比容量为481 mA·h/g。
三元锰基氧化物(AMn2O4)具有尖晶石或者类似尖晶石的晶体结构。其在锂离子电池负极材料中也得到了广泛的研究。ZnMn2O4作为一种特殊的 锂离子电池负极材料,具有高的理论比容量 (1008 mA·h/g)和相对较低的氧化电势(Zn-1.2 V,Mn-1.5 V)。相比于ZnFe2O4和ZnCo2O4,其低的氧化电势可以有效地提高锂离子电池的输出电压从而增大电池的能量密度。ZHOU等[115]采用共沉淀法成功制备了ZnMn2O4中空微球,在400 mA/g电流密度下循环100圈后,其放电比容量为607 mA·h/g。CHEN等[116]利用MnCO3作为模板制备了由25~50 nm的ZnMn2O4颗粒组成的中空多孔微球,在100 mA/g电流密度下循环40圈后,仍有599 mA·h/g的可逆比容量保留。CoMn2O4具有不完整的尖晶石结构,作为锂离子电池负极材料也引起了研究者的兴趣。MIN等[117]利用喷雾热解的方法制备了蛋黄壳状和空心结构的CoMn2O4纳米球,在800 mA/g高电流密度下循环40圈后,比容量分别为519 mA·h/g和573 mA·h/g,而且蛋黄壳状结构的材料具有更优异的倍率性能。ZHOU等[118]通过简单的共沉淀法制备了双壳层结构的CoMn2O4微米立方块,在 200 mA/g电流密度下循环50圈后,比容量维持在624 mA·h/g左右。
ZnO基纳米材料作为锂离子电池负极材料,具有高的理论容量(987 mA·h/g),易于制备、形貌多样以及锂离子扩散系数高等优点[119]。然而,其较低的库仑效率、较快的容量衰减以及较弱的电化学动力学性质,都限制了其在锂离子电池中的实际应用。鉴于这些问题,对ZnO负极材料的改性就显得必不可少。如在ZnO表面包覆碳材料,不仅能有效地缓解体积膨胀效应,提高循环性能,而且能够提高嵌脱锂动力学性能和大倍率性能。本课题组在空心微米球结构ZnO负极材料上做了大量的研究工作。首先通过温和的水浴方法制备了柠檬酸锌微米球,通过控制熟化的时间分别得到实心、蛋黄壳和空心结构的微米球。对空心结构的微米球进行修饰,最后通过煅烧得到相应结构的ZnO基负极材料[52-53,58]。制备的蛋黄壳结构的ZnO-C复合纳米微球在 100 mA/g的电流下循环150圈后,其比容量达到520 mA·h/g。利用柠檬酸锌中的羧酸根带负电的特点,在溶液中吸附带正电的金属离子,制备了空心的ZnO/Ni/C复合材料,在100 mA/g的电流下循环120圈后,容量仍有466 mA·h/g[54]。制备的ZnO-NiO微球中在100 mA/g的电流下循环200圈后,保留了1179 mA·h/g的可逆比容量,其循环性能与容量都有了较大的改善。当对ZnO微米球进行ZnCo2O4修饰后,在100 mA/g的电流下循环200圈后,比容量达到1199 mA·h/g[57]。如图10所示,本课题组还通过静电吸附方法制备了Ag-C@ZnO-C@Ag‑C三明治空心结构微米球,壳层内部的碳基体和内外的Ag层有效地提高了ZnO的导电性能,极大提高了储锂性能,在0.2 A/g电流密度下循环200圈后,其比容量为1670 mA·h/g;当电流密度增加至10 A/g时仍有526 mA·h/g的容量保留[59]。
4 结 语
综上所述,本文重点总结了多种空心结构金属氧化物的制备方法以及它们作为锂离子电池负极材料的储锂性能。通过一系列的制备技术,可以得到不同形貌的微纳米空心结构金属氧化物。如通过模板法或免模板法可以制备形貌均一、尺寸和壳层厚度可控的金属氧化物空心球、空心管和空心立方块等。在用作锂离子电池负极材料时,微纳米空心结构氧化物拥有比块状或纳米颗粒材料更高的容量、更稳定的循环性能和更好的倍率性能,这主要是因为空心结构金属氧化物具有3个显著的优点:①空心结构能够增加电极/电解液之间的接触面积,并通过纳米孔洞提供额外的储锂位置,增加了材料的整体容量;②较薄的壳层同时缩短了电子和离子的扩散距离,从而提高了倍率性能;③中空结构有效缓冲了循环过程中的体积变化,抑制了结构的破坏和材料的粉化脱落,从而保证了更好的循环稳定性。
但是,空心结构金属氧化物材料的制备和电化学性能改善仍然存在许多挑战。在制备方法上,仍然没有一种普适的方法可以制备所有微纳米空心结构金属氧化物材料,并且现有的方法耗时费力、价格昂贵,无法实现大规模工业生产。而且,作为金属氧化物负极固有的两个缺点,低的导电率和大的体积变化仍然阻碍了其在倍率性能和循环寿命方面的进一步提高。此外,金属氧化物负极材料普遍存在问题就是首次库仑效率较低,尤其是合金型的负极材料在第一次循环中存在较高的不可逆容量 损失。
近年来,将金属氧化物与一些导电性好、延展性高的材料进行纳米复合已经成为常用的优化手段,如进行碳包覆、石墨烯及金属复合等。这些紧密结合的复合结构不仅能够提高材料的导电率,减少电极材料表面的副反应,还能够为体积膨胀提供缓冲空间,进而有效提高材料的综合电化学性能。此外,预锂化技术的应用能够显著增加氧化物负极材料的首次库仑效率,达到工业使用的要求[120-122];喷雾热解技术的发展使得大规模、低价格地制备微纳米空心结构金属氧化物成为可能。这些改进的制备方法和优化手段能够进一步促进金属氧化物负极材料实现商业化应用,帮助实现能量密度更高、充放电速度更快、更加安全的下一代锂离子电池。
[1] Goodenough J B, Kim Y. Challenges for rechargeable Li batteries[J]. Chemistry of Materials, 2010, 22: 587-603.
[2] Tarascon J M, Armand M. Issues and challenges facing rechargeable lithium batteries[J]. Nature, 2001, 414: 359-367.
[3] Dunn B, Kamath H, Tarascon J M. Electrical energy storage for the grid: A battery of choices[J]. Science, 2011, 334: 928-935.
[4] Liu J, Zhang J G, Yang Z, et al. Materials science and materials chemistry for large scale electrochemical energy storage: From transportation to electrical grid[J]. Advanced Functional Materials, 2013, 23: 929-946.
[5] Poizot P, Laruelle S, Grugeon S, et al. Nano-sized transition-metal oxides as negative-electrode materials for lithium-ion batteries[J]. Nature, 2000, 407: 496-499.
[6] Reddy M V, Subba Rao G V, Chowdari B V. Metal oxides and oxysalts as anode materials for Li ion batteries[J]. Chemical Reviews, 2013, 113: 5364-5457.
[7] Obrovac M N, Chevrier V L. Alloy negative electrodes for Li-ion batteries[J]. Chemical Reviews, 2014, 114 (23) : 11444.
[8] Idota Y, Kubota T, Matsufuji A, et al. Tin-based amorphous oxide: A high-capacity lithium-ion-storage material[J]. Science, 1997, 276: 1395-1397.
[9] LIU J, LI W, MANTHIRAM A. Dense core-shell structured SnO2/C composites as high performance anodes for lithium ion batteries[J]. Chemical Communications, 2010, 46: 1437-1439.
[10] Wen Z, Wang Q, Zhang Q, et al.growth of mesoporous SnO2on multiwalled carbon nanotubes: A novel composite with porous-tube structure as anode for lithium batteries[J]. Advanced Functional Materials, 2007, 17: 2772-2778.
[11] Khan M, Tahir M N, Adil S F, et al. Graphene based metal and metal oxide nanocomposites: Synthesis, properties and their applications[J]. Journal of Materials Chemistry A, 2015, 3: 18753-18808.
[12] Shao Q G, Chen W M, Wang Z H, et al. SnO2-based composite coaxial nanocables with multi-walled carbon nanotube and polypyrrole as anode materials for lithium-ion batteries[J]. Electrochemistry Communications, 2011, 13: 1431-1434.
[13] Li Y, Shi J. Hollow-structured mesoporous materials: Chemical synthesis, functionalization and applications[J]. Advanced Materials, 2014, 26: 3176-3205.
[14] Wang H, Wu Y, Bai Y, et al. The self-assembly of porous microspheres of tin dioxide octahedral nanoparticles for high performance lithium ion battery anode materials[J]. Journal of Materials Chemistry, 2011, 21: 10189-10194.
[15] Zhang F, Qi L. Recent progress in self-supported metal oxide nanoarray electrodes for advanced lithium-ion batteries[J]. Advanced Science, 2016,3: doi: 10.1002/advs.201600049.
[16] Sun Y, Feng X Y, Chen C H. Hollow Co3O4thin films as high performance anodes for lithium-ion batteries[J]. Journal of Power Sources, 2011, 196: 784-787.
[17] Wang Y, Li H, He P, et al. Nano active materials for lithium-ion batteries[J]. Nanoscale, 2010, 2: 1294-1305.
[18] Zhang Q, Uchaker E, Candelaria S L, et al. Nanomaterials
for energy conversion and storage[J]. Chemical Society Reviews, 2013, 42: 3127-3171.
[19] Bruce P G, Scrosati B, Tarascon J M. Nanomaterials for rechargeable lithium batteries[J]. Angewandte Chemie International Edition, 2008, 47: 2930-2946.
[20] YIN Y X, XIN S, GUO Y G. Nanoparticles engineering for lithium-ion batteries[J]. Particle & Particle Systems Characterization, 2013, 30: 737-753.
[21] Poizot P, Laruelle S, Grugeon S, et al. Nano-sized transition-metal oxides as negative-electrode materials for lithium-ion batteries[J]. Nature, 2000, 407: 496-499.
[22] Shukla A K, Prem K T. Nanostructured electrode materials for electrochemical energy storage and conversion[J]. Wiley Interdisciplinary Reviews: Energy and Environment, 2013, 2: 14-30.
[23] Arico A S, Bruce P, Scrosati B, et al. Nanostructured materials for advanced energy conversion and storage devices[J]. Nature Materials, 2005, 4: 366-377.
[24] Wu H B, Chen J S, Hng H H, et al. Nanostructured metal oxide-based materials as advanced anodes for lithium-ion batteries[J]. Nanoscale, 2012, 4: 2526-2542.
[25] Liu J, Xue D. Hollow nanostructured anode materials for Li-ion batteries[J]. Nanoscale Research Letters, 2010, 5: 1525-1534.
[26] Wang Z, Zhou L. Metal oxide hollow nanostructures for lithium-ion batteries[J]. Advanced Materials, 2012, 24: 1903-1911.
[27] Yang Z, Niu Z, Lu Y, et al. Templated synthesis of inorganic hollow spheres with a tunable cavity size onto core-shell gel particles[J]. Angewandte Chemie International Edition, 2003, 42: 1943-1945.
[28] Yang M, Ma J, Zhang C, et al. General synthetic route toward functional hollow spheres with double-shelled structures[J]. Angewandte Chemie International Edition, 2005, 44: 6727-6730.
[29] Yang M, Ma J, Niu Z, et al. Synthesis of spheres with complex structures using hollow latex cages as templates[J]. Advanced Functional Materials, 2005, 15: 1523-1528.
[30] Ding S, Zhu T, Chen J S, et al. Controlled synthesis of hierarchical NiO nanosheet hollow spheres with enhanced supercapacitive performance[J]. Journal of Materials Chemistry, 2011, 21: 6602.
[31] Zeng Y, Wang X, Wang H, et al. Multi-shelled titania hollow spheres fabricated by a hard template strategy: enhanced photocatalytic activity[J]. Chemical Communications, 2010, 46: 4312-4314.
[32] Li Z, Lai X, Wang H, et al. General synthesis of homogeneous hollow core-shell ferrite microspheres[J]. The Journal of Physical Chemistry C, 2009, 113: 2792-2797.
[33] Dong Z, Lai X, Halpert J E, et al. Accurate control of multishelled ZnO hollow microspheres for dye-sensitized solar cells with high efficiency[J]. Advanced Materials, 2012, 24: 1046-1049.
[34] Xu S, Hessel C M, Ren H, et al. α-Fe2O3multi-shelled hollow microspheres for lithium ion battery anodes with superior capacity and charge retention[J]. Energy & Environmental Science, 2014, 7: 632-637.
[35] Wang J, Tang H, Ren H, et al. pH-regulated synthesis of multi-shelled manganese oxide hollow microspheres as supercapacitor electrodes using carbonaceous microspheres as templates[J]. Advanced Science, 2014, 1: 1400011.
[36] Wang J, Yang N, Tang H, et al. Accurate control of multishelled Co3O4hollow microspheres as high-performance anode materials in lithium-ion batteries[J]. Angewandte Chemie International Edition, 2013, 52: 6417-6420.
[37] Ren H, Yu R, Wang J, et al. Multishelled TiO2hollow microspheres as anodes with superior reversible capacity for lithium ion batteries[J]. Nano Letters, 2014, 14: 6679-6684.
[38] Dong Z, Ren H, Hessel C M, et al. Quintuple-shelled SnO2hollow microspheres with superior light scattering for high-performance dye-sensitized solar cells[J]. Advanced Materials, 2014, 26: 905-909.
[39] Wang Y, Lee J Y, Zeng H C. Polycrystalline SnO2nanotubes preparedinfiltration casting of nanocrystallites and their electrochemical application[J]. Chemistry of Materials, 2005, 17: 3899-3903.
[40] Wang Z, Luan D, Boey F Y, et al. Fast formation of SnO2nanoboxes with enhanced lithium storage capability[J]. Journal of the American Chemical Society, 2011, 133: 4738-4741.
[41] Wang Z, Luan D, Li C M, et al. Engineering nonspherical hollow structures with complex interiors by template-engaged redox etching[J]. Journal of the American Chemical Society, 2010, 132: 16271-16277.
[42] Ding S, Chen J S, Qi G, et al. Formation of SnO2hollow nanospheres inside mesoporous silica nanoreactors[J]. Journal of the American Chemical Society, 2010, 133: 21-23.
[43] Lou X W, Yuan C, Archer L A. Double-walled SnO2nano-cocoons with movable magnetic cores[J]. Advanced Materials, 2007, 19: 3328-3332.
[44] Fei J B, Cui Y, Yan X H, et al. Controlled preparation of MnO2hierarchical hollow nanostructures and their application in water treatment[J]. Advanced Materials, 2008, 20: 452-456.
[45] Wang L, Tang F, Ozawa K, et al. A general single-source route for the preparation of hollow nanoporous metal oxide structures[J]. Angewandte Chemie International Edition, 2009, 48: 7048-7051.
[46] Wang B, Chen J S, Wu H B, et al. Quasiemulsion-templated formation of α-Fe2O3hollow spheres with enhanced lithium storage properties[J]. Journal of the American Chemical Society, 2011, 133: 17146-17148.
[47] Xu H, Wang W. Template synthesis of multishelled Cu2O hollow spheres with a single-crystalline shell wall[J]. Angewandte Chemie International Edition, 2007, 46: 1489-1492.
[48] Wang X, Wu X L, Guo Y G, et al. Synthesis and lithium storage properties of Co3O4nanosheet-assembled multishelled hollow spheres[J]. Advanced Functional Materials, 2010, 20: 1680-1686.
[49] Zeng S, Tang K, Li T, et al. Hematite hollow spindles and microspheres: selective synthesis, growth mechanisms, and application in lithium ion battery and water treatment[J]. The Journal of Physical Chemistry C, 2007, 111: 10217-10225.
[50] Lou X W, Wang Y, Yuan C, et al. Template-free synthesis of SnO2hollow nanostructures with high lithium storage capacity[J]. Advanced Materials, 2006, 18: 2325-2329.
[51] Chen Y, Xia H, Lu L, et al. Synthesis of porous hollow Fe3O4beads and their applications in lithium ion batteries[J]. Journal of Materials Chemistry, 2012, 22: 5006-5012.
[52] Xie Q, Li J, Tian Q, et al. Template-free synthesis of zinc citrate yolk-shell microspheres and their transformation to ZnO yolk-shell nanospheres[J]. Journal of Materials Chemistry, 2012, 22: 13541.
[53] Xie Q, Zhang X, Wu X, et al. Yolk-shell ZnO-C microspheres with enhanced electrochemical performance as anode material for lithium ion batteries[J]. Electrochimica Acta, 2014, 125: 659-665.
[54] Xie Q, Ma Y, Zhang X, et al. ZnO/Ni/C composite hollow microspheres as anode materials for lithium ion batteries[J]. Journal of Alloys and Compounds, 2014, 619: 235-239.
[55] Xie Q, Guo H, Zhang X, et al. A facile approach to fabrication of well-dispersed NiO-ZnO composite hollow microspheres[J]. Rsc Advances, 2013, 3: 24430.
[56] Xie Q, Ma Y, Zeng D, et al. Facile fabrication of various zinc-nickel citrate microspheres and their transformation to ZnO-NiO hybrid microspheres with excellent lithium storage properties[J]. Scientific Reports, 2015, 5: 8351.
[57] Xie Q, Zeng D, Ma Y, et al. Synthesis of ZnO-ZnCo2O4hybrid hollow microspheres with excellent lithium storage properties[J]. Electrochimica Acta, 2015, 169: 283-290.
[58] Xie Q, Ma Y, Zeng D, et al. Hierarchical ZnO-Ag-C composite porous microspheres with superior electrochemical properties as anode materials for lithium ion batteries[J]. Acs Applied Materials & Interfaces, 2014, 6: 19895-19904.
[59] Xie Q, Ma Y, Wang X, et al. Electrostatic assembly of sandwich-like Ag-C@ZnO-C@Ag-C hybrid hollow microspheres with excellent high-rate lithium storage properties[J]. Acs Nano, 2016, 10: 1283-1291.
[60] Yin Y, Rioux R M, Erdonmez C K, et al. Formation of hollow nanocrystals through the nanoscale Kirkendall effect[J]. Science, 2004, 304: 711-714.
[61] Huang J, Chen W, Zhao W, et al. One-dimensional chainlike arrays of Fe3O4hollow nanospheres synthesized by aging iron nanoparticles in aqueous solution[J]. The Journal of Physical Chemistry C, 2009, 113: 12067-12071.
[62] Xia X h, Tu J p, Mai Y j, et al. Self-supported hydrothermal synthesized hollow Co3O4nanowire arrays with high supercapacitor capacitance[J]. Journal of Materials Chemistry, 2011, 21: 9319-9325.
[63] Song X, Gao L, Mathur S. Synthesis, characterization, and gas sensing properties of porous nickel oxide nanotubes[J]. The Journal of Physical Chemistry C, 2011, 115: 21730-21735.
[64] Wu P, Du N, Zhang H, et al. Self-templating synthesis of SnO2-carbon hybrid hollow spheres for superior reversible lithium ion storage[J]. Acs Applied Materials & Interfaces, 2011, 3: 1946-1952.
[65] Liu Y, Yang Y. Recent progress of TiO2-based anodes for Li ion batteries[J]. Journal of Nanomaterials, 2016, 2016: 1-15.
[66] Lou X W, Archer L A. A general route to nonspherical anatase TiO2hollow colloids and magnetic multifunctional particles[J]. Advanced Materials, 2008, 20: 1853-1858.
[67] Wang Z, Lou X W. TiO2nanocages: Fast synthesis, interior functionalization and improved lithium storage properties[J]. Advanced Materials, 2012, 24: 4124-4129.
[68] Yu X Y, Wu H B, Yu L, et al. Rutile TiO2submicroboxes with superior lithium storage properties[J]. Angewandte Chemie International Edition, 2015, 54: 4001-4004.
[69] Zhang G, Wu H B, Song T, et al. TiO2hollow spheres composed of highly crystalline nanocrystals exhibit superior lithium storage properties[J]. Angewandte Chemie International Edition, 2014, 53: 12590-12593.
[70] Ding S, Chen J S, Wang Z, et al. TiO2hollow spheres with large amount of exposed (001) facets for fast reversible lithium storage[J]. Journal of Materials Chemistry, 2011, 21: 1677-1680.
[71] Chen J S, Lou X W. SnO2-based nanomaterials: Synthesis and application in lithium-ion batteries[J]. Small, 2013, 9: 1877-1893.
[72] Zhao Q, Ma L, Zhang Q, et al. SnO2-based nanomaterials: Synthesis and application in lithium-ion batteries and supercapacitors[J]. Journal of Nanomaterials, 2015, 2015: 1-15.
[73] Liu L, Xie F, Lyu J, et al. Tin-based anode materials with well-designed architectures for next-generation lithium-ion batteries[J]. Journal of Power Sources, 2016, 321: 11-35.
[74] Zhao M, Zhao Q, Qiu J, et al. Tin-based nanomaterials for electrochemical energy storage[J]. Rsc Advances, 2016, 6: 95449-95468.
[75] Zhong Z, Yin Y, Gates B, et al. Preparation of mesoscale hollow spheres of TiO2and SnO2by templating against crystalline arrays of polystyrene beads[J]. Advanced Materials, 2000, 12: 206-209.
[76] Wang Y, Su F, Lee J Y, et al. Crystalline carbon hollow spheres, crystalline carbon-SnO2hollow spheres, and crystalline SnO2hollow spheres: synthesis and performance in reversible Li-ion storage[J]. Chemistry of Materials, 2006, 18: 1347-1353.
[77] Sun X, Liu J, Li Y. Use of carbonaceous polysaccharide microspheres as templates for fabricating metal oxide hollow spheres[J]. Chemistry, 2006, 12: 2039-2047.
[78] Lou X W, Yuan C, Archer L A. Shell-by-shell synthesis of tin oxide hollow colloids with nanoarchitectured walls: Cavity size tuning and functionalization[J]. Small, 2007, 3: 261-265.
[79] Yuan C, Wu H B, Xie Y, et al. Mixed transition-metal oxides: Design, synthesis, and energy-related applications[J]. Angewandte Chemie International Edition, 2014, 53: 1488-1504.
[80] Xie Q, Ma Y, Zhang X, et al. Synthesis of amorphous ZnSnO3-C hollow microcubes as advanced anode materials for lithium ion batteries[J]. Electrochimica Acta, 2014, 141: 374-383.
[81] Ma Y, Xie Q, Liu X, et al. Synthesis of amorphous ZnSnO3double-shell hollow microcubes as advanced anode materials for lithium ion batteries[J]. Electrochimica Acta, 2015, 182: 327-333.
[82] Wang Y, Li D, Liu Y, et al. Fabrication of novel rugby-like ZnSnO3/reduced graphene oxide composites as a high-performance anode material for lithium-ion batteries[J]. Materials Letters, 2016, 167: 222-225.
[83] Wang Y, Li D, Liu Y, et al. Self-assembled 3D ZnSnO3hollow cubes@reduced graphene oxide aerogels as high capacity anode materials for lithium-ion batteries[J]. Electrochimica Acta, 2016, 203: 84-90.
[84] Tian D, Zhou X L, Zhang Y H, et al. MOF-derived porous Co3O4hollow tetrahedra with excellent performance as anode materials for lithium-ion batteries[J]. Inorganic Chemistry, 2015, 54: 8159-8161.
[85] Shao J, Wan Z, Liu H, et al. Metal organic frameworks-derived Co3O4hollow dodecahedrons with controllable interiors as outstanding anodes for Li storage[J]. Journal of Materials Chemistry A, 2014, 2: 12194-12200.
[86] Wu R, Qian X, Rui X, et al. Zeolitic imidazolate framework 67-derived high symmetric porous Co3O4hollow dodecahedra with highly enhanced lithium storage capability[J]. Small, 2014, 10: 1932-1938.
[87] Yan N, Hu L, Li Y, et al. Co3O4nanocages for high-performance anode material in lithium-ion batteries[J]. The Journal of Physical Chemistry C, 2012, 116: 7227-7235.
[88] Lou X W, Deng D, Lee J Y, et al. Self-supported formation of needlelike Co3O4nanotubes and their application as lithium-ion battery electrodes[J]. Advanced Materials, 2008, 20: 258-262.
[89] Sun H, Sun X, Hu T, et al. Graphene-wrapped mesoporous cobalt oxide hollow spheres anode for high-rate and long-life lithium ion batteries[J]. The Journal of Physical Chemistry C, 2014, 118: 2263-2272.
[90] Sasidharan M, Gunawardhana N, Senthil C, et al. Micelle templated NiO hollow nanospheres as anode materials in lithium ion batteries[J]. Journal of Materials Chemistry A, 2014, 2: 7337-7344.
[91] Xie D, Yuan W, Dong Z, et al. Facile synthesis of porous NiO hollow microspheres and its electrochemical lithium-storage performance[J]. Electrochimica Acta, 2013, 92: 87-92.
[92] Zhong C, Wang J Z, Chou S L, et al. Nanocrystalline NiO hollow spheres in conjunction with CMC for lithium-ion batteries[J]. Journal of Applied Electrochemistry, 2010, 40: 1415-1419.
[93] Liu L, Guo Y, Wang Y, et al. Hollow NiO nanotubes synthesized by bio-templates as the high performance anode materials of lithium-ion batteries[J]. Electrochimica Acta, 2013, 114: 42-47.
[94] Zhang L, Wu H B, Lou X W D. Iron-oxide-based advanced anode materials for lithium-ion batteries[J]. Advanced Energy Materials, 2014, 4: 1300958.
[95] Zheng X, Li J. A review of research on hematite as anode material for lithium-ion batteries[J]. Ionics, 2014, 20: 1651-1663.
[96] Cho J S, Hong Y J, Kang Y C. Design and synthesis of bubble-nanorod-structured Fe2O3-carbon nanofibers as advanced anode material for Li-ion batteries[J]. Acs Nano, 2015, 9: 4026-4035.
[97] Zhou L, Xu H, Zhang H, et al. Cheap and scalable synthesis of alpha-Fe2O3multi-shelled hollow spheres as high-performance anode materials for lithium ion batteries[J]. Chemical Communications, 2013, 49: 8695-8697.
[98] Wang B, Wu H B, Zhang L, et al. Self-supported construction of uniform Fe3O4hollow microspheres from nanoplate building blocks[J]. Angewandte Chemie International Edition, 2013, 52: 4165-4168.
[99] Zhang Q, Shi Z, Deng Y, et al. Hollow Fe3O4/C spheres as superior lithium storage materials[J]. Journal of Power Sources, 2012, 197: 305-309.
[100] Chen D, Ji G, Ma Y, et al. Graphene-encapsulated hollow Fe3O4nanoparticle aggregates as a high-performance anode material for lithium ion batteries[J]. Acs Applied Materials & Interfaces, 2011, 3: 3078-3083.
[101] Xu J, Gu P, Zhang J, et al. Copper-based nanomaterials for high-performance lithium-ion batteries[J]. Particle & Particle Systems Characterization, 2016, 33: 784-810.
[102] Ju J H, Ryu K S. Synthesis and performance of CuO with complex hollow structure as anode material for lithium secondary batteries[J]. Journal of the Electrochemical Society, 2011, 158: A814-A817.
[103] Guan X, Li L, Li G, et al. Hierarchical CuO hollow microspheres: Controlled synthesis for enhanced lithium storage performance[J]. Journal of Alloys and Compounds, 2011, 509: 3367-3374.
[104] Hu Y, Huang X, Wang K, et al. Kirkendall-effect-based growth of dendrite-shaped CuO hollow micro/nanostructures for lithium-ion battery anodes[J]. Journal of Solid State Chemistry, 2010, 183: 662-667.
[105] Wang J, Liu Y, Wang S, et al. Facile fabrication of pompon-like hierarchical CuO hollow microspheres for high-performance lithium-ion batteries[J]. Journal of Materials Chemistry A, 2014, 2: 1224-1229.
[106] Wang S Q, Zhang J Y, Chen C H. Dandelion-like hollow microspheres of CuO as anode material for lithium-ion batteries[J]. Scripta Materialia, 2007, 57: 337-340.
[107] Zhou J, Ma L, Song H, et al. Durable high-rate performance of CuO hollow nanoparticles/graphene-nanosheet composite anode material for lithium-ion batteries[J]. Electrochemistry Communications, 2011, 13: 1357-1360.
[108] Deng Y, Wan L, Xie Y, et al. Recent advances in Mn-based oxides as anode materials for lithium ion batteries[J]. Rsc Advances, 2014, 4: 23914-23935.
[109] Yue J, Gu X, Chen L, et al. General synthesis of hollow MnO2, Mn3O4and MnO nanospheres as superior anode materials for lithium ion batteries[J]. Journal of Materials Chemistry A, 2014, 2: 17421-17426.
[110] Jian G, Xu Y, Lai L C, et al. Mn3O4hollow spheres for lithium-ion batteries with high rate and capacity[J]. Journal of Materials Chemistry A, 2014, 2: 4627-4632.
[111] Sekhar B C, Kalaiselvi N. Pristine hollow microspheres of Mn2O3as a potential anode for lithium-ion batteries[J]. CrystEngComm, 2015, 17: 5038-5045.
[112] Qiao Y, Yu Y, Jin Y, et al. Synthesis and electrochemical properties of porous double-shelled Mn2O3hollow microspheres as a superior anode material for lithium ion batteries[J]. Electrochimica Acta, 2014, 132: 323-331.
[113] Lin H B, Rong H B, Huang W Z, et al. Triple-shelled Mn2O3hollow nanocubes: force-induced synthesis and excellent performance as the anode in lithium-ion batteries[J]. Journal of Materials Chemistry A, 2014, 2: 14189.
[114] Li B, Rong G, Xie Y, et al. Low-temperature synthesis of α-MnO2hollow urchins and their application in rechargeable Li+batteries[J]. Inorganic Chemistry, 2006, 45: 6404-6410.
[115] Zhou L, Wu H B, Zhu T, et al. Facile preparation of ZnMn2O4hollow microspheres as high-capacity anodes for lithium-ion batteries[J]. Journal of Materials Chemistry, 2012, 22: 827-829.
[116] Chen X F, Qie L, Zhang L L, et al. Self-templated synthesis of hollow porous submicron ZnMn2O4sphere as anode for lithium-ion batteries[J]. Journal of Alloys and Compounds, 2013, 559: 5-10.
[117] Kim M H, Hong Y J, Kang Y C. Electrochemical properties of yolk-shell and hollow CoMn2O4powders directly prepared by continuous spray pyrolysis as negative electrode materials for lithium ion batteries[J]. Rsc Advances, 2013, 3: 13110-13114.
[118] Zhou L, Zhao D, Lou X W. Double-shelled CoMn2O4hollow microcubes as high-capacity anodes for lithium-ion batteries[J]. Advanced Materials, 2012, 24: 745-748.
[119] Zhang J, Gu P, Xu J, et al. High performance of electrochemical lithium storage batteries: ZnO-based nanomaterials for lithium-ion and lithium-sulfur batteries[J]. Nanoscale, 2016, 8: 18578-18595.
[120] WU H, CHAN G, CHOI J W, et al. Stable cycling of double-walled silicon nanotube battery anodes through solid-electrolyte interphase control[J]. Nature nanotechnology, 2012, 7: 310-315.
[121] LI X, GU M, HU S, et al. Mesoporous silicon sponge as an anti-pulverization structure for high-performance lithium-ion battery anodes[J]. Nature Communications, 2014, 5: 4105.
[122] LIU N, HU L, MCDOWELL M T, et al. Prelithiated silicon nanowires as an anode for lithium ion batteries[J]. ACS nano, 2011, 5: 6487-6493.
Hollow micro/nanostructures metal oxide as advanced anodes for lithium-ion batteries
MA Yating, HUANG Jian, LIU Xiang, LIU Pengfei, CAI Yuxin, XIE Qingshui, PENG Dongliang
(Collaborative Innovation Center of Chemistry for Energy Materials, Department of Materials Science and Engineering, College of Materials, Xiamen University, Xiamen 361005, Fujian, China)
More efforts are needed to upgrade the performances of lithium-ion batteries (LIBs) for their further applications in various large electrical appliances such as electric vehicles and smart grid as these devices require high capacity, power density, high rate capability and especially safety. Electrode materials are the key to the performance of LIBs. Recently, metal oxides with much higher capacities and better safety have the prospect of becoming alternative anode materials of commercial graphite. However, the intrinsic low charge/ionic conductivity and poor cycling structural stability lead to poor cycling and rate performances, which greatly hinder their commercial applications. To overcome these disadvantages of metal oxide anodes for LIBs, several strategies have been developed during the past decade. Among them, metal oxide hollow micro-nanostructures exhibit excellent electrochemical properties as anode material for LIBs. In this review, we first describe the current commonly preparation methods to synthesize metal oxide hollow structures and comment on their advantages and shortages. According to some typical examples, we show the promising use of metal oxides hollow-structured anode materials for LIBs. Finally, the direction and prospect of metal oxide hollow micro-nanostructures using as anode materials are further discussed.
hollow micro-nanostructures; metal oxides; lithium-ion battery; anode materials
10.12028/j.issn.2095-4239.2017.0084
TM 911.1
A
2095-4239(2017)05-871-18
2017-06-01;
2017-07-10。
国家重点研究计划“纳米科技”重点专项(2016YFA0202602),国家自然科学基金(51371154,51571167和51701169),福建省自然科学基金项目(2017J05087),厦门大学校长基金(20720160082)。
麻亚挺(1991—),男,博士研究生,主要从事锂离子电池电极材料方面的研究,E-mail:mayating@stu.xmu.edu.cn;
谢清水,助理教授,主要研究方向为纳米储能材料,E-mail:xieqsh@xmu.edu.cn;彭栋梁,教授,主要研究方向为磁性材料、纳米和低维功能材料、能源材料,E-mail:dlpeng@xmu.edu.cn。
