钛酸纳米管/活性炭复合材料对水体中铅和亚甲基蓝的吸附
2017-09-07董川马骏刘宏芳梁文婷宋胜梅
董川,马骏,,刘宏芳,梁文婷,宋胜梅
(1.山西大学 环境科学研究所,山西 太原 030006;2.太原科技大学 环境与安全学院,山西 太原 030024)
钛酸纳米管/活性炭复合材料对水体中铅和亚甲基蓝的吸附
董川1,马骏1,2,刘宏芳2,梁文婷1,宋胜梅1
(1.山西大学 环境科学研究所,山西 太原 030006;2.太原科技大学 环境与安全学院,山西 太原 030024)
钛酸盐纳米管(TNTs)由于具有较大的比表面积和优异的离子交换性能,显示出对重金属和阳离子染料高效的吸附性。文章通过一步水热法合成了粉末活性炭负载的钛酸纳米管(TNTs/PAC)材料,并应用于对铅离子(Pb)和阳离子染料亚甲基蓝的吸附。TNTs/PAC对Pb(Ⅱ)和MB都体现了很快的动力学,60 min即可达到吸附平衡且符合准二级反应动力学(R2=1)。吸附等温线符合Langmuir模型 (R2>0.998),拟合的单层饱和最大吸附量Pb(Ⅱ)为318.5 mg/g,MB为234.5 mg/g。Pb(Ⅱ)在TNTs@PAC上的吸附受溶液pH影响较大,碱性条件由于材料表面带更多的负电荷而利于吸附。TNTs@PAC对两种污染物的主要吸附机理为金属和染料阳离子与TNTs层间Na+和H+的交换作用。另外,该材料经EDTA解吸或紫外光照再生后易于循环利用。高效的吸附性能与良好的可再生性使该材料在修复重金属及染料污染水体方面成为一种极具前途的纳米复合材料。
钛酸纳米管;活性炭;重金属;染料
0 引言
纳米TiO2由于其独特的性质,如纳米尺度下的光电转化效应,量子尺寸效应,比表面和体积效应等,广泛应用于环境、化学领域[1-3]。通过对二氧化钛进行碱性水热处理,即可合成钛酸盐纳米材料[4-5]。近年来,钛酸纳米材料由于其特殊的理化性质,如大比表面积、均一的纳米尺度的管型结构、良好的离子交换性能和光量子效应等,因而在环境修复方面受到关注。其中,钛酸盐纳米管(titanate nanotubes,TNTs)是最重要的钛酸纳米材料之一,已应用于阳离子(如重金属和阳离子染料)吸附剂和光催化剂[6-8]。An等发现TNTs对Cu2+和Ag+具有良好的吸附性能[9,11];Yang等研究证明,TNTs可以有效吸附Sr2+、Ra2+[10];;熊林等发现相同条件下,TNTs对Pb2+、Cd2+和Cr3+的吸附量达到520.83、238.61和51.58 mg/g[12]。
铅(Pb)在饮用水和环境体系中属于第一类水污染物,它的性质稳定,毒性强,长期蓄积将对人体健康及动植物生长产生严重影响[15-16]。吸附法由于操作简易、成本低、效率高,被广泛应用于水体中铅的去除[17]。另外,染料是一种较难处理的废水污染物,它的来源广泛,包括纺织、印刷、染料制造和食用食物等;同时具有水量大、水质复杂、色度高等特点[19-21]。在染料的处理方法中,活性炭虽然处理效果较好,但由于其成本较高、再生困难且易造成二次污染等问题限制了其应用,因此,对活性炭进行改性以开发高效廉价的复合吸附剂尤为重要[6-7]。
以活性炭为基底合成负载钛酸纳米管的复合材料(TNTs@PAC),在水体中可有效富集并光降解疏水性多环芳烃等有机污染物,增强了对污染物的吸附能力和光催化活性。[14,18]。实际中重金属往往与有机污染物共存,成为传统吸附剂(包括活性炭)吸附能力的一个瓶颈问题[22],本研究中采用一步水热法合成TNTs/PAC复合复合材料,并研究其对重金属Pb(Ⅱ)和阳离子染料MB的去除效果和行为,考察溶液pH对材料吸附两种污染的影响以及材料的再生回用性能。
1 材料与方法
1.1 材料和试剂
合成TNTs@PAC 时原料使用P25型纳米TiO2(包含80%锐钛矿和20%金红石,Evonik,德国), NaOH和粉末活性炭(100目,DARCO,美国)。以相应的重金属氯化物PbCl2、亚甲基蓝去配置1 000 mg/L 的储备液。Pb(Ⅱ)的储备液用浓盐酸调节溶液pH约3.5左右备用。HNO3选用优级纯, EDTA以及实验中所使用的试剂均为分析纯及以上。所有的溶液都以去离子水配制。
1.2 TNTs@PAC的合成及表征
TNTs@PAC的合成通过一步水热法合成。首先1.2 g的粉末活性炭和1.2 g的TiO2(P25)颗粒混合,并分散在66.7 mL的10 mol/L NaOH溶液里。磁力搅拌12 h充分混合后,混合物被转移到带有不锈钢外衬的聚四氟乙烯反应器中,在130℃下进行72 h的水热反应。反应后溶液离心,分离所得的灰黑色材料用去离子水洗涤到pH 9左右,105 ℃下烘干4 h备用。
用高分辨透射电镜tecnai30 FEG(TEM,FEI,美国)观察TNTs @ PAC的形貌。材料的晶型结构经X射线晶型衍射(XRD) 分析所得,表征在D/max-2400型X 射线衍射仪(Rigaku,日本) 上于100 kV和40 mA下进行。XRD以Cu Kα (λ=1.542 Å) 为射线源,扫速为4°/min。
1.3 吸附实验
Pb(Ⅱ)在TNTs/AC上的吸附动力实验于500 ml的玻璃锥形瓶中进行。实验使用吸附材料TNTs @ PAC 0.2 g/L,反应溶液Pb(Ⅱ)离子初始浓度为50 mg/L,稀盐酸和NaOH溶液调节溶液pH值为5。之后悬浊液置于摇床上,于常温(25℃)、200 r/min下震荡4 h。隔时取样,滤液经过0.22 μm的醋酸纤维素膜过滤,用去离子水稀释后进行溶液中剩余Pb(Ⅱ)离子的测定。亚甲基蓝动力平衡实验同铅的过程一致,初始浓度50 mg/L,pH值为6,吸附材料增至0.3 g/L。
铅的等温吸附实验在40 mL的带盖玻璃瓶中进行,初始Pb(Ⅱ)的浓度范围设定为10至200 mg/L,材料的剂量0.2 g/L,溶液pH值为5,4 h摇床震荡达到吸附平衡后计算吸附量。亚甲基蓝的等温吸附也同铅的过程一致,初始浓度范围为10至200 mg/L,pH值为6,材料投加量为0.3 g/L。
铅的pH值影响实验中,为防止高pH(>7)下Pb(Ⅱ)的沉淀,以稀盐酸和NaOH调节溶液pH值从2~7,初始溶液Pb(Ⅱ)浓度50 mg/L,吸附材料量0.2 g/L。亚甲基蓝的pH值影响实验中,选取溶液pH值从3~10,初始溶液亚甲基蓝浓度50 mg/L,吸附材料量0.3 g/L。吸附平衡后,取样测定结果。
溶液中Pb(Ⅱ)离子浓度测定采用电感耦合等离子体-原子发射光谱仪(ICP-OES,710-ES,Varian,美国)。溶液中亚甲基蓝浓度采用紫外分光光度计(SpectraMax M2.USA.)于664 nm波长下测定。
吸附平衡后,Pb(Ⅱ)和亚甲基蓝的吸附量(qe, mg/g)和去除率(R%)由下式计算[6]:

(1)
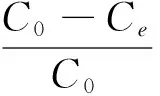
(2)
此处C0和Ce(mg/L)分别为溶液中Pb(Ⅱ)离子和亚甲基蓝的初始和平衡浓度,V(L)为反应溶液体积,m(g) 为吸附剂TNTs@PAC的投加质量。
1.4 TNTs@PAC的再生与循环再利用
在Pb(Ⅱ)的吸附中,对照先前TNTs的再生方法,本实验对吸附平衡后的材料采取两种再生循环利用途径。其一,依照TNTs路线,反应后将材料进行收集,离心后将其浸入200 mL 0.1mol/L HNO3中解吸Pb(Ⅱ),由于酸处理可能会导致材料的一些损伤,因此还需将其浸入200 mL 0.3 mol/L NaOH溶液中修复部分结构和吸附位点[14]。其二,利用一种非破坏性的螯合剂将污染物置换使材料达到再生循环目的,本实验采用200 mL 0.2 mol/L EDTA-Na2作为再生环境。解吸再生后的吸附材料要继续在相同的实验条件下重复利用3次,确定其可再生利用性。
2 结果与讨论
2.1 TNTs @ PAC的形貌及晶型
图1所示为合成的TNTs/PAC的TEM图。钛酸纳米管交织附着在活性炭颗粒表面。钛酸纳米管本身是一类内径约为5 nm和外径约为9 nm的中空两端开后的纳米管[6,14],其外直径小于PAC的微孔,因而部分纳米管可以嵌入活性炭的孔道内部。另外,经水热法剖离的活性炭的一些微粒也可能会附着在TNTs上而实现对TNTs的改性[14]。

Fig.1 TEM images of TNTs@PAC图1 TNTs @ PAC的TEM
图2为TNTs@ PAC的XRD图谱。其中在9.5°,24.2°,28.1°,48.1° 和 61.7°的衍射峰与钛酸钠(NaxH2-xTi3O7·nH2O,x为 0~0.75,取决于pH值和洗涤后剩余的钠量)的晶格衍射一致[6,14]。该钛酸钠为三钛酸组成,具体而言,三联[TiO6]八面体错位相接构成材料的基本骨架,Na+和H+填充于层间。金属和染料阳离子极容易与层间的Na+和H+发生离子交换而被吸附。另外,9.5°处的峰代表了TNTs的层间结构。此外,26°峰值来自于活性炭中的石墨晶格,证明了活性炭的存在,但由于表面被TNTs覆盖而使其峰值减弱。
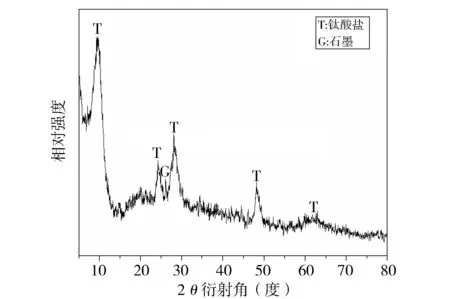
Fig.2 XRD patterns of TNTs@PAC图2 TNTs @ PAC的XRD图谱
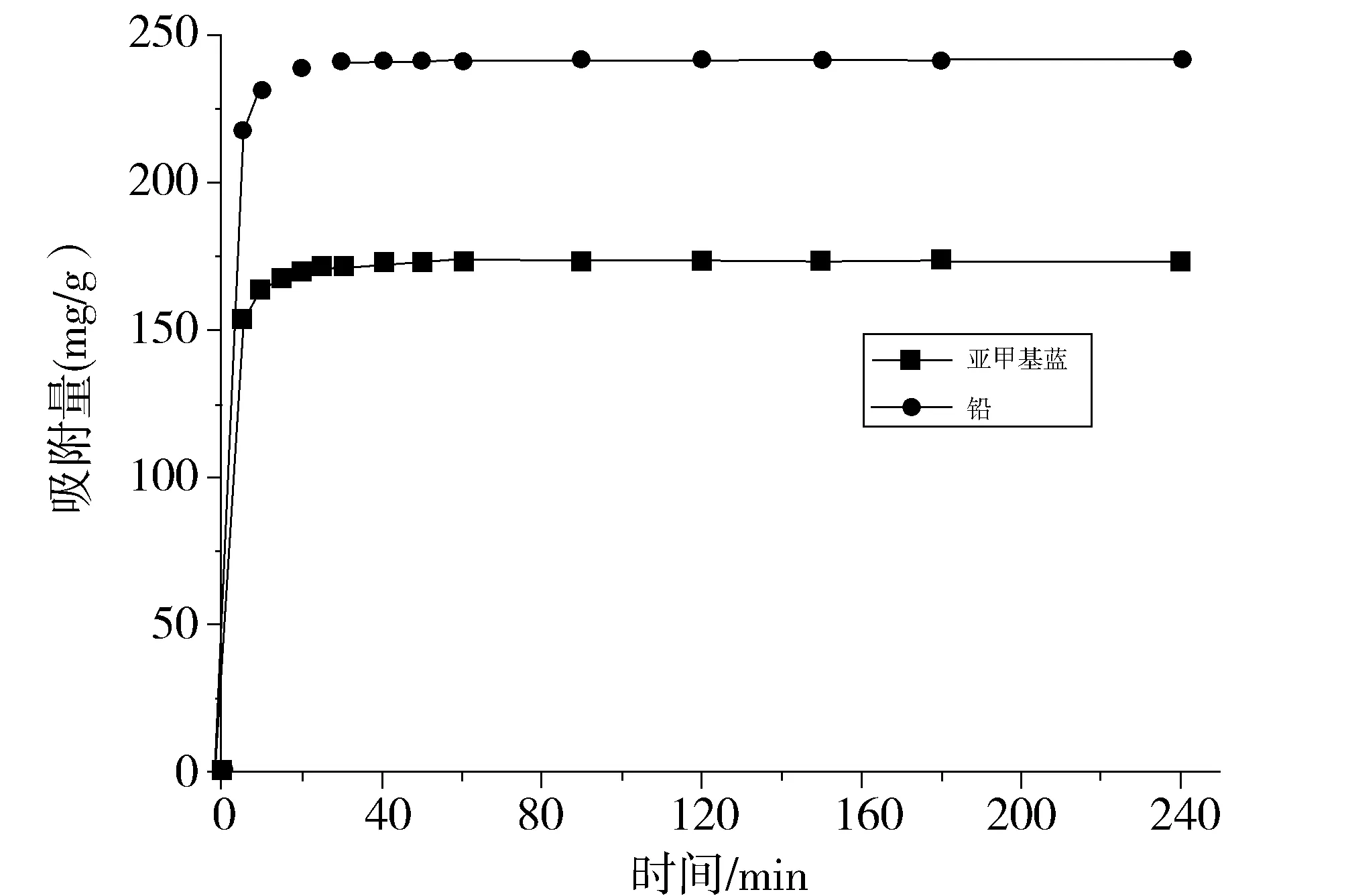
Fig.3 Kinetic adsorption curves of TNTs @PAC图3 TNTs @ PAC的动力学吸附曲线
2.2 TNTs @ PAC的动力学和等温吸附
图3所示为TNTs@ PAC吸附Pb(Ⅱ)和亚甲基蓝的动力学曲线。由图可知,TNTs @ PAC无论吸附Pb(Ⅱ)还是亚甲基蓝均为一个快速的过程,吸附主要发生在前15 min,60 min时即可达到吸附平衡。快速的动力学过程得益于TNTs/AC的大比表面积和离子交换的机理。污染物初始浓度为50 mg/L时,铅的平衡吸附量可达241.5 mg/g,去除率高达99.4%[6];甲基蓝的吸附量达173.3 mg/g,去除率高达99.9 %。
以准一级和准二级反应动力学模型分析吸附动力学结果,模型表达式分别如下[13-14]:
qt=qe-qeexp(-k1t)
(3)
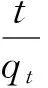
(4)
此处qt和qe(mg/L)分别是Pb(Ⅱ)和亚甲基蓝的吸附时间和平衡时污染物的吸附量;k1(min-1)和k2(g/(mg·min))分别是准一级和准二级动力学模型常数。

表1 TNTs@ PAC吸附Pb(Ⅱ)和亚甲基蓝的动力学参数
拟合所得污染物在TNTs @ PAC上吸附的动力学参数见表1。准二级动力学模型能够更好地描述TNTs @ PAC对两种污染物的吸附,拟合系数R2=1,另外,拟合所得的吸附量也非常接近实测值(<1%)。吸附符合准二级动力学模型,说明了TNTs @ PAC对污染物的吸附是化学过程,表现在溶液中的Pb(Ⅱ)和MB阳离子被补集到材料表面后与—ONa官能团发生作用,进而被离子交换。
在亚甲基蓝的吸附过程中,对比准一级动力学模型来说更符合准二级动力学模型,拟合系数R2=1,模拟吸附量和实际吸附量基本接近。准二级动力学中的吸附量也要比海泡石、天然沸石、硅藻土等多种材料的吸附性能更强[21-23](见表2)。

表2 不同材料对Pb(Ⅱ)和MB的吸附容量
利用经典Langmuir和Freundlich等温吸附模型对TNTs@PAC吸附Pb(Ⅱ)和亚甲基蓝的等温吸附实验结果进行拟合,模型方程为[14]:
Langmuir 模型:
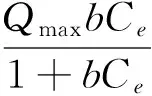
(5)
Freundlich 模型:
(6)
此处,qe(mg/g)为平衡时的吸附量,Ce(mg/L)为溶液浓度,Qmax(mg/g)为Langmuir吸附中的饱和吸附量,b(L/mg)是与吸附位点结合能相关的常数,KF是与吸附容量有关的常数,n是与吸附能有关的常数。
从表3中可知,Langmuir吸附模型能更好地描述TNTs/AC对两种污染物的吸附等温结果,相关系数R2分别为0.998 6和0.999 2。这说明TNTs/AC对两种污染物的吸附属于单层吸附,且吸附质之间没有相互作用。TNTs/AC对Pb(Ⅱ)和MB的吸附可分为两部分:(1)附着的TNTs的离子交换作用和(2)基底活性炭颗粒对污染物的补集。两种材料组分相辅相成,表现出高效的吸附性能。其中,Pb2+和MB阳离子(表示为“MB+”)在TNTs上的离子交换过程可表达如下:
Pb2++(NaO)2≡Ti3O7→ PbO2≡Ti3O7+2Na+
(7)
Pb2++(HO)2≡Ti3O7→ PbO2≡Ti3O7+2H+
(8)
2MB++(NaO)2≡Ti3O7→MB2O2≡Ti3O7+2Na+
(9)
2MB++(HO)2≡Ti3O7→MB2O2≡Ti3O7+2H+
(10)
其中,“(NaO)2≡Ti3O7”和(HO)2≡Ti3O7代表钛酸纳米管。
拟合的Langmuir单层饱和最大吸附容量对Pb(Ⅱ)可达318.5mg/g,对MB可达234.5mg/L。表明TNTs@PAC对Pb(Ⅱ)和MB都具有良好吸附的性能。实验结果也表明了TNTs@PAC比其他传统吸附材料具有更高的吸附性能力,如改性的二氧化硅(Pb(Ⅱ) 38mg/g)、膨润土(Pb(Ⅱ) 53mg/g)、离子交换树脂(Pb(Ⅱ) 84mg/g)等,因此该材料展现了其在去除污水中重金属和染料阳离子的应用潜力[6-7,14]。(见表2)

表3 TNTs @ PAC吸附铅和亚甲基蓝的等温吸附模型参数
2.3pH值的影响
图4显示了pH对TNTs/PAC吸附Pb(Ⅱ)和MB的影响,图5中描绘了材料zeta电位随pH的变化。由于材料具有很低的等电点(pHPZC=3.1),因此在广泛的pH范围内(pH≥4)材料表面都带负电,这有利于对阳离子的吸附。在低pH值(2~3)时,平衡时Pb(Ⅱ)的吸附量仅有105.4和173.0mg/g,这是因为低pH下,材料表面带正电,不利于从溶液中补集Pb2+,且溶液中大量存在的H+与Pb2+之间还存在竞争作用。在pH为4时,TNTs@PAC表面电荷转为负电荷,对Pb(Ⅱ)的吸附量也迅速提高(达230.2mg/g,R=94.0%)[6],pH值≥5时,材料对Pb(Ⅱ)的去除就几近完全(>99%)。pH更高(pH>7)会导致Pb(Ⅱ)的沉淀,因此吸附Pb(Ⅱ)选取的pH范围为2~7。对于MB来说,由于材料的投加量较大(0.3 g/L),导致材料对MB的去除率整体较大。但酸性条件依然不利于MB的吸附,如pH 3时,吸附量为168.1 mg/g;而当pH≥4时,材料对MB的吸附量可达175.5 mg/g,去除率高达99%。

Fig.4 Effect of pH on adsorption of Pb(Ⅱ) and MB by TNTs@PAC图4 pH值对TNTs@PAC吸附Pb(Ⅱ)和MB的影响
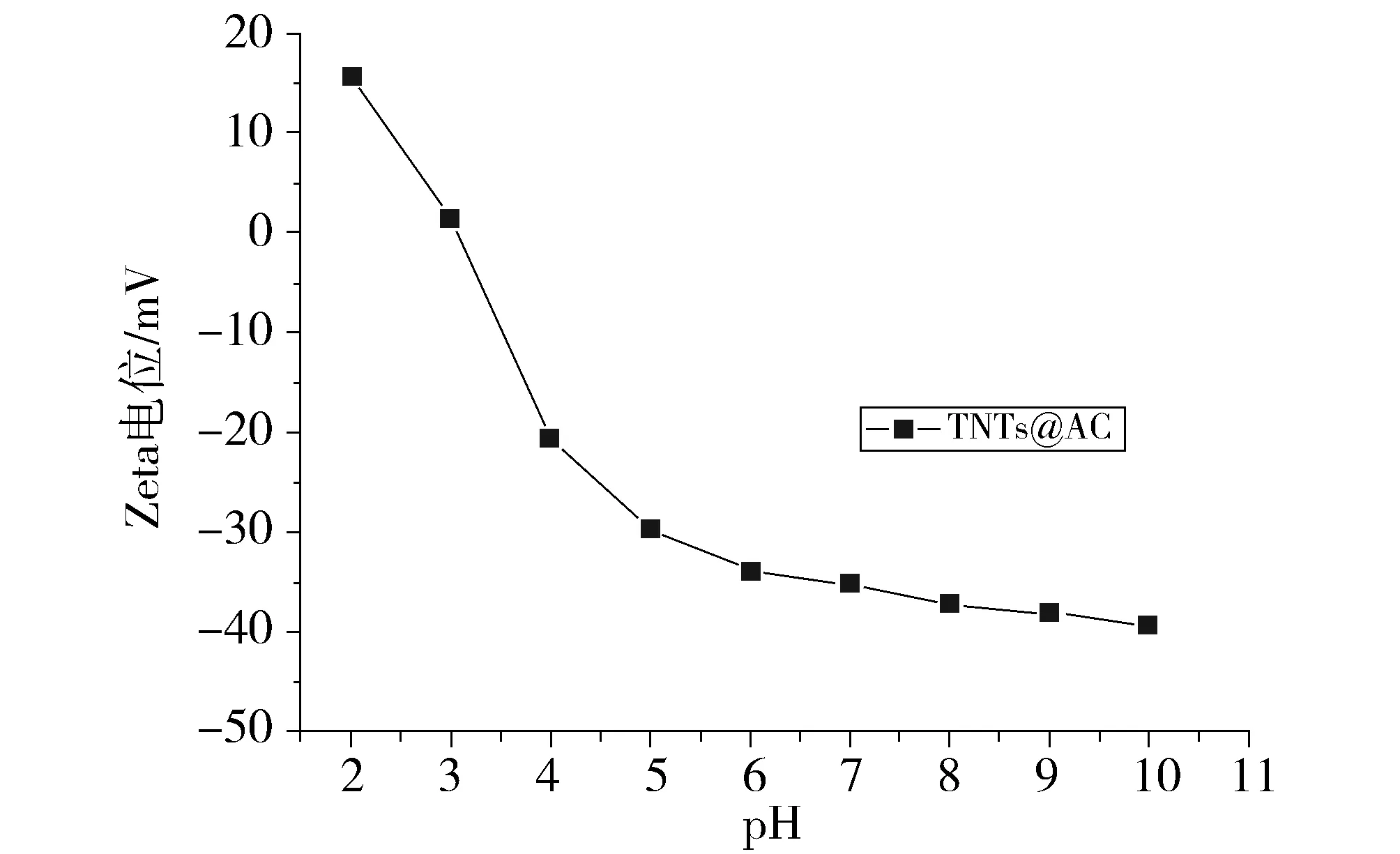
Fig.5 Zata potentials at different pH图5 zeta电位随pH的变化
2.4 材料的再生与循环利用
以铅为例,研究解吸再生后材料的回用性能。采取两种途径对材料TNTs@PAC进行再生循环利用:(1)HNO3解吸和NaOH碱法;(2)EDTA解吸再生法。本研究采用此方法进行3次完整的循环利用(1次循环包含1次完整的吸附+1次酸解吸+1次NaOH再生)。酸解吸是在以高浓度的H+替换被吸附的Pb2+, 而碱再生是在恢复被耗尽的—ONa位点。从表3中可以看出,3次循环中经HNO3解吸材料都具有很高的解吸率(82.1%~87.2%)。然而,经再生后Pb(Ⅱ)的去除率却从99.4%下降到了47.3%。这是由于酸解吸吸附过程中会产生一些不利的影响,如酸处理可能会使Ti(Ⅳ)离子溶解而导致钛酸管结构的破坏,另外在与无机离子(Pb2+)交换的过程中H+的有效性要远远低于Na+,若再生过程中补Na不足会大大降低材料的吸附性能。因此采取第二种途径是一种既有效又不破坏钛酸纳米管结构的方法,螯合剂(EDTA-Na2)表现出对Pb(Ⅱ)很高的解吸率,第三次循环后的解吸率依然高达93.0%。另外,由于其既可以有效地解吸Pb2+同时还可以补充充足的Na+且不破坏材料管结构,3次的循环后对Pb(Ⅱ)的吸附去除率依然高达91.3%(见表4)。

表4 TNTs@PAC的再生与循环利用
在对亚甲基蓝吸附的再生中,由于材料具有一定的光降解作用,因此本实验采取紫外灯直接照射的方法,将反应平衡后材料离心,放在紫外灯下照射1 h,再进行二次循环使用。从表3中可以看出,经过3次的循环使用,材料依旧具有良好的吸附量。
3 结论
以纳米TiO2和颗粒活性炭为原料,经一步水热法合成新型复合材料TNTs/PAC。该材料对重金属阳离子Pb(Ⅱ)和有机染料亚甲基蓝都表现出很高的吸附效率,在实际水体中金属-有机复合污染治理中有很好的应用前景。其中复合材料TNTs@PAC是由钛酸盐纳米管和颗粒活性炭组成的,钛酸纳米管附着于活性炭表面以及填充于孔道内部,而活性炭是复合材料的骨架;TNTs@PAC能够快速的吸附水体中的Pb(Ⅱ)和MB,60 min内即可达到吸附平衡。对两种污染物的吸附均符合准二级动力学模型(R2=1),表明Pb(Ⅱ)和MB吸附由化学吸附控制;TNTs@PAC对Pb(Ⅱ)和MB的等温吸附符合Langmuir模型,拟合所得最大吸附容量对Pb(Ⅱ)可达318.5 mg/g,对MB可达234.5 mg/g,远高于传统吸附剂的吸附量;钛酸纳米管中层间填充的Na+和H+是吸附的主要位点。Pb2+及MB阳离子与材料层间离子的交换作用是其主要吸附机理;经ETDA-Na2解吸再生处理后,材料具有高效的循环利用性能,经过3次的循环使用后对Pb(Ⅱ)的去除率依然高达91%。
[1] Chen X B,Mao S S.Titanium Dioxide Nanomaterials:Synthesis,Properties, Modifications,and Applications[J].ChemicalReviews,2007,107(7):2891-2959.DOI:10.1021/cr0500535.
[2] Bavykin D V,Walsh F C.Titanate and Titania Nanotubes:Synthesis, Properties and Applications[M].Cambridge,UK,Royal Society of Chemistry,2010.
[3] 雷立等.碱热-酸热法合成二氧化钛-钛酸纳米管复合纳米材料对Cd(Ⅱ)和苯酚的同步去除[J].环境科学,2015,36(7):2573-2580.DOI:10.13227/j.hjkx.2015.07.033.
[4] Chen Q,Zhou W,Du G,etal.Trititanate Nanotubes Made Via a Single Alkali Treatment[J].AdvMater,2002,14:1208-1211.DOI:10.1002/chin.200247219.
[5] Thorne A,Kruth A,Tunstall D,etal.Formation,Structure,and Stability of Titanate Nanotubes and Their Proton Conductivity[J].JPhysChemB,2005,109:5439-5444.DOI:10.1021/jp047113f.
[6] Ma J,Li F,Qian T W,etal.Natural Organic Matter Resistant Powder Activated Charcoal Supported Titanate Nanotubes for Adsorption of Pb(Ⅱ)[J].ChemicalEngineeringJournal,2017,315:191-200.DOI:10.1016/j.cej.2017.01.029.
[7] Liu W,Wang T,Borthwick A G,etal.Adsorption of Pb2+, Cd2+,Cu2+and Cr3+Onto Titanate Nanotubes:Competition and Effect of Inorganic Ions[J].SciTotalEnviron,2013,456:171-180.DOI:10.1016/j.scitotenv.2013.03.082.
[8] Camposeco R,Castillo S,Mejia-Centeno I,etal.Behavior of Lewis and Brönsted Surface Acidity Featured by Ag,Au,Ce,La,Fe,Mn,Pd,Pt,V and W Decorated on Protonated Titanate Nanotubes[J].MicroporousandMesoporousMaterials,2016,236:235-243.DOI:10.1016/j.micromeso.2016.08.033.
[9] An H Q,Zhu B L,Wu H Y,etal.Synthesis and Characterization of Titanate and CS2-modified Titanate Nanotubes as Well as Their Adsorption Capacities for Heavy Metal Ions [J].ChemicalJournalofChineseUniversities-Chinese,2008,29(3):439-444.
[10] Yang D J,Zheng Z F,Liu H W,etal.Layered Titanate Nanofibers as Efficient Adsorbents for Removal of Toxic Radioactive and Heavy Metal Ions from Water[J].JournalofPhysicalChemistryC,2008,112(42):16275-16280.DOI:10.1021/jp803826g.
[11] Liu S S,Lee C K,Chen H C,etal.Application of Titanate Nanotubes for Cu(Ⅱ) Ions Adsorptive Removal from Aqueous Solution[J].ChemicalEngineeringJournal,2009,147(2-3):188-193.DOI:10.1016/j.cej.2008.06.034.
[12] 熊林.钛酸纳米管吸附Pb2+、Cd2+、Cr3+和光催化降解双酚A的机理研究[D].北京:北京大学,2011.
[13] Xiong L,Yang Y,Mai J,etal.Adsorption Behavior of Methylene Blue Onto Titanate Nanotubes[J].ChemicalEngineeringJournal,2010,156:313-320.DOI:10.1016/j.cej.2009.10.023.
[14] Liu W,Cai Z,Zhao X,etal.High-capacity and Photo-regenerable Composite Material for Efficient Adsorption and Degradation of Phenanthrene in Water[J].EnvironSciTechnol,2016,50:11174-11183.DOI:10.1021/acs.est.6b02623.
[15] Flora G,Gupta D,Tiwari A.Toxicity of Lead:A Review with Recent Updates[J].InterdiscipToxicol,2012,5:47-58.DOI:10.2478/v10102-012-0009-2.
[16] Hsu P S,Guo Y L.Antioxidant Nutrients and Lead Toxicity[J].Toxicology,2002,180:33-44.DOI:10.1016/S0300-483X(02)00380-3.
[17] Xiong L,Chen C,Chen Q,etal.Adsorption of Pb(Ⅱ) and Cd(Ⅱ) from Aqueous Solutions using Titanate Nanotubes Prepared Via Hydrothermal Method[J].JHazardMater,2011,189:741-748.DOI:10.1016/j.jhazmat.2011.03.006.
[18] Liu W,Sun W,Han Y,etal.Adsorption of Cu (Ⅱ) and Cd (Ⅱ) on Titanate Nanomaterials Synthesized Via Hydrothermal Method Under Different NaOH Concentrations:Role of Sodium Content[J].ColloidSurfaceA,2014,452:138-147.DOI:10.1016/j.colsurfa.2014.03.093.
[19] Ho Y S,Chiang C C.Sorption Studies of Acid Dye by Mixed Sorbents[J].AdsorptJIntAdsorptSoc,2001,7:139-147.DOI:10.1023/A:1011652224816.
[20] Dogan M,Ozdemir Y,Alkan M.Adsorption Kinetics and Mechanism of Cationicmethyl Violet and Methylene Blue Dyes Onto Sepiolite[J].DyesandPigments,2007,75:701-713.DOI:10.1016/j.dyepig.2006.07.023.
[21] Al-Ghouti M A,Khraisheh M A M,Ahmad M N M,etal.Adsorption Behaviour of Methylene Blue Onto Jordanian Diatomite:A Kinetic Study[J].JournalofHazardousMaterials,2009,165:589-598.DOI: 10.1016/j.jhazmat.2008.10.018.
[22] Mouni L,Merabet D,Bouzaza A,etal.Adsorption of Pb(Ⅱ) from Aqueous Solutions using Activated Carbon Developed from Apricot Stone[J].Desalination,2011,276:148-153.DOI:10.1016/j.desal.2011.03.038.
[23] Han R P,Zhang J J,Han P,etal.Study of Equilibrium,Kinetic and Thermodynamic Parameters about Methylene Blue Adsorption Onto Natural Zeolite[J].ChemEngJ,2009,145:496-504.DOI:10.1016/j.cej.2008.05.003.
Titanate Nanotubes/Activated Carbon Composite Material for the Adsorption of Lead and Methylene Blue in Water
DONG Chuan1,MA Jun1,2,LIU Hongfang2,LIANG Wenting1,SONG Shengmei1
(1.Environmental science research institute of Shanxi University,Taiyuan 030006,China;2.Environmental and safety institute of Taiyuan University of Science and Technology,Taiyuan 030024,China)
Titanate nanotubes (TNTs) have been shown effective for adsorption of heavy metals and cationic dyes due to large specific surface area and outstanding ion-exchange property.Powder activated charcoal supported TNTs (TNTs@PAC) are synthesized through a one-step hydrothermal method, and applied to the adsorption of heavy metal cationic lead (Pb) and cationic dye methylene blue. TNTs@PAC shows rapid adsorption kinetics for Pb(Ⅱ) and MB. In the 60 minutes, the adsorption equilibrium can be achieved, which conforms to quasi-second order reaction kinetics (R2=1). The adsorption isotherm is in accordance with the Langmuir model (R2>0.998). The maximum Langmuir capacity of Pb(Ⅱ) TNTs@PAC is determined to be 318.5 mg/g, and the MB is 234.5 mg/g. The adsorption of Pb(Ⅱ) on TNTs @ PAC is greatly influenced by the solution pH, and because of more negative charge on the surface of the material, the alkaline condition is favorable for adsorption. The primary adsorption mechanism of TNTs@PAC is the exchange between ion of heavy metals and dyes and interlayered Na+and H+in TNTs. In addition, TNTs@PAC is easily recycled after desorption by EDTA or UV-irradiation. The high adsorption capacity combined with good regeneration make TNTs@PAC a promising nanomaterial for remediation of heavy metals and dye-contaminated water.
titanate nanotubes;activated charcoal;heavy metals;dyes
10.13451/j.cnki.shanxi.univ(nat.sci.).2017.03.023
2017-06-08;
2017-06-27
国家自然科学基金(21575084);校博士科研启动基金(20152029)
董川(1963-),男,山西太原人,博士,教授,主要从事环境分析化学方面研究。E-mail:dc@sxu.edu.cn
O658.1
A
0253-2395(2017)03-0569-08
