药品医保支付价格形成机制的国际经验及启示Δ
2017-09-07刘远立中国医学科学院北京协和医学院公共卫生学院北京100730
陈 吟,孙 静,刘远立(中国医学科学院北京协和医学院公共卫生学院,北京 100730)
药品医保支付价格形成机制的国际经验及启示Δ
陈 吟*,孙 静#,刘远立(中国医学科学院北京协和医学院公共卫生学院,北京 100730)
目的:为我国制定合理的药品医保支付价格提供借鉴。方法:通过检索分析国内外正式发表的学术文章、官方网站和政府文件、新闻报道等资料和知情人访谈,总结国际主要药品医保支付价格形成机制,高值药可持续的公平可及的解决方式,为我国制定合理的药品价格政策提出建议。结果与结论:国际通用的医药支付价格的确定依据为内部参考定价法、增量成本-效果评价法、外部参考定价法。国际社会还采取以公平药价计划、药品专利池、开源药物研发组织等形式促进高值药可持续地公平可及。我国实现全民医保目标后,应积极探索制定合理的医保支付价格。可以在仿制药质量和临床疗效一致性评价后,采用内部参考定价法确定有仿制药竞争品种的支付标准,采用外部参考定价法或增量成本-效果评价法确定创新专利药品价格谈判的参考价格,对高值药物采用公平定价的理念。
药品价格;价格形成机制;国际经验
1 内部参考定价法确定竞争性药品医保支付价格
1.1 内部参考定价的起源及流程
内部参考定价法起源于德国。1989年,德国出台了《药物参考价格体系法案》,实行参考定价制度,以消除治疗效果相似的不同药品之间的价格差异,提高药品市场的透明度,控制药品费用[1]。欧洲国家相继仿效德国的做法,将内部参考定价法用于制定药品医保报销价格定价流程[2]。内部参考定价流程如下:
1)分组:定义每组可替代药品的数量和范围,确定实施内部参考定价的市场范围,包括通用名参考定价与治疗参考定价。通用名参考定价是将包括相同活性成分的药品归为1个参考组;治疗参考定价是将具有相同药理作用或相同适应证的药品归为1个治疗组。
2)确定参考价格:依据药品市场价格分布情况制定,采用组内药品价格的最小值、中位数、平均数、百分位数或其他函数关系制定参考价格[3](见表1)。
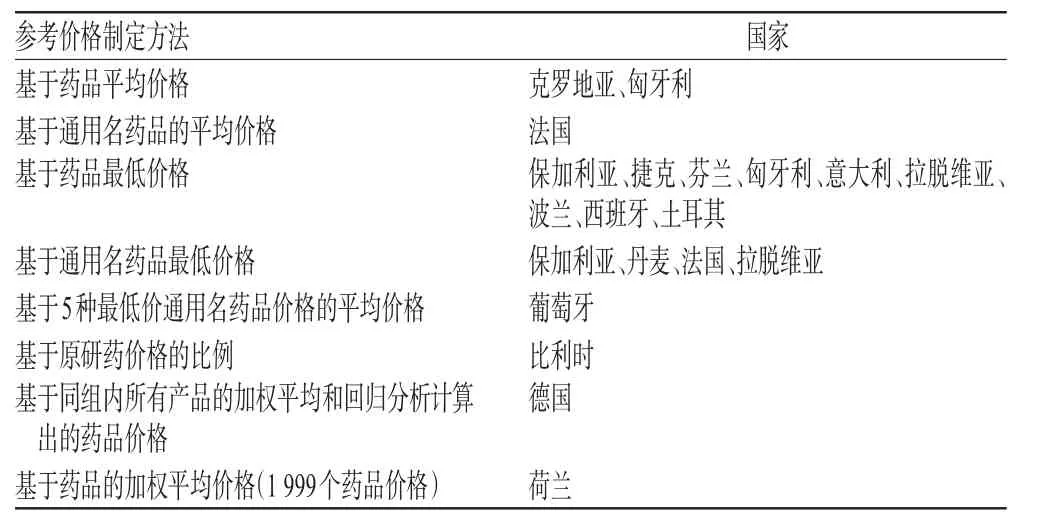
表1 欧洲主要国家采用内部参考定价法确定药品价格的具体方法Tab 1 Specific methods of setting medicines price with internal reference pricing method in key European countries
3)建立定义药品类别和设定医保补偿水平的决策程序,形成决策机制,并明确决策流程。
4)设置例外机制:在设计参考价格制度设计时允许一些合理的例外,如临床医师根据药物不良反应选择是否让患者转用内部参考定价体系内的其他药品。
1.2 德国内部参考定价法案例
以德国为例,内部参考定价法具体实施过程如下:
德国联邦联合委员会(Gemeinsamer Bundesausschuss,G-BA)依据活性成分将药品分组并划分不同的参考价格,仅列出活性成分,不列出商品名或通用名。依据参考价格流程和标准将药品划分为3个级别:级别1为具有相同活性成分的药品;级别2为药理学或治疗学具有相似活性成分的药品,尤其是化学结构类似的药品;级别3为治疗效果相似的药品。G-BA根据日均用量、个人剂量或处方平均剂量计算参考价格。中央法定健康保险基金协会(Central Association of Statutory Health Insurance Funds,FDSHI)依据处方平均剂量设置参考价格,制定各分组的最高补偿额,分别为标准包装和非标准包装制定参考价格。如果市场上各种包装类型所占比例大致相同,则由市场上的最大处方量来确定标准包装[4]。
德国《社会保险法典》(第五版)规定,医保选取价格区间的下1/3价格作为参考价格支付,同组药品中应至少涵盖20%的处方量。市场份额<1%的药品不纳入计算范围[5]。非标准包装的药品根据回归方程结果与标准包装药品参考价格相乘获得参考价格。药品参考价格由德国医学文献和信息研究所将参考价格信息在网上公布。FDSHI计算出来的药品价格是药品最大补偿金额,药品生产商依此制定药品零售价格,如果零售价格低于最大补偿金额,则由医保按计算的补偿金额支付;如果高于最大补偿金额,超出部分需患者支付,详见表2[6]。
2 以增量成本-效果评价为基础确定新药的医保支付价格
针对没有设置参考价格的新药,德国于2010年出台了《药品市场整治法案》,规定当一种新药进入市场时,需比较疗效是否优于原有治疗方案,并形成系统的报告。联邦联合委员会(Federal Jonit Commitment,FJC)授权给卫生保健质量与效益研究机构(Institute for Quality and Efficiency in Health Care,IQWiG)进行评估,并根据评估结果在3个月内对该药是否能够产生额外效果作出评定:如果该药没有增量成本-效果,则直接进入内部参考定价体系;如果该药并不能根据已有的参考组价格分级,则该药的价格不能超出标准治疗方案的费用。企业可在1年内提出重新评估要求:如果该药确有增量成本-效果,联邦基金委员会与企业、私人保险公司协会进行谈判,确定折扣范围,谈判的结果适用于法定医保和私人保险。在新药上市的1年内,企业可以自由定价,不受价格谈判限制;若第1年谈判无法达成一致,则由仲裁机构代表医保和企业参考国际价格制定该药价格,制定的价格适用于法定医保与私人保险。仍达不成一致的,向FJC提出依据增量成本-效果评估设定价格[7]。

表2 德国法定医保患者共付情况Tab 2 Patient co-payment of the social health insurance in Germany
3 外部参考定价法确定新药的医保支付价格
外部参考定价法也称国际参考定价法,是指采用药品在一个或多个国家的价格来形成一个基准或参考,目的在于帮助国家制定价格或进行价格管理[8]。外部参考定价法被欧洲国家广泛应用,主要用于专利药品定价及价格谈判,其参考价格来自其他国家的药品价格,包括出厂价、批发价或零售价[9]。使用外部参考定价法有助于价格谈判、制定及核实等3个方面的管理[10]。外部参考定价法流程[11]包括:(1)确定参考定价范围,即基于地理环境、经济水平、历史关联性、价格信息可用性、公共卫生状况、医保水平等因素选取参考国家,一般选取5个国家[12];(2)通过企业申报、官方数据查询或政府间价格信息分享等价格获取方式获取价格信息;(3)按参考国家药品的平均价格、最低价格、中间价格等制定相应的参考价格计算标准,通过对包装标准、规格、单位价格折算等方式对价格数据进行标准化;(4)定时更新和调整。
由于每个国家的疾病负担、药品倾向性、市场结构、税率、社会保障水平等不同,药品价格在不同国家可比性不同。因此,在选取参比国家时,综合评估经济水平、政策、市场结构,同时需考虑价格信息的可获得性。确定参比国家后,需要制定每个国家的参比权重,如选入的参比国家既有经济水平比本国好的,也有经济水平较落后的,可考虑增加经济水平次之的国家的权重。不同国家的外部参考价格体系不同:如,加拿大采用参比国家同一新药的中位数价格作为外部参考价格水平;荷兰选用药品最小剂量作为价格单位,选择同种药品在参比国家的平均价格作为外部参考价格水平;日本将同种药品出现两个以上价格且最高价格和最低价格相差5倍时,去除最高价格,剩下药品价格作为平均价格,如果同种药品出现3个以上价格且最高价格为其除外的平均价格2倍以上,则规定最高价格为最高价格除外的平均价格的2倍,然后计算平均价格作为外部参考价格水平。
4 药品价格形成新机制促进高值药可持续的公平可及
近年来,快速发展的生物技术产出的靶向治疗药品为很多绝症患者带来新的生机,但靶向治疗药品高昂的价格使一般个人和家庭难以承受。这类药品多数处于全球市场垄断地位,价格奇高。仅1个治疗丙肝的新药——索非布韦(Sofosbuvir)就已经为很多将这类高值药纳入公共保障体系的国家公共财政带来难以承受之重。1项在全球30个国家的研究发现,按照索非布韦目前的价格——经济与合作发展组织(Organization for Economic Cooperation and Development,OECD)国家每疗程花费40 591~1 311 250美元计算,治疗丙肝药品的费用占国家药品总费用的比例最低为10.5%(荷兰),最高达190.5%(波兰)[13]。
促进高值药的可及性与卫生资源分配的公平性存在伦理矛盾,在有限的卫生资源投入的前提下,资源分配应惠及更多普通疾病患者还是挽救重大疾病患者,是各个国家均面临的问题,在卫生资源相对匮乏的发展中国家尤为突出[14]。以现行的新药定价方法定价,经药物经济学评价增量成本-效果好的高值药,其价格有可能是很多包括OECD国家在内的卫生体系都根本无法承受的。
4.1 公平药价计划(Fair pricing of medicines)
为了从根本上解决高值药的可负担性,WHO于2016年提出了公平药价计划,试图打破现有的药品定价模式,建立更为透明的医药产业研发和市场运作模式。有学者研究发现,索非布韦并不是专利权人Gilead的原创,而是在该药完成Ⅱ期临床后收购而来。Gilead从该药获得了3倍于收购投资的回报,公众为此支付了高额费用,但大多数利润并未用于进一步新药研发,而是被投资人通过股权回购分走了巨额利润。WHO从价格制定者——药品生产商获得药品定价的证据,寻找药品生产商制定的药品价格受到质疑的原因,梳理政府、支付方和卫生体系管理药品价格的策略和方法并对其有效性进行评估,并通过促进各国政府、患者组织和药品生产商就药品价格和支付方式进行谈判,共同探讨合理的药品价格定价协议。建立公平的药品价格形成机制,需要打破现有的药品定价模式,通过规范医药商业投资股份回购,建立新型鼓励新药研发的方法等来解决高值药的可及性问题[15]。
4.2 药品专利池(Medicines Patent Pool,MPP)
MPP是国际药品采购组织于2010年建立的,通过与药品专利权人达成协议,获得专利期内药品的专利许可,授予仿制药生产企业专利许可。仿制药生产企业需支付5%税费给专利持有企业,并承诺给予更低的价格,从而达到降低专利期内药品价格的目的。仿制药企业还可以将得到授权的药品销售至原研药企业已获得专利政策的95个国家以外的国家。2010-2015年期间,MPP分别与7个专利权人签订了12个抗逆转录病毒(Antiretrovirals,ARVs)首选药品的自愿许可证和14个药品生产商的59个副许可证。MPP的合作伙伴给117个国家/地区的超过600万患者供应WHO推荐的ARVs药品。迄今为止,该组织的许可证通过降低ARVs药品价格为国际社会节约了7.9亿美元,相当于625 000名患者1年的治疗费用[16]。
4.3 开源药物研发组织(Open Source Medicines Discovery Initiative,OSDD)
OSDD是由印度科学与工业研究委员会联合印度财团和全球合作伙伴于2008年创建的,通过提供全球平台,共同协作研发针对肺结核、丝虫病、疟疾、利什曼病等发展中国家需要的新的治疗方案。OSDD招募了包括学生、科学家、临床医师、学者等组建团体,通过在线平台和线下实验室联系与企业合作。至今为止,该平台已有来自130个国家、13个招募的科学与工业研究理事会(CSIR)实验室的超过7 600名参与者、39个科研机构和14个工业机构成员。
OSDD是一个开放创新的交流平台,所有项目的目的和研究结果都公布在平台上,让独立的研究者们能够通过网络自由地分享他们的工作、讨论和进行合作。OSDD强调通过协作、开放共享实现一体化科学,探寻新药研发及获得的不同途径。因为这种开放资源模式是基于社区参与,因此可通过建立一个储存库持续发展并持续追求新药研发。为保证可获得性,从OSDD平台研发的药品不受专利限制,依赖已建立的仿制药企业的商业模式运作。
OSDD与MPP不同之处在于,MPP是利用已有的药品专利形成资源共享来降低药品价格,让新药惠及更多人,减少患者的疾病负担。尽管MPP已覆盖多个国家,但主要集中于欧美发达国家,较少惠及中低收入国家。OSDD旨在通过鼓励新药研发机制,提高不发达国家的新药研发能力,打破大企业垄断,提高贫困国家药品的可及性和可负担性[17]。
5 国际经验对我国的启示
目前,我国仿制药定价面临着两难的境地,一方面,药品医保支付价格政策改革需要医保尽快制定一个以治疗药物通用名为基础的支付价格;另一方面,由于仿制药质量尚未能全面保证与原研产品质量和疗效一致,难以实现以通用名确定医保支付价。2016年,我国开始开展仿制药质量和疗效一致性评价。一致性评价后可参照德国的内部参考定价法对药品进行分组,确定参考价格,为制定医保支付标准提供参考。德国针对新药采取增量成本-效果评价确定医保支付价,和将不具有良好增量成本-效果的新药与通用名药一视同仁,采取内部参考定价体系的不同价格形成机制和监管体制非常值得我国借鉴。
在我国药物经济学评价体系尚未建立起来的情况下,外部参考定价法相比增量成本-效果评价法确定新药品的价格,短期内实施更具有可行性[18],可作为药品谈判的参考。但外部参考定价法虽然能够起到控制药价的作用,却并不能根据本国市场制定更加灵活的药品价格、缩小药品的定价范围,长期应建立更加科学可持续的定价机制促进药品的可及性及可负担性。采用外部参考定价法或增量成本-效果评价法确定创新专利药品价格谈判的参考价格,对高值药物采用公平定价的理念健全药物经济学评价是发达国家已经广泛实践的成功经验。
随着保障水平的不断提高,我国也会像多数发达国家一样,逐步把高值药纳入保障体系。促进高值药可持续的公平可及,必须将药物经济学评价手段中增量成本-效果评价和国家卫生体系的预算影响分析相结合,根据我国的社会、经济、人文和政治发展环境,综合考虑需要优先解决的健康问题,确定将高值药纳入公共保障体系的顺序和保障程度,并借鉴国际经验,建立药品价格形成新机制。
作为全球最大的发展中国家,我国医疗费用投入逐年增加,医疗费用的快速增长也会很快成为我国政府“烦恼”的问题。2015年中国的卫生总费用超过4万亿,其中60%~70%为医保基金支付,而未来人口老龄化、高值药不断纳入保障体系,保障体系增强等会进一步增加医保基金的压力[19]。单纯靠控制药品价格并不能从根源上控制药品费用的增长,还需提高本国药品创新和研发能力,真正掌握药品定价权利,印度的OSDD机制给予了很好的启示。我国可以通过创建联合本国研究机构、企业和第三方组织等多方合作机构,联合研发药品,解决单个企业药品研发能力不足的困境,同时在不损害企业利益的情况下,制定出更加可负担的药品价格。而在未能形成该机制前,本国仿制药生产企业可以积极争取加入MPP,获取原研药的专利生产许可,以降低本国原研药销售价格。
[1] 常峰,崔鹏磊,夏强,等.德国药品参考价格体系对构建我国医保支付标准的启示[J].中国卫生政策研究,2015,8(7):55-60.
[2] World Health Organization.Drugs and money-prices,affordability and cost containment[EB/OL].[2016-12-17]. http://apps.who.int/medicinedocs/en/d/Js4912e/3.3.html.
[3] Dylst P,Vulto A,Simoens S.Reference pricing systems in Europe:characteristics and consequences[J].GaBi,2012,1(3/4):127-131.
[4] 姚东宁,邵蓉.德国药品参考定价制度对我国的启示[J].价格理论与实践,2014(9):58-60。
[5] Herr A,Suppliet M.Pharmaceutical prices under regulation:Tiered co-payments and reference pricing in Germany[R].http://EconPapers.repec.org/RePEc:zbw:dicedp:48.
[6] Herr A,Suppliet M.Co-payment exemptions and reference prices:an empirical study of pharmaceutical prices in Germany[R].University of York,2011.
[7] Ognyanova D.Pharmaceutical reform 2010 in Germany [J].Eurohealth,2012,17(1):11-13.
[8] 常峰,孙洁.欧洲药品国际参考定价体系的分析与借鉴[J].中国卫生经济,2014,33(9):94-96.
[9] 常峰,罗修英,路云.药品支付价格制定方法的国际经验及其启示[J].价格理论与实践,2015(9):49-51.
[10] World Health Organization.WHO guideline on country pharmaceutical pricing policies[EB/OL].[2016-12-17]. http://www.who.int/medicines/publications/pharm_guide_ country_price_policy/en/.
[11] Leopold C,Voglera S.Differences in external price referencing in Europe—A descriptive overview[J].Health Policy,2012,104(1):50-60.
[12]Nguyen T,Knight R,Roughead EE,et al.中低收入国家药品定价和采购的政策选择[J].中国卫生政策研究,2015,8(4):1-11.
[13] Iyengar S.Prices,costs,and affordability of new medicines for hepatitis C in 30 countries:an economic analysis[J].Plos Med,2016,13(5):e1002032.
[14] 孙静,蒋锋,赵琪,等.一个发展中国家实现高值救命药全民可及的成功经验及对我国的启示[J].中国药房,2017,28(3):289-294.
[15] World Health Organization.Global report on access to hc treatment-focus on overcoming barriers[R].WHO:Geneva,2016.
[16] Medicine Patent Pool.Progress and achievements of the Medicines Patent Pool 2010-2015[EB/OL].[2016-12-17]. http://www.medicinespatentpool.org/progess-and-achievements-report/.
[17] Open Source Drug Discovery.What is OSDD[DB/OL].(2016-10-10)[2016-12-17].http://www.osdd.net/aboutus/What-is-OSDD.
[18] 常峰,李思函.药品国际参考定价制度对我国的启示:以加拿大、荷兰、日本三国为例[J].价格理论与实践,2013(7):62-63.
[19] E药脸谱网.人社部医保司司长:力保医疗保险基金可持续[N/OL].(2016-10-17)[2016-12-17].http://mt.sohu. com/20161017/n470467934.shtml.
International Experiences of Medicines Insurance Payment Pricing Mechanisms and the Implications to China
CHEN Yin,SUN Jing,LIU Yuanli(School of Public Health,Chinese Academy of Medical Sciences&Peking Union Medical College,Beijing 100730,China)
OBJECTIVE:To provide reference for setting reasonable medicines insurance payment price in China.METHODS:We retrieved and analyzed academic articles formally published at home and abroad,official websites and government documents,summarized.medicines insurance payment pricing mechanism as well as fair solutions to high-cost medicines,so as to put forward the suggestions to formulate reasonable medicines pricing policy in China.RESULTS&CONCLUSIONS:The international medicines payment prices are usually determined by internal reference pricing method,incremental cost-effectiveness evaluation method and external reference pricing method.The sustainable and fair accessibility of high-cost medicines are promoted by fair medicines pricing program,medicines patent pool,open source medicines discovery znitiative and so on.After the goal of universal health care has been achieved in china,reasonable medical insurance payment price should be explored and formulated.It is necessary to adopt,internal reference pricing method to determine the payment standard of completitive eneric products,external reference pricing method or incremental cost-effectiveness evaluation method to determine the reference price for price negotiation of the innovative patented medicines;the concept of fair pricing for high-cost medicines.
Medicines price;Pricing mechanism;International experience我国的药品价格监管体制目前正经历从政府定价转向企业自主定价,并按医保支付价格支付的阶段。药品定价体系的改革旨在充分利用市场机制,发现合理价格,并以此建立经济激励机制,鼓励医院、医师和患者使用具有成本-效果的药品。本文通过检索分析国内外正式发表的学术文章、官方网站和政府文件、新闻报道等资料和知情人访谈梳理了国际常用的药品价格形成机制,旨在为我国药品医保支付标准的制定提出政策建议。
R12
A
1001-0408(2017)24-3317-04
2017-01-03
2017-04-06)
(编辑:张 静)
中央级公益性科研院所基本科研业务费项目;国家卫生计生委药政司委托研究课题(No.药政〔2016〕9号)
*硕士研究生。研究方向:卫生政策。E-mail:chenyin811@163. com
#通信作者:副教授,博士。研究方向:药物政策与卫生政策。E-mail:sunjing@sph.pumc.edu.cn
DOI10.6039/j.issn.1001-0408.2017.24.02
