肠道微生物与人类膳食、心理健康及生理疾病的相互作用关系
2017-08-11杨淑敬
杨淑敬
(秦皇岛市职业技术学校,河北秦皇岛 066200)
肠道微生物与人类膳食、心理健康及生理疾病的相互作用关系
杨淑敬
(秦皇岛市职业技术学校,河北秦皇岛 066200)
肠道微生物菌群是人类机体的终生陪伴者,肠道微生物的种类、数量、结构与人类膳食和周围环境关系密切并相互作用。肠道微生物失衡直接导致生理疾病。经由肠脑轴,肠道微生物对人类的心理、情绪和行为产生重要影响。肠道微生物与人类膳食、生理疾病和心理健康彼此之间,均呈现双向反馈作用关系,整体构成一个彼此密切关联的系统。
肠道微生物;肠脑;心理健康;菌群干预
食物与肠道微生物、微生物与生理健康乃至心理健康之间有着密切的关联,把所有的关联放在一起系统分析,能够全面认识肠道微生物与人类健康的相互作用关系。
1 肠道微生物与肠道微生态
1.1 肠道微生物
人体肠道中微生物的细胞数量达1014个,占人体微生物总量的78%。肠道微生物约400 ~500种,分为原籍菌群和外籍菌群。当前分子生物学技术的研究初步揭示出宿主与肠道微生物之间互惠共生的分子机制:人肠道向肠道微生物提供栖息和繁殖环境,其中包括天然的厌氧条件、丰富的营养物质、以及适宜的温度和pH等;肠道微生物及其代谢产物影响人体的营养物质加工、能量平衡、免疫功能、胃肠道发育及其他多种重要的生命活动,这种互惠共生关系是宿主与肠道微生物之间在长期协同进化中相互选择和适应的结果,也是一个持续发展进化的过程。
1.2 肠道微生态
肠道菌群与其宿主相互作用相互影响的统一体称为肠道微生态。人体微生态系统包括口腔、皮肤、泌尿、胃肠道四个微生态系统,以肠道微生态系统最为主要、最为复杂。微生态平衡包括微生物与微生物之间、微生物与机体之间、以及微生物、机体、环境三者之间的平衡关系。肠道微生态的平衡,既受宿主遗传性的控制,也受宿主所处外环境的影响,宿主对微生态平衡的影响因素包括:宿主的种族、年龄、性别、发育状况、生理功能、习性、营养及精神紧张、应激反应、感染、老衰、创伤、癌症、外科手术等[1]。环境对微生态平衡的影响因素包括:气候、食物、药物、失重、外来刺激、缺氧、放化疗、辐射、激素治疗等。
人类肠道中的菌群生态系统复杂多样,肠道微生物之间形成并保持一定的共生或拮抗关系,英国牛津大学卡瑟瑞恩·考伊特(Katharine Z. Coyte)等科学家建立了数学模型用于研究人类肠道中成百上千种细菌如何能够成功共存[2]。
2 关于肠脑的研究
除颅脑之外,在我们的身体里还有另一套独立的神经系统——肠神经系统,其机制非常复杂,也被称为“第二个大脑”。它包含了一亿个细胞,是人类大脑细胞的1 000倍;它大约9 m长,从食道一直延伸到肛门。
1907年,美国医学博士拜伦·罗宾逊(Byron Robinson)正式出版《腹部和盆腔脑》理论专著,把位于腹腔内游离的神经网称为“腹脑”[3]。1993年,中国脑外科医生王锡宁认为:“传统意义上的人其实是由两个上下、内外反向对称的身体构成的,以颈部为界分别称为颈上人与颈下人。”[4]1998年,美国哥伦比亚大学解剖学和细胞生物学教授迈克尔·格肖恩(Michael Gershon)出版了他的《第二大脑》理论专著,提出每个人都有第二个大脑,它位于人的肚子里,负责“消化”食物、信息、外界刺激、声音和颜色[5]。
通常认为,脑神经细胞是思考和记忆的细胞,研究发现这种细胞不仅存在于头脑,也存在于人类的消化道。“第二个大脑”、“腹脑”基本类似于目前各类研究中命名的肠脑。肠脑位于食管、胃脏、小肠与结肠内层组织的鞘中,是含有神经细胞、神经传递质、蛋白质和复杂的环行线路。分子生物学、细胞学、免疫学、病理学、生理学等方面的研究为肠脑的存在与功能发挥提供了相关证据。
相对于大脑独立而高级的神经活动和功能,如记忆、思维、分析、逻辑推理、语言等等,肠脑的功能还不够强大,但即使人体在休息状态下肠道仍在运动,除参与消化吸收食物外,还参与身体内其他器官功能的调节,包括影响人的情绪和行为。肠道也能够思考、记忆和学习,它主要负责我们下意识的活动,即对情势或环境的直观感受。迈克尔·格肖恩(Michael Gershon)指出:“肠道向大脑发送的大量信息,都会影响我们的幸福感——我们甚至都意识不到[6]。”
3 肠脑轴——肠道微生物对心理影响的研究
近年来,肠道微生物与心理健康的关联开始得到关注,肠脑轴的发现揭示了肠道微生物影响心理健康的神经生物学机制。
3.1 肠脑轴——肠道微生物对心理产生影响的结构基础
颅脑与肠脑的相互作用可通过三个层次来实现:第一层次是肠神经系统的局部调整;第二层次是椎前神经节,接受和调控来自肠神经系统和中枢神经系统两方面的信息;第三层次是中枢神经系统,由颅脑的各级中枢和脊髓接受内外环境变化时传入的各种信息,经过整合,再有自主神经系统和神经—内分泌系统将调控信息传送到肠神经系统或直接作用于肠效应细胞。这种在不同层级将肠道神经系统与中枢神经系统联系起来的神经—内分泌网络称为肠—脑轴[7]。机体通过肠脑轴之间的神经—内分泌网络的双向回路发生的相互作用称为肠脑互动。肠神经系统既可以独立工作,也可以跟大脑通力合作。
通过哪些物质来实现信息在双脑之间的传递呢?肠脑和颅脑存在共通的联系物质,构成了肠脑互动的化学基础。肠脑中几乎能找到颅脑赖以运转和控制的所有物质,如血清素(五羟色胺)、多巴胺、谷氨酸、去甲肾上腺素、一氧化氮等。肠脑中还存在多种被称为神经肽的脑蛋白、脑啡肽以及对神经起显著作用的化学物质。人体的神经传递物质——血清素95%都产生于肠脑。肠脑负责向颅脑递送全身所需95%的血清素和50%的多巴胺[8]。物质的联系构成了信息、情绪和能量联系的基础,并且这种联系的通路是双向的。
颅脑面临惊恐或情绪压抑时释出的应激激素会刺激食管感到吞咽困难,冲击胃脏产生痉挛,严重时会导致腹泻[9]。
1990年,科学家马克·莱特(Mark Lyte)提出了“Stress ->Immune ->Disease”理论,并开展了很多实验探究微生物是怎样响应宿主的压力、以及探究微生物能否诱发宿主的压力[10]。世界各地类似研究不断增多,在随后的研究中他指出可以将益生菌“定制”、改善肠道环境以针对性的治疗特定的精神和心理疾病[11]。
众多研究表明,肠脑与颅脑之间具有神经介质的双向应答系统,反馈作用是双向的,二者的相互作用统一体形成肠脑轴,肠脑轴在肠脑与颅脑的心理调控功能联结中起到关键作用。
3.2 肠道微生物对肠脑轴的启动与调控作用
3.2.1 肠道微生物——肠脑发挥功能的生物催化媒介
双脑发挥功能的方式有所不同,颅脑发挥功能没有微生物的直接参与运行,而肠脑必须有肠道微生物共生复合才能有效发挥作用。
肠道内的微生物分泌着大量的化学物质,不但有和代谢、免疫相关的因子,也包括了与神经细胞用来沟通和调节情绪的物质相同的东西——多巴胺、血清素和γ-氨基丁酸(GABA)等。人类肠道上皮细胞90%都可以产生五羟色胺,肠道菌群的代谢产物能促进肠道细胞产生五羟色胺[12]。肠道菌群能直接改变神经递质水平,这说明细菌和神经元之间可以产生通讯联系。肠道微生物直接影响着宿主肠道神经系统发挥作用,肠道微生物是肠脑轴的启动调节键。
3.2.2 肠道微生物——颅脑发育和发挥功能的重要影响因素
一方面,微生物及其“副产品”主要通过激活神经纤维,或者通过调节宿主机体的免疫激素、神经化学系统,对颅脑产生影响;另一方面肠道微生物对颅脑的影响主要通过肠脑轴的互动来实现。
除以上两方面,肠道微生物作为重要的环境因素影响着颅脑的发育和功能。围产期暴露于致病微生物后,可引起焦虑行为和认知功能受损。肠道微生物很可能辅助着神经、大脑生物化学、行为,特别是与压力、焦虑和抑郁相关的正常发育。
艾莫伦·梅尔(Emeran Mayer)教授曾用MRI扫描来查看数以千计志愿者的大脑来比较大脑的结构和肠道内不同细菌的类型的关系。他发现大脑区域间的连接是不同的,是依哪类细菌主导性地寄生一个人的肠道中而定的,所以他推断出特定的某些不同微生物混合在人类肠道中可能帮助塑造了大脑的某些类型[13]。即肠道微生物在人体生理生长的同时参与塑造大脑的结构,并且在成年时影响着情绪、行为、感觉。研究发现,肠道细菌一旦缺席,脑部的结构和功能也随之变化。
4 肠道微生物与生理疾病的相互作用
一个人的内脏在75年中大约要通过30多吨的营养物质和5万多升的液体,这些东西的通过量由肠脑高智能地操纵着。肠脑能分析成千上万种化学物质的成分,并使人体免受各种毒物和危险的侵害。肠是人体中最大的免疫器官,它拥有人体70%的防御细胞,大量的防御细胞与肠脑相通。
肠道微生物作为人体的体外细胞,其正常新城代谢过程中的物质交换过程直接在肠道内进行,各种代谢物质对于机体来讲,属于外来抗原,肠道响应自体和外界环境中多种抗原、生成对抗特定抗原的单一抗体,发生的化学作用均有体外抗原与体内抗体之间的免疫反应过程。当毒素进入身体时,机体发生相应的免疫反应,肠脑最先察觉,然后立即向大脑发出警告信号,接着采取行动:呕吐、痉挛或排泄。
肠道免疫系统能够对病原微生物产生免疫应答,却对食物和肠道微生物产生免疫耐受,即通常所说的免疫学矛盾。前肠中抗原主要来自于食物,而回肠和结肠中抗原不仅来自于食物,还增加了复杂的肠道微生物。这些食物和肠道微生物与普通抗原一样,在体外试验中均能引起免疫应答,在体内却通常产生免疫惰性。
在一项针对小鼠的新研究中,来自美国加州大学伯克利分校等机构的研究人员揭示出从母乳中获得的免疫球蛋白G抗体有助抑制在生命早期对新获得的微生物产生的免疫反应[14]。
根据波士顿儿童医院杜恩·威斯曼(Duane Wesemann)博士和弗莱德里克·艾尔特(Frederick Alt)博士发表的一项研究,证实肠道细菌显著地影响了免疫系统的B淋巴细胞,B细胞在肠道中早期发育,并且微生物影响了这一过程。肠道免疫系统对食物和肠道微生物产生免疫耐受,即从出生开始,肠道微生物就在一点一点塑造着肠道免疫系统。
肠道微生态平衡是生理健康的必要条件。微生物的失衡,影响肠道和人体正常的免疫功能,是过敏、糖尿病、肥胖等一些生理疾病的根源。
5 膳食结构与肠道微生物的相互作用
膳食结构的合理与稳定,对维持肠道微生态非常重要,肠道菌群又通过参与食物的消化、吸收、以及合成部分营养素等,调节着人体的新陈代谢。
肠道菌群改变的方向因宿主基因型不同和宿主肠道菌群背景不同而存在差异。同时在实验中发现,饮食对肠道菌群的影响可能掩盖了因基因型不同而导致的本已存在的差异。肠道菌群的变化对饮食的应答呈现明显的剂量依赖关系,饮食的微妙变化会引起肠道菌群成分结构的改变;肠道内长期稳定的菌群成分、结构影响着个人的饮食偏好和习惯,二者在一定限度内按照正相关相互影响相互作用。
6 肠道微生物与人类膳食、心理健康与生理疾病相互作用关系图
肠道微生物与人类膳食、心理健康与生理疾病相互作用关系可以通过下图进行概括说明:
7 结语
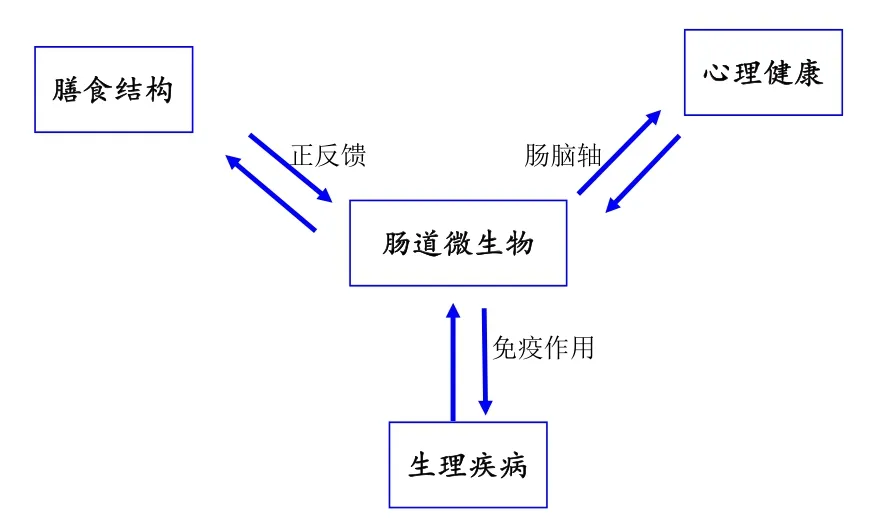
图1 肠道信息交换
肠道共生微生物与人类膳食结构、心理健康和生理疾病密切相关,在机体物质和信息交换过程中,肠道处于枢纽位置。肠道微生物是肠道基因表达过程和信息传递过程中不可或缺的程序编译员。深入研究人类共生微生物与健康和疾病的关系,将为一些疾病的预防和治疗提供指导和方向。人类作为自身微生物菌群的管理者,应学会科学利用微生物促进身心健康。
[1] Nathalie M Delzenne,Patrice D Cani. Interaction Between Obesity and the Gut Microbiota: Relevance in Nutrition[J]. Annual Review of Nutrition,2011,31:15-31.
[2] Katharine Z Coyte,Jonas Schluter,Kevin R Foster. The ecology of the microbiome: Networks,competition,and stability[J]. science,2015,350:663-666.
[3] Byron Robinson. The abdominal and pelvic brain[M]. Hammond: Frank S. Betz, 1907:123-126.
[4] 王锡宁.论人体巨系统的解剖构成原理:结绳原理[J]. 医学理论与实践,1993,6(01):40-43+15.
[5] 田在善.有关“腹脑(第二大脑)”之说[J].中国中西医结合外科杂志,2005,12(05):454-457.
[6] http://www.360doc.com/content/15/0615/19/11542102_478 343952.shtml,2016/05.
[7] A J Montiel Castro,RM González-Cervantes,G Bravo-Ruiseco,G Pacheco-López .The Microbiota-gutbrain Axis: Neurobehavioral Correlates,Health and Sociality[J]. Frontiers in Integrative Neuroscience,2013,7:70.
[8] P C Konturek,etal. Stress And the Gut: Pathophysiology,Clinical Consequences,Diagnostic Approach And Treatment Options[J]. Physio & Pharm,2011,62(6):591-599.
[9] Dréau Didier,Mark Lyte,Fowler Nina etal.Social Conflict Stress,Immune Responses,And Resistance to Infection[J]. Shock, 1997, 7(4):419-438.
[10] D Dreau,G Sonnenfeld,N Fowler,DS Morton,Mark Lyte. Social stress alters splenocyte phenotype and function[J]. Physiology & Behavior, 1999, 67(1):119-125.
[11] Hsiao EY,McBride SW,Hsien S,Sharon G,Hyde ER,etal. The microbiota modulates behavioral and physiological abnormalities associated with neurodevelopmental disorders[J].Cell,2013,155:1451-1463.
[12] Emeran Mayer. Gut feelings: the emerging biology of gut-brain communication[J]. Nat Rev Neurosci, 2011;12(8):453-66.
[13] Meghan A. Koch,Gabrielle L Reiner,Kyler A Lugo etal. Maternal IgG and IgA Antibodies Dampen Mucosal T Helper Cell Responses in Early Life[J]. Cell,2016,165(4):827-841.
[14] Duane Wesemann,Andrew J Portuguese.Microbial colonization influences early B-lineage development in the gut lamina propria[J]. Nature,2013,501(7465):112-115.
The Interaction Between Intestinal Microorganism and Human Diet,Mental Health and Physiological Diseases
Yang Shujing
(Qinhuangdao vocational technical school,Qinhuangdao Hebei 066200,China)
intestinal microbiome is a lifelong companion of human organism,and the species,quantity and structure of intestinal microorganism are closely related to human diet and surrounding environment. Intestinal microbial imbalance leads to physical illness. Through the gut brain,gut microbes have an important influence on human psychology,mood and behavior. Intestinal microorganism and human diet,physical disease and mental health are all present in a two-way feedback function,and the whole constitute a system closely related to each other.
intestinal microorganism;the gut brain;mental health;flora intervention
杨淑敬,教育学硕士,副高级,研究方向:肠道微生物学。
