Co2Z型铁氧体的制备及其吸附性能
2017-08-08冯菊红葛燕丽胡学雷
何 方 ,冯菊红 *,葛燕丽 ,胡学雷
1.武汉工程大学化工与制药学院,湖北 武汉 430205;2.绿色化工过程教育部重点实验室(武汉工程大学),湖北 武汉 430205
Co2Z型铁氧体的制备及其吸附性能
何 方1,2,冯菊红1,2*,葛燕丽1,2,胡学雷1,2
1.武汉工程大学化工与制药学院,湖北 武汉 430205;2.绿色化工过程教育部重点实验室(武汉工程大学),湖北 武汉 430205
以硝酸钡、硝酸铁和硝酸钴为原料,采用共沉淀法制备了Co2Z型铁氧体(Ba3Co2Fe24O41)粉末,制备工艺的最佳条件为溶液pH=12、煅烧温度为1 300℃和煅烧时间为4 h.通过X射线衍射仪、扫描电子显微镜对产物晶型和形貌进行了表征.考察了Co2Z型铁氧体对溶液中亚甲基蓝的吸附作用.结果表明:铁氧体质量为0.10 g、溶液pH=12、亚甲基蓝的初始质量浓度为10 mg∕L时,铁氧体对亚甲基蓝的吸附率可达89.49%,最大吸附量为9.181 mg∕g.Co2Z型铁氧体(Ba3Co2Fe24O41)对亚甲基蓝有较好的吸附作用,可用于亚甲基蓝染料废水处理.
Co2Z型铁氧体;共沉淀法;亚甲基蓝;吸附
我国属于染料生产大国,纺织染料工业快速发展的同时,大量工业染料废水排放使得污染问题日益严重.如何有效去除水中的有害物质,净化水体成为当今治理工业废水领域的热点与难点.现今对各种染料废水治理方法大致可分为:物理法(吸附法、膜技术、磁分离技术等)、化学法(氧化法、混凝法、电化学法等)、生化法(好氧法、厌氧法、厌氧-好氧结合法等)三大类[1-3].与其他两种方法相比,物理法具有效率高、操作简单、不会造成二次污染等优点.近年来,关于采用铁氧体作为物理法吸附剂处理染料废水的研究越来越多.与其他价格昂贵、再生困难的吸附剂相比,铁氧体的成本更为经济低廉[4-6].已有文献报道尖晶石型铁氧体处理有机染料,能达到比较好的饱和吸附量[4].从性质上看,磁铅石型铁氧体比尖晶石型铁氧体磁性更强,对染料应具有更好的选择性和良好的吸附性[7-9].但是,磁铅石型铁氧体用以吸附染料的研究还未见报道.
因 此 ,我 们 以 Ba(NO3)2、Fe(NO3)3·9H2O、Co(NO3)2·6H2O为原料,采用共沉淀法合成了磁铅石型Co2Z型铁氧体Ba3Co2Fe24O41,研究了其最佳制备条件,并详细探讨了Co2Z型铁氧体对亚甲基蓝(methylene blue,MB)染料吸附的性能及其影响因素,以期为磁铅石铁氧体在工业废水及污水处理中的应用研究提供理论依据.
1 实验部分
1.1 主要原料
硝酸钡、硝酸铁、硝酸钴、MB(均为分析纯试剂,国药集团化学试剂有限公司).实验用水为自制去离子水.
1.2 仪器与设备
紫外可见分光光度计(ultraviolet-visible light detector,UV-Vis):T6 新世纪,北京普析通用仪器有限责任公司;X射线衍射(X-ray diffractometer,XRD)仪:日本 D∕Max-RB;扫描电子显微镜(scan⁃ning electron microscopy,SEM):日本JSM-5610LV;离心机(德国 Universal 360R),马弗炉(合肥KSL-1700X-A).
1.3 Co2Z型铁氧体的制备
按照一定的比例称量硝酸钴、硝酸铁和硝酸钡,并溶于蒸馏水中.用机械搅拌在60℃水浴中搅拌至固体颗粒全部溶解,得到其混合液.加入适量的Na2CO3(碳酸钠)与NaOH(氢氧化钠)混合溶液,可得到沉淀.在机械搅拌下,往其中慢慢滴加碱溶液调节pH值,静置,过滤,用蒸馏水洗至中性,干燥,即得到前体粉末.将前驱体用刚玉坩埚放入马弗炉中煅烧,即得到Co2Z型铁氧体[10-12].
1.4 测试与表征
用XRD仪分析样品的晶型,从而获得制备铁氧体的最佳煅烧时间、煅烧温度与pH值.利用扫描电子显微镜测定样品形貌,从而选出制备最佳条件.
1.5 吸附测试
取一定质量的铁氧体置于玻璃烧杯中,加入100 mL的MB溶液,试验在室温下以磁力搅拌,考察一定质量铁氧体在不同初始浓度MB溶液中的吸附去除效果、不同pH值对染料吸附效果的影响、吸附时间对染料吸附的影响、铁氧体投料量对染料吸附的影响[13-15].
各试验均定时取样品,在4 000 r∕min条件下离心,并用磁铁吸附铁氧体后迅速进行分析测定.
MB浓度用紫外分光光度计测定,检测波长采用其最大吸收波长664 nm.
2 结果与讨论
2.1 最佳铁氧体的制备条件
2.1.1 pH值的影响 研究共沉淀剂用量对Co2Z型铁氧体的影响,按照不同的滴加量,调节溶液pH值.在1 300℃煅烧4 h作为实验反应条件,不同pH值制备Co2Z型铁氧体的XRD图如图1所示.

图1 不同pH值制备的Co2Z型铁氧体的XRD图谱(Z#19-97:Co2Z型铁氧体标准图)Fig.1 XRD patterns of Co2Z-type barium hexaferrite at different pH(Z#19-97:standard diagram of Co2Z-type barium hexaferrite)
由图1可知,当pH=12时,所得样品的衍射峰与标准图谱对应较好.pH值偏小时,小的特征峰不明显;pH值过大时,杂峰较多.当pH值大于10时,前驱体沉淀更加完全,杂质减少;但是,当pH值过大时,则会使反应后的废液碱性过强,不利于后续处理,有害环境.故选择pH=12作为反应条件.
2.1.2 煅烧温度的影响 实验选取在pH值为12,煅烧时间为4 h的条件下,分别采用1 200℃,1 250℃,1 300℃,1 350℃煅烧铁氧体前驱体,不同煅烧温度制备铁氧体的XRD图如图2所示.

图2 不同煅烧温度制备的Co2Z铁氧体的XRD图(Z#19-97:Co2Z型铁氧体标准图)Fig.2 XRD patterns of Co2Z-type barium hexaferrite calcinated at different temperatures(Z#19-97:standard diagram of Co2Z-type barium hexaferrite)
煅烧温度1 200℃时特征峰不明显,峰形不尖锐.而随着煅烧温度的升高,Co2Z型铁氧体的特征峰逐渐产生.但在1 250℃时还存在少量其他型铁氧体的特征峰,可能原因是烧结温度过低,需要进一步升温.但是当温度过高,在1 350℃时,杂峰增加,故最终选择1 300℃为最佳煅烧温度.
2.1.3 煅烧时间的影响 实验选取pH=12,煅烧温度为1 300℃的条件下,前驱体采用2 h、2.5 h、3 h和4 h的煅烧时间,不同煅烧时间制备的铁氧体的XRD图如图3所示.
由图3可知,在煅烧时间为2 h~3 h时,衍射度较强的特征峰并未完全出现,57°的特征峰基本没有,且此时相对于Co2Z型铁氧体的标准图谱看来,未知杂质峰较多,故选取煅烧时间为4 h.

图3 不同煅烧时间制备的Co2Z铁氧体的XRD图(Z#19-97:Co2Z型铁氧体标准图)Fig.3 XRD patterns of Co2Z-type barium hexaferrite calcinated at different times(Z#19-97:standard diagram of Co2Z-type barium hexaferrite)
综上所述,最佳反应条件为pH=12、1 300℃温度下煅烧4 h时,所得样品的衍射峰与标准图谱对应较好.通过SEM检测在此条件下的成品,可以清晰的看见形貌完整的六角片状Co2Z型铁氧体,如图4所示.

图4 pH=12,1 300℃温度下煅烧4 h的Co2Z铁氧体的SEM图Fig.4 SEM image of Co2Z-type barium hexaferrite calinated at 1 300℃for 4 h
2.2 影响吸附效果的因素
2.2.1 pH值的影响 吸附剂的官能团、电离程度、染料分子的结构性质会受到pH值的影响,实验结果如图5所示.选取铁氧体0.10 g,MB质量浓度为10 mg∕L,在 MB溶液 pH值为4、6、8、10、12、14的条件下吸附率由5.11%升高到89.49%,pH值为14时吸附率下降到72.31%.随着pH值的升高,吸附剂与负电性MB分子之间的静电作用力增强,促进了染料分子在吸附剂表面的吸附作用.当pH值过高时,溶液中OH-和吸附剂表面活性位点结合,减弱了MB与吸附剂结合的机会.故选定MB溶液pH值12为反应条件.

图5 pH对MB吸附的影响Fig.5 Effect of solution pH on adsorption of MB
2.2.2 吸附时间的影响 称取铁氧体0.10 g,放入质量浓度为10 mg∕L的MB溶液中,分别吸附0.5 h、1 h、2 h、3 h、6 h、9 h、12 h、15 h.当溶液pH=12和铁氧体投料量为0.10 g时,探讨吸附时间对吸附效果的影响.实验结果如图6所示,随着吸附时间的增加,吸附率逐渐增加.当吸附时间为12 h时,吸附逐渐达到平衡并且吸附率最大,达到89.49%;超过12 h后,吸附率并没有明显增加,因此吸附平衡时间为12 h.
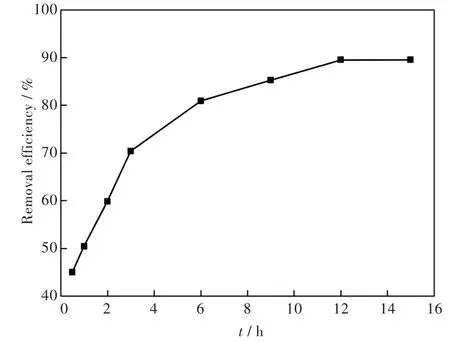
图6 吸附时间对MB吸附的影响Fig.6 Effect of time on adsorption of MB
2.2.3 初始质量浓度的影响 选用条件为pH=12,铁氧体质量为0.10 g,在不同的MB初始质量浓 度 下(10 mg∕L、20 mg∕L、30 mg∕L、40 mg∕L、50 mg∕L),探讨保持溶液 pH=12、铁氧体投料量为0.10 g、吸附时间为12 h时溶液初始浓度对吸附效果的影响.
反应达到平衡后,随着质量浓度的增加,平衡吸附容量从 3.286 mg∕g增加到 9.181 mg∕g,去除率由89.49%下降到28.86%.吸附剂表面随着初始质量浓度的增加,有效吸附位点与染料分子结合而减少,使初始浓度变为固液扩散的驱动力,如图7所示.

图7 初始质量浓度对MB吸附的影响Fig.7 Effect of initial mass concentration on adsorption of MB
2.2.4 投料量的影响 分别取0.10 g、0.15 g、0.20 g、0.25 g、0.30 g铁氧体加入质量浓度为 10 mg∕L 的MB溶液,经吸附12 h.探讨保持pH值12和吸附时间12 h不变,投料量的多少对吸附效果的影响,实验结果如图8所示.从图8中可看出吸附率随着铁氧体的添加量增加而增加,然后趋于平稳.当铁氧体添加量为0.20 g时,吸附率最大,达到93.40%.说明当投料量为0.20 g时,吸附已基本达到饱和.
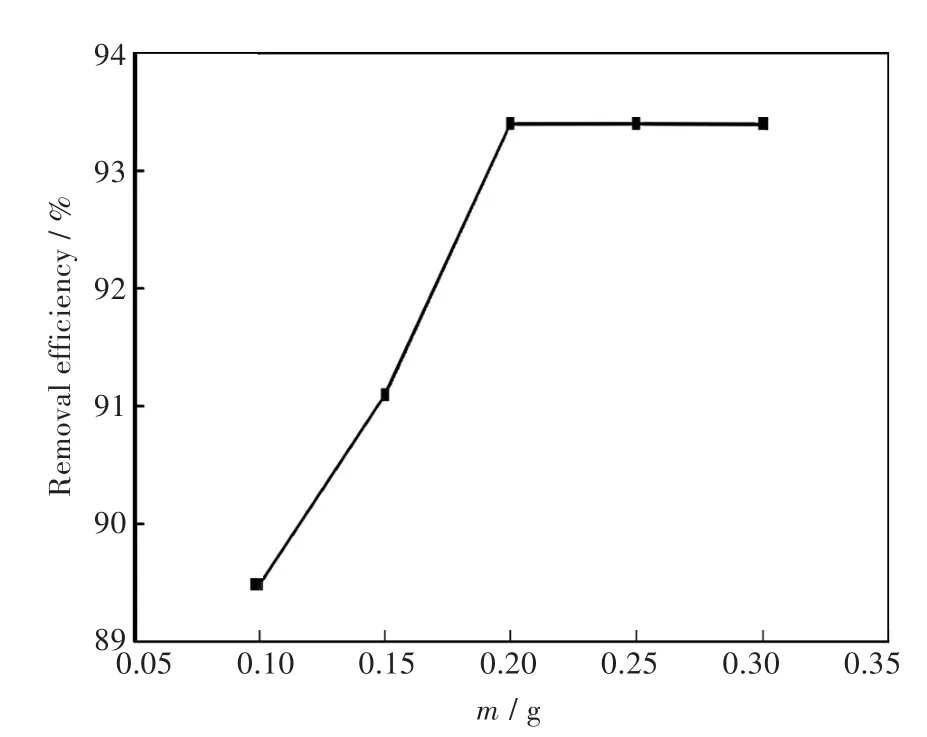
图8 投料量对MB吸附效果的影响Fig.8 Effect of adsorbent dosage on adsorption of MB
2.3等温吸附模型
Langmuir等温模型线性方程为:

将实验所得数据带入方程进行拟合,其中Q为铁氧体对MB的吸附量(mg∕g),b为与吸附强度有关的常数,Ce是吸附平衡时吸附质质量浓度,qe为吸附平衡时吸附剂对吸附质的吸附量.拟合表明MB在吸附剂表面的吸附符合Langmuir吸附等温线,如图9所示.拟合所得参数R2值为0.956 19,理论最大吸附量为10.56 mg∕g,与实验最大吸附量为9.181 mg∕g较为接近.结果表明,拟合效果较好,可以用此方程描述铁氧体的吸附,并预测吸附量.

图9 朗缪尔等温吸附线Fig.9 Langmuir adsorption isotherm
2.4 Z型铁氧体吸附剂再生性试验
将0.10 g的Z型铁氧体加入100 mL的10 mg∕L的MB溶液中,调节pH值至12,磁力搅拌至吸附平衡.将铁氧体与溶液磁分离后,取上层清液,测其吸光度并计算吸附率.将分离后的铁氧体放入马弗炉中[16],于350 ℃煅烧2.5 h.干燥冷却后,再将吸附剂加入100 mL的10 mg∕L的MB溶液中,pH值调至12,磁力搅拌吸附至平衡,以此循环5次.得到脱附再生吸附剂的吸附效果如图10所示.
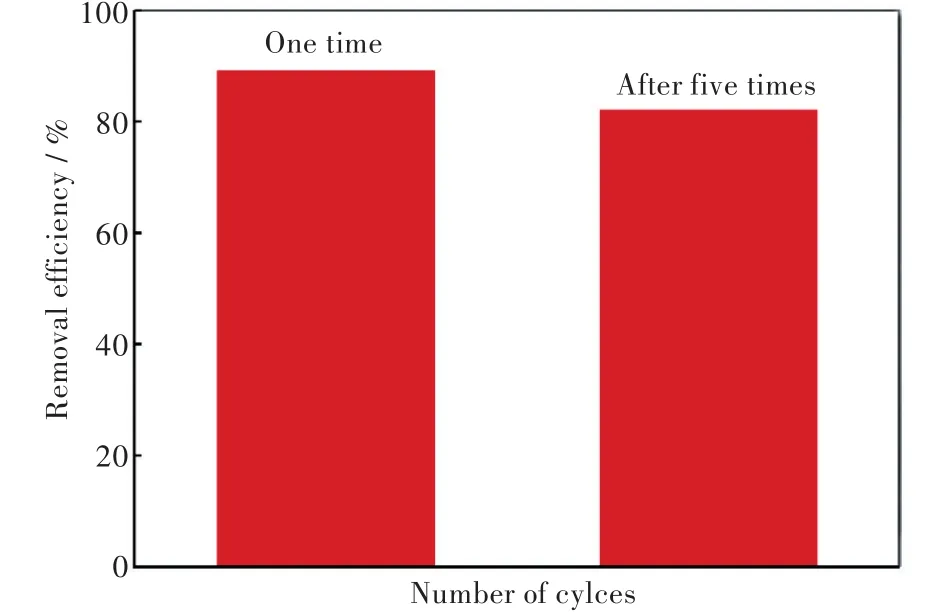
图10 Co2Z型铁氧体的脱附再生Fig.10 Desorption and regeneration ofCo2Z-type barium hexaferrite
在5次洗脱后,铁氧体对MB的吸附率虽下降至82.3%,但仍然具有良好的吸附效果.因此,Z型铁氧体可对MB再生吸附作用.
3 结 语
采用共沉淀法制备了六角片状磁铅石Co2Z型铁氧体(Ba3Co2Fe24O41)粉体,对制备条件进行了优化,pH为12时获得的共沉淀前驱体在1 300℃温度下煅烧4 h时制备的铁氧体Ba3Co2Fe24O41,晶相单一且形貌较好.研究了目标产物对MB染料吸附性能,结果表明:在pH=12、MB质量浓度为10 mg∕L时,目标吸附剂对染料的最大吸附量为9.181 mg∕g,吸附率达89.49%,吸附行为通过拟合符合朗缪尔吸附模型,并通过模型计算的理论量为10.56 mg∕g,与实验值接近.将吸附染料的铁氧体粉体进行5次吸附脱附后测试吸附率测试,仍有82.3%的吸附率.因此,本文制备的Co2Z型铁氧体(Ba3Co2Fe24O41)粉体吸附剂可用于MB染料废水的脱色,并可再次重复利用,具有良好的应用前景.
[1]AHMARUZZAMAN M,REZA A R.Decontamination of cationic and anionic dyes in single and binary mode from aqueous phase by mesoporous pulp waste[J].Environmental Progress&Sustainable Energy,2015,34(3):724-735.
[2]SENTHAMARAI C,SENTHIL K P,PRIYADHARSHINI M P,et al.Adsorption behavior of methylene blue dye onto surface modified strychnos potatorum seeds[J].Environmental Progress&Sustainable Energy,2013,32(3):624-632.
[3]SINGH K,ARORA S.Removal of synthetic textile dyes from wastewaters:a critical review on present treatment technologies[J].Critical Reviews in Environmental Science and Technology,2010,41(9):807-878.
[4]马荣伟.生物膜板法制备尖晶石吸附剂及其性能研究[D].济南:济南大学,2014.
[5]张秀蓉,龚继来,曾光明,等.磁性氧化石墨烯制备及去除水中刚果红的研究[J].环境污染与防治,2013,33(7):1379-1385.ZHANG X R,GONG J L,ZENG G M,et al.Synthesis of magnetic grapheme oxide adsorbent for Congo red removal from aqueous solution[J].China Environmental Science,2013,33(7):1379-1385.
[6]GHOLIVAND M B,YAMINI Y,DAYENI M,et al.Removalofmethyleneblueandneutralred from aqueous solutions by surfactant-modified magnetic nanoparticles as highly efficient adsorbent [J].Environmental Progress&Sustainable Energy,2016,34(6):1683-1693.
[7]CAFFARENA V D R,PINHO M S,CAPITANEO J L,et al.Synthesis and characterization of Ba3Co2Fe24O41and Ba3Co0.9Cul.1Fe24O41nanopowders and their application as radar absorbing materials[J].Ceramic Engineering&Science Proceedings,2008 ,28(2):3-13.
[8]HANPHIL R,CHANG W,LEE B.DVB-H antenna structure using Z-type hexagonal ferrite for folder-type mobile phones[J].Microwave and Optical Technology Letters,2009,51(9):2196-2199.
[9]LIU B S,WEN L,NAKATA K,et al.Polymeric adsorption of methylene blue in TiO2colloids—highly sensitive thermochromism and selective photocatalysis[J].Chemistry,2012,18(40):12705-12711.
[10]YU B Y,KWAK S Y.Self-assembled mesoporous Co and Ni-ferrite spherical clusters consisting of spinel nanocrystals prepared using a template-free approach[J].Dalton Transactions,2011,40 (39):9989-9998.
[11]LI H F,GONG R Z,FAN L R,et al.Synthesis,characterization and electromagnetic waveabsorption properties of Z-type hexaferrites prepared by molten salt method[J].Advanced Material Reasearch,2009,66(66):69-72.
[12]TAINAKA T,KIKUCHI T,NAKAMURA T,et al.Synthesis of the Sr3Zn2Fe24O41Z-Type ferrite by polymerizable complex method[J].Key Engineering Materials,2013,566:231-234.
[13]NEELESH B S,GIRIDHAR M.Kinetics of adsorption of methylene blue and rhodamine 6G on acrylic acid-based superabsorbents[J].Journal of Applied Polymer Science,2012,126(2):463-472.
[14]闫宗兰,尉震,宋学立.活性炭对孔雀石绿和酸性铬蓝K的吸附性能研究[J].天津农学院学报,2012,19(1):45-47.YAN Z L,WEI Z,SONG X L.Studies on adsorption properties of activated carbon for malachite green and acid chrome blue K[J].Journal of Tianjin Agricultural University,2012,19(1):45-47.
[15]陈秋芳,农文贵,崔巍.磁技术在污废水处理中的作用机理及应用[J].环境科学与管理,2012,37(8):110-114.CHEN Q F,NONG W G,CUI W.Mechanism and application ofmagnetic technology in wastewater treatment [J]. Environmental Science and Management,2012,37(8):110-114.
[16]方巧,林建伟,詹艳慧,等.羟基磷灰石-四氧化三铁-沸石复合材料制备及去除水中刚果红研究[J].环境科学,2014,35(8):2992-3001.FANG Q,LIN J W,ZHAN Y H,et al.Synthesis of hydroxyapatite∕magnetite∕zeolite composite for congo red removal from aqueous solution[J].Environmental Science,2014,35(8):2992-3001.
本文编辑:苗 变
Preparation and Adsorption Property of Co2Z-Type Barium Hexaferrite
HE Fang1,2,FENG Juhong1,2*,GE Yanli1,2,HU Xuelei1,2
1.School of Chemical Engineering and Pharmacy,Wuhan Institute of Technology,Wuhan 430205,China;2.Key Laboratory of Green Chemical Process(Wuhan Institute of Technology),Ministry of Education,Wuhan 430205,China
The Co2Z-type barium hexaferrite(Ba3Co2Fe24O41)powder was prepared by coprecipitation method using barium nitrate,ferric nitrate and cobalt nitrate as raw materials.The optimal conditions for the preparation process were found at solution pH of 12,calcination temperature of 1 300℃ and calcination time of 4 h.The crystal form and morphology of the product were characterized by X-ray diffraction and scanning electron microscopy.The adsorption of methylene blue on Co2Z-type barium hexaferrite was explored.The results show that adsorption rate is 89.49%and the maximum adsorption capacity is 9.181 mg∕g at mass of Co2Z-type barium hexaferrite of 0.10 g,solution pH of 12 and initial mass concentration of methylene blue of 10 mg∕L.Therefore,the as-prepared Co2Z-type barium hexaferrite(Ba3Co2Fe24O41)has a good adsorption effect on methylene blue and can be used for the treatment of methylene blue wastewater.
Co2Z-type barium hexaferrite;coprecipitation method;methylene blue;adsorption
O614.81
A
10.3969∕j.issn.1674⁃2869.2017.04.008
2017-01-16
武汉工程大学研究生创新基金(CX2015074);湖北省自然科学基金重点项目(2011CDA048)
何 方,硕士研究生.E-mail:510000181@qq.com
*通讯作者:冯菊红,博士,讲师.E-mail:jhfeng@wit.edu.cn
何方,冯菊红,葛燕丽,等.Co2Z型铁氧体的制备及其吸附性能[J].武汉工程大学学报,2017,39(4):353-358.
HE F,FENG J H,GE Y L,et al.Preparation and adsorption property of Co2Z-type barium hexaferrite[J].Journal of Wuhan Institute of Technology,2017,39(4):353-358.
1674-2869(2017)04-0353-06
