Cs2.5H0.5PMo12O40/TiO2复合物的制备及光催化性能研究
2017-08-08门春艳
门春艳
(新疆应用职业技术学院,新疆伊犁哈萨克自治州833200)
Cs2.5H0.5PMo12O40/TiO2复合物的制备及光催化性能研究
门春艳
(新疆应用职业技术学院,新疆伊犁哈萨克自治州833200)
以钛酸丁酯、磷钼酸、硝酸铯为主要原料,采用溶胶-凝胶法及水热合成技术制备了Cs2.5H0.5PMo12O40/TiO2复合光催化剂,以甲基橙为模拟污染物,考察了不同条件下催化剂的光催化活性。结果表明,复合光催化剂的用量、酸度、甲基橙初始浓度等是影响催化降解效果的重要因素。适宜的光催化降解甲基橙的条件:复合物凝胶在190℃水热处理1 h(升温速率控制为1℃/min),Cs2.5H0.5PMo12O40/TiO2负载量为35%,溶液pH为4~5,450 W高压汞灯照射,0.05 g复合催化剂降解50 mL 10 mg/L甲基橙溶液,2 h内甲基橙降解率可达到80%以上。复合光催化剂重复使用3次后降解率仍可达60%.该复合光催化剂对罗丹明B、次甲基蓝等也有较好的光催化降解效果。
TiO2;溶胶-凝胶法;水热合成;光催化
光催化氧化技术能利用紫外光或者太阳光彻底将有机污染物降解成CO2、H2O以及其他无机小分子,在处理低浓度难降解有机污染物方面具有广泛的应用前景。TiO2是一种研究最早、最深入的金属半导体光催化材料,因其光催化氧化能力强、安全无毒、性能稳定、生物化学和光化学稳定性好等优点,作为一种有效的光催化材料得到了广泛的关注和研究[1-3]。TiO2有3种晶体结构,即锐钛矿、金红石和板钛矿,它们晶体结构的基本单元是TiO6八面体,一般认为,锐钛矿的光催化氧化活性最高,也有报道锐钛矿和金红石混合晶相活性更高。TiO2是一种宽禁带半导体,其禁带宽度为Eg=3.2 eV。当入射光波长小于387.5 nm时,其价带上的电子被激发跃迁到导带上,产生电子-空穴对。光生电子可以被氧气或金属离子俘获;而光生空穴可以将吸附在TiO2表面的OH-和H2O氧成·HO。·O2-和·HO具有很强的氧化能力,可以将有机物氧化成CO2、H2O以及一些简单的无机物,为消除环境污染和水处理开辟了新的道路。但是TiO2带隙较宽,只能被紫外光激发,对太阳光的利用率低;而且光生载流子的复合率高,光催化效率低。这些缺陷限制了TiO2光催化剂的应用前景,也促使人们开始对TiO2进行改性研究。
杂多酸具有类似半导体氧化物能带结构,其光催化性得到广泛的关注。杂多酸对TiO2修饰的研究也处于探讨之中。已有的研究显示,TiO2和杂多酸在光催化降解有机污染物的反应中,都显示了良好的催化活性。将两者复合,不仅可以降低受激发所需要的能量,使复合催化剂的光谱响应范围向可见光区移动,提高了可见光区的利用率,而且多酸被束缚在TiO2网络上,具有合适的能隙结构,能迅速使TiO2所产生的光生电子转移,从而减少了电子与空穴的复合数量,提高了光催化效率。2种光催化剂的协同作用,在一定程度上提高了复合材料的光催化活性。但是由于多酸易溶于水,负载后的多酸在反应体系中因溶脱而使催化剂的重复使用受到限制。本文采用溶胶-凝胶法及水热合成技术制备了Cs2.5H0.5PMo12O40/TiO2,选择可溶性有机染料甲基橙作为模型污染物,考察了复合物的光催化活性以及重复使用情况,获得了较为满意的结果。
1 实验部分
1.1 实验所用试剂及仪器
1.1.1 实验试剂
磷钼酸、钛酸丁酯、甲基橙、酸性品红、次甲基蓝、罗丹明B、氢氧化钠、盐酸、硝酸铯、无水乙醇均属于分析纯试剂。
1.1.2 实验仪器
实验仪器:UV-3010紫外可见分光光度计、722型可见分光光度计、ХYJ-802离心沉淀机、LХJ-64-01离心机、GYZ-250型自镇流荧光高压汞灯(450 W)、79-1型磁力加热搅拌器、AM5250A型磁力搅拌器、高压釜、烘箱。
1.2 Cs2.5H0.5PMo12O40的制备
准确称取1.067 g的H3PMo12O40和0.248 g的CsNO3,分别溶解在6 mL和12 mL的蒸馏水中,配置成物质的量浓度为0.08 mol/L的H3PMo12O40和0.1 mol/L的CsNO3溶液,在H3PMo12O40溶液中逐滴加入CsNO3溶液(磁搅拌条件下),有黄色乳状沉淀生成,搅拌30 min,静置12 h,控制温度55℃旋转蒸发至干,得样品Cs2.5H0.5PMo12O40。
1.3 Cs2.5H0.5PMo12O40/TiO2复合物的制备
称取3.560 7 g的酞酸丁酯溶解在10 mL的无水乙醇中,称取一定量制备的Cs2.5H0.5PMo12O40,用1 mL蒸馏水将其溶解,在磁力搅拌条件下缓慢地逐滴加入到酞酸丁酯溶液中,瓶中剩余的Cs2.5H0.5PMo12O40用5~6 mL的无水乙醇分次洗,完全滴入酞酸丁酯溶液中,调节pH至1~2(得黄色乳状液),持续搅拌1 h,控制磁搅拌加热温度50℃左右,加热搅拌2 h,得黄色凝胶物质。将黄色凝胶物质转移至高压釜中持续升温至190℃(1℃/min),然后在190℃恒温1 h,自然冷却后取出,将高压釜中物质的温度控制为55℃,真空旋转蒸发至干,得样品。
2 结果与讨论
2.1 催化剂用量对降解效果的影响
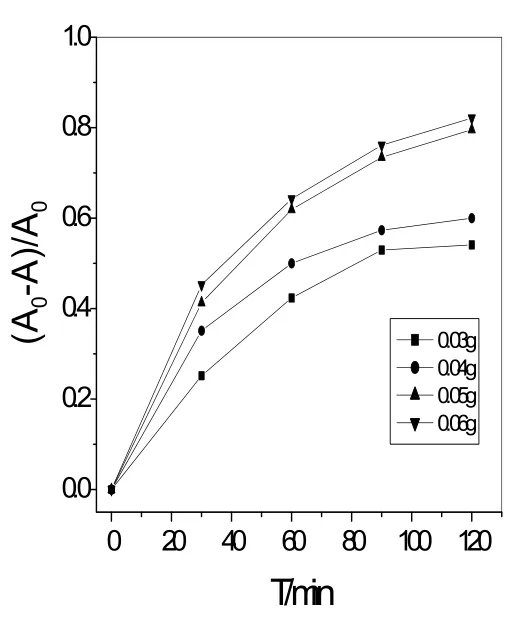
图1 催化剂用量对降解效果比较
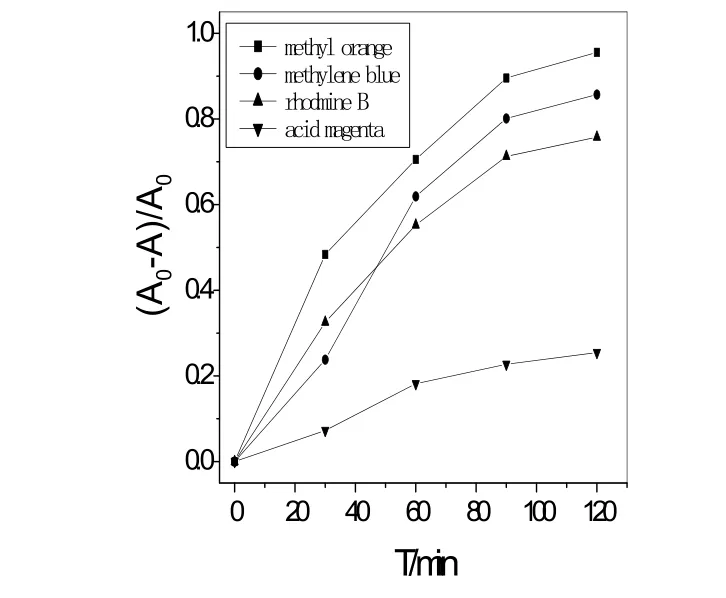
图3 对不同有机染料的降解效果
催化剂用量对甲基橙的光催化降解影响结果见图1.由图1可以看出,随着催化剂用量的增加,相同时间内甲基橙溶液的催化降解呈上升趋势;但随着催化剂用量的再增大,降解率变化不大。这是由于光催化反应是在催化剂表面进行的,在甲基橙溶液浓度一定的情况下,催化剂的用量增多,提供反应的活性位增多,有光照产生的活性基团(比如-OH)也增多,因此光催化反应的速率增大。若进一步增加催化剂的用量,就提供了足够多的活性位,反应达饱和;若继续增大催化剂的用量,由于催化剂对光的散射和屏蔽作用,光照效率下降,使甲基橙溶液降解率达到平衡。本实验反应体系中,甲基橙溶液的质量浓度为10 mg/L,最适宜的催化剂用量为0.050 0 g。
2.2 体系酸度对催化效果的影响
在同体积下,相同浓度的甲基橙溶液中加入0.050 0 g负载量为35%的Cs2.5H0.5PMo12O40/TiO2复合光催化剂,由于Cs2.5H0.5PMo12O40/TiO2复合光催化剂为弱酸性,且难溶于水,催化剂悬浮于甲基橙中,溶液显弱酸性,通过高氯酸或氢氧化钠调节溶液的pH值,考察pH值对催化效率的影响,结果见图2.由图2可以看出,在强酸性(pH=1~2)和中性至碱性条件下,甲基橙的降解率很低;在弱酸性条件下,甲基橙的降解率较高。
在碱性条件下,多酸会发生分解,破坏了复合光催化剂,导致光催化降解效率大大下降。最适宜的体系酸度pH值为4~5.在中性和碱性介质中,复合催化剂活性较低的原因是在高pH值的条件下,杂多阴离子会发生分解;在强酸性介质中,催化剂活性较低的原因可能是该酸度条件不利于甲基橙在复合催化剂表面吸附。
2.3 复合光催化剂对不同有机染料的光催化降解
选用负载量45%的Cs2.5H0.5PMo12O40/TiO2(Cs2.5H0.5PMo12O40,m=0.376 0 g)复合光催化剂催化降解甲基橙溶液时的最佳条件为催化剂用量0.050 0 g,pH=4~5.研究了Cs2.5H0.5PMo12O40/TiO2复合光催化剂对甲基橙、酸性品红、次甲基蓝、罗丹明B的降解催化活性,如图3所示,结果表明:Cs2.5H0.5PMo12O40/TiO2复合光催化剂不仅能够很好地降解甲基橙溶液,还能够很好地降解罗丹明B、次甲基蓝溶液,2 h的降解率分别达到76%,85%;但是在相同条件下对酸性品红的降解活性不好,2 h降解率只有25%左右,这可能与染料的结构有关。4种染料的结构式如图4所示。
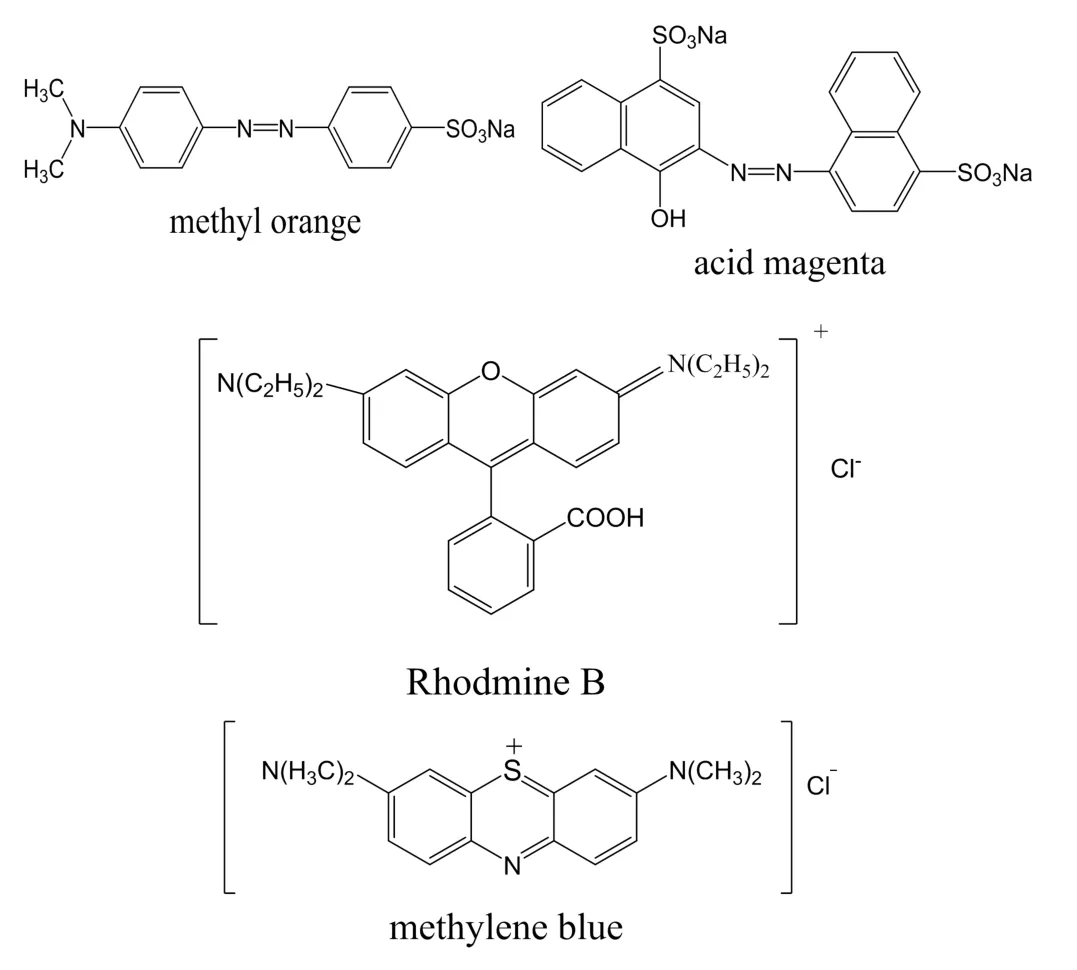
图4 4种染料的结构式
分析染料的分子结构可知,虽然都是偶氮类结构,但是Cs2.5H0.5PMo12O40/TiO2复合光催化剂对甲基橙溶液、罗丹明B溶液、次甲基蓝溶液都具有较好的光催化降解活性,可能是因为偶氮类结构更易于与多酸形成配合物,并且因分子结构中良好的电子共轭性,使得电子的转移更易于进行。而酸性品红染料分子中N原子周围较大基团的结构中大的空间位阻可能是阻碍多酸与有机物形成复合物,从而降低多酸催化活性的主要原因,因而降低了光催化反应的效率。
3 结论
本文采用溶胶-凝胶法及水热合成技术制备了Cs2.5H0.5PMo12O40/TiO2复合光催化剂,以甲基橙为模板,考察催化剂的光催化效果,实验结果表明:该复合光催化剂在450 W高压汞照射下有较好的光催化活性,复合光催化剂的用量、酸度、甲基橙浓度等是影响催化降解效果的重要因素。最适宜的催化降解条件为:50 mL 10 mg/L的甲基橙溶液中加入Cs2.5H0.5PMo12O40/TiO2复合光催化剂0.050 0 g,溶液的体系酸度pH=4~5,450 W高压汞灯照射下,在2 h内甲基橙的光催化降解转化率可达到80%以上。溶液为弱酸性时,降解效率较好。在相同条件下,该复合光催化剂对酸性品红的降解催化活性的降解效果不理想,可能与染料的分子结构及空间结构位阻较大有关,具体的机理还有待于进一步研究。Cs2.5H0.5PMo12O40/TiO2复合光催化剂对甲基橙、罗丹明B、次甲基蓝的降解的研究预示了较为乐观的应用前景。
[1]孙伟,刘保顺,赵修建,等.TiO2光催化中价电子的转移过程及其作用[J].材料导报,2004,18(7):83-86.
[2]岳斌,许静玉,金松林,等.多酸的光化学和光催化(上)[J].上海化工,2001(13):24-26.
[3]岳斌,许静玉,金松林,等.多酸的光化学和光催化(下)[J].上海化工,2001(14):15-17.
〔编辑:刘晓芳〕
O614.4
:A
10.15913/j.cnki.kjycx.2017.15.017
2095-6835(2017)15-0017-03
