高振实密度圆饼状LiFePO4/C的制备及电化学性能
2017-08-07吴仪娜徐国庆涛刘文明唐新村
吴仪娜 周 乐 徐国庆 黄 洁 方 雄 王 涛刘文明 晋 媛 汪 洋 唐新村
高振实密度圆饼状LiFePO4/C的制备及电化学性能
吴仪娜 周 乐 徐国庆 黄 洁 方 雄 王 涛刘文明 晋 媛 汪 洋 唐新村*
(中南大学化学化工学院,长沙 410083)
以乙二醇为溶剂,采用溶剂热法一步合成圆饼状LiFePO4,然后以葡萄糖为碳源与合成的LiFePO4前躯体高温烧结得到碳包覆的LiFePO4/C复合材料,其振实密度高达1.3 g·cm-3。采用X射线衍射(XRD)、扫描电子显微镜(SEM)和透射电子显微镜(TEM)对LiFePO4/C复合材料进行了物相和形貌表征,研究结果表明制备得到的LiFePO4呈圆饼状,且生成的圆饼是由单晶LiFePO4纳米片堆积而成。此外,LiFePO4颗粒表面碳层包覆均匀。将制备的LiFePO4/C用作锂离子电池正极材料,电化学性能测试表明其具有高的充放电比容量(在0.1C时放电,其初始放电比容量为157.7 mAh·g-1)与良好的循环性能(500次循环后容量保持率为82.4%)。
磷酸铁锂;溶剂热法;圆饼状;电化学性能
0 引 言
近年来,锂离子电池以其高能量密度和优异循环性能等特点受到了研究者的广泛关注,其现已在便携式电子产品、通讯工具、电动汽车(EV)和混合电动汽车(HEV)等行业中得到大量应用[1-2]。橄榄石型LiFePO4作为锂离子电池正极材料具有价格低廉、理论比容量高(170 mAh·g-1)、循环稳定性好和绿色环保等优点[3-5],被认为是最实用的锂离子电池正极材料之一,也是目前商业化最成功的锂离子电池正极材料。然而LiFePO4在实际应用中仍然面临一些问题,首先其较低的电子电导率(10-7~10-10S·cm-1)和锂离子扩散系数(10-12~10-16cm2·s-1)使得未经改性的LiFePO4材料的充放电比容量低且倍率性能差。其次,相比于其它锂离子电池正极材料[6](LiCoO2、LiMn2O4等),其相对低的振实密度也限制了LiFePO4电池的体积比容量,从而难于满足迅猛发展的电动汽车等大功率移动储能设备对高能量密度电池的需求[7-8]。因此开发储锂性能优良的高能量密度的LiFePO4正极材料变得尤为迫切。
目前改善LiFePO4在锂离子电池中的电化学性能的方法主要有纳米化[7-9]、表面包覆[10]和金属离子掺杂[11-12]等方法。Wang等[13]通过高温固相法合成了20~40 nm的LiFePO4纳米颗粒,在0.6C(1C=170 mAh·g-1)倍率下的放电容量达到了168 mAh·g-1。此外,Li[14]通过溶剂热法合成出了超薄纳米片,其在20C倍率下的放电容量为122 mAh·g-1。然而,比表面积较大的低维纳米材料(纳米粒子、纳米线和纳米片等)在充放电循环过程中容易引发活性物质团聚,阻挡电子的离子传输路径,从而造成电池的循环性能降低。此外简单的低维纳米LiFePO4材料的振实密度通常小于1 g·cm-3,不利于提高LiFePO4正极材料的体积比容量。研究表明,三维分级结构的纳米材料具有优异的物理和化学性能[15-18]。由低维的纳米粒子或者纳米片组装而成的三维分级结构的LiFePO4,不仅保留了LiFePO4充放电平台长、充放电容量高等特点,而且提高了材料的电化学稳定性和振实密度,因此三维分级结构的LiFePO4材料通常具有高的充放电比容量和良好的循环稳定性。Sun等[19]采用溶剂热法制备出了由80 nm厚的纳米片组装成的大小为1~3μm的多孔花状LiFePO4,振实密度达到1.1 g·cm-3,其在0.1C倍率下的放电容量为140 mAh·g-1。我们课题组前期通过溶剂热法制备出了纳-微球形LiFePO4[20],振实密度达到1.4 g·cm-3,其在 0.1 C倍率下的放电容量为 132.5 mAh·g-1。然而,由纳米片或纳米粒子过于紧密堆积而成的材料虽然具有较高的振实密度,但电解液很难渗透进入材料体相内部,导致电子和锂离子扩散距离过长,从而在充放电过程中难于达到LiFePO4的理论比容量。因此,合成一种兼顾高比容量以及高振实密度的LiFePO4材料显得尤为重要。
本文中,我们通过溶剂热法制备了圆饼状三维分级结构LiFePO4,该分级结构LiFePO4由单晶纳米片自组装而成,纳米片之间适度的堆积,既保证了材料的振实密度(振实密度达到1.3 g·cm-3),有利于提高材料的电解液充分渗透到颗粒内部,缩短了电子和锂离子的扩散距离,使得材料具有优异的储锂性能。同时我们也探讨了圆饼状分级结构LiFePO4的生长机理。
1 实验部分
1.1 材料的制备
将20 mmol CH3COOLi·2H2O(天津市风船化学试剂科技有限公司)和10 mmol NH4H2PO4(西陇化工股份有限公司)溶于35 mL乙二醇中,然后将10 mmol FeSO4·7H2O(国药集团化学试剂有限公司)加入到乙二醇溶液中磁力搅拌5 h后,转入到100 mL聚四氟乙烯反应釜中,密闭后置入恒温磁力搅拌器中,于180℃下反应8 h。自然冷却后,分别用去离子水和无水乙醇离心洗涤3次。80℃下真空干燥12 h,得LiFePO4前驱体样品。将LiFePO4前驱体与适量葡萄糖混合均匀后,转至氢氩混合气(5%H2+ 95%Ar)气氛管式炉中,在700℃温度下煅烧6 h,冷却得到LiFePO4/C样品。
1.2 材料的表征
采用日本理学 Rigaku公司生产的 D/Max 2500VB+X线衍射分析仪(Cu Kα,λ=0.154 056 nm,管电压40 kV,管电流250 mA,扫描范围为2θ=10°~85°)对产物进行物相分析;采用美国FEI公司生产的QUANTA 200环境扫描电子显微镜观察粒子的粒径和形貌;采用日本电子公司生产的JEM-2100F场发射高分辨透射电子显微镜观察样品的微观结构和晶型。
1.3 电化学性能测试
将制备的LiFePO4/C、乙炔黑、PVDF按质量比80∶10∶10混合,充分研磨混合均匀后加入一定量的NMP溶剂,搅拌均匀后在铝箔上涂膜,制成正极片,80℃下真空干燥24 h。以金属锂片为负极,1 mol· L-1LiPF6/EC+DMC(质量比为1∶1)为电解液,在手套箱中组装成双电极电池。采用NEWARE电池测试检测系统测试电池在2.5~4.2 V范围内的充放电性能。采用上海辰华电化学工作站(CHI660e)测试电池的循环伏安曲线(扫速为0.4 mV·s-1,电压范围为2.5~4.2 V)和交流阻抗(频率范围为0.01 Hz~0.1 MHz)。
2 结果与讨论
2.1 XRD分析
图1为溶剂热法合成的LiFePO4前驱体和高温碳包覆后的LiFePO4/C样品的XRD图。由图可知LiFePO4样品在煅烧前后X射线衍射峰位置和峰强度并无明显变化,且LiFePO4/C样品中没有出现碳对应相关的衍射峰。2个样品衍射峰位置均与正交晶系橄榄石型结构的LiFePO4标准卡片(JCPDS No. 40-1499)的衍射峰位置对应完好,没有发现其它杂峰,其主要衍射峰为(011)、(111)、(121)、(131)。峰强且半峰宽窄,说明我们制得的LiFePO4具有很好的结晶度。由XRD图计算出LiFePO4/C样品中LiFePO4的晶胞参数分别为a=0.601 9 nm,b=1.034 7 nm,c= 0.470 4 nm。根据谢乐公式,估算得出煅烧后的LiFePO4/C样品的平均晶粒度为66 nm。

图1 LiFePO4前驱体和LiFePO4/C样品的XRD图Fig.1 XRD patterns of the LiFePO4 precursor and LiFePO4/C
2.2 SEM和TEM表征
LiFePO4正极材料的形貌对其振实密度和电化学性能有着非常重要的影响,图2(a)和(b)为制得的LiFePO4/C样品的扫描电镜图,由图可知我们制备的LiFePO4呈圆饼状且圆饼尺寸均一,其直径为2~3μm,厚度为500~700 nm。此外我们看到圆饼状的LiFePO4表面较为光滑且堆积紧密,有利于提高材料的振实密度,经测的样品的振实密度高达1.3 g· cm-3。图2(c)和(d)是制备的LiFePO4/C的高分辨透射电镜图。如图2(d)所示,我们可以看到LiFePO4晶体晶格条纹排列明显且非常完整,说明我们制备的样品中LiFePO4结晶度高,与XRD结果相符合。由其放大图可知,晶格条纹间距为0.35 nm,与LiFePO4的(111)晶面的晶面间距相一致。图2(d)里插图对应着其傅里叶转换图,光斑排列规整,表明样品为单晶 LiFePO4纳米片。同时我们在图 2(c)中看到LiFePO4晶体表面有明显的碳层,碳层没有明显的晶格条纹,说明包覆碳层为无定形碳,碳层厚度约为2.5 nm左右。

图2 (a)、(b)为LiFePO4/C样品的扫描电镜图;(c)、(d)为LiFePO4/C样品的高分辨透射电镜图Fig.2 SEM images of LiFePO4/C(a,b); HRTEM images of LiFePO4/C(c,d)
2.3 Raman分析
为进一步表征包覆碳层的石墨化程度,如图3所示,我们通过LiFePO4/C的拉曼散射光谱发现其在1 340和1 579 cm-1处有2个宽峰,分别对应的是无定形C(D band)和石墨化C(G band)。计算ID/IG= 1.06,说明其石墨化程度较低,与TEM结果一致。

图3 LiFePO4/C样品的Raman谱图Fig.3 Raman spectra of the LiFePO4/C
2.4 圆饼状分级结构LiFePO4生长机理分析

图4 不同溶剂热时间下LiFePO4的SEM图Fig.4 SEM images of LiFePO4 after differentreaction time
为了研究LiFePO4晶体的生长过程,我们通过调控溶剂热反应时间,获得了不同反应时间下产物的SEM图,探究了圆饼状分级结构LiFePO4的结构变化及形貌演变过程。图4显示了不同反应时间制得的产物的SEM图,在反应1 h的最初阶段,产物是由细小的纳米颗粒组成。当反应进行到2 h时,纳米颗粒消失,产物中出现大量的纳米薄片。当反应进行到4 h时,纳米片组装成直径为1~2μm,300~500 nm厚的圆饼。继续延长反应时间至8 h时,明显观察到相比4 h的产物,形貌并未发生太大变化,但尺寸增大,圆饼直径为2~3μm,厚度为500~700 nm。相比于低维结构的的LiFePO4纳米材料,这种三维分级圆饼状的材料有更高的振实密度,有利于提高材料在锂离子电池中得到体积比容量。同时这种结构也有利于电解液渗透到圆饼状结构的内部,缩短锂离子在材料内部的扩散距离,提高材料的电化学性能。
通过一系列时间条件对比试验,我们提出了圆饼状LiFePO4的生长机理。首先,分散在乙二醇的Li+、Fe2+、PO43-随着反应釜内温度压强的升高发生反应生成LiFePO4纳米粒子(Step 1)。随着反应时间的延长,在乙二醇[21]的作用下,LiFePO4纳米粒子逐渐聚合生成LiFePO4纳米片 (Step 2)。由于这些薄的LiFePO4纳米片有着巨大的比表面能,使其在之后的反应过程中发生堆积生成层层堆积状的圆饼状LiFePO4(Step 3)。
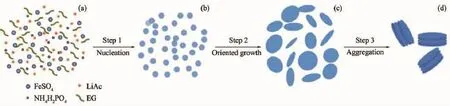
图5 圆饼状分级结构LiFePO4生长机理示意图Fig.5 Schematic illustration of the growth mechanism of cake-like LiFePO4 hierarchical structures
2.5 电化学性能分析
将制得的LiFePO4/C样品组装成扣式锂离子电池,并对其进行电化学性能研究。图6为LiFePO4/C样品的循环伏安图,扫描范围为2.5~4.2 V,扫速为0.4 mV·s-1。从图中可以看出,LiFePO4/C电极在第二次和第三次的循环曲线重合度高,说明电极具有优良的循环稳定性。
图7(a)为LiFePO4/C样品在0.1 C倍率下的充放电曲线,其充放电比容量分别为 160.2、157.7 mAh·g-1,首次充放电库伦效率为98%。图7(b)为LiFePO4/C样品在不同倍率下的充放电曲线。在0.2C、0.5C、1C和2C下放电时,LiFePO4/C样品的放电比容量分别为141.8、131.1、116.5和99.2 mAh· g-1,保持了0.1C倍率时容量的90%、83.1%、73.9%和62.9%。与文献[22-23]报道合成的LiFePO4相比,我们合成的圆饼状分级结构材料LiFePO4充放电性能有很大的提高。图7(c)为LiFePO4/C样品的倍率性能图,LiFePO4样品在0.1C升至5C倍率下充放电,放电容量都很平稳,并没有明显的衰减。经过倍率测试之后,在0.1C倍率下对LiFePO4/C材料进行恢复,容量仍能保持在154.6 mAh·g-1,容量保持率为98%。图7(d)为LiFePO4/C样品的循环性能图,在1C倍率下充放电,经过500次循环后,LiFePO4/C样品的放电比容量保持在97.28 mAh·g-1,容量保持率为82.4%。说明材料具有优异的稳定性和循环性能。
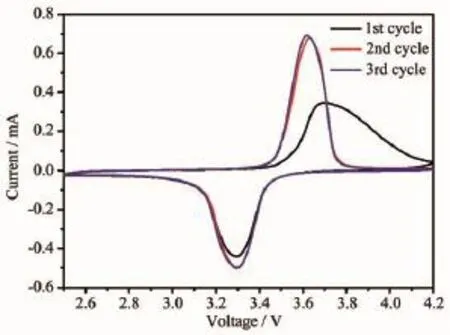
图6 LiFePO4/C样品的循环伏安图Fig.6 Cyclic voltammogram(CV)of LiFePO4/C

图7 (a)LiFePO4/C样品在0.1C倍率下的充放电曲线;(b)LiFePO4/C样品在不同倍率下的充放电曲线; (c)倍率性能;(d)循环性能(在1C倍率下)Fig.7 (a)Charge-discharge curves of LiFePO4/C cathode at 0.1C;(b)Charge-discharge curves at various current rates, (c)rate capability and(d)cycling performance of LiFePO4/C at 1C

图8 (a)LiFePO4/C样品的交流阻抗图;(b)Z′~ω-1/2的直线拟合Fig.8 (a)Electrochemicalimpedance spectra measurements(EIS)of LiFePO4/C;(b)linear fitting of Z′~ω-1/2
图8(a)为LiFePO4/C样品的交流阻抗图,高频区出现的半圆对应的是电荷转移电阻,低频区出现的直线对应的是锂离子扩散系数。我们合成的圆饼状分级结构LiFePO4/C的电荷转移电阻Rct为120 Ω,比文献[24-25]报道合成的LiFePO4小。根据公式D=R2T2/(2A2n4F4C2σ2)计算锂离子扩散系数,其中R为气体常数,T为开尔文温度,A为电极面积,n为反应过程中转移的电子数,F为法拉第常数96 500,σ是直线拟合Z′~ω-1/2的斜率(40.53),如图8(b),C为锂离子体相浓度(2.28×10-2mol·cm-3),代入计算得出锂离子扩散系数为3.25×10-14cm2·s-1。
3 结 论
本文以乙二醇为溶剂采用剂热法一步合成了三维圆饼状分级结构LiFePO4,其是由二维的单晶纳米片叠加堆积而成的直径约为2μm圆饼形貌。通过溶剂热反应时间对比实验分析了圆饼形状分级结构LiFePO4生长机制,在乙二醇的作用下其产物相貌演化过程为纳米颗粒纳米片圆饼状分级结构。圆饼状分级结构LiFePO4/C在0.1C倍率放电时,放电比容量为157.7 mAh·g-1,在1C倍率下循环500次后的容量保持率为82.4%。本文制备的圆饼状三维分级结构LiFePO4,纳米片之间适度的堆积,既保证了材料具有较高的振实密度 (1.3 g·cm-3),又缩短了电子和锂离子的扩散距离,使得材料具有优异的电化学性能。
[1]Scrosati B,Garche J.J.Power Sources,2010,195(9):2419-2430
[2]Xu G,He H,Wan H,et al.J.Appl.Electrochem.,2016,46 (8):879-885
[3]Gibot P,Casas-Cabanas M,Laffont L,et al.Nat.Mater., 2008,7(9):741-747
[4]Amol N,Sajan C P.Dalton Trans.,2016,45(19):8021-8027
[5]HANG Fu-Qin(黄富勤),TANG Xin-Cun(唐新村),XIAO Yuan-Hua(肖元化),et al.Chinese J.Inorg.Chem.(无机化学学报),2014,30(2):235-241
[6]Parakandy M P,Erabhoina H M,Bulusu V S,et al.Phys. Chem.Chem.Phys.,2017,19:175-188
[7]Li L,Tang X,Liu H,et al.Electrochim.Acta,2010,56(2): 995-999
[8]Churikov A V,Ivanishchev A V,Ivanishcheva I A,et al. Electrochim.Acta,2010,55(8):2939-2950
[9]Liu Y,Gu J,Zhang J,et al.Electrochim.Acta,2015,173: 448-457
[10]Zhao J,He J,Zhou J,et al.J.Phys.Chem.C,2011,115(6): 2888-2894
[11]Kang B,Ceder G.Nature,2009,458(7235):190-193
[12]Chung S Y,Chiang Y M.Electrochem.Solid-State Lett.,2003, 6(12):A278-A281
[13]Oh S W,Bang H J,Myung S T,et al.J.Electrochem.Soc., 2008,155(6):A414-A420
[14]Li Z,Peng Z,Zhang H,etal.Nano Lett.,2016,16(1):795-799 [15]Ding Y S,Shen X F,Gomez S,et al.Adv.Funct.Mater., 2006,16(4):549-555
[16]He Z,Chen Z,Li Y,et al.CrystEngComm,2011,13(7):2557 -2565
[17]Lu F,Cai W,Zhang Y.Adv.Funct.Mater.,2008,18(7):1047-1056
[18]ZHENG Zhen-Miao(郑贞苗),TANG Xin-Cun(唐新村), WANG Yang(汪洋),et al.Chinese J.Inorg.Chem.(无机化学学报),2014,30(2):235-241
[19]Sun C,Rajasekhara S,Goodenough J B,et al.J.Am.Chem. Soc.,2011,133(7):2132-2135
[20]Jin Y,Tang X C,Wang H Y.RSC Adv.,2016,6:75602-75608
[21]Kang W,Zhao C,Liu R,et al.CrystEngComm,2012,14(6): 2245-2250
[22]Zhou N,Uchaker E,Wang H Y,et al.RSC Adv.,2013,3 (42):19366-19374
[23]Di Lupo F,Meligrana G,Gerbaldi C,et al.Electrochim. Acta,2015,156:188-198
[24]Fathollahi F,Javanbakht M,Omidvar H,et al.J.Alloys Compd.,2015,627:146-152
[25]Huang Y,Zheng F,Zhang X,et al.Solid State Ionics,2013, 29:158-164
Synthesis and Electrochemical Properties of Cake-like LiFePO4/C with High Tap Density
WU Yi-Na ZHOU Le XU Guo-Qing HUANG Jie FANG Xiong WANG Tao LIU Wen-Ming JIN Yuan WANG Yang TANG Xin-Cun*
(School of Chemistry and Chemical Engineering,Central South University,Changsha 410083,China)
The cake-like LiFePO4is synthesized through a solvothermal method with ethylene glycol as the solvent.After that,the LiFePO4precursor and glucose are mixed and calcined in an reduced atmosphere to obtain the LiFePO4/C composite with a high tap density of 1.3 g·cm-3.The LiFePO4/C samples were characterized by X-ray diffraction,scanning and transmission electron microscopies,whose results demonstrate that the cakelike LiFePO4/C consists of single-crystalline LiFePO4nanoplates.Additionally,an amorphous carbon layer is evenly coated on LiFePO4.The electrochemical properties of the cathode material LiFePO4/C indicate that it possess a high charge/discharge specific capacity (the initial discharge capacity reach to 157.7 mAh·g-1 at 0.1C) and good cycle stability(82.4%ofcapacity retention at 1C after 500 cycles).
LiFePO4;solvothermal method;cake-like;electrochemical performance
TB333
A
1001-4861(2017)08-1423-06
10.11862/CJIC.2017.163
2017-03-06。收修改稿日期:2017-04-19。
国家自然科学基金(No.21476268,21276286)、新疆镍钴资源与CoxNiyMn1-x-yO2三元(No.738010043)资助项目。
*通信联系人。E-mail:tangxincun@163.com
