利奈唑胺致乳酸酸中毒及全血细胞减少1例报道及50例文献复习
2017-08-07张岩岩张静萍陈佰义
张岩岩, 朱 婉, 张静萍, 陈佰义
利奈唑胺致乳酸酸中毒及全血细胞减少1例报道及50例文献复习
张岩岩, 朱 婉, 张静萍, 陈佰义
目的 了解利奈唑胺在临床应用过程中不良反应发生情况,尤其是导致乳酸酸中毒或全血细胞减少的发病特点。方法 报告1例长疗程应用利奈唑胺致乳酸酸中毒及全血细胞减少的病例,并对2000-2015年国内外报道的相关文献进行复习,对患者的年龄、性别、基础疾病、不良反应出现时间、预后等情况进行总结分析。结果 50例统计分析结果:患者男女比例为1.78∶1,65岁以上患者占42.0 %,肝、肾功能不全者20例(占40.0 %),乳酸酸中毒平均出现于用药后5.5周,全血细胞减少平均出现于用药后3.5周。结论 利奈唑胺致乳酸酸中毒或全血细胞减少更多出现于肝功能受损、长疗程用药和高龄的患者。
利奈唑胺; 乳酸酸中毒; 全血细胞减少; 不良反应
1 病例报告
患者男性,37岁。既往体健,入院前6个月于劳作时右手受外力创伤,手背侧局部皮肤破损,伴红肿,因活动不受限,未处理,至入院前3个月患者逐渐出现左手背侧多处皮肤破溃伴周围红肿,右手背侧皮肤反复破溃未愈合,不影响日常活动,仍未就诊。入院前1周,患者因双手皮肤破溃加重,并出现双手及双上肢弥漫性肿胀,就诊于当地医院,行局部清创,应用头孢菌素类药物(具体不详)静脉滴注1周,治疗过程中出现高热,体温最高可达40 ℃,抽取血培养结果提示金黄色葡萄球菌感染(未做药敏),于2013年3月20日转至我院。入院时临床检查:体温38.1 ℃,脉搏116次 / min,呼吸16次 / min,血压140 / 70 mmHg。双手背多处破溃,表面流脓,双上肢弥漫性肿胀,表面发红,皮温升高,皮肤触痛阳性,心、肺、腹检查未见异常。化验血常规提示白细胞18.80×109/ L,粒细胞比率0.961,红细胞3.36×1012/ L,血红蛋白112 g / L,血小板216×109/ L;炎性反应指标C反应蛋白(CRP)180.00 mg / L,降钙素原(PCT)0.30 ng / L。上肢局部彩超提示病变处肌间液性病变伴气体样回声,皮下软组织不规则低密度影。入院诊断考虑为社区获得性cSSTI,坏死性筋膜炎,金黄色葡萄球菌血流感染。经验性给予万古霉素1.0 g静脉滴注每12小时1次,治疗1周患者仍反复寒战、高热,局部症状无好转,复查血常规示白细胞12.80×109/ L,红细胞2.96×1012/ L,血红蛋白94 g / L,血小板260×109/ L;CRP 137 mg / L,PCT 0.27 ng / L;血清乳酸1.30 mmol / L(正常参考值0.50~1.78 mmol / L),再次抽取血培养及局部脓液培养,结果均提示金黄色葡萄球菌,甲氧西林耐药。考虑万古霉素在局部组织中的渗透性不足,以及患者可能存在混合感染(如革兰阴性杆菌、厌氧菌等),将治疗方案调整为利奈唑胺0.6 g静脉滴注每12小时1次,同时合用美罗培南1.0 g每8小时1次静脉滴注,监测血常规、血乳酸等指标。利奈唑胺应用2周患者体温逐渐下降,双上肢肿痛略有缓解,应用5周体温基本降至正常,上肢肿痛症状明显缓解,复查血常规提示白细胞4.16×109/ L,红细胞2.80×1012/ L,血红蛋白74 g / L,血小板213×109/ L;血清乳酸1.70 mmol / L,考虑患者可能出现药物相关骨髓抑制,将利奈唑胺改为糖肽类抗生素静脉滴注,患者在应用万古霉素、替考拉宁后均出现寒战、高热、皮肤潮红伴瘙痒等症状,复查血常规白细胞3.43×109/ L,红细胞2.76×1012/ L,血红蛋白93 g / L,血小板181×109/ L;CRP 9.03 mg / L,PCT 0.05 ng / L;过敏原总IgE 1 560 ng / mL;血清乳酸1.75 mmol / L,考虑患者可能对糖肽类药物过敏,再次更换为利奈唑胺静脉滴注。利奈唑胺累计应用8周时,患者体温已恢复正常水平,双手皮肤破溃处愈合良好,双上肢肿胀消退,但逐渐出现乏力、恶心症状,复查血常规白细胞2.67×109/ L,红细胞1.90×1012/ L、血红蛋白59 g / L,血小板35×109/ L,血清乳酸水平升高至2.60 mmol / L,考虑患者出现药物相关乳酸酸中毒及全血细胞减少,立即停用利奈唑胺,更换为达托霉素0.5 g每天1次静脉滴注。停用利奈唑胺1周后,患者乏力、恶心等症状好转,复查血清乳酸及血常规均恢复至用药前水平,随访至停用利奈唑胺后6周,血清乳酸及血常规维持正常水平。
2 文献复习
为进一步了解利奈唑胺在临床应用过程中导致乳酸酸中毒或全血细胞减少的发病特点,我们对2000-2015年国内外报道的相关病例进行复习。
2.1 纳入标准
原始的临床病例报告;应用利奈唑胺后出现乳酸酸中毒或全血细胞减少。
2.2 排除标准
重复报道的病例;联合用药方案中包含可能导致乳酸升高或血细胞减少的其他药物;存在饮酒、肥胖、怀孕、剧烈运动等可能导致乳酸升高或血细胞减少的因素。
2.3 指标定义
乳酸酸中毒:“确切的”乳酸酸中毒定义为血清乳酸≥5 mmol / L,并动脉血pH<7.25。“可能的”乳酸酸中毒定义为血清乳酸值升高,但血pH值不确定;或明确有代谢性酸中毒,但血清乳酸值不确定。根据Naranjo的药物不良反应标准,药物性乳酸酸中毒的定义应与“可能的”级别一致[5]。
全血细胞减少:药物所致的血细胞(包括白细胞、红细胞、血红蛋白、血小板)减少的定义为:基线正常者,用药后血细胞<正常值下限的75 %,其中中性粒细胞为<50 %;基线异常者,为用药后血细胞计数<75 %基线值,中性粒细胞<基线值50 %[5]。
2.4 结果
共38篇文献50例病例[1-4、6-39]被纳入统计,包括乳酸酸中毒36例(国内2例),全血细胞减少16例(国内4例),其中2例乳酸酸中毒合并全血细胞减少。
2.4.1 人口学情况 50例病例中,男32例,女18例,男女比例为1.78∶1。年龄6个月~88岁,平均年龄52.7岁,其中65岁以上患者21例,占42.0 %。见表1。

表1 人口学情况Table 1 Demographic data
2.4.2 患者的基础疾病情况 50例患者中8例既往无基础疾病,11例合并肾脏疾病,9例合并肝脏疾病。见表2。
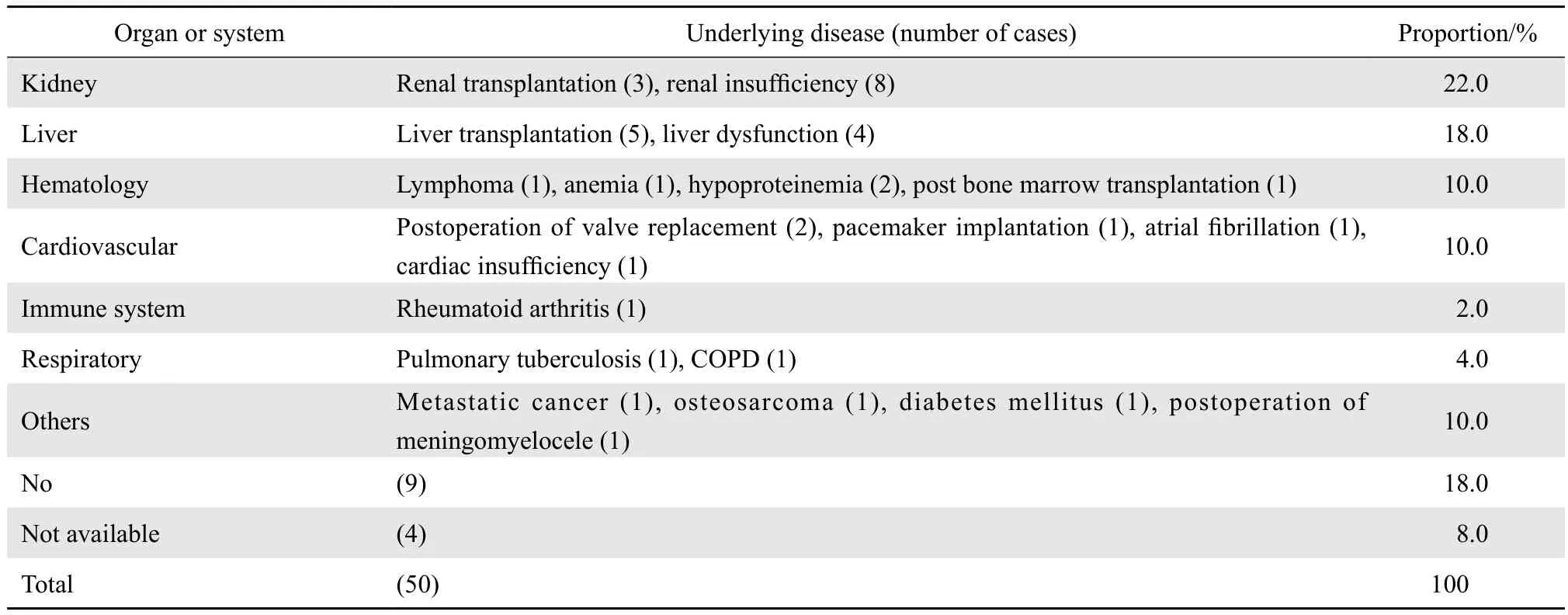
表2 基础疾病情况Table 2 Prof i le of underlying diseases
2.4.3 不良反应出现时间 乳酸酸中毒患者血清乳酸峰值范围2.8~38.0 mmol / L,中位数10.8 mmol / L,最早出现于用药后4 h,最晚出现于用药后16周,平均5.5周,有1例出现于停药后2 d。全血细胞减少患者白细胞最低值范围(1.6~5.9)×109/ L、中位数2.6×109/ L,血红蛋白42~102 g / L、中位数73.5 g / L,血小板(13~93)×109/ L、中位数47.5×109/ L,最早出现于用药后4 d,最晚出现于用药后8周,平均3.5周。见表3。
2.4.4 临床表现 乳酸酸中毒患者多以消化道症状为主,全血细胞减少患者多无明显临床症状。见表4。
2.4.5 转归 50例病例中,34例患者好转, 8例患者死亡,另有8例患者未提及预后情况。34例好转患者中5例未报道好转时间,1例经药物减量后好转,余28例患者指标好转出现于停药后
1~28 d,平均10.2 d,其中24例于14 d内好转。8例死亡患者出现的不良反应均为乳酸酸中毒,其中4例因原发病病情较重且未及时停药,
乳酸酸中毒未得到纠正,最终抢救无效,2例死亡原因为原发病白血病,1例为转移性癌。

表3 不良反应出现时间Table 3 Onset time of adverse reaction
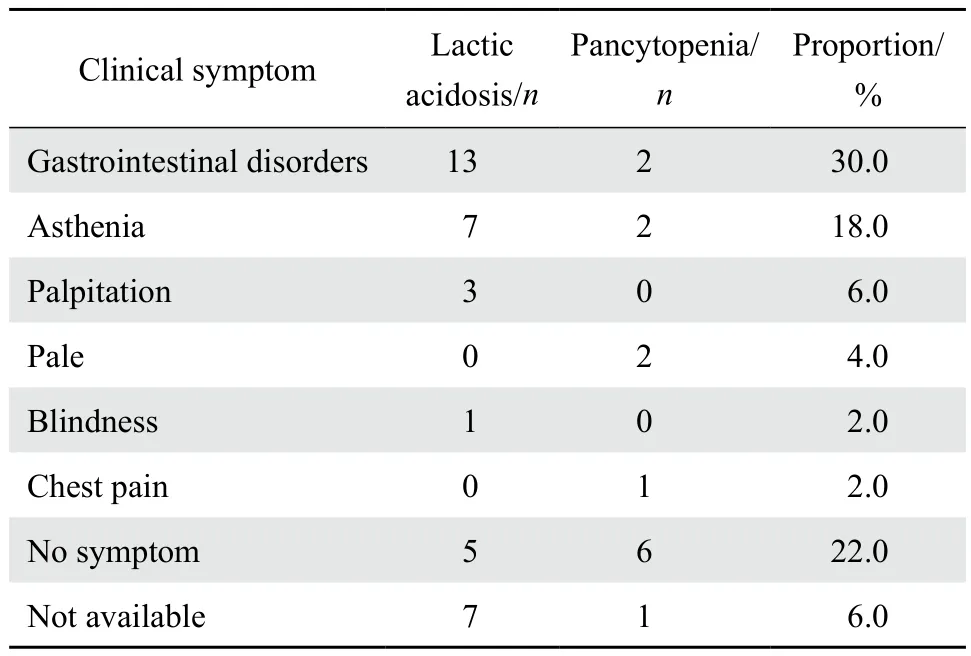
表4 利奈唑胺所致不良反应的临床表现Table 4 Clinical manifestations of the linezolid-induced adverse reactions
3 讨论
乳酸酸中毒是利奈唑胺相关的严重不良反应,可导致多器官衰竭,甚至死亡;利奈唑胺致血液系统不良反应中血小板减少和白细胞减少均已有不少报道,但全血细胞减少仍较为少见。我院这例患者为皮肤软组织感染,创面深达筋膜,入院后参照2011年美国感染性疾病学会(IDSA)专家组发布的MRSA感染的循证治疗指南,诊断为社区获得性cSSTI,坏死性筋膜炎,金黄色葡萄球菌血流感染。对于cSSTI住院患者,该指南指出应给予手术清创、使用广谱抗生素,并在培养结果得出前进行抗MRSA经验性治疗。本例患者在治疗过程中表现出对糖肽类药物过敏,在利奈唑胺累计应用8周时出现乳酸酸中毒及全血细胞减少,经及时停药与支持治疗,患者血象及血乳酸水平均恢复。
通过对国内外文献的统计分析,应用利奈唑胺后发生不良反应的患者男性多于女性,这与国内许多文献相似[40-44],但目前国内外暂无统计学数据说明不良反应的发生情况是否与性别有关。利奈唑胺的Ⅲ期临床研究中,共2 046例患者接受了利奈唑胺治疗,未见高龄患者安全性和有效性与年轻患者有统计学差异[45],而本文统计的50例患者中高龄患者所占比例较高,田瑛等[46]的研究提出老年患者用药后全血细胞减少的发生率及严重程度都明显高于其他人群,可能由于老年患者免疫功能相对较低、合并基础疾病多、各种脏器功能减退、药物代谢减缓等多方面因素共同作用,从而导致不良反应更多见于高龄患者。但目前尚无研究报道明确提出高龄是利奈唑胺发生不良反应的独立危险因素。
所有病例中以肝肾功能不全患者发生不良反应居多,利奈唑胺在体内代谢后经肝(约65 %)、肾(约35 %)双通道排泄[47],Stalker等[48]在不同人群中研究发现轻至重度肾功能损害患者利奈唑胺的主要药动学参数与健康志愿者相似,说明肾脏在利奈唑胺的代谢中可能并不发挥主要的作用。乳酸的清除也主要在肝脏(约60 %)、肾脏(约30 %)中进行,其余少量在骨骼肌、心肌被清除,当肝、肾功能受损时,可通过影响血乳酸清除率,进一步加重乳酸酸中毒的发展程度,因此严重肾功能不全会影响乳酸酸中毒的严重程度及死亡率。有研究表明,肝脏移植术后患者利奈唑胺血药浓度是肝功能正常患者的4~6倍[49],由此推测肝功能受损可影响药物排泄进而发生不良反应的风险也随之增加。
经统计后可见长疗程用药后出现不良反应所占比例更高,美国食品和药品监督管理局(FDA)批准利奈唑胺的疗程为1~2周,最长不超过4周,然而一些患者因人工关节感染、骨髓炎等复杂感染,用药常常超过推荐疗程,本院这例患者因对糖肽类药物过敏,可供选择的抗菌药物有限,利奈唑胺累积应用达8周。Im等[50]提出超过6周的长疗程用药是利奈唑胺相关乳酸酸中毒的危险因素,Birmingham等[51]研究表明,随着用药时间的延长,血液系统不良反应的发生率也逐渐升高。但由表3可以看出利奈唑胺在规定疗程内也可出现不良反应,用药数小时出现的早发乳酸酸中毒也已被报道[6]。Pea等[7]提出早发高乳酸血症可能与利奈唑胺药物浓度过高有关,晚发高乳酸血症与利奈唑胺的治疗时间有关。因此,我们推测长疗程应用利奈唑胺与不良反应发生有关,但并不是独立的危险因素。
利奈唑胺引起乳酸酸中毒的机制目前多认为可能与线粒体蛋白质合成抑制和线粒体基因多态性有关,临床表现多以消化道症状为主,大多数患者经及时停药和对症支持治疗后可好转,而长时间应用利奈唑胺可能会导致更大的线粒体损伤,如未能及时发现并停药,会导致严重后果。全血细胞减少的机制一般认为是骨髓抑制,近年来也有学者认为是免疫介导学说,多为可逆性[8],患者大多无明显临床症状。
综上,临床医师在应用利奈唑胺过程中应高度关注乳酸酸中毒、全血细胞减少等罕见的、严重的不良反应,尤其是合并肝功能受损、长疗程用药以及高龄的患者,建议在使用利奈唑胺早期或患者出现消化道症状即开始监测血乳酸及血常规,一旦发现血乳酸超过正常范围或血细胞减少,应立即停药并及时调整治疗方案,避免因治疗给患者带来不必要的损害,更加安全、合理的应用利奈唑胺,使患者在最大程度上获益。
[1] APODACA AA, RAKITA RM. Linezolid-induced lactic acidosis [J]. N Engl J Med, 2003, 348(1): 86-87.
[2] PALENZUELA L, HAHN NM, NELSON JR RP, et al. Does linezolid cause lactic acidosis by inhibiting mitochondrial protein synthesis? [J]. Clin Infect Dis, 2005, 40(12): e113-e116.
[3] DE VRIESE AS, COSTER RV, SMET J, et al. Linezolidinduced inhibition of mitochondrial protein synthesis [J]. Clin Infect Dis, 2006,42(8): 1111-1117.
[4] GARRABOU G, SORIANO A, LOPEZ S, et al. Reversible inhibition of mitochondrial protein synthesis during linezolidrelated hyperlactatemia [J]. Antimicrob Agents Chemother,2007,51(3):962-967.
[5] NARANJO CA, BUSTO U, SELLERS EM, et al. A method for estimating the probability of adverse drug reactions[J]. Clin Pharm Ther, 1981,30(2):239-245.
[6] CONTOU D, FICHET J, GRIMALDI D, et al. Early lifethreatening lactic acidosis following a single infusion of linezolid [J]. Int J Antimicrob Agents, 2011,38(1): 84-85.
[7] PEA F, SCUDELLER L, LUGANO M, et al. Hyperlactacidemia potentially due to linezolid overexposure in a liver transplant recipient [J]. Clin Infect Dis, 2006,42(3):434-435.
[8] 熊晓东,胡永芳.利奈唑胺致全血细胞减少[J].药物不良反应杂志,2011,13(5):319-321.
[9] SASSE J, TEICHMANN D. Disseminated multi organ MDR-TB resistant to virtually all f i rstline drugs [J]. Eur Respir Rev, 2009,18(114): 291-294.
[10] HALPERN M. Linezolid-induced pancytopenia [J]. Clin Infect Dis,2002, 35(3): 347-348.
[11] BERNARD L, STERN R, LEW D, et al. Serotonin syndrome after concomitant treatment with linezolid and citalopram [J]. Clin Infect Dis, 2003,36(9): 1197.
[12] NIMEIRI HS, NEMIARY DS. Challenges with linezolid therapy and reversible pancytopenia[J]. Ann Hematol, 2003,82(8):533.
[13] LAKHANI N, THOMPSON W, BOMBASSARO AM. Probable linezolid-induced pancytopenia [J]. Can J Infect Dis Med Microbiol, 2005,16(5): 286-288.
[14] SORIANO A, MIRO O, MENSA J. Mitochondrial toxicity associated with linezolid [J]. N Engl J Med, 2005,353(21):2305-2306.
[15] KOPTERIDES P, PAPADOMICHELAKIS E. ARMAGANIDIS A. Linezolid use associated with lactic acidosis [J]. Scand J Infect Dis, 2005,37(2):153-154.
[16] VU NS, WALIA R. Linezolid-induced lactic acidosis [J]. Chest J, 2006, 130(4): 337-338.
[17] THORELL EA, SHARMA M, JACKSON MA, et al. Disseminated nontuberculous mycobacterial infections in sickle cell anemia patients [J]. J Pediatr Hematol Oncol, 2006,28(10):678-681.
[18] WIENER M, GUO Y, PATEL G, et al. Lactic acidosis after treatment with linezolid [J]. Infection, 2007,35(4): 278-281.
[19] FAGUER S, KAMAR N, FILLOLA G, et al. Linezolid-related pancytopenia inorgan-transplant patients: report of two cases [J]. Infection, 2007,35(4): 275-277.
[20] SCOTTON P, FUSER R, TORRESAN S, et al. Early linezolidassociated lactic acidosis in a patient treated for tuberculous spondylodiscitis [J]. Infection, 2008,36(4): 387-388.
[21] GORCHYNSKI J, ROSE JK. Complications of MRSA treatment: linezolid-induced myelosuppression presenting with pancytopenia [J]. West J Emerg Med, 2008, 9(3): 177-178.
[22] FERNÁNDEZD OL, DIAZ V, RAMIREZ M, et al. Linezolidinduced lacticacidosis [J]. Enferm Infec Microbiol Clin, 2009,27(9): 550-551.
[23] BOUTOILLE D, GROSSI O, DEPATUREAUX A, et al. Fatal lactic acidosis after prolonged linezolid exposure for treatment of multidrug-resistant tuberculosis [J]. Eur J Intern Med, 2009, 20(6): e134-e135.
[24] GOWRINATH K, BAIG WW, PRABHU AR, et al. Pulmonary nocardiosis due to Nocardia farcinica in a renal transplant recipient [J]. Indian J Chest Dis Allied Sci, 2009, 51(4):237-239.
[25] VELEZ JC, JANECH MG. A case of lactic acidosis induced by linezolid [J]. Nat Rev Nephrol, 2010,6(4): 236-242.
[26] DE BUS L, DEPUYDT P, LIBBRECHT L, et al. Severe druginduced liver injury associated with prolonged use of linezolid [J]. J Med Toxicol, 2010,6(3): 322-326.
[27] COPE TE, MCFARLAND R, SCHAEFER A. Rapid-onset,linezolid-induced lactic acidosis in MELAS [J]. Mitochondrion,2011, 11(6): 992-993.
[28] SU E, CROWLEY K, CARCILLO JA, et al. Linezolid and lactic acidosis: a role for lactate monitoring with long-term linezolid use in children [J]. Pediatr Infect Dis J, 2011, 30(9):804-806.
[29] CARBAJO T, FENOLLOSA M, PONS R, et al. Lactic acidosis and linezolid-induced pancytopaenia [J]. Nefrologia, 2011,31(1): 107-108.
[30] 谢诚,高杰,赵玉琴,等.利奈唑胺致全血细胞减少[J].药物不良反应杂志,2011,13(6):377-378.
[31] 赵新菊,王梅.利奈唑胺致慢性肾脏病患者转氨酶升高、血小板减少、乳酸酸中毒1例[J].实用药物与临床,2012,1(10):665-668.
[32] 潘敏,江开勇,文富强,等.利奈唑胺致全血细胞减少[J].中国医学工程,2012,20(5):174-175.
[33] LEE HJ, CHOI JH, KIM SY, et al. A case of linezolidassociated lactic acidosis [J]. Korean J Med, 2012,82(3):371-373.
[34] 庞昶,白玉兰.利奈唑胺致肝功能异常及乳酸酸中毒1例[J].中国感染与化疗杂志,2013,13(2):148-149.
[35] KRALETI S, SOULTANOVA I. Pancytopenia and lactic acidosis associated with linezolid use in a patient with empyema [J]. J Ark Med Soc, 2013,110(4):62-63.
[36] DELPOZO JL, FERNANDEZ-ROS N, SAEZ E, et al. Linezolid-induced lactic acidosis in two liver transplant patients with the mitochondrial DNA A2706G polymorphism [J]. Antimicrob Agents Chemother, 2014,58(7): 4227-4229.
[37] 刘建清,吴国兰,陈晓红,等.长疗程利奈唑胺致全血细胞减少1例临床分析[J].中国医药指南,2014,12(23):287-288.
[38] JOHNSON PC, VADUGANATHAN M, PHILLIPS KM,et al. A triad of linezolid toxicity: hypoglycemia, lactic acidosis, and acute pancreatitis [J]. Proc (Bayl Univ Med Cent), 2015,28(5): 466-468.
[39] PARLAK E, TAN H. Pancytopenia due to linezolid treatment[J]. Turk Pediatri Ars, 2015, 50(3):185-188.
[40] 傅晓琴,余雄杰,刘生友. 17例利奈唑胺所致不良反应文献分析[J].中国药事,2011,25(11):1130-1131.
[41] 刘晓东,管凌燕,王法.利奈唑胺不良反应的文献分析[J].医药导报,2012,31(6):811-812.
[42] 孙景生,崔国金,刘俊杰.利奈唑胺致不良反应44例文献分析[J].现代药物与临床,2013,28(2):220-223.
[43] 陆奇志,曾嵘,李俊.利奈唑胺不良反应文献分析[J].内科,2013,8(3):297-299.
[44] 杨元勋,李刚,钱正刚.利奈唑胺不良反应文献分析[J].实用药物与临床,2013,16(7):621-623.
[45] RUBINSTEIN E, ISTURIZ R, STANDIFORD HC, et al. Worldwide assessment of linezolidd’s clinical safety and tolerability: comparator-controlled phase Ⅲ studies [J]. Antimicrob Agents Chemother, 2003,47(6):1824-1831.
[46] 田瑛,谭漫红,姜春燕,等.利奈唑胺对老年患者血液系统的影响[J].临床和实验医学杂志,2014,13(17):1457-1460.
[47] 王建国,陈建.临床治疗中利奈唑胺的药效学和药动学研究进展[J].中国抗生素杂志,2013,38(10):730-735.
[48] STALKER DJ, JUNGBLUTH GL. Clinical pharmacokinetics of linezolid, a novel oxazolidinone antibacterial [J]. Clin Pharmacokinet, 2003,42(13):1129-1140.
[49] MIYAWAKI A, UEDA T, NAKAO A, et al. Linezolid-induced lactic acidosis followed by severe hypophosphatemia after discontinuation of linezolid [J]. Surg Infect, 2013,14(2):229-230.
[50] IM JH, BAEK JH, KWON HY, et al. Incidence and risk factors of linezolid-induced lactic acidosis [J]. Int J Infect Dis, 2015,31:47-52.
[51] BIRMINGHAM MC,RAYNER CR, MEAGHER AK, et al. Linezolid for the treatment of multidrug-resistant, Gram-positive infections:experience from a compassionate use program [J]. Clin Infect Dis, 2003,36(2):159-168.
Linezolid-induced lactic acidosis and pancytopenia: one case report and literature review of 50 cases
ZHANG Yanyan, ZHU Wan, ZHANG Jingping, CHEN Baiyi. (Department of Infectious Diseases, the First Hospital of China Medical University, Shenyang 110001, China)
Objective To understand the adverse reaction pro fi le of linezolid during clinical treatment, especially lactic acidosis and pancytopenia. Methods One case of linezolid-induced lactic acidosis and pancytopenia was described in a patient receiving long-term treatment in our hospital. Similar cases were searched and identi fi ed from literatures reports both in China and abroad from 2000 to 2015 for further review. The data were analyzed in terms of patient age, sex, underlying conditions, as well as onset time, clinical characteristics, and outcomes of the adverse reaction. Results A total of 50 similar cases (male/female ratio: 1.78:1) were analyzed, 42.0 % of which were old patients (at least 65 years old). Liver and/or renal insuf fi ciency was found in 20 cases (40.0 %). The onset of lactic acidosis was at 5.5 weeks after initiation of linezolid on average, and the onset of pancytopenia was at 3.5 weeks after initiation of linezolid. Conclusions Linezolid-induced lactic acidosis or pancytopenia is more frequently found in the elderly patients with hepatic dysfunction and long-term treatment.
linezolid; lactic acidosis; pancytopenia; adverse reaction
R978.1
A
1009-7708 ( 2017 ) 04-0365-06
10.16718/j.1009-7708.2017.04.004
2016-07-05
2017-04-01
辽宁省科技厅项目(2013225303)。
中国医科大学附属第一医院感染科,沈阳 110001。
张岩岩(1988—),女,硕士研究生,主要从事感染性疾病的诊治。
张静萍,E-mail:zjp809302@163.com。
